一种含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物及其制备和应用
技术领域
1.本发明属于有机化学合成技术领域,尤其涉及一种含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物及其制备方法和应用。
背景技术:
2.c-3位五元螺环吲哚酮是指在2-吲哚酮的c-3位具有五元螺环结构的吲哚衍生物。该结构广泛存在于具有生物活性的天然生物碱和药物分子中,具有抗肿瘤、抗菌、抗hiv、抗疟、抗病毒、解热剂和钠通道阻滞剂等功能(chem.commun.2018,54,6607;bioorg.med.chem.lett,2011,21,5916)。同时,全碳四取代烯烃结构经常出现在天然产物及药物分子中,由于其结构的特殊性,全碳四取代烯基在生物、材料、物理等领域也应用的非常广泛(chem.rev.2007,107,4698-4745)。现有合成c-3位五元螺环吲哚酮衍生物的方法主要是通过分子内以及分子间的环加成反应、过渡金属催化反应以及氧化反应等。但还未见报道过含有全碳四取代烯烃结构的c-3位螺环吲哚酮衍生物的制备方法。为了更好扩大螺环吲哚酮的利用度,研发一种新的c-3位五元螺环吲哚酮的制备方法是十分必要的,且该方法具备原料易得、条件简单、原子经济性高的优点。
技术实现要素:
3.针对上述技术问题,本发明提出一种含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物及其制备方法和应用,该方法简单,且可以通过优化反应条件达到产物选择性单一,产率高、纯度高的效果。
4.为实现上述技术目的,本发明采取如下技术方案:
5.一种含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物,所述含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物结构式如式(i)所示:
[0006][0007]
其中,r1、r2、r3、r4独立地选自h、氰基、硝基、羟基、苯基、取代苯基、亚甲二氧基、c
1-c6烷基、c
2-c6烯基、c
1-c6烷氧基、卤素、卤代c
1-c6烷基和卤代c
1-c6烷氧基中的任意一种。
[0008]
一种含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物的制备方法,包括以下步骤:在有机溶剂中加入式(ii)所示的具有烯炔的2-碘芳基丙烯酰胺化合物、式(iii)所示的苯硼酸类化合物、有机配体和碱,在催化剂作用下进行反应,即得含有全碳四取代烯
烃结构的c-3位螺环吲哚酮衍生物;
[0009][0010]
其中,r1、r2、r3、r4独立地选自h、氰基、硝基、羟基、苯基、取代苯基、亚甲二氧基、c
1-c6烷基、c
2-c6烯基、c
1-c6烷氧基、卤素、卤代c
1-c6烷基和卤代c
1-c6烷氧基中的任意一种。
[0011]
所述c
1-c6烷基的含义是指具有1-6个碳原子的直链或支链烷基,其包括c1烷基、c2烷基、c3烷基、c4烷基、c5烷基和c6烷基;可以为甲基、乙基、正丙基、异丙基、正丁基、仲丁基、异丁基、叔丁基、正戊基、异戊基和正己基等。
[0012]c1-c6烷氧基是指c
1-c6烷基与氧原子相连后的基团。
[0013]
卤素的含义是指卤族元素,可以为f、cl、br和i。
[0014]
卤代c
1-c6烷基的含义是指被卤素取代的c
1-c6烷基,可以为三氟甲基、五氟乙基、二氟甲基、氯甲基等。
[0015]
本发明的制备方法中,可以将式(ii)所示的具有烯炔的2-碘芳基丙烯酰胺化合物与式(iii)所示的苯硼酸类化合物一起混合进行反应,在反应过程中,首先,具有烯炔的2-碘芳基丙烯酰胺化合物(ii)先发生氧化加成,再发生分子内heck反应,然后发生分子内碳金属化反应生成烯基钯络合物,接着苯硼酸类化合物(iii)与烯基钯络合物发生金属转移,最后还原消除生成含有全碳四取代烯烃结构的c-3位螺环吲哚酮衍生物(i)。
[0016]
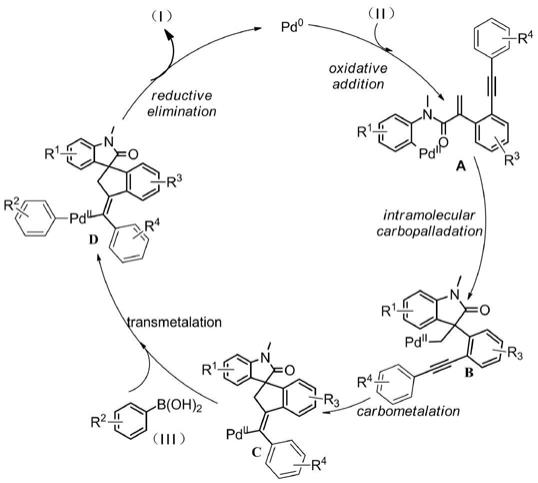
本发明的反应机理如下:
[0017][0018]
首先,pd0先与具有烯炔的2-碘芳基丙烯酰胺化合物(ii)的c-i键氧化加成生成中间体a,a再发生分子内heck反应形成-烷基pd(ii)物种b,然后由于钯与炔键合适的距离发生b分子内碳金属化反应生成烯基钯络合物c,接着苯硼酸类化合物(iii)与c发生金属转移生成中间体d,最后d经还原消除生成含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍
生物(i)并pd0再生。
[0019]
进一步地,所述有机溶剂包括甲醇、乙醇、乙腈、四氢呋喃、n,n-二甲基甲酰胺、1,4-二氧六环、二甲基亚砜、甲苯、二甲苯和n-甲基吡咯烷酮中的任意一种。
[0020]
进一步地,所述有机配体包括三苯基膦、三叔丁基膦、三环己基膦、三(2-甲氧基苯基)膦、三(4-氟苯基)膦、1,1'-双(二苯基膦)二茂铁和2-二环己基磷-2,4,6-三异丙基联苯中的任意一种。
[0021]
进一步地,所述碱包括碳酸钾、碳酸氢钠、磷酸钾、碳酸铯、三乙胺、三丁烯二胺中的任意一种。
[0022]
进一步地,所述催化剂为钯化合物;所述钯化合物包括醋酸钯、氯化钯、溴化钯、碘化钯、四三苯基膦钯、三氟乙酸钯、三(二亚苄基丙酮)二钯和双(二亚苄基丙酮)钯中的任意一种。
[0023]
进一步地,所述具有烯炔的2-碘芳基丙烯酰胺化合物和苯硼酸类化合物的摩尔比为1:1-3;所述具有烯炔的2-碘芳基丙烯酰胺化合物与催化剂的摩尔比为1:0.05-0.4;所述具有烯炔的2-碘芳基丙烯酰胺化合物与有机配体的摩尔比为1:0.1-2;所述具有烯炔的2-碘芳基丙烯酰胺化合物与碱的摩尔比为1:1-5;所述具有烯炔的2-碘芳基丙烯酰胺化合物与有机溶剂的用量比为1mmol:5-15ml;例如1mmol:5ml、1mmol:8ml、1mmol:10ml、1mmol:12ml和1mmol:15ml。
[0024]
进一步地,所述反应温度为25-140℃,时间为1-24h。
[0025]
进一步地,所述制备方法还包括后处理纯化步骤。
[0026]
更进一步地,所述后处理纯化步骤包括:反应结束后,冷却至室温,震荡萃取,收集有机层并干燥,旋转蒸发浓缩,得粗产物;然后经结晶、重结晶、层析,洗脱,即可得到最终纯度高、收率高的产物。
[0027]
具体的,以水和乙酸乙酯作为萃取剂萃取1-3次,其中水与乙酸乙酯的体积比为2-5:1,收集上层液体;用无水na2so4干燥,干燥后用旋转蒸发仪蒸除乙酸乙酯,残留物(粗产物)结晶、重结晶后过200-400目硅胶柱色谱层析;以乙酸乙酯和石油醚为洗脱剂,乙酸乙酯与石油醚的体积比为1:1-10。
[0028]
进一步地,还可以以乙酸乙酯和饱和食盐水等体积比混合作为萃取剂进行萃取。
[0029]
一种含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物在药物中间体中的应用。
[0030]
与现有技术相比,本发明的有益效果为:
[0031]
本发明使用钯化合物作为催化剂、使用膦类化合物作为配体,可由式(ii)中的具有烯炔的2-碘芳基丙烯酰胺化合物、式(iii)中的苯硼酸类化合物在有机溶剂中反应,一步得到含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物。本发明采用一锅法制备目标产物,具有产物选择性单一,通过优化条件使其产率高、纯度高、原子经济性高等诸多优点,为含有全碳四取代烯烃结构的c-3位五元螺环吲哚酮衍生物提供了全新路线和新思路,可在药物中间体、农药中间体等领域中发挥重要作用,在工业和科研上具有良好的应用价值和潜力。
附图说明
[0032]
图1为实例1所得产物核磁谱图;
[0033]
图2为实例2所得产物核磁谱图;
[0034]
图3为实例3所得产物核磁谱图;
[0035]
图4为实例4所得产物核磁谱图;
[0036]
图5为实例5所得产物核磁谱图;
[0037]
图6为实例6所得产物核磁谱图;
[0038]
图7为实例7所得产物核磁谱图;
[0039]
图8为实例8所得产物核磁谱图。
具体实施方式
[0040]
现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
[0041]
应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
[0042]
除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
[0043]
在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见的。本技术说明书和实施例仅是示例性的。
[0044]
关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
[0045]
实施例1
[0046][0047]
向甲苯中加入上式(ii)n-(2-碘苯基)-n-甲基-2-(2-(苯基乙炔基)苯基)丙烯酰胺、(iii)苯硼酸、醋酸钯(pd(oac)2)、三苯基膦(pph3)和碳酸铯(cs2co3),然后在室温下搅拌密封反应24h。
[0048]
其中,式(ii)化合物与醋酸钯(pd(oac)2)的摩尔比为1:0.05;式(ii)化合物与三苯基膦(pph3)的摩尔比为1:0.1;式(ii)化合物与碳酸铯(cs2co3)的摩尔比为1:3;式(ii)化合物与(iii)化合物的摩尔比为1:1.2;以及以毫摩尔(mmol)和毫升(ml)计,所述式(ii)化合物与甲苯的比为1:5。
[0049]
反应结束后,将反应体系自然冷却至室温,加入等体积比的乙酸乙酯和饱和食盐水的混合液,振荡萃取3次,收集有机层、干燥,旋转蒸发浓缩,得粗产物,将粗产物经结晶、重结晶后过300目硅胶柱色谱层析,以乙酸乙酯和石油醚混合液为洗脱剂,其中乙酸乙酯与石油醚的体积比1:5,即得到外观为白色固体的目标产物式(i)化合物(c
30h23
no)。
[0050]
对本实施例得到的产物c
30h23
no进行核磁共振分析,结果为:1hnmr(500mhz,氘代氯仿cdcl3)δ:7.41-7.34(m,5h),7.27-7.23(m,5h),7.18-7.15(m,1h),7.11(d,j=7.0hz,1h),7.02-6.99(m,2h),6.91(t,j=7.5hz,1h),6.86(d,j=7.5hz,1h),6.72(d,j=7.5hz,1h),6.54(d,j=8.0hz,1h),3.57(d,j=15.5hz,1h),3.25(s,3h),3.17(d,j=15.0hz,1h)。
[0051]
13
cnmr(125mhz,氘代氯仿cdcl3)δ:178.9,147.3,143.1,142.9,142.1,141.7,137.2,136.5,134.2,129.9,129.2,128.8,128.2(double),128.0,127.4,127.3,126.9,125.4,123.3,123.1,123.0,108.0,58.1,46.5,26.4。
[0052]
经测算:产物c
30h23
no产率为96%,纯度为98.9%(hplc),熔点:179-180℃。
[0053]
实施例2
[0054][0055]
向甲苯中加入上式(ii)n-(2-碘-4-甲氧基苯基)-n-甲基-2-(2-(苯基乙炔基)苯基)丙烯酰胺、(iii)苯硼酸、醋酸钯(pd(oac)2)、三苯基膦(pph3)和碳酸铯(cs2co3)然后室温下搅拌密封反应24h。
[0056]
其中,式(ii)化合物与醋酸钯(pd(oac)2)的摩尔比为1:0.05;式(ii)化合物与三苯基膦(pph3)的摩尔比为1:0.1;式(ii)化合物与碳酸铯(cs2co3)的摩尔比为1:3;式(ii)化合物与(iii)化合物的摩尔比为1:1.2;以及以毫摩尔(mmol)和毫升(ml)计,所述式(ii)化合物与甲苯的比为1:10。
[0057]
反应结束后,将反应体系自然冷却至室温,加入等体积比的乙酸乙酯和饱和食盐水的混合液,振荡萃取3次,收集有机层、干燥,旋转蒸发浓缩,得粗产物,将粗产物经结晶、重结晶后过300目硅胶柱色谱层析,以乙酸乙酯和石油醚混合液为洗脱剂,其中乙酸乙酯与石油醚的体积比1:3,即得到外观为白色固体的目标产物式(i)化合物(c
31h25
no2)。
[0058]
对本实施例得到的产物c
31h25
no2进行核磁共振分析,结果为:1hnmr(500mhz,氘代氯仿cdcl3)δ:7.39-7.33(m,5h),7.28-7.22(m,4h),7.16(t,j=6.5hz,1h),7.00(t,j=7.5hz,1h),6.91(t,j=7.5hz,1h),6.79-6.73(m,4h),6.54(d,j=8.0hz,1h),3.72(s,3h),3.58(d,j=15.5hz,1h),3.23(s,3h),3.17(d,j=15.5hz,1h)。
[0059]
13
cnmr(125mhz,氘代氯仿cdcl3)δ:178.5,156.2,147.3,142.8,142.1,141.6,137.1,136.6,136.4,135.4,129.9,129.2,128.8,128.2,127.9,127.4,127.3,126.8,125.4,123.3,112.1,110.6,108.3,58.4,55.6,46.5,26.5。
[0060]
经测算:产物c
31h25
no2产率为91%,纯度为98.1%(hplc),熔点:238-239℃。
[0061]
实施例3
[0062][0063]
向甲苯中加入上式(ii)2-(5-氟-2-(苯基乙炔基)苯基)-n-(2-碘苯基)-n-甲基丙烯酰胺、(iii)苯硼酸、醋酸钯(pd(oac)2)、三苯基膦(pph3)和碳酸铯(cs2co3)然后室温下搅拌密封反应24h。
[0064]
其中,式(ii)化合物与醋酸钯(pd(oac)2)的摩尔比为1:0.05;式(ii)化合物与三苯基膦(pph3)的摩尔比为1:0.1;式(ii)化合物与碳酸铯(cs2co3)的摩尔比为1:3;式(ii)化合物与(iii)化合物的摩尔比为1:1.2;以及以毫摩尔(mmol)和毫升(ml)计,所述式(ii)化合物与甲苯的比为1:10。
[0065]
反应结束后,将反应体系自然冷却至室温,加入等体积比的乙酸乙酯和饱和食盐水的混合液,振荡萃取3次,收集有机层、干燥,旋转蒸发浓缩,得粗产物,将粗产物经结晶、重结晶后过300目硅胶柱色谱层析,以乙酸乙酯和石油醚混合液为洗脱剂,其中乙酸乙酯与石油醚的体积比1:5,即得到外观为白色固体的目标产物式(i)化合物(c
30h22
fno)。
[0066]
对本实施例得到的产物c
30h22
fno进行核磁共振分析,结果为:1hnmr(500mhz,氘代氯仿cdcl3)δ:7.42-7.36(m,5h),7.29-7.23(m,5h),7.17-7.16(m,1h),7.12(d,j=7.0hz,1h),7.03(t,j=7.5hz,1h),6.87(d,j=8.0hz,1h),6.63-6.60(m,1h),6.48-6.45(m,1h),6.42-6.40(m,1h),3.60(d,j=15.5hz,1h),3.26(s,3h),3.20(d,j=15.5hz,1h)。
[0067]
13
cnmr(125mhz,氘代氯仿cdcl3)δ:178.3,163.4,161.4,149.3,149.2,143.1,142.7,141.9,137.9,136.0,135.9,133.4,129.9,129.1,128.9,128.5,128.0,127.4,126.9,126.8,126.7,123.1,115.0,114.8,110.4,110.2,108.2,57.9,46.7,26.5。
[0068]
经测算:产物c
30h22
fno产率为96%,纯度为98.7%(hplc),熔点:170-171℃。
[0069]
实施例4
[0070]
[0071]
向甲苯中加入上式(ii)n-(2-碘苯基)-2-(5-甲氧基-2-(苯基乙炔基)苯基)-n-甲基丙烯酰胺、(iii)苯硼酸、醋酸钯(pd(oac)2)、三苯基膦(pph3)和碳酸铯(cs2co3)然后室温下搅拌密封反应24h。
[0072]
其中,式(ii)化合物与醋酸钯(pd(oac)2)的摩尔比为1:0.05;式(ii)化合物与三苯基膦(pph3)的摩尔比为1:0.1;式(ii)化合物与碳酸铯(cs2co3)的摩尔比为1:3;式(ii)化合物与(iii)化合物的摩尔比为1:1.2;以及以毫摩尔(mmol)和毫升(ml)计,所述式(ii)化合物与甲苯的比为1:10。
[0073]
反应结束后,将反应体系自然冷却至室温,加入等体积比的乙酸乙酯和饱和食盐水的混合液,振荡萃取3次,收集有机层、干燥,旋转蒸发浓缩,得粗产物,将粗产物经结晶、重结晶后过300目硅胶柱色谱层析,以乙酸乙酯和石油醚混合液为洗脱剂,其中乙酸乙酯与石油醚的体积比1:3,即得到外观为白色固体的目标产物式(i)化合物(c
31h25
no2)。
[0074]
对本实施例得到的产物c
31h25
no2进行核磁共振分析,结果为:1hnmr(500mhz,氘代氯仿cdcl3)δ:7.44-7.41(m,4h),7.37-7.32(m,1h),7.29-7.23(m,5h),7.16(t,j=7.0hz,1h),7.10(d,j=7.0hz,1h),7.01(t,j=7.0hz,1h),6.85(d,j=7.5hz,1h),6.61-6.57(m,2h),6.02(d,j=1.0hz,1h),3.58(d,j=15.5hz,1h),3.36(s,3h),3.24(s,3h),3.19(d,j=15.5hz,1h)。
[0075]
13
cnmr(125mhz,氘代氯仿cdcl3)δ:179.1,158.9,143.1(double),142.7,142.1,139.6,137.3,136.4,134.3,130.1,129.2,128.8,128.1,128.0,127.3,126.9,123.9,123.1,122.9,116.3,109.0,108.0,57.4,54.7,47.0,26.4。
[0076]
经测算:产物c
31h25
no2产率为96%,纯度为98.0%(hplc),熔点:170-171℃。
[0077]
实施例5
[0078][0079]
向甲苯中加入上式(ii)n-(2-碘苯基)-n-甲基-2-(2-(对-甲苯乙炔基)苯基)丙烯酰胺、(iii)苯硼酸、醋酸钯(pd(oac)2)、三苯基膦(pph3)和碳酸铯(cs2co3)然后室温下搅拌密封反应24h。
[0080]
其中,式(ii)化合物与醋酸钯(pd(oac)2)的摩尔比为1:0.05;式(ii)化合物与三苯基膦(pph3)的摩尔比为1:0.1;式(ii)化合物与碳酸铯(cs2co3)的摩尔比为1:3;式(ii)化合物与(iii)化合物的摩尔比为1:1.2;以及以毫摩尔(mmol)和毫升(ml)计,所述式(ii)化合物与甲苯的比为1:10。
[0081]
反应结束后,将反应体系自然冷却至室温,加入等体积比的乙酸乙酯和饱和食盐水的混合液,振荡萃取3次,收集有机层、干燥,旋转蒸发浓缩,得粗产物,将粗产物经结晶、重结晶后过300目硅胶柱色谱层析,以乙酸乙酯和石油醚混合液为洗脱剂,其中乙酸乙酯与石油醚的体积比1:5,即得到外观为白色固体的目标产物式(i)化合物(c
31h25
no)。
[0082]
对本实施例得到的产物c
31h25
no进行核磁共振分析,结果为:1hnmr(500mhz,氘代氯仿cdcl3)δ:7.27-7.24(m,7h),7.20-7.19(m,2h),7.16(d,j=6.5hz,1h),7.11(d,j=7.0hz,1h),7.00(t,j=7.5hz,2h),6.93(t,j=7.5hz,1h),6.86(d,j=7.5hz,1h),6.72(d,j=7.5hz,1h),6.62(d,j=8.0hz,1h),3.56(d,j=15.0hz,1h),3.26(s,3h),3.15(d,j=15.0hz,1h),2.41(s,3h)。
[0083]
13
cnmr(125mhz,氘代氯仿cdcl3)δ:179.0,147.3,143.2(double),141.9,139.2,137.1,136.9,136.6,134.3,130.0,129.6,129.3,128.2(double),128.0,127.4,126.9,125.5,123.4,123.2,123.1,108.1,58.2,46.7,26.6,21.4。
[0084]
经测算:产物c
31h25
no产率为96%,纯度为98.7%(hplc),熔点:223-224℃。
[0085]
实施例6
[0086][0087]
向甲苯中加入上式(ii)2-(2-((4-氯苯基)乙炔基)苯基)-n-(2-碘苯基)-n-甲基丙烯酰胺、(iii)苯硼酸、醋酸钯(pd(oac)2)、三苯基膦(pph3)和碳酸铯(cs2co3)然后室温下搅拌密封反应24h。
[0088]
其中,式(ii)化合物与醋酸钯(pd(oac)2)的摩尔比为1:0.05;式(ii)化合物与三苯基膦(pph3)的摩尔比为1:0.1;式(ii)化合物与碳酸铯(cs2co3)的摩尔比为1:3;式(ii)化合物与(iii)化合物的摩尔比为1:1.2;以及以毫摩尔(mmol)和毫升(ml)计,所述式(ii)化合物与甲苯的比为1:10。
[0089]
反应结束后,将反应体系自然冷却至室温,加入等体积比的乙酸乙酯和饱和食盐水的混合液,振荡萃取3次,收集有机层、干燥,旋转蒸发浓缩,得粗产物,将粗产物经结晶、重结晶后过300目硅胶柱色谱层析,以乙酸乙酯和石油醚混合液为洗脱剂,其中乙酸乙酯与石油醚的体积比1:5,即得到外观为白色固体的目标产物式(i)化合物(c
30h22
clno)。
[0090]
对本实施例得到的产物c
30h22
clno进行核磁共振分析,结果为:1hnmr(500mhz,氘代氯仿cdcl3)δ:7.38-7.32(m,4h),7.30-7.22(m,5h),7.18(t,j=7.0hz,1h),7.12-7.09(m,1h),7.05-7.01(m,2h),6.97(t,j=7.5hz,1h),6.88(d,j=7.5hz,1h),6.72(d,j=7.5hz,1h),6.63(d,j=8.0hz,1h),3.51(d,j=15.5hz,1h),3.25(s,3h),3.19(d,j=15.5hz,1h)。
[0091]
13
cnmr(125mhz,氘代氯仿cdcl3)δ:178.7,147.4,143.3,142.5,141.5,140.6,137.9,135.0,133.9,133.2,131.5,129.2,129.1,128.4,128.3,128.1,127.5,127.1,125.3,123.5,123.1,123.0,108.1,58.0,46.8,26.5。
[0092]
经测算:产物c
30h22
clno产率为88%,纯度为98.5%(hplc),熔点:206-207℃。
[0093]
实施例7
[0094][0095]
向甲苯中加入上式(ii)n-(2-碘苯基)-n-甲基-2-(2-(苯基乙炔基)苯基)丙烯酰胺、(iii)3-甲氧基苯硼酸、醋酸钯(pd(oac)2)、三苯基膦(pph3)和碳酸铯(cs2co3)然后室温下搅拌密封反应24h。
[0096]
其中,式(ii)化合物与醋酸钯(pd(oac)2)的摩尔比为1:0.05;式(ii)化合物与三苯基膦(pph3)的摩尔比为1:0.1;式(ii)化合物与碳酸铯(cs2co3)的摩尔比为1:3;式(ii)化合物与(iii)化合物的摩尔比为1:1.2;以及以毫摩尔(mmol)和毫升(ml)计,所述式(ii)化合物与甲苯的比为1:10。
[0097]
反应结束后,将反应体系自然冷却至室温,加入等体积比的乙酸乙酯和饱和食盐水的混合液,振荡萃取3次,收集有机层、干燥,旋转蒸发浓缩,得粗产物,将粗产物经结晶、重结晶后过300目硅胶柱色谱层析,以乙酸乙酯和石油醚混合液为洗脱剂,其中乙酸乙酯与石油醚的体积比1:5,即得到外观为白色固体的目标产物式(i)化合物(c
31h25
no2)。
[0098]
对本实施例得到的产物c
31h25
no2进行核磁共振分析,结果为:1hnmr(500mhz,氘代氯仿cdcl3)δ:7.39-7.32(m,5h),7.25(t,j=15.5hz,1h),7.17(t,j=8.0hz,1h),7.11(d,j=7.0hz,1h),7.02-6.98(m,2h),6.90(t,j=7.5hz,1h),6.86(d,j=7.5hz,2h),6.82-6.81(m,1h),6.72(d,j=7.5hz,2h),6.54(d,j=7.5hz,1h),3.71(s,3h),3.58(d,j=15.5hz,1h),3.25(s,3h),3.18(d,j=15.0hz,1h)。
[0099]
13
cnmr(125mhz,氘代氯仿cdcl3)δ:178.8,159.2,147.3,144.3,143.1,141.9,141.6,137.3,136.3,134.1,129.8,128.9,128.8,128.2(double),127.3(double),125.4,123.3,123.1,122.9,121.8,115.0,112.1,108.0,58.0,55.1,46.5,26.4。
[0100]
经测算:产物c
31h25
no2产率为90%,纯度为98.8%(hplc),熔点:243-244℃。
[0101]
实施例8
[0102][0103]
向甲苯中加入上式(ii)n-(2-碘苯基)-n-甲基-2-(2-(苯基乙炔基)苯基)丙烯酰胺、(iii)3-溴苯硼酸、醋酸钯(pd(oac)2)、三苯基膦(pph3)和碳酸铯(cs2co3)然后室温下搅拌密封反应24h。
[0104]
其中,式(ii)化合物与醋酸钯(pd(oac)2)的摩尔比为1:0.05;式(ii)化合物与三
苯基膦(pph3)的摩尔比为1:0.1;式(ii)化合物与碳酸铯(cs2co3)的摩尔比为1:3;式(ii)化合物与(iii)化合物的摩尔比为1:1.2;以及以毫摩尔(mmol)和毫升(ml)计,所述式(ii)化合物与甲苯的比为1:10。
[0105]
反应结束后,将反应体系自然冷却至室温,加入等体积比的乙酸乙酯和饱和食盐水的混合液,振荡萃取3次,收集有机层、干燥,旋转蒸发浓缩,得粗产物,将粗产物经结晶、重结晶后过300目硅胶柱色谱层析,以乙酸乙酯和石油醚混合液为洗脱剂,其中乙酸乙酯与石油醚的体积比1:5,即得到外观为白色固体的目标产物式(i)化合物(c
30h22
brno)。
[0106]
对本实施例得到的产物c
30h22
brno进行核磁共振分析,结果为:1hnmr(500mhz,氘代氯仿cdcl3)δ:7.42-7.36(m,6h),7.31-7.27(m,2h),7.20(d,j=8.0hz,1h),7.12(t,j=8.0hz,2h),7.05-7.01(m,2h),6.93-6.88(m,2h),6.72(d,j=8.0hz,1h),6.51(d,j=8.0hz,1h),3.54(d,j=15.5hz,1h),3.27(s,3h),3.16(d,j=15.5hz,1h)。
[0107]
13
cnmr(125mhz,氘代氯仿cdcl3)δ:178.7,147.4,145.0,143.2,141.4(double),138.4,134.9,133.9,131.9,129.9,129.6,129.0,128.5,128.3,127.9,127.6,127.4,125.5,123.4,123.1,123.0,122.2,108.1,58.0,46.4,26.5。
[0108]
经测算:产物c
30h22
brno产率为86%,纯度为98.6%(hplc),熔点:155-156℃。
[0109]
实施例9-16
[0110]
按照表1所示的对应关系,以实施例1为例,将催化剂醋酸钯(pd(oac)2替换为相同摩尔量的其他钯化合物,其他操作相同,得到的产物收率如表1所示。
[0111]
表1不同催化剂下的产物收率
[0112][0113]
由此可见,在不同的钯化合物催化下,均能得到相应的产物,总体零价钯化合物的反应效果比二价的要好,且其中pd(oac)2的催化效果最好。
[0114]
实施例17-22
[0115]
按照表2所示的对应关系,以实施例1为例,将实施例1中的配体三苯基膦(pph3)替
换为相同摩尔量的其他配体,替换为相同摩尔量的其他配体,其他操作相同,得到的产物收率如表2所示。
[0116]
表2不同配体下的产物收率
[0117][0118]
由此可见,在所有的配体中,三苯基膦(pph3)具有合适的配位性,而其它配体则产率均有显著降低。
[0119]
实施例24-28
[0120]
按照表3所示的对应关系,以实施例1为例,将实施例1的碱碳酸铯替换为相同体积的其他碱,其他操作相同,得到的产物收率如表3所示。
[0121]
表3.不同溶剂下的产物收率
[0122][0123]
由此可见,碱同样对最终结果有着一定的影响,其中碳酸铯具有最好的效果,磷酸钾次之,其他溶剂的产率都有大幅度的降低。
[0124]
实施例29-33
[0125]
按照表4所示的对应关系,以实施例1为例,将实施例1的溶剂甲苯替换为相同体积的其他溶剂,其他操作相同,得到的产物收率如表4所示。
[0126]
表4.不同溶剂下的产物收率
[0127][0128]
由此可见,溶剂同样对最终结果有着一定的影响,其中甲苯具有最好的效果,1,4-二氧六环次之,其他溶剂的产率都有大幅度的降低。
[0129]
综上所述,由上述所有实施例可明确看出,当采用本发明的方法时,能够使式(ii)和(iii)化合物顺利发生反应,从而得到目标产物,且产率良好、后处理简单,这些效果的取得,依赖于多个因素如催化剂、配体、碱、溶剂的综合协同作用。
[0130]
对比例1和对比例2
[0131]
同实施例1,区别在于,乙酸乙酯与石油醚的体积比1:3。
[0132]
经检测,对比例1、对比例2得到的产物纯度较实施例1均有下降。分析原因是由于不同洗脱剂分离效果不一样,洗脱剂极性太高或者太低都会降低产物的纯度。
[0133]
对比例3
[0134]
同实施例1,区别在于,所述反应温度为110℃。
[0135]
对比例4
[0136]
同实施例1,区别在于,所述反应温度为130℃。
[0137]
经检测,对比例3得到的产物纯度与实施例1相近,基本无差异,对比例4产物产率较实施例1稍有下降,分析原因是由于温度过高,导致部分反应在生成烯基钯时就发生还原消除,苯硼酸未充分参与反应。
[0138]
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
