具有髓鞘蛋白零启动子的aav载体及其用于治疗雪旺细胞相关疾病如charcot-marie-tooth疾病的用途
技术领域
1.本发明涉及靶向与雪旺细胞相关的疾病的病毒载体。
背景技术:
2.charcot-marie-tooth(cmt)疾病包括多种类型的非综合症遗传性神经病,它们一起被认为是最常见的神经遗传性疾病之一,受影响个体的频率达到一般人群的1:2500(1,2)。cmt神经病的特点是涉及越来越多的致病基因和由不同基因引起的重叠表型。此外,几个不同的基因可能会导致相同的表型。尽管对支持cmt神经病的复杂遗传基础和多种疾病机制的了解越来越多,但目前还没有针对任何cmt形式的有效治疗方法,只能向患者提供对症和支持疗法。因此,非常需要新的cmt治疗策略。在过去的二十年中,一直致力于开发用于治疗cmt的基因疗法。虽然不同的基因治疗方法有望在未来治疗中枢和外周神经系统(pns)疾病,但仍有许多挑战需要克服(3)。
3.例如,(49)显示如何使用慢病毒载体在cmt4c的治疗中达到治疗效果。然而,这种效果是部分的,慢病毒载体对于体内人类治疗具有安全性限制。以前,其他载体如腺相关病毒载体(aav)不被认为是有用的,尽管它们更稳定且不会整合到宿主基因组中,由于它们最大包装容量为约4.4kb长度的插入片段,aav在基因治疗策略中的应用是有限的,尤其是在要替换的基因相对较长的情况下。
4.以雪旺细胞为靶点的基因治疗技术可以应用到除cmt外的许多与雪旺细胞相关的疾病,例如运动神经元疾病(mnd),包括那些不仅仅由遗传因素引起的疾病。许多这些疾病有多种原因并且尚未被很好地理解,因此使用病毒载体靶向这些疾病可能特别有利。
5.总体而言,仍然需要针对与雪旺氏细胞相关的疾病(包括脱髓鞘神经病(如cmt))的改进方法,以实现更好的治疗效果。
技术实现要素:
6.本发明人首次开发一种将多核苷酸例如治疗性多核苷酸递送到外周神经系统(pns)的雪旺细胞并在雪旺细胞中特异性地驱动所述多核苷酸的表达的有用方式。本发明可以用于治疗与雪旺细胞相关的疾病,当应用于治疗脱髓鞘性神经病如charcot-marie-tooth疾病(cmt)时,被认为是特别有益的。然而,本发明的潜在机制被认为适用于影响雪旺氏细胞的许多其他疾病,并且也被认为在其中将多核苷酸递送到雪旺氏细胞被认为是有利的任何情况下,例如在雪旺氏细胞成像中具有普遍效用。
7.本发明的一个方面的特征是使用aav载体来实现第一核酸的转录,导致在pns的施旺细胞中特异性地产生第一目的多核苷酸。在一些实施方案中,这种细胞类型特异性表达使用髓磷脂特异性启动子实现,并且在一些实施方案中,这使用髓磷脂特异性启动子的最小版本实现。
8.本发明的另一个特征是提供最小髓鞘特异性启动子,其在一些实施方案中基于全
长髓鞘蛋白零(mpz)启动子的序列。在一些实施方案中,包含较短最小启动子的病毒载体允许将较大的核酸序列,例如治疗性核酸序列,包括在载体中并递送到雪旺细胞。这被认为具有提供用于将核酸递送到雪旺细胞的通用载体的有利特性,并且可以用于治疗大范围的疾病,因为当前的方法受限于例如可由于它们的大小从病毒载体表达的基因。
具体实施方式
9.本发明根据权利要求书中所限定。
10.本发明通常提供如本文所述的用于医学的病毒载体,并且还提供包括施用根据本发明的载体的治疗方法,例如通过本文所述的任何方式施用。
11.本发明的第一方面提供用于治疗或预防与雪旺细胞相关的疾病的病毒载体。在一些实施方案中,病毒载体包含可转录为第一多核苷酸的第一核酸序列。
12.病毒载体可以是任何病毒载体。
13.病毒载体是本领域众所周知的并且实例包括但不限于:腺相关病毒载体(aav载体);慢病毒载体(例如源自人类免疫缺陷病毒(hiv)的那些);逆转录病毒载体(例如mmlv)。
14.在一些实施方案中,病毒载体是腺相关病毒载体(aav载体)。在优选的实施方案中,本发明提供用于治疗或预防与雪旺细胞相关的疾病的aav载体,其中aav载体包含可转录为第一多核苷酸的第一核酸序列。
15.如果第一核酸序列被转录,例如在靶细胞或靶生物体中被转录,则是优选的。因此,进一步的实施方案提供用于治疗或预防与雪旺细胞相关的疾病的病毒载体,其中所述病毒载体包含转录成第一多核苷酸的第一核酸序列。
16.另一个实施方案提供用于治疗或预防与雪旺细胞相关的疾病的aav,其中所述病毒载体包含转录成第一多核苷酸的第一核酸序列。
17.第一核酸序列可以在靶细胞或靶生物中转录成第一多核苷酸,例如在施旺细胞中转录。雪旺细胞可以在体内,例如可以在哺乳动物生物体中,例如可以是人、猫、狗、小鼠、兔、马。
18.雪旺细胞是周围神经系统(pns)的神经胶质细胞,它包裹感觉和运动神经元的轴突并产生周围的髓鞘。髓鞘由几种蛋白质成分(例如髓磷脂零蛋白)组成并且是神经元的重要绝缘成分,允许神经冲动(动作电位)沿神经快速传导。
19.当前一些基于病毒载体的治疗策略利用具有不良特征的载体。例如,一些病毒载体整合到宿主基因组中,具有明显的潜在有害后果。因此,在一个实施方案中,病毒载体不是整合到宿主细胞基因组中的病毒载体,例如不会整合到施旺细胞的核酸中。在一些实施方案中,不被认为整合到宿主基因组中的病毒载体是特别优选的,并且包括aav和腺病毒载体。aav载体感染靶细胞,递送的遗传材料不会整合到宿主细胞的基因组中。相反,递送的遗传材料保持游离。
20.被认为整合到宿主基因组中的病毒载体包括逆转录病毒载体,例如慢病毒载体。因此,在一个实施方案中,病毒载体不是整合到宿主基因组中的载体,例如不是逆转录病毒载体,例如不是慢病毒载体。
21.一些载体也不能转导雪旺氏细胞。技术人员将理解可以和不能转导雪旺氏细胞的载体类型。因此,在一个实施方案中,本发明的病毒载体不是不能转导雪旺氏细胞的病毒载
体。在一些实施方案中,病毒载体具有转导雪旺氏细胞的能力。“转导”是指病毒载体能够感染靶细胞并将其中发现的多核苷酸构建体递送到靶细胞中。此类载体的实例包括aav和慢病毒载体。
22.在一个实施方案中,载体是其中在变得不稳定之前只能掺入有限大小的插入物的载体。例如,这样的载体包括aav载体。
23.优选地,病毒载体是aav载体,并且在一些实施方案中,aav载体选自包括或由以下组成的组:aav9和aavrh10。在一个特别优选的实施方案中,aav是aav9。
24.优选地,第一核酸的转录仅发生或基本上仅发生在施旺细胞中。因此,在一些实施方案中,病毒载体还包含与第一核酸可操作地连接的雪旺细胞特异性启动子。
[0025]“雪旺细胞特异性启动子”包括在雪旺细胞中导致显著表达而在非雪旺细胞中不表达或低表达的启动子的含义。例如,雪旺细胞特异性启动子可以在雪旺细胞中驱动来自第一个核酸的高水平转录(例如,在雪旺细胞中出现95%,或更多的总表达),而第一多核苷酸的表达在其他细胞类型中较低,例如中枢神经系统的表达(例如,在除雪旺细胞外的细胞中小于总表达的5%)。例如,在一个实施方案中,雪旺细胞与非雪旺细胞中的转录比例为至少100:0;95:5;90:10;85:15;80:20;75:25;70:30;65:35;60:40;或55:45。
[0026]
在一个实施方案中,雪旺细胞中的转录水平为任何其他非雪旺电池的至少1.5、2、3、4、5、6、7、8、9、10、20、30、40、50、60、70、80、90、100、250、500、750、1000、2500、5000、7500、10000倍。
[0027]
在一个实施方案中,雪旺细胞特异性启动子导致大部分表达发生在雪旺细胞中而不是非雪旺细胞中。
[0028]
技术人员将理解,即使是非常特异的启动子也可能导致其他细胞或组织中的一些表达。技术人员非常清楚将启动子分类为细胞或组织特异性,例如雪旺细胞特异性所需的靶细胞或组织与非靶细胞或组织之间的差异表达水平。例如,(66)和(67)证明中枢神经系统(cns)中细胞特异性启动子的鉴定。技术人员会意识到,对于具有细胞特异性的启动子,它必须包含仅在某些细胞类型中激活启动子的调控元件(例如转录因子的结合位点),并且启动子必须能够驱动报告基因或其他基因体外和体内的可证明表达。
[0029]
优选地,雪旺细胞特异性启动子导致仅在雪旺细胞中可检测水平的第一核酸的转录。技术人员熟知检测转录的常规方法,例如northern印迹、基于pcr的技术和免疫荧光标记。在一个实施方案中,当使用北印迹分析进行检测时,雪旺细胞特异性启动子导致雪旺细胞中第一核酸的可检测转录,但不会导致非雪旺细胞中,例如在外周神经系统或脑的其他细胞中第一核酸的可检测水平的转录。在另一个实施方案中,当使用带有细胞标记物的免疫荧光标记分析进行检测时,雪旺细胞特异性启动子导致雪旺细胞中第一核酸的可检测转录,但不会导致非雪旺细胞,例如外周神经系统或脑的其他细胞中第一核酸的可检测水平的转录。
[0030]
例如(32)和(33)表明,使用慢病毒载体由全长mpz启动子驱动的构建体可以在体外和体内实现雪旺细胞特异性表达。
[0031]
在一些实施方案中,雪旺细胞特异性启动子包括髓鞘特异性启动子。“髓鞘特异性启动子”是指通常驱动编码构成髓鞘的蛋白质的基因表达的启动子。髓鞘特异性启动子的实例包括但不限于:髓鞘蛋白零(mpz)启动子;外周髓鞘蛋白22(pmp22)启动子;髓鞘相关糖
蛋白(mag)启动子。
[0032]
在一些实施方案中,第一多核苷酸的表达受全长髓鞘蛋白零(mpz)启动子,例如序列定义在seq id no.4中的全长大鼠髓鞘蛋白零(mpz)启动子控制在一些实施方案中,mpz启动子的序列具有与seq id no.4至少75%序列同源性或序列同一性,任选地与seq id no.4至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列。
[0033]
在一些实施方案中,技术人员清楚启动子序列优选源自人或人源化的启动子序列。在一些实施方案中,第一多核苷酸的表达在其序列在seq id no.18中定义的全长人髓鞘蛋白零(hp0)启动子的控制下在一些实施方案中,hp0启动子的序列具有与seq id no.18至少75%序列同源性或序列同一性,任选地与seq id no.18至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列。
[0034]
如上所述,如果启动子尽可能短被认为是有利的,特别是其中载体是在变得不稳定之前只能处理有限的插入片段的载体。因此,在一些实施方案中,第一多核苷酸的表达在长度在100bp和1100bp之间的启动子的控制下,任选地其中所述启动子的长度范围为200bp至900bp、长度为300bp至800bp、长度为400bp至700bp,任选地其中所述启动子的长度在500bp和600bp之间,例如长度为410bp。在相同或其他实施方案中,启动子长度小于1100bp,例如长度小于1000bp、900bp、800bp、700bp、600bp、500bp、400bp、300bp、200bp或小于100bp。
[0035]
在一些实施方案中,启动子是如本文定义的长度的天然存在的mpz启动子。在备选实施方案中,启动子是如本文定义的长度的工程化mpz启动子。“天然存在的启动子”是指与野生型雪旺细胞中发现的相应启动子序列相比没有被修饰、缩短或延长的启动子。“工程化启动子”是指经过某种方式改变的野生型启动子。例如,序列可以被修饰以具有例如与天然存在的启动子序列至少75%序列同源性或序列同一性,任选地至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在另一个或相同的实施方案中,启动子的长度也可以被修饰,例如野生型启动子的长度可以从更长的序列减少到例如在100bp和1100bp之间的长度,任选地200bp至900bp的长度,300bp至800bp的长度,400bp至700bp的长度,任选地500bp至600bp的长度,例如410bp的长度,或小于1100bp的长度,例如小于1000bp、900bp、800bp、700bp、600bp、500bp、400bp、300bp、200bp或小于100bp的长度。
[0036]
在另一个实施方案中,相对于野生型启动子,启动子长度可能已经增加。
[0037]
本领域技术人员将理解,对于启动子活性实际上需要被认为是启动子的特定核酸区域的仅一部分是可能的。在另一个实施例中,工程化启动子包括野生型启动子的部分序列,或包括野生型启动子的整个序列作为较长启动子序列的一部分。如所讨论的,优选地,启动子在施旺细胞中具有特异性活性。技术人员将能够测试全长启动子的特定片段是否导致在所述启动子片段控制下的蛋白质的雪旺细胞特异性表达,例如通过筛选报告基因在雪旺细胞中的表达。在一些实施例中,报告基因是egfp。
[0038]
在另一个实施方案中,工程化启动子是野生型启动子的截短形式,并且可以具有与天然存在的启动子序列例如至少75%序列同源性或序列同一性,任选地与天然存在的启
动子序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0039]
除了是天然启动子的截短形式外,工程化启动子可以额外地或替代地包含相对于天然启动子序列的突变、取代、缺失和插入。例如,工程化启动子可以在一个连续序列中包含天然启动子的各种不同区域。
[0040]
长度比相应的天然或野生型启动子短的工程化启动子可称为最小启动子。
[0041]
在一些实施方案中,工程化启动子保留与其来源的相应天然存在的启动子相同的功能,即它仍然可以有效地驱动多核苷酸序列从与该启动子可操作地连接的核酸序列转录,并且在优选的情况下可以有效地驱动以细胞特异性方式,即以雪旺细胞特异性方式转录。
[0042]
在一些实施方案中,第一多核苷酸的表达可以在例如缩短的天然存在的髓鞘特异性启动子的控制下,该启动子在本文中称为最小髓鞘特异性启动子,任选地这是最小髓鞘蛋白零(mpz)启动子。在一些实施方案中,最小髓鞘特异性启动子的序列包含如seq id no.5中定义的410bp序列或由其组成,该序列衍生自全长大鼠mpz启动子序列。在一些实施方案中,最小髓鞘特异性启动子包含具有与seq id no.5至少75%序列同源性或序列同一性,任选地与seq id no.5至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列或由其组成。
[0043]
在一些实施方案中,优选最小启动子源自人或人源化启动子序列。在一些实施方案中,最小髓鞘特异性启动子的序列包含如seq id no.22中定义的429bp序列或由其组成,该序列衍生自全长人hp0启动子序列。在一些实施方案中,最小髓鞘特异性启动子包含具有与seq id no.22至少75%序列同源性或序列同一性,任选地与seq id no.22至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列或由其组成。源自大鼠mpz或人hp0的最小髓鞘特异性启动子在本文中称为minimpz。
[0044]“序列同一性”或“序列同源性”是指特定dna区域中碱基对的相同序列。例如,在具有与参考序列75%序列同源性或序列同一性的序列中,75%的碱基对是相同的。
[0045]
可以使用适合的计算机程序,例如威斯康星大学遗传计算组(university of wisconsin genetic computing group)的gap程序确定两个多肽之间的序列同一性百分比,并且应了解,相对于序列已最佳比对的多肽计算同一性百分比。
[0046]
或者可以使用clustal w程序进行比对(如thompson等人,(1994)nucleic acids res 22,4673-80)。所用参数可以如下:
[0047]
快速成对比对参数:k-元组(字)大小;1,窗口大小;5,空位罚分(gap penalty);3,顶部对角线数量;5。评分方法:x百分比。
[0048]
多个比对参数:空隙开口罚分;10,空隙延伸罚分;0.05。
[0049]
评分矩阵:blosum。
[0050]
在一个实施方案中,本文所述的最小mpz启动子可以如实施例9中所述产生,例如通过取全长启动子的起始密码子上游的410个碱基对区域,例如全长髓鞘蛋白零(mpz)启动子。在另一个实施方案中,可以如实施例13中所述生产本文所述的最小mpz启动子。aav载体
具有携带约4.4kb多核苷酸的最大能力,因此使用如本文所述的较短mpz启动子,而不是长度约为1.1kb的全长mpz启动子,具有允许可操作地连接到启动子区域以包装到aav中的更长的第一核酸序列的优点。在其中所述启动子是例如长度为100bp至1100bp长、200bp至900bp、300bp至800bp、400bp至700bp、500bp至600bp或410bp的长度,或具有小于1100bp,例如小于1000bp、900bp、800bp、700bp、600bp、500bp、400bp、300bp、200bp或小于100bp的长度的较短启动子,例如工程化启动子或最小启动子的一些实施方案中,这允许本发明可应用于比使用全长启动子的aav载体更长的范围更广的基因。例如,目前存在一些情况,无法将特定长度的核酸序列(例如基因)插入aav中,因为当启动子较长时,核酸的长度可能会超过aav的最大容量,例如使用全长mpz启动子。例如,如果第一核酸,例如治疗基因,长度超过3.0-3.3kb(4.4kb
–
1.1kb=3.3kb)。在这种情况下,使用本文所述的有利的较短启动子,例如最小髓鞘特异性启动子,允许将本发明应用于例如较大基因的替换,例如引起cmt4c型的sh3tc2基因(cmt4c),长度约为3.9kb。其他雪旺细胞相关基因可能接近aav的稳定性极限,因此将在最小mpz启动子下进行最佳递送,包括与cmt4e相关的egr2(2.98kb)和与cmt4h相关的fgd4(2.3kb)。
[0051]
在另外的其他实施方案中,可以在反向末端重复区段中修饰本文所述的载体以进一步减小它们的大小。例如,土拨鼠肝炎病毒转录后调控元件(wpre),如实施例1中所述,可以被去除和/或polya序列可以被最小合成polya(68、69)替换。这种修饰可以进一步减小载体的大小,使其能够在aav的最大容量内重新邮寄,并在递送更大的基因时实现高效包装。在另外的其他实施方案中,可以通过例如还使用最小版本的待递送蛋白质编码基因来进一步减小载体的大小,其中所述最小版本的蛋白质编码基因仍然能够产生功能性蛋白质。
[0052]
在一些实施方案中,本文所述的病毒载体可以如实施例12中所述生产。在一些实施方案中,病毒载体具有seq id no:20中所示的序列,该序列去除wpre并具有合成的polya序列。在一些实施方案中,合成的polya序列包含mrna构建体的有效聚腺苷酸化所需的最小序列或由其组成(68、69)。在一些实施方案中,合成的polya序列包含seq id no:24的序列或由其组成,该序列包含在seq id no:20和21的序列中。在其他实施方案中,合成的polya序列具有与seq id no.24至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0053]
在一些实施方案中,病毒载体还包含egr2和sox10转录因子的结合位点。例如,病毒载体还可以包含例如egr2和sox10等转录因子可以结合的增强子元件。
[0054]
在一些实施方案中,病毒载体的第一核酸被转录成在一些实施方案中编码并翻译成第一多肽或蛋白质的第一多核苷酸。在一些实施方案中,第一核酸是基因序列或对应于基因序列的cdna的开放阅读框(orf)。在一些实施方案中,第一核酸是野生型或其他治疗上有益的基因序列的orf或cdna。在优选的实施方案中,第一核酸是神经病相关基因的野生型或治疗上有益序列的orf或cdna,任选地其中神经病是脱髓鞘神经病。
[0055]
通过“野生型或治疗上有益形式”,我们包括编码多肽或蛋白质的任何形式的基因序列,该多肽或蛋白质可以用于有效治疗与雪旺细胞相关的疾病。技术人员会理解,在其中疾病通过雪旺细胞对野生型多肽的生产不足引起的情况下,这通常是蛋白质的野生型形式(即,天然存在于雪旺细胞中的蛋白质),但可以还包括与野生型序列相比具有突变或插入或被截短以提供治疗优势的蛋白质形式,例如增加的表达水平、对降解的抗性、增加的稳定
性、增加的活性或有利的功能获得或抑制有毒的功能获得。例如,在后一种情况下,多肽可以是能够结合毒性获得功能突变体并抑制毒性的抗体。
[0056]
技术人员会知道,蛋白质表达通常通过将相关基因的orf或cdna引入病毒载体来进行。在一个实施方案中,第一核酸是当转录时产生第一多核苷酸的cdna序列,该第一多核苷酸被翻译成第一多肽或蛋白质。例如,cdna可以是转录成gjb1 mrna的cdna序列,其随后被翻译成cx32蛋白。
[0057]
技术人员将理解,在某些情况下,使用orf序列而不是cdna序列可能是优选的,因为orf序列缺少在cdna中发现的额外非编码元件并且尺寸更小,当病毒载体是当大小增加到高于特定阈值时变得不稳定的载体,这在本发明中特别有利。
[0058]
在一些另外的实施方案中,除了基因的cdna或orf外,本文所述的第一核酸序列还任选地包含其他调控元件。这些其他元件可能位于orf的下游。
[0059]
如上所述,本发明可以用于预防或治疗与雪旺细胞相关的疾病。通过“与雪旺细胞相关的疾病”,我们包括与雪旺细胞功能异常相关的所有疾病的含义。这包括与雪旺细胞形成的髓鞘破坏相关的疾病和/或与雪旺细胞形成的髓鞘表达降低相关的疾病。在一些实施方案中,与雪旺氏细胞相关的疾病是脱髓鞘性神经病。脱髓鞘神经病的实例包括但不限于charcot-marie-tooth疾病(cmt)。
[0060]“与雪旺细胞相关的疾病”在其含义上还包括与雪旺细胞相关但也与例如其他细胞类型或组织相关的疾病。认为本发明在这种情况下是有用的,因为雪旺细胞功能的改进可以减轻一些症状,即使本发明不针对与疾病相关的任何其他细胞类型。
[0061]
因此,在一个实施方案中,本文所述的病毒载体可以用于治疗或预防选自由以下组成的组的疾病:charcot-marie-tooth疾病(cmt);易患压力性麻痹的遗传性神经病(hnpp);糖尿病和其他中毒性周围神经病;运动神经元疾病(mnd)。
[0062]
在一些具体实施方案中,本文所述的病毒载体可以用于治疗或预防charcot-marie-tooth1x型(cmt1x);charcot-marie-tooth 1a-1f型(即cmt1a、cmt1b、cmt1c、cmt1d、cmt1e和cmt1f);charcot-marie-tooth 4a-4h型(即cmt4a、cmt4b、cmt4c、cmt4d、cmt4e、cmt4f、cmt4g和cmt4h)。在更具体的实施方案中,本文所述的病毒载体可以用于治疗或预防charcot-marie-tooth 1x型。在另一个更具体的实施方案中,本文所述的病毒载体可以用于治疗或预防4c型charcot-marie-tooth疾病。
[0063]
charcot-marie tooth疾病(cmt)是一组脱髓鞘性神经病,由许多不同基因的突变引起,导致表型重叠。charcot-marie-tooth 1x型(cmt1x)神经病是第二常见的cmt形式(4,5)并且表现为典型的cmt1症状,包括从腿部远端肌肉开始的进行性虚弱和萎缩、跑步困难和经常扭伤脚踝,并且大多数受影响的男性在10岁或更早(6-8)发作。该疾病缓慢进展,导致前腿肌肉无力、足下垂、足部畸形、手部肌肉无力和远端感觉丧失,有时在青春期后期或成年早期出现疼痛性感觉异常,并在整个生命周期中缓慢进展。患有cmt1x的杂合女性可能无症状或在年龄较大时出现较轻的临床表现,但已报告异常严重的神经病变(9,10)。一过性cns表现可能发生在一些,主要是年轻的cmt1x患者中(11)。运动神经传导速度(mncv)的中间减慢(30-40m/s)和由于长度依赖性轴索变性导致的运动单位逐渐丧失是典型的电生理特征(6,7)。神经活检显示混合轴突和脱髓鞘异常(12,13),髓鞘薄,和被再生轴突簇取代的大的有髓纤维损失(6,14)。
[0064]
cx32是通过非致密髓鞘层形成间隙连接(gj)通道的跨膜蛋白,该非致密髓鞘层由外周神经系统(pns)中的髓鞘化雪旺氏细胞以及cns中的少突胶质细胞亚群特异性表达。由cx32形成的gj通道具有重要的稳态和信号传导功能,这些功能对于髓鞘和轴突的功能和存活至关重要(4,5)。编码cx32的相应基因是gjb1。
[0065]
迄今为止,已经报道400多个gjb1突变发生在整个开放阅读框(orf)中,并且许多发生在多于一个家族中,包括:498个错义(71%);3个stop-lost;49个框内indels(7%);25个stop-gained(4%);和122个移码indels(17%)(http://hihg.med.miami.edu/code/http/cmt/public_html/index.html#/)。在非编码gjb1区域也报道几种突变。移码、过早终止和非编码突变可能导致蛋白质合成完全丧失或快速降解,预计不会导致任何显性负效应。体外表达的几种错义和框内突变显示在内质网和/或高尔基体(17-21)中的细胞内滞留(15-17),未能形成功能性通道。有些还对共表达的wt cx32(15)产生显性负效应。其他突变体形成具有改变生物物理特征的功能性通道(19)。完全删除gjb1/cx32基因的cx32敲除(ko)小鼠在大约三个月大时开始出现进行性的、主要是运动性脱髓鞘性周围神经病变,并伴有坐骨mncv和运动幅度降低(24,25)。由大鼠mpz/p0启动子驱动的wt人cx32蛋白的表达阻止cx32 ko小鼠的脱髓鞘(26),证实cx32的施旺细胞自主表达的丧失足以引起cmt1x病理。
[0066]
因此,cmt1x突变体的几项体外和体内研究支持cx32功能丧失主要导致cmt1x神经病变的总体结论(8,17-19,21-23)。因此,在一个实施方案中,使用如本文所述的病毒载体和治疗方法的基因替代疗法用于治疗或预防cmt1x,例如当病毒载体包含编码野生型或治疗上有益的cx32蛋白的第一核酸序列时。
[0067]
在ko背景下具有导致cmt1x的突变的转基因小鼠在175fs突变系中没有显示出可检测的cx32蛋白(27),而r142w、t55i、r75w和n175d转基因小鼠在核周区域显示出突变蛋白的保留,类似于体外模式(上图)并发展类似于cx32 ko小鼠的脱髓鞘神经病变(22、28、29)。在存在高尔基体保留的r142w、r75w和n175d突变体(而不是er保留的t55i突变体)的情况下,内源性小鼠wt cx32的表达降低,表明高尔基体保留的突变体可能对wt cx32具有显著的消极影响。这对于在每个细胞中仅表达一个gjb1等位基因的cmt1x患者没有临床意义,但在计划基因添加治疗时必须考虑。体内表达的突变体对其他共表达的连接蛋白没有任何其他毒性或显性影响(22,28)。c-末端突变体c280g和s281x在cx32 ko小鼠中被正确定位并防止脱髓鞘,尚不清楚它们如何导致人类神经病变(30)。
[0068]
因此,cmt1x也可能是由cx32蛋白中的显性失活突变引起的。在这种情况下,技术人员将理解如果本发明的病毒载体包含被转录成非编码rna的第一核酸是有益的,该非编码rna本身针对突变cx32 mrna以防止突变蛋白的翻译。技术人员将理解如何获得合适的核酸序列,例如,靶向突变的cx32 mrna而不是野生型或治疗上有利的cx32 mrna。这样,在一个实施方案中,受试者可以用病毒载体治疗,该病毒载体包含转录成靶向突变cx32的非编码rna的第一核酸,并且受试者也可以用根据本发明的第二病毒载体治疗,其中所述第二病毒载体包含编码野生型或治疗上有利的cx32蛋白的第二核酸。在一些实施方案中,第一和第二核酸可以在根据本发明的相同病毒载体上。可以在治疗或预防本文所述的任何雪旺细胞相关疾病中采用类似的方法。
[0069]
在一些实施方案中,第一核酸可以是神经病相关基因的野生型基因序列的orf或
cdna。在一些实施方案中,第一核酸可以是间隙连接β1(gjb1)基因的野生型序列的cdna,其被认为具有如seq id no.6中定义的序列。在一些实施方案中,第一核酸具有与seq id no.6至少75%序列同源性或序列同一性,任选地与seq id no.6至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在其他实施方案中,第一核酸具有与gjb1的orf序列至少75%序列同源性或序列同一性,任选地与gjb1的orf序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0070]
cmt1x是由gjb1基因突变引起的,导致野生型功能性cx32蛋白表达不足。因此,在一些实施方案中,本文所述的病毒载体可以用于通过递送gjb1基因的开放阅读框或cdna的野生型拷贝或其他治疗上有益的拷贝来治疗或预防cmt1x。
[0071]
charcot-marie-tooth 4c型(cmt4c)病是一种常染色体隐性遗传性神经病,在整体罕见的cmt4型隐性脱髓鞘性神经病中似乎最为普遍,几乎占所有cmt4病例的一半(35)。cmt4c患者通常在生命的最初十年出现足部畸形和脊柱侧弯、虚弱、反射消失和感觉丧失(36-38)。颅神经受累伴有听力障碍、瞳孔光反射缓慢和舌束颤是常见的,并且已经描述具有相同突变的患者的表型变异(39-41)。cmt4c患者中的电生理研究证实在22.6m/s的平均正中运动神经传导速度(ncv)下脱髓鞘过程。神经活检结果的特征是有髓鞘、脱髓鞘和无髓鞘轴突周围的基底膜增加,洋葱球相对较少,并且最典型的是雪旺细胞的大细胞质延伸(36,37,42)。
[0072]
cmt4c的分子遗传学:连锁分析研究和纯合子作图(43)导致在染色体5q32上发现疾病基因座,随后最初发现sh3tc2基因中的11个不同突变,大部分是截断但也有错义(42)。迄今为止,至少已经描述28种不同的sh3tc2突变,它们可能在某些具有可能创始人效应的种族群体(44)中更常见(39)。完整的转录本cdna长度为3864bp。sh3tc2编码1,288个氨基酸的蛋白质,其包含两个src同源性3(sh3)和10个四三肽重复序列(tpr)结构域,10个四三肽重复序列(tpr)结构域与具有已知功能的任何其他人类蛋白质没有整体显著相似性。sh3和tpr结构域的存在表明sh3tc2可以作为支架蛋白(42)。sh3tc2在脊椎动物物种中非常保守,而没有鉴定出非脊椎动物直向同源物。sh3tc2存在于包括早期和晚期内体的内吞途径的几个组件以及靠近反式高尔基体网络和质膜的网格蛋白包被的囊泡中。这种定位在cmt4c(45)中发生改变。
[0073]
cmt4c的sh3tc2-/-ko小鼠模型出现早发性但进行性周围神经病变,伴有运动和感觉神经传导速度减慢以及早发性髓鞘形成不足(46,47)。这种表型在2个月和12个月大时随着髓鞘病理学的增加而进行。鼠sh3tc2在雪旺氏细胞中特异性表达并定位于质膜和核周内吞循环室,表明在髓鞘形成和/或轴突相互作用区域中的可能功能(48)。突变小鼠外周神经髓鞘的超微结构分析显示ranvier节点的异常组织,这种表型在cmt4c患者的神经活检中得到证实。这些发现表明sh3tc2基因产物在髓鞘形成和ranvier节点完整性中的作用(46)。因此,sh3tc2-/-小鼠概括cmt4c疾病的所有主要特征,并提供测试疗法的相关模型。
[0074]
因此,在一些实施方案中,第一核酸可以是基因sh3结构域和四三肽重复序列2(sh3tc2)基因的野生型序列的orf或cdna。sh3tc2的orf被认为具有如seq id no.7中定义的序列。在一些实施方案中,第一核酸具有与seq id no.7至少75%序列同源性或序列同一性,任选地与seq id no.7至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或
94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在其他实施方案中,第一核酸具有与sh3tc2的cdna序列至少75%序列同源性或序列同一性,任选地与sh3tc2的cdna序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0075]
如上所述,cmt4c是由sh3tc2基因突变引起的,导致野生型功能性sh3tc2蛋白表达不足。因此,在一些实施方案中,本文所述的病毒载体可以用于通过递送sh3tc2的开放阅读框或cdna的野生型拷贝或其他治疗上有益的拷贝来治疗或预防cmt4c,以例如增加野生型sh3tc2的表达。
[0076]
在另一个实施方案中,本文所述的病毒载体可以用于治疗或预防其他类型的常染色体显性脱髓鞘性cmt的方法。
[0077]
cmt1b是由髓鞘蛋白零(mpz)基因突变引起的,导致野生型功能性mpz蛋白表达不足。
[0078]
因此,在一些实施方案中,第一核酸可以是髓鞘蛋白零(mpz)基因的野生型序列的orf或cdna。mpz的orf被认为具有如seq id no.9中定义的序列。在一些实施方案中,第一核酸具有与seq id no.9至少75%序列同源性或序列同一性,任选地与seq id no.9至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在其他实施方案中,第一核酸具有与mpz的cdna序列至少75%序列同源性或序列同一性,任选地与mpz的cdna序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0079]
因此,在一些实施方案中,除了递送mpz基因的开放阅读框或cdna的野生型拷贝或其他治疗上有益的拷贝外,本文所述的病毒载体可以用于通过递送如本文所述的mpz基因的靶向和敲低毒性突变等位基因的非编码rna来治疗或预防cmt1b。
[0080]
cmt1d是由egr2基因突变引起的,导致野生型功能性egr2蛋白表达不足。
[0081]
因此,在一些实施方案中,第一核酸可以是早期生长反应2(egr2)基因的野生型序列的orf或cdna。egr2的orf被认为具有如seq id no.10中定义的序列。在一些实施方案中,第一核酸具有与seq id no.10至少75%序列同源性或序列同一性,任选地与seq id no.10至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在其他实施方案中,第一核酸具有与egr2的cdna序列至少75%序列同源性或序列同一性,任选地与egr2的cdna序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0082]
因此,在一些实施方案中,本文所述的病毒载体可以用于通过递送egr2基因的开放阅读框或cdna的野生型拷贝或其他治疗上有益的拷贝来治疗或预防cmt1d。
[0083]
在另一个实施方案中,本文所述的病毒载体可以用于治疗或预防其他类型的常染色体隐性脱髓鞘性cmt的方法。cmt4a是由gdap1基因突变引起的,导致野生型功能性gdap1蛋白表达不足。
[0084]
因此,在一些实施方案中,第一核酸可以是神经节苷脂诱导分化相关蛋白1(gdap1)基因的野生型序列的orf。gdap1的orf被认为具有如seq id no.11中定义的序列。
在一些实施方案中,第一核酸具有与seq id no.11至少75%序列同源性或序列同一性,任选地与seq id no.11至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在其他实施方案中,第一核酸具有与gdap1的cdna序列至少75%序列同源性或序列同一性,任选地与gdap1的cdna序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0085]
因此,在一些实施方案中,本文所述的病毒载体可以用于通过递送gdap1基因的开放阅读框或cdna的野生型拷贝或其他治疗上有益的拷贝来治疗或预防cmt4a。
[0086]
cmt4d是由ndrg1基因突变引起的,导致野生型功能性ndrg1蛋白表达不足。
[0087]
因此,在一些实施方案中,第一核酸可以是n-myc下游调节1(ndrg1)基因的野生型序列的orf或cdna。ndrg1的orf被认为具有如seq id no.12中定义的序列。在一些实施方案中,第一核酸具有与seq id no.12至少75%序列同源性或序列同一性,任选地与seq id no.12至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在其他实施方案中,第一核酸具有与ndrg1的cdna序列至少75%序列同源性或序列同一性,任选地与ndrg1的cdna序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0088]
因此,在一些实施方案中,本文所述的病毒载体可以用于通过递送ndrg1基因的开放阅读框或cdna的野生型拷贝或其他治疗上有益拷贝来治疗或预防cmt4d。
[0089]
cmt4e是由egr2基因突变引起的,导致野生型功能性egr2蛋白表达不足。
[0090]
因此,在一些实施方案中,第一核酸可以是早期生长反应2(egr2)基因的野生型序列的orf或cdna。egr2的orf被认为具有如seq id no.10中定义的序列。在一些实施方案中,第一核酸具有与seq id no.10至少75%序列同源性或序列同一性,任选地与seq id no.10至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在其他实施方案中,第一核酸具有与egr2的cdna序列至少75%序列同源性或序列同一性,任选地与egr2的cdna序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。
[0091]
因此,在一些实施方案中,本文所述的病毒载体可以用于通过递送egr2基因的开放阅读框或cdna的野生型拷贝或其他治疗上有益的拷贝来治疗或预防cmt4e。
[0092]
易患压力性麻痹(hnpp)的遗传性神经病与pmp22基因突变有关,导致野生型功能性pmp22蛋白表达不足。
[0093]
因此,在一些实施方案中,第一核酸可以是外周髓鞘蛋白22(pmp22)基因的野生型序列的orf或cdna。pmp22的orf被认为具有如seq id no.8中定义的序列。在一些实施方案中,第一核酸具有与seq id no.8至少75%序列同源性或序列同一性,任选地与seq id no.8至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在其他实施方案中,第一核酸具有与pmp22的cdna序列至少75%序列同源性或序列同一性,任选地与pmp22的cdna序列至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或
99%,或100%序列同一性或序列同源性。
[0094]
因此,在一些实施方案中,本文所述的病毒载体可以用于通过递送pmp22基因的开放阅读框或cdna的野生型拷贝或其他治疗上有益的拷贝来治疗或预防hnpp。
[0095]
在另一个实施方案中,第一核酸可以是与脱髓鞘神经病和/或雪旺氏细胞功能障碍相关的另一个基因的orf或cdna。因此,在一些实施方案中,本文所述的病毒载体可以用于通过递送与此类疾病相关的基因的开放阅读框或cdna的野生型拷贝或其他治疗上有益的拷贝来治疗或预防与脱髓鞘神经病和/或雪旺细胞功能障碍相关的疾病。
[0096]
运动神经元病(mnd)(也称为肌萎缩侧索硬化)是尚未完全确定的病因复杂的神经退行性疾病。在一些实施方案中,本文所述的病毒载体可以用于递送编码营养因子(例如脑源性神经营养因子(bdnf)、神经胶质细胞源性神经营养因子(gdnf)、神经营养因子-3(nt-3)、血管内皮生长因子(vegf))。这种营养因子在靶细胞中的表达被认为可以用于再生和拯救受压的运动神经元。
[0097]
因此,在一些实施方案中,本文所述的病毒载体用于治疗或预防mnd的方法。
[0098]
本领域技术人员清楚,本文公开的蛋白质的野生型或治疗上有益形式可以从完整基因的核苷酸序列、仅从开放阅读框序列(orf)或仅从cdna序列表达。所有这些类型的序列都可以由技术人员从序列数据库,例如genbank访问(可在此处访问:https://www.ncbi.nlm.nih.gov/genbank/)。
[0099]
在一些实施方案中,第一多核苷酸编码并翻译成第一多肽或蛋白质。在一些实施方案中,第一多核苷酸编码蛋白质的野生型形式。在一些实施方案中,蛋白质的野生型形式用于替代或补充由有需要的受试者表达的相同蛋白质的突变形式的表达。
[0100]
在一些实施方案中,第一多核苷酸可以编码一种或多种以下蛋白质的野生型或治疗上有益形式:连接蛋白-32(cx32);sh3结构域和四肽重复序列2(sh3tc2);外周髓鞘蛋白22(pmp22);髓鞘蛋白零(mpz);早期生长反应2(egr2);神经节苷脂诱导分化相关蛋白1(gdap1);n-myc下游调节1(ndrg1)。技术人员会理解,本文公开的蛋白质的氨基酸序列可以容易地从序列数据库,例如ncbi蛋白质数据库访问(可在此处访问:https://www.ncbi.nlm.nih.gov/protein)。
[0101]
因此,在一些实施方案中,本发明可以通过提供包含待替换基因的野生型形式或其他治疗上有益形式的aav载体而应用于基因替换方法。在一些非限制性实例中,被替换的基因可以以不编码蛋白质的方式突变,它编码野生型蛋白质的截短形式(例如存在过早终止密码子),它编码减少数量的功能性蛋白质或它编码蛋白质的非功能性突变形式。
[0102]
在附加或备选实施方案中,第一核酸编码并翻译成营养因子(例如脑源性神经营养因子(bdnf)、神经胶质细胞源性神经营养因子(gdnf)、神经营养因子-3(nt-3)、血管内皮生长因子(vegf))。通过营养因子,我们包括支持发育中和成熟神经元的生长、分化和/或发育的生物分子(例如蛋白质或肽)。在另一个附加或备选实施方案中,第一多核苷酸编码再生因子(例如血管生成素、oct-6、egr2、sox-10)。在另一个附加或备选实施方案中,第一多核苷酸编码生长因子(例如igf)。
[0103]
在一些实施方案中,使用本文所述的载体递送编码上述营养因子、再生因子和/或生长因子的核酸可以用于治疗或预防获得性周围神经疾病。在一个实施例中,可以通过将编码营养因子和/或生长因子的如本文所述的载体递送到雪旺细胞和轴突来治疗糖尿病和
其他毒性外周神经病。在另一个实施例中,运动神经元疾病(mnd)(也称为肌萎缩侧索硬化)可以通过递送如本文所述的编码营养因子的载体来治疗,所述营养因子可递送到受压运动神经元的轴突以追溯保存所述运动神经元。
[0104]
在另一个实施方案中,包含编码第一蛋白质或多肽的第一核酸的病毒载体的施用导致雪旺细胞功能改进和/或髓鞘形成增加。在一些实施方案中,当与治疗前受试者中雪旺细胞形成髓鞘时相比,通过雪旺细胞形成髓鞘的增加实现这种功能改进,并且可以经由检测增加的髓鞘产生来检测功能的改进。在一些实施方案中,与治疗前受试者的这些测量相比,功能的改进可以通过肌肉力量的改进和/或坐骨神经传导速度的改进和/或血液生物标志物的潜在反应的变化来测量。技术人员知道确定雪旺细胞功能改进和/或髓鞘形成增加的技术。在实施例中提供一些此类技术。
[0105]
在一些具体的实施方案中,雪旺细胞增加的髓鞘形成导致周围神经的髓鞘形成改进。外周神经髓鞘形成的改进是指与治疗前的受试者相比外周神经的髓鞘形成增加。这包括脱髓鞘和再髓鞘纤维的减少和/或异常有髓鞘纤维的减少。在一些实施方案中,改进的髓鞘形成也可能与泡沫巨噬细胞数量的减少有关,泡沫巨噬细胞是炎症的标志物。髓鞘形成的改进也可能与髓鞘厚度增加和g比值降低(轴突直径除以有髓纤维直径)有关。
[0106]
如上所述,第一核酸可编码具有治疗益处的多肽或蛋白质,例如当天然蛋白质突变或以太低而无法产生正常功能的水平表达时。
[0107]
应当理解,在备选实施方案中,第一核酸可以转录成不是mrna的rna,即不是翻译成蛋白质的rna。因此,第一核酸可以转录成非编码rna。
[0108]“非编码rna”是指未翻译成多肽或蛋白质的任何rna分子。技术人员将了解此类rna聚合物以及如何使用它们来影响多肽的表达。在一个实施方案中,第一核酸被转录成非编码微rna(mir)。在另一个其他备选实施方案中,第一核酸被转录成短发夹rna(shrna)。在另一个实施方案中,第一核酸被转录成引导rna(grna),例如作为基于crispr的系统的一部分。
[0109]
当病毒载体在靶生物体中时,上述非编码rna的表达可导致靶多核苷酸的表达降低,任选地其中靶多核苷酸是位于靶生物体中的基因,任选地其中它位于靶生物体中的细胞中。在一些实施方案中,靶多核苷酸是基因序列。因此,在一些实施方案中,本文所述的发明可以用于敲低靶基因的表达。“敲低”是指靶基因的表达与病毒载体处理前的表达水平相比降低。
[0110]
例如,本发明可应用于靶核酸,例如靶基因,过表达的情况。病毒载体可以用于递送被转录成非编码rna的第一核酸,例如以靶向由过度表达的基因产生的mrna进行降解(例如通过risc复合物,这很好本领域已知的)或直接阻断所述mrna翻译成蛋白质。本发明的实施方案也适用于靶核酸自身转录为非编码rna的情况,有利于降低细胞内宿主非编码rna的水平。
[0111]
本发明的该实施方案还可以用于靶向有害的功能获得突变体并降低它们的蛋白质或mrna表达水平。
[0112]
因此,在一些实施方案中,非编码rna的表达导致靶核酸、多核苷酸或基因的表达减少。在一个实施方案中,靶生物体中靶多核苷酸的表达或过表达被认为与与雪旺细胞相关的疾病有关,任选地其中所述疾病是显性脱髓鞘神经病(cmt1),任选地其中损失靶多核
苷酸是突变的等位基因髓鞘蛋白零(mpz/p0)并且雪旺氏细胞相关疾病为cmt1b,或其中靶多核苷酸为与cmt1相关的另一种显性基因。
[0113]
在一些实施方案中,编码第一核酸的病毒载体的施用导致非编码rna的表达,其导致雪旺细胞功能的改进。如上所述,在一些实施方案中,与治疗前受试者的雪旺细胞形成髓鞘相比,通过雪旺细胞形成髓鞘的增加来实现这种功能改进。在一些实施方案中,当与治疗前受试者中的这些测量值相比时,可以通过肌肉力量的改进和/或坐骨神经传导速度的改进和/或血液生物标志物的潜在反应的变化来测量这种功能改进。
[0114]
在一些实施方案中,本文所述的病毒载体包含编码第一多肽或蛋白质的第一核酸序列,并且该载体还可包含被转录成非编码rna的第二核酸。因此,本发明可以用于一些实施方案以使用非编码rna敲低突变基因的表达,并且还用所述基因的野生型拷贝替换突变基因,导致完全的基因替换。当需要治疗的受试者在特定蛋白质中具有功能获得突变时,认为该方法特别有用。
[0115]
在一些实施方案中,病毒载体还包含编码转录因子的第二或第三核酸序列,所述转录因子能够驱动来自雪旺细胞特异性启动子,任选地如本文定义的髓鞘特异性启动子或最小髓鞘特异性启动子的表达或表达增加。可以在雪旺细胞特异性启动子控制下驱动多核苷酸表达的此类转录因子的实例包括egr2和sox10。
[0116]
病毒载体还可包含编码在crispr技术及其变体中常规使用的cas9多肽或类似物的核酸序列,例如死cas9。
[0117]
应当理解,本文所述的病毒载体可以多种方式施用到受试者。在一个优选的实施方案中,本文所述的病毒载体通过鞘内注射施用。通过“鞘内注射”,我们包括注射到椎管内,这导致注射的物质到达脑脊液(csf)。在一个特别优选的实施方案中,本文所述的病毒载体通过腰椎鞘内注射施用。本文所述的病毒载体也适用于胸腔鞘内注射或宫颈鞘内注射施用。或者,本文所述的病毒载体可以通过直接注射到外周神经中来施用。或者,本文所述的病毒载体可以通过直接静脉内注射施用。
[0118]
鞘内注射优于其他施用方法,例如神经内和静脉内注射。与神经内注射相比,鞘内注射为多个脊髓根和神经提供更广泛的分布。相比之下,神经内注射仅在注射的神经内提供分布。另外,鞘内注射在临床上可以常规进行,不需要手术并且被认为是安全的,而神经内注射则需要手术,并且暴露多根神经,风险较高,因此在临床上转移难度更大。
[0119]
虽然静脉注射在临床上更容易施用,但与鞘内施用相比,它的缺点是需要更高剂量的载体才能到达神经系统。由于更高剂量的病毒和肝毒性风险,静脉施用也可能导致更大的毒性。此外,静脉注射可能会引起更多的免疫反应,而鞘内施用提供逃避免疫系统较低免疫反应的可能性。
[0120]
一旦本文所述的aav载体转导靶细胞,所递送的遗传材料保持稳定和游离,前提是靶细胞已分化且未分裂,如成熟雪旺细胞是这种情况。因此,aav载体的单次施用应该足以达到治疗效果,并且在一些实施方案中,本文所述的病毒载体通过单次鞘内注射施用。然而,在某些情况下,可能需要在不同的时间点向受试者施用多剂不同的aav载体。这些不同的载体可以表达不同的第一多核苷酸,或可以表达相同的第一多核苷酸并且所使用的aav类型不同。因此,在一些实施方案中,本文公开的病毒载体可以用于治疗或预防与多个不同基因相关的雪旺细胞相关疾病。
[0121]
应当理解,本文公开的病毒载体适用于人类受试者。病毒载体也适用于一般哺乳动物,例如:猫、狗、小鼠、兔、马。可以在与雪旺细胞相关的疾病的症状出现之前或在所述疾病的症状出现之后用本文公开的病毒载体治疗受试者。待治疗的受试者可以是治疗开始时的任何年龄。例如,一旦确认受试者具有损害雪旺细胞性能的突变或其他缺陷,就可以用本发明的载体治疗受试者。这可能是在出现任何症状之前。
[0122]
应当理解,所用病毒载体的剂量将根据有需要的受试者的需要进行调节,例如可以根据受试者的年龄、体重或身高进行调节。作为一般示例,可以使用3.5x 10
13
载体基因组(vg)、3.3倍高剂量1.2x 10
14
vg和5倍高剂量1.8x 10
14
vg的递增剂量的剂量(用于鞘内递送)。这些剂量以前曾在使用aav的临床试验中使用过(例如https://clinicaltrials.gov/ct2/show/nct02362438),并且技术人员将意识到它们可以应用于本发明。
[0123]
本领域技术人员清楚,除了预防或治疗与雪旺细胞相关疾病的治疗方法外,本发明还提供病毒载体本身。因此,另一方面,本发明提供如本文所述的病毒载体,其包含如本文定义的核酸序列。在一个优选的实施方案中,病毒载体是aav。在一个特别优选的实施方案中,aav是aav9。该方面特征的偏好如本说明书别处所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0124]
另一方面,本发明提供包含如seq id no.5中定义的序列或由如seq id no.5中定义的序列组成的最小髓鞘特异性启动子,或具有与seq id no.5至少75%序列同源性或序列同一性的序列,任选地与seq id no.5至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列。该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0125]
另一方面,本发明提供包含如seq id no.22中定义的序列或由如seq id no.22中定义的序列组成的最小髓鞘特异性启动子,或具有与seq id no.22至少75%序列同源性或序列同一性的序列,任选地与seq id no.22至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列。该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。在一些实施方案中,本发明提供人最小髓鞘特异性启动子,其中所述人最小髓鞘特异性启动子具有与seq id no.22至少75%、80%,或82%,或84%,或86%,或88%序列同源性,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同源性或序列同源性的序列。
[0126]
另一方面,本发明提供包含第一核酸序列的多核苷酸构建体,所述第一核酸序列是雪旺细胞特异性启动子,任选地为髓鞘特异性启动子,任选地包含如本文定义的髓鞘蛋白零(mpz)启动子或最小髓鞘特异性启动子,可操作地连接到转录成第一多核苷酸的第二核酸序列,其中所述第二核酸:
[0127]
a)是基因的开放阅读框或cdna或其他元件;或b)转录为非编码rna。
[0128]
本发明还提供包含这种多核苷酸构建体的病毒载体,例如提供包含该构建体的aav载体。该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。例如,在一个实施方案中,本发明的多核苷酸构建体包含雪旺细胞特异性启动子,其中所述启动子是a)最小雪旺细胞特异性启动子,任选地如本文所述的最小
mpz启动子,例如其中所述启动子具有与seq id no.5或seq id no.22至少75%、80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同源性或序列同一性的序列;或b)全长mpz启动子,任选地其中所述启动子具有与seq id no.4或seq id no.18至少75%、80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同源性或序列同一性的序列。
[0129]
优选地,本发明的多核苷酸构建体包含如本文所述的人最小mpz或人全长mpz启动子。
[0130]
另一方面,本发明提供以下病毒载体:
[0131]
a)包含aav9载体、髓鞘蛋白零(mpz)启动子和egfp报告基因(seq id no.1)的aav-mpz.egfp载体,任选地其中所述启动子具有与seq id no.4或seq id no.18至少75%、80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同源性或序列同一性的序列;
[0132]
b)包含aav9载体、髓鞘蛋白零(mpz)启动子和间隙连接β1(gjb1)基因(seq id no.2)的开放阅读框(orf)的aav9-mpz-gjb1载体,任选地其中所述启动子具有与seq id no.4或seq id no.18至少75%、80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同源性或序列同一性的序列;
[0133]
c)包含aav9载体、最小髓鞘蛋白零(minimpz)启动子和egfp报告基因(seq id no.3)的aav9-minimpz.egfp载体,任选地其中所述minimpz启动子具有与seq id no.5或seq id no.22至少75%、80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同源性或序列同一性的序列;
[0134]
d)包含aav9载体、人髓鞘蛋白零(hp0)启动子和间隙连接β1(gjb1)基因(seq id no.17)的开放阅读框(orf)的aav9-人mpz-gjb1载体;
[0135]
e)包含aav9载体、人髓鞘蛋白零(hp0)启动子和egfp报告基因(seq id no.19)的aav9-人mpz-egfp载体;
[0136]
f)包含aav9载体、最小髓鞘蛋白零(mpz)启动子和sh3tc2基因(seq id no.20)的开放阅读框(orf)的aav9-minimpz-sh3tc2.myc.itr载体;
[0137]
g)包含aav9载体、人最小髓鞘蛋白零(hp0)启动子和sh3tc2基因(seq id no.21)的开放阅读框(orf)的aav9-human-minimpz-sh3tc2载体
[0138]
h)包含aav9载体、人最小髓鞘蛋白零(hp0)启动子和egfp报告基因(seq id no.23)的aav9-human-minimpz-egfp载体;或i)aav,任选地其中所述aav载体是aav9;该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0139]
在一个具体实施方案中,本发明还提供一种用于在有需要的受试者中治疗或预防与雪旺细胞相关的疾病的病毒载体,其中所述病毒载体包含转录成第一多核苷酸的第一核酸序列,并且其中所述第一核酸的转录在最小髓鞘特异性启动子的控制下,该启动子任选地包含由seq id no.5或seq id no.22中定义的序列或由seq id no.5或seq id no.22中定义的序列组成或具有与seq id no.5或22至少75%序列同源性或序列同一性,任选地与seq id no.5或22至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或
96%,或97%,或98%,或99%,或100%序列同一性或序列同源性。在一个实施方案中,病毒载体可以是aav载体。在另一个备选实施方案中,病毒载体可以是慢病毒载体。该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0140]
另一方面,本发明还提供包含本文所述的任何病毒载体的药物组合物。在一些实施方案中,药物组合物包含适量的病毒载体,并进一步包含药学上可接受的赋形剂、稀释剂、载体、缓冲剂或佐剂。该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0141]
如本文所用,“药物组合物”是指用于治疗或预防与雪旺细胞相关的疾病的治疗有效制剂。
[0142]
药物组合物可以以本领域已知的具有足够的储存稳定性并且适合施用到人的方式制备。
[0143]
关于“药学上可接受的”,我们意指不降低活性成分例如病毒载体的生物活性的效果的无毒材料。此类药学上可接受的载体或赋形剂是本领域众所周知的(参见《雷明顿药物科学(remington's pharmaceutical sciences)》,第18版,编者:a.r gennaro,麦克出版公司(mack publishing company)(1990)和《药物赋形剂手册(handbook of pharmaceutical excipients)》,第3版,编者:a.kibbe,药物出版公司(pharmaceutical press)(2000),其公开内容通过引用并入本文)。
[0144]
术语“缓冲剂”旨在表示含有酸-碱混合物的水溶液,目的是稳定ph。缓冲液的实例为氨基丁三醇(trizma)、二甘氨酸(bicine)、麦黄酮(tricine)、mops、mopso、mobs、三羟甲基氨基甲烷(tris)、hepes、hepbs、mes、磷酸盐、碳酸盐、乙酸盐、柠檬酸盐、乙醇酸盐、乳酸盐、硼酸盐、aces、ada、酒石酸盐、amp、ampd、ampso、bes、cabs、二甲胂酸盐、ches、dipso、epps、乙醇胺、甘氨酸、heppso、咪唑、咪唑乳酸、pipes、ssc、sspe、popso、taps、tabs、tapso和tes。
[0145]
术语“稀释剂”旨在表示水溶液或非水溶液,目的是稀释药物制剂中的病毒载体。稀释剂可以是盐水、水、聚乙二醇、丙二醇、乙醇或油(如红花油、玉米油、花生油、棉籽油或芝麻油)中的一种或多种。
[0146]
术语“佐剂”旨在表示加到制剂以增加病毒载体的生物学效应的任何化合物。佐剂可以是具有不同阴离子的胶态银,或锌、铜或银盐中的一种或多种,例如但不限于氟化物、氯化物、溴化物、碘化物、硫氰酸盐、亚硫酸盐、氢氧化物、磷酸盐、碳酸盐、乳酸盐、羟乙酸盐、柠檬酸盐、硼酸盐、酒石酸盐和不同酰基组合物的乙酸盐。佐剂也可以是阳离子聚合物,如phmb、阳离子纤维素醚、阳离子纤维素酯、脱乙酰化透明质酸、壳聚糖、阳离子树枝状聚合物、阳离子合成聚合物(如聚(乙烯基咪唑))和阳离子多肽(如聚组氨酸、聚赖氨酸、聚精氨酸)和含有这些氨基酸的肽。
[0147]
赋形剂可以是碳水化合物、聚合物、脂质和矿物质中的一种或多种。碳水化合物的实例包含乳糖、蔗糖、甘露醇和环状糊精,它们被加到该组合物中,例如用于促进冷冻干燥。聚合物的实例是淀粉、纤维素醚、纤维素、羧甲基纤维素、羟丙基甲基纤维素、羟乙基纤维素、乙基羟乙基纤维素、乙基纤维素、甲基纤维素、丙基纤维素、褐藻酸盐、角叉菜胶、透明质酸和其衍生物、聚丙烯酸、聚磺酸盐、聚乙二醇/聚环氧乙烷、聚环氧乙烷/聚环氧丙烷共聚物、不同水解度的聚乙烯醇/聚乙酸乙烯酯、聚(乳酸)、聚(乙醇酸)或其具有各种组成的共
聚物,和聚乙烯吡咯烷酮,其分子量都不同,这些聚合物被加到组合物中,例如用于粘度控制、用于实现生物粘附或用于保护活性成分免于化学和蛋白水解降解。脂质的实例是脂肪酸、磷脂、甘油单酯、甘油二酯和甘油三酯、神经酰胺、鞘脂和糖脂,其酰基链长度和饱和度都不同,蛋卵磷脂、大豆卵磷脂、氢化蛋卵磷脂和大豆卵磷脂,其出于与聚合物类似的原因被加到组合物中。矿物质的实例是滑石、氧化镁、氧化锌和氧化钛,其被加到组合物中以获得益处,如减少液体积聚或有利的颜料性质。
[0148]
另一方面,本发明提供如本文所述的病毒载体在制备用于治疗或预防与雪旺细胞相关的疾病的药物的方法中的用途。在一些实施方案中,疾病引起雪旺氏细胞破坏和/或髓鞘形成减少。在一个优选的实施方案中,该疾病是charcot-marie-tooth疾病。该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0149]
另一方面,本发明提供使用本文所述的任何病毒载体治疗或预防与雪旺细胞相关的疾病的方法。在一个具体的实施方案中,本发明提供治疗或预防charcot-marie-tooth疾病的方法。在一个优选的实施方案中,该疾病是charcot-marie-tooth疾病1x型或4c型。该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0150]
技术人员将理解,本文所述的病毒载体可以用于crispr/cas系统以用于基因编辑或基因沉默,例如通过使用死cas9多肽。因此,另一方面,本发明包括如本文所述的用于crispr/cas9系统的病毒载体或多核苷酸构建体,其包含以下任何一个或多个:
[0151]
a)编码靶向目标基因的单一引导rna(sgrna)的多核苷酸;
[0152]
b)编码cas9多肽的多核苷酸;
[0153]
c)编码目标多肽的多核苷酸。
[0154]
该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0155]
本领域技术人员清楚,本文公开的病毒载体除了用于治疗或预防与雪旺细胞相关的疾病外,还可具有多种用途。例如,本文公开的病毒载体可以用于标记雪旺氏细胞的方法,例如用荧光蛋白,例如绿色荧光蛋白(gfp)或增强型绿色荧光蛋白(egfp),或用其他非荧光报告基因。在一些实例中,雪旺细胞的标记可以用于诊断与雪旺细胞相关的疾病的方法中。
[0156]
该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0157]
在另一个实施例中,本文公开的病毒载体可以用于诱导雪旺细胞分化成替代细胞类型,例如神经元、少突胶质细胞或星形胶质细胞的方法。
[0158]
在又一个实施例中,本文公开的病毒载体可以用于刺激雪旺细胞以支持有需要的受试者的再生,例如在受伤或外伤后。该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾病的偏好如本文定义。
[0159]
在又一个实施例中,本文公开的病毒载体可适用于治疗与雪旺细胞相关的疾病的离体方法。例如,靶细胞可以从需要治疗的受试者中取出,并在重新引入受试者之前用本文所述的病毒载体转导。
[0160]
该方面特征的偏好如本说明书中所述,例如载体、核酸、启动子、雪旺细胞相关疾
病的偏好如本文定义。
[0161]
本发明还提供已被本发明的病毒载体转导的细胞,例如雪旺细胞。
[0162]
本发明还提供包含本发明的核酸构建体的细胞,所述核酸构建体包含相关启动子和第一核酸。技术人员会知道本发明的病毒载体可以在培养细胞中产生,优选hek293细胞,例如如(58)中所述。
[0163]
应当理解,本文所述的载体和方法可以在体内进行,但也可以在离体或体外使用,例如可以在体外或离体转导诸如雪旺氏细胞的细胞用于随后的治疗或研究目的。
[0164]
本发明还提供可以用于实施本文所述的任何病毒载体的试剂盒。例如,本发明提供用于与前述权利要求中任一项所述的病毒载体或多核苷酸一起使用的试剂盒,其中所述试剂盒包含以下中的一个或多个:
[0165]
a)如本文定义的病毒载体;
[0166]
b)如本文定义的多核苷酸构建体;
[0167]
c)病毒载体;
[0168]
d)包含本文定义的多核苷酸构建体的病毒载体;
[0169]
e)药学上可接受的载体和/或赋形剂;
[0170]
f)一次性注射器,例如适用于腰椎鞘内注射的一次性注射器;
[0171]
g)使用说明。
[0172]
在一个实施方案中,试剂盒包含多于一种根据本发明的病毒载体,例如试剂盒可以包含两种不同的如本文定义的病毒载体。
[0173]
本领域技术人员将清楚,在本发明的任何治疗用途中,可以向受试者施用多于一种根据本发明的病毒载体。技术人员清楚,在某些情况下这是有利的,例如如果已知多于一个基因与雪旺细胞相关疾病相关,则可以施用多种病毒载体,每种载体针对表达不同的治疗蛋白质。或者,单个载体可以表达多于一种治疗性蛋白质或非编码rna。在其他情况下,例如上述那些情况,可以使用一种病毒载体在雪旺细胞中表达例如cas9蛋白,并且可以使用不同的病毒载体来表达相关的grna以将cas9靶向所需的核酸。
[0174]
本说明书中对显然在前公开的文件的列举或讨论不应必然地被视为是承认所述文件是现有技术的一部分或是公知常识。
[0175]
除非上下文另外指示,否则本发明的给定方面、特征或参数的偏好和选项应该被视为已经与本发明的所有其它方面、特征和参数的任何和所有偏好和选项结合而进行了公开。
[0176]
因此,并且为了举例说明本发明的一个方面的公开内容如何与本发明的其他方面相关,并展示这些方面可以如何组合,在一些实施方案中,本发明提供:
[0177]
一种用于治疗或预防与雪旺细胞相关疾病的病毒载体,其中所述病毒载体是aav,并且其中所述病毒载体包含可转录成第一多核苷酸的第一核酸,其中所述第一多核苷酸的表达是在最小髓鞘特异性(mpz)启动子的控制下;
[0178]
一种用于治疗或预防与雪旺细胞相关疾病的病毒载体,其中所述病毒载体是aav,并且其中所述病毒载体包含可转录成第一多核苷酸的第一核酸,其中所述第一多核苷酸的表达是在a)髓鞘蛋白零(mpz)启动子的控制下,任选地其中所述启动子具有与seq id no.4或seq id no.1至少75%、80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,
或96%,或97%,或98%,或99%,或100%序列同源性或序列同一性的序列;或b)最小髓鞘特异性启动子(minimpz),任选地包含seq id no.5或seq id no.22中定义的序列或由seq id no.中定义的序列或由seq id no.5或seq id no.22中定义的序列组成,任选地其中minimpz启动子具有与seq id no.5或seq id no.22至少75%、80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同源性或序列同一性的序列;
[0179]
包含第一核酸序列的多核苷酸构建体,该第一核酸序列是与第二核酸序列可操作地连接的最小髓鞘特异性(mpz)启动子,其中所述第二核酸序列是基因序列的开放阅读框或编码非编码rna;
[0180]
最小髓鞘特异性(mpz)启动子,其可在雪旺细胞中驱动高水平表达并适用于本文所述的病毒载体。
[0181]
本发明还提供:
[0182]
一种用于治疗或预防cmt1x的病毒载体,其中所述载体包含与gjb1基因有效连接的人mpz启动子(根据seq id no:18),其中所述病毒载体是aav9;
[0183]
病毒载体在制备用于治疗或预防cmt1x的药物的方法中的用途,其中所述载体包含与gjb1基因可操作连接的人mpz启动子(根据seq id no:18),其中所述病毒载体是aav9;和
[0184]
一种治疗或预防cmt1x的方法,其中所述方法包括向有需要的患者施用病毒载体,其中所述病毒载体包含与gjb1基因可操作连接的人mpz启动子(根据seq id no:18),并且其中所述病毒载体是aav9。
[0185]
本发明还提供:
[0186]
一种用于治疗或预防cmt4c的病毒载体,其中所述载体包含与sh3tc2基因有效连接的人最小mpz启动子(根据seq id no:22),其中所述病毒载体是aav9;
[0187]
病毒载体在制备用于治疗预防cmt4c的药物的方法中的用途,其中所述载体包含与sh3tc2基因可操作连接的人mpz启动子(根据seq id no:22),其中所述病毒载体是aav9;和
[0188]
一种治疗或预防cmt4c的方法,其中所述方法包括向有需要的患者施用病毒载体,其中所述病毒载体包含可操作地连接到sh3tc2基因的人mpz启动子(根据seq id no:22),并且其中所述病毒载体是aav9。
[0189]
有需要的患者包括已表现出症状或以其他方式接受本文公开的疾病之一的诊断的患者,还包括怀疑患有或将发展本文公开的疾病之一的患者。
附图说明
[0190]
图1:为雪旺细胞靶向基因表达生成的aav载体转移质粒:paav-mbz.gjb1载体包含表达cx32(完整)的人类gjb1开放阅读框和表达报告基因egfp(模拟)的paav-mpz.egfp。
[0191]
图2:aav9介导的雪旺细胞靶向基因表达。a-d:在2个月大的野生型(wt)小鼠中腰椎鞘内(i.th.)注射aav9-mpz-egfp载体后4周,用egfp抗体(a2,b)对腰椎根切片(ab)进行免疫染色显示在低(左)和高(右)放大倍数下雪旺细胞亚群中的核周表达(星号)。egfp表达也可见于在没有抗体染色(c2)的情况下低放大倍数的坐骨神经切片中,和在用egfp抗体免
疫染色(d2)的梳理坐骨神经纤维的更高放大倍数。a1、c1和d1仅显示a2、c2、d2中显示的相同区域的dapi核染色。e:腰椎根和坐骨神经中egfp阳性雪旺细胞比率的量化。f:腰椎根、坐骨神经近端和远端部分的载体拷贝数(vcn)表明鞘内注射后载体向周围神经的生物分布梯度。g:来自不同小鼠(1-4)的腰椎根(lr)、股神经(fn)和坐骨神经(sn)裂解物的免疫印迹分析显示,与来自转基因样品的阳性对照(+)相对应的注射小鼠的大部分组织中存在特异性egfp特异性条带,而它在阴性(-)对照中不存在(kagiava等人,未发表)。
[0192]
图3:鞘内递送aav9-mpz.gjb1载体在2个月cx32 ko和r75wko小鼠中的表达。a.相关组织中的载体拷贝数(vcn)。wt(b)和cx32 ko(c)坐骨神经纤维的免疫染色表明,cx32位于wt纤维(箭头)的副结节髓鞘区域,而cx32 ko中不存在这种定位。尽管在核周区域(星号和空心箭头)中存在r75w突变体,aav9-mpz.gjb1i.th.注射导致偏节点cx32表达不仅在cx32 ko坐骨纤维(d)中,还在r75wko纤维(e)中。f:腰椎根和坐骨神经样本中cx32表达的蛋白质印迹分析(tg+:转基因阳性;ko:未经治疗的cx32 ko阴性对照)(kagiava等人,未发表)。
[0193]
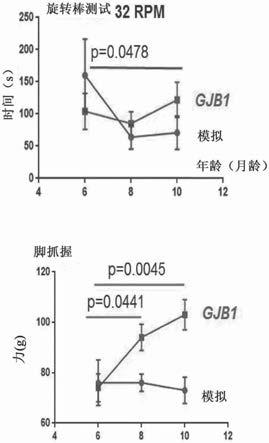
图4:与aav9-mpz.egfp(模拟)治疗的同窝小鼠相比,在6个月大的cx32 ko小鼠发病后注射aav9-mpz.gjb1(完整)的行为分析。如图所示,与模拟治疗的cx32 ko小鼠相比,aav9-mpz.gjb1处理(gjb1)中运动性能的旋转杆(左)和足部抓握(右)测试结果。每组的时间过程分析显示,在注射后2个月(8个月大)的旋转杆和足部抓握分析中,完整治疗的cx32 ko小鼠的运动性能得到改进,然后运动性能保持稳定,直至10个月大。相比之下,如这两种行为测试都表明,模拟治疗的小鼠并没有随着时间的推移而改进。
[0194]
图5:坐骨神经运动传导研究的结果。与注射模拟载体的同窝小鼠相比,10个月大的完整治疗的cx32 ko小鼠的运动神经传导速度(mncv)得到改进,接近wt的值。
[0195]
图6:与模拟治疗的小鼠载体相比,aav9-mpz.gjb1发病后鞘内递送后cx32 ko小鼠前脊髓根的形态学分析。在10个月大(治疗后4个月)下,在低(a-b)和更高(c-d)放大倍数下连接到脊髓的前腰椎脊髓根的半薄切片的代表性图像,以及模拟或完整(gjb1)载体治疗的小鼠的形态测量分析结果(e-f),如图所示。aav9-mpz.gjb1注射的小鼠根(b,d)显示出与模拟治疗的同窝仔(a,c)的根相比有更好的髓鞘形成,脱髓鞘(*)和髓鞘再生(r)纤维较少。对多根中异常有髓纤维的比率进行量化证实,与模拟载体治疗的同窝仔猪相比,完整治疗的异常有髓纤维(e)的数量显著改进,并且泡沫巨噬细胞(f)的数量显著减少。
[0196]
图7:aav9-mpz.gjb1载体发病后鞘内递送后cx32 ko小鼠坐骨神经的形态学分析。在10个月大(治疗后4个月)下,在低(a-b)和更高(c-d)放大倍数下的坐骨神经半薄切片的代表性图像,以及模拟或完整(gjb1)载体治疗的小鼠的形态测量分析结果(e-f),如图所示。aav9-mpz.gjb1注射的小鼠神经(b、d)与模拟治疗的同窝仔(a、c)的神经相比显示改进的髓鞘形成,脱髓鞘(*)和髓鞘再生(r)纤维较少。对多根神经中异常有髓纤维的比率进行量化证实,与模拟载体治疗的同窝仔畜相比,完整治疗的异常有髓纤维(e)的数量显著改进,泡沫巨噬细胞(f)的数量显著减少。
[0197]
图8:aav9-mpz.gjb1载体发病后鞘内递送后cx32 ko小鼠股神经的形态学分析。在10个月大(4个月)治疗后)下,在低(a-b)和高(c-d)放大倍数下股神经半薄切片的代表性图像,以及模拟或完整(gjb1)载体处理小鼠的形态测量分析结果(ef),如图所示。aav9-mpz.gjb1注射的小鼠神经(b、d)与模拟治疗的同窝仔(a、c)的神经相比显示改进的髓鞘形
成,脱髓鞘(*)和髓鞘再生(r)纤维较少。对多根神经中异常有髓纤维的比率进行量化证实,与模拟载体治疗的同窝仔畜相比,完整治疗的异常有髓纤维(e)的数量显著改进,泡沫巨噬细胞(f)的数量显著减少。
[0198]
图9:在pcr扩增来自1127bp全长大鼠mpz启动子的410bp序列后,将minimpz-egfp构建体克隆到aav转移质粒中。
[0199]
图10:在具有egfp抗体的2个月大wt小鼠中腰椎鞘内注射aav9-minimpz-egfp载体后4周腰椎根和坐骨神经纵向切片免疫染色显示雪旺细胞亚群中的核周表达(a、c)。b和c是阴性对照,仅显示dapi的核染色。e:egfp阳性雪旺细胞的百分比(n=5-6只小鼠)。f:腰椎根和坐骨神经中的载体拷贝数证明鞘内注射后载体的充分生物分布(n=6只小鼠)。
[0200]
图11:aav9-minimpz-egfp载体的最小cns表达。在2个月大的wt小鼠中腰椎鞘内用egfp抗体结合细胞标记neun(a,标记神经元),gfap(b,标记星形胶质细胞),cc-1(c-d,标记少突胶质细胞)注射aav9-minimpz-egfp载体后4周腰脊髓纵向切片的免疫染色显示每种细胞类型只有少数细胞表达egfp(通过箭头表示的实例),而大多数是egfp阴性的(通过用空心箭头表示的实例)。e.每个细胞标记染色在n=3-5只小鼠中的量化显示在所有三种cns细胞类型中的表达率低,为约2-3%。
[0201]
图12:在2个月大时用完整治疗(aav9-mpz-gjb1)载体或模拟载体(aav9-mpz-egfp)在发作前治疗的cx32 ko小鼠(cmt1x模型)组的运动行为测试。在治疗前(2个月大)和4(图12a)和6(图12b)个月大时进行足部抓握强度测试。在治疗组中在4个月和6个月时存在显著的功能改进。图12c显示治疗后随时间的显著改进,而模拟治疗的小鼠没有显示任何改进。
[0202]
图13:发作前治疗(完整)和模拟治疗的6个月大cx32 ko小鼠的电生理研究。在6个月大时进行坐骨运动神经传导研究,与模拟治疗相比,在2个月大时,基因治疗治疗后坐骨神经传导速度显著改进。
[0203]
图14:6个月大的cx32 ko小鼠在2个月大时用完整治疗(aav9-mpz-gjb1)载体或模拟载体(aav9-mpz-egfp)进行发作前治疗后的前(运动)腰椎前根的形态学分析。前(运动)腰椎根半薄切片的代表性图像。aav9-mpz-gjb1治疗的小鼠(b,d)与模拟治疗的小鼠(a,c)相比显示出改进的髓鞘形成,具有较少的脱髓鞘(*)和再髓鞘(r)纤维。如通过定量分析(e,f)证实,与模拟治疗的小鼠相比,在治疗的小鼠中发现更少的脱髓鞘(*)或再髓鞘化(r)纤维(e)和更少的泡沫巨噬细胞(f)。
[0204]
图15:6个月大的cx32 ko小鼠在2个月大时用完整治疗(aav9-mpz-gjb1)载体或模拟载体(aav9-mpz-egfp)进行发作前治疗后的中坐骨神经形态学分析。中坐骨神经半薄切片的代表性图像。aav9-mpz-gjb1治疗的小鼠(b,d)与模拟治疗的小鼠(a,c)相比显示出改进的髓鞘形成,具有较少的脱髓鞘(*)和再髓鞘(r)纤维。如通过定量分析(e,f)证实,与模拟治疗的小鼠相比,在治疗的小鼠中发现更少的脱髓鞘(*)或再髓鞘化(r)纤维(e)和更少的泡沫巨噬细胞(f)。
[0205]
图16:6个月大的cx32 ko小鼠在2个月大时用完整治疗(aav9-mpz-gjb1)载体或模拟载体(aav9-mpz-egfp)进行发作前治疗后股骨运动神经的形态学分析。股骨运动神经半薄切片的代表性图像。aav9-mpz-gjb1治疗的小鼠(b,d)与模拟治疗的小鼠(a,c)相比显示出改进的髓鞘形成,具有较少的脱髓鞘(*)和再髓鞘(r)纤维。如通过定量分析(e,f)证实,
与模拟治疗的小鼠相比,在治疗的小鼠中发现更少的脱髓鞘(*)或再髓鞘化(r)纤维(e)和更少的泡沫巨噬细胞(f)。
[0206]
图17:在鞘内递送新型治疗载体aav9-mini-mpz-sh3tc2.myc后,sh3tc2在sh3tc2-/-小鼠周围神经系统中的表达分析。在鞘内注射aav9-minimpz-sh3tc2myc载体到sh3tc2-/-小鼠中后4周,人正常sh3tc2蛋白(红色)主要在腰椎根(a)和坐骨神经(d中的部分和f中的梳理纤维)的髓鞘雪旺细胞的核周细胞质中表达。未注射小鼠的组织在a、c、e中显示为阴性对照。细胞核被染成蓝色。图17g显示n=5小鼠腰椎根和坐骨神经中表达率(%sh3tc2阳性细胞)的量化。
[0207]
序列
[0208]
seq id no.1:aav-mpz.egfp构建体
[0209]
[0210]
[0211][0212]
粗体=itr序列
[0213]
斜体=mpz启动子
[0214]
下划线=egfp
[0215]
斜体下划线=wpre序列
[0216]
seq id no.2:aav-mpz.gjb1构建体
[0217]
[0218]
[0219][0220]
粗体=itr序列
[0221]
斜体=mpz启动子
[0222]
下划线=cx32
[0223]
斜体下划线=wpre序列
[0224]
seq id no.3:aav-minimpz.egfp构建体
[0225]
[0226]
[0227][0228]
粗体=itr序列
[0229]
斜体=mini-mpz启动子
[0230]
下划线=egfp
[0231]
斜体下划线=wpre序列
[0232]
seq id no.4:mpz启动子
[0233]
cctgttcagactcgtttcctgctgtaccctttcaatggccccacatcaaatcaaacacagatggcacatatctactctaaatatatgcagagcttcacaaacgtcatacacgtacgtgtgtcacacacgcacacacacacccttccacctctgcccttacctttgctgtcccatctagacattatccctcccatccccttatttcccttatcaaaatggctgctccttcaaggttccaaataacactgcttcctggacctgactcctctttcctctgaacttcctgtgttaagtgtattcctagtgcactgtgccttggtagttgttgagattgccctctgcttctcccttctgcctcctcatctagtgatcttgagcttgtagaaagaactgaattaccattctaatacgagcattctcgaactctccaaatagccaccaagcaggacaataggcagtcttgatcatttaaactgctgcatggcaaaaggaatcgaaggatttcttaacagaagtgggggggggggagatctgggcttcttcctggaagtttcctgatagagaaaatcttctgcctgggtagaatctcccaggatgcagggagatggaaaaagtgttccccaaggactttgtagtctacaggttgtggagccatcggaacaacgagacaccctaatttgggagtgctctgaaagaaacttgcctctaggccctagggctctcaggcaaggaggctaagaaggaatcctttg
ctgtagccttttggatttaggtttctcagcttatctatccctcagagaagtgtgtctatgtcccttttctgtccctctgcctcaccccaccccaacattccaacctagggtagggggaggtcagtatacacaaagccctctgtgtaaggggtggtatgtgtccccccacccccctacccagagtatacaatgccccttctgctccatgcccctgccaccctcccaccacctctcaattgcacatgccaggctgcaattggtcactggctcaggacagccccctcatgctggggatccaggggattttaagcaggttccagaaaacaccactcagttccttgtcccccgctctctccaccccacagacgctctgcc
[0234]
seq id no.5:minimpz启动子
[0235]
gctctcaggcaaggaggctaagaaggaatcctttgctgtagccttttggatttaggtttctcagcttatctatccctcagagaagtgtgtctatgtcccttttctgtccctctgcctcaccccaccccaacattccaacctagggtagggggaggtcagtatacacaaagccctctgtgtaaggggtggtatgtgtccccccacccccctacccagagtatacaatgccccttctgctccatgcccctgccaccctcccaccacctctcaattgcacatgccaggctgcaattggtcactggctcaggacagccccctcatgctggggatccaggggattttaagcaggttccagaaaacaccactcagttccttgtcccccgctctctccaccccacagacgctctgcc
[0236]
seq id no.6:连接蛋白-32(cx32):genbank:ay408135.1
[0237]
atgaactggacaggtttgtacaccttgctcagtggcgtgaaccggcattctactgccattggccgagtatggctctcggtcatcttcatcttcagaatcatggtgctggtggtggctgcagagagtgtgtggggtgatgagaaatcttccttcatctgcaacacactccagcctggctgcaacagcgtttgctatgaccaattcttccccatctcccatgtgcggctgtggtccctgcagctcatcctagtttccaccccagctctcctcgtggccatgcacgtggctcaccagcaacacatagagaagaaaatgctacggcttgagggccatggggaccccctacacctggaggaggtgaagaggcacaaggtccacatctcagggacactgtggtggacctatgtcatcagcgtggtgttccggctgttgtttgaggccgtcttcatgtatgtcttttatctgctctaccctggctatgccatggtgcggctggtcaagtgcgacgtctacccctgccccaacacagtggactgcttcgtgtcccgccccaccgagaaaaccgtcttcaccgtcttcatgctagctgcctctggcatctgcatcatcctcaatgtggccgaggtggtgtacctcatcatccgggcctgtgcccgccgagcccagcgccgctccaatccaccttcccgcaagggctcgggcttcggccaccgcctctcacctgaatacaagcagaatgagatcaacaagctgctgagtgagcaggatggctccctgaaagacatactgcgccgcagccctggcaccggggctgggctggctgaaaagagcgaccgctgctcggcctgctga
[0238]
seq id no.7:sh3结构域和四肽重复序列2(sh3tc2):genbank:bc114486.1
[0239]
atgggtggctgcttctgcatccccagggagcggagtctgacccggggcccaggtaaagaaactccttccaaggatccaactgtatcgagtgagtgtatagcctcatctgaatacaaggaaaaatgttttctgccacagaacattaatccagacctgacactctccttctgtgtaaagagccgctccaggaggtgtgtaaatggacccctacaggaagctgctcggaggcggctctgggcactggagaatgaggaccaggaggtgcgcatgctgtttaaggacctctcagcaaggttggtcagtatccagtctcagagggcccagtttctcatcaccttcaagaccatggaggaaatctggaagttctccacctaccttaatttagaacatctcctctttgaccacaagtactggctcaactgcatattggtggaggatacagagatccaagtgtctgtagatgataaacacctggaaacaatatacctgggactcctgatacaggaaggccacttcttctgcagagccctgtgctccgtgactccaccagccgagaaggaaggggaatgcttgacactttgcaagaatgagttaatctcagtgaagatggcagaagctggctccgagttggaaggcgtgtctttggtgacaggtcagcggggcctggtactggtgtcagccttggagcctctgcctctccctttccaccagtggttcctaaagaattatccaggaagctgtggcctttccaggaagagggattggacaggctcctatcagattggcagaggacgctgtaaggccttgacgggttatgagccaggagaaaaggatgaactgaatttctaccagggagaaagcattgagatcatcggctttgtcatacctgggcttcagtggttcattggaaagtcgacaagttcaggacaagtgggctttgtccccaccaggaacatagatcctgattcttattccccaat
gagcaggaactctgcctttctcagtgatgaggagagatgctccctgttggccctgggaagtgataagcagactgagtgttccagcttcctccacactcttgctcgcactgacatcacatctgtctaccggctcagtgggtttgaatccatccagaatcctccaaatgatctgagtgcatcccagcctgaaggcttcaaggaggtcaggcctggcagagcctgggaggagcatcaggccgtggggtccagacagtccagcagctctgaggactccagcctggaggaggagctcctctcggccacctcagacagctatcgcctgccggagcctgatgaccttgatgacccggaactgctcatggacctaagcactggtcaggaggaggaggctgagaacttcgcccccatattggcttttctggatcatgagggttatgctgaccactttaagagtctctatgacttctccttctctttcctcacttcttccttttatagcttctctgaggaggatgagtttgtggcctacctggaggcatcaagaaagtgggccaagaagagccacatgacctgggcccatgcccggctctgcttcctcctgggccggctgagcatcaggaaggtcaaactctctcaggccagggtgtacttcgaggaggccatccacattctcaatggagcatttgaggacctatccttggtggccactctgtacatcaatttggctgccatctacctgaaacagaggctgagacataaaggctccgccctgttggaaaaggcaggtgccctgctggcctgcctgcctgaccgtgagtctagtgccaagcatgaactcgacgtggtggcctacgtgctgcgccaggggattgtggtgggcagcagcccgctggaggccagggcctgctttctggccatccgcttgctcctgagcctaggccggcacgaggaggtcctgccctttgccgagcgcctgcagctcctctctggacaccctcctgcctctgaggctgtggccagtgttttgagttttctgtatgacaagaaatatcttccacaccttgcagtggcctctgtccagcaacatggtatccagagtgcccaagggatgtctcttcctatttggcaggtccaccttgtcctccagaacacaaccaagctccttggctttccttccccaggctggggtgaagtttctgccttggcctgcccaatgctcagacaggccctggctgcctgtgaggaactagcagaccggagcacccagagggccctgtgtctcatcctttccaaagtgtacctcgagcacaggtctcctgacggtgccatccactacctgagccaggccttggtgctagggcagctgctgggtgagcaggaatcctttgagtcttctctctgcctggcatgggcctatctcttagccagccaggccaagaaggctttggatgtgcttgagccactgctatgctccctgaaggagacagagagtctcactcaaaggggagtcatctataacctcctgggacttgcactccaaggtgaaggccgggtgaacagggcagccaagagctatcttcgggccttgaacagagcccaggaggtgggagatgtgcataaccaggcagtggctatggccaatcttggccacctgagccttaagtcctgggctcagcatccagccagaaactatctcctgcaggctgtacgactctattgtgaacttcaggccagtaaggagacagacatggaattagtacaggtgtttctctggttggcccaagttctggtgtctggacaccagctgacccatggccttctttgttatgaaatggcattgctgtttggcttaaggcatcgacatctaaagagtcagcttcaggccaccaaatccctctgccatttctacagctctgtgtccccaaaccctgaggcatgcatcacctaccatgagcactggctggccctggctcagcaactcagggaccgggagatggaagggaggctgctggagtccctggggcagctttatcggaacctaaataccgccaggtccctcaggaggtcactcacatgcatcaaggagagcctgcgtatcttcattgacctgggggagacagacaaggctgctgaggcctggcttggggcggggcgactccactacctcatgcaggaagacgagctggtggagctgtgcctgcaggcagccatccagacagccctgaagtcagaggagcctttgctggctctcaaactttatgaagaagcaggtgatgtgttcttcaatgggacccgccacaggcatcatgcagtggagtactaccgagctggagctgttcctttagcaaggaggttgaaggcggtgagaactgagctccggattttcaataagctgacagagctgcagattagcctcgaaggctatgagaaggctttggaatttgccaccctggccgccaggctcagcacagtcacaggagatcagaggcaagagctggtggcctttcaccgcctggctacagtgtactactccctgcacatgtatgagatggctgaggactgctacctgaagaccctgtccctctgtccaccctggctgcagagtcccaaggaggccctgtactatgccaaggtgtattatcgcctgggcagactcaccttctgccagctgaaggatgcccatgatgccactgagtacttccttctggccctggcagcagcggtcctgctgggtgatgaggagcttcaggacaccattaggagcaggctggacaacatctgccagagccccctgtggcacagcaggccctccgggtgctcctcagagagggcgcggtggctgagtggtggtggcctggccctctga
[0240]
seq id no.8:外周髓鞘蛋白22(pmp22):ncbi参考序列:nm_000304.4
[0241]
agttacagggagcaccaccagggaacatctcggggagcctggttggaagctgcaggcttagtctgtcggctgcgggtctctgactgccctgtggggagggtcttgccttaacatcccttgcatttggctgcaaagaaatctgcttggaagaaggggttacgctgtttggccgggcagaaactccgctgagcagaacttgccgccagaatgctcctcctgttgctgagtatcatcgtcctccacgtcgcggtgctggtgctgctgttcgtctccacgatcgtcagccaatggatcgtgggcaatggacacgcaactgatctctggcagaactgtagcacctcttcctcaggaaatgtccaccactgtttctcatcatcaccaaacgaatggctgcagtctgtccaggccaccatgatcctgtcgatcatcttcagcattctgtctctgttcctgttcttctgccaactcttcaccctcaccaaggggggcaggttttacatcactggaatcttccaaattcttgctggtctgtgcgtgatgagtgctgcggccatctacacggtgaggcacccggagtggcatctcaactcggattactcctacggtttcgcctacatcctggcctgggtggccttccccctggcccttctcagcggtgtcatctatgtgatcttgcggaaacgcgaatgaggcgcccagacggtctgtctgaggctctgagcgtacatagggaagggaggaagggaaaacagaaagcagacaaagaaaaaagagctagcccaaaatcccaaactcaaaccaaaccaaacagaaagcagtggaggtgggggttgctgttgattgaagatgtatataatatctccggtttataaaacctatttataacactttttacatatatgtacatagtattgtttgctttttatgttgaccatcagcctcgtgttgagccttaaagaagtagctaaggaactttacatcctaacagtataatccagctcagtatttttgttttgttttttgtttgtttgttttgttttacccagaaataagataactccatctcgccccttccctttcatctgaaagaagatacctccctcccagtccacctcatttagaaaaccaaagtgtgggtagaaaccccaaatgtccaaaagcccttttctggtgggtgacccagtgcatccaacagaaacagccgctgcccgaacctctgtgtgaagctttacgcgcacacggacaaaatgcccaaactggagcccttgcaaaaacacggcttgtggcattggcatacttgcccttacaggtggagtatcttcgtcacacatctaaatgagaaatcagtgacaacaagtctttgaaatggtgctatggatttaccattccttattatcactaatcatctaaacaactcactggaaatccaattaacaattttacaacataagatagaatggagacctgaataattctgtgtaatataaatggtttataactgcttttgtacctagctaggctgctattattactataatgagtaaatcataaagccttcatcactcccacatttttcttacggtcggagcatcagaacaagcgtctagactccttgggaccgtgagttcctagagcttggctgggtctaggctgttctgtgcctccaaggactgtctggcaatgacttgtattggccaccaactgtagatgtatatatggtgcccttctgatgctaagactccagaccttttgtttttgctttgcattttctgattttataccaactgtgtggactaagatgcattaaaataaacatcagagtaactca
[0242]
seq id no.9:髓鞘蛋白零(mpz):genbank:ak313555.1
[0243]
agttcctggtcccccactttctcaaccccacagatgctccgggcccctgcccctgccccagctatggctcctggggctccctcatccagccccagccctatcctggctgtgctgctcttctcttctttggtgctgtccccggcccaggccatcgtggtttacaccgacagggaggtccatggtgctgtgggctcccgggtgaccctgcactgctccttctggtccagtgagtgggtctcagatgacatctccttcacctggcgctaccagcccgaagggggcagagatgccatttcgatcttccactatgccaagggacaaccctacattgacgaggtggggaccttcaaagagcgcatccagtgggtaggggaccctcgctggaaggatggctccattgtcatacacaacctagactacagtgacaatggcacgttcacttgtgacgtcaaaaaccctccagacatagtgggcaagacctctcaggtcacgctgtatgtctttgaaaaagtgccaactaggtacggggtcgttctgggagctgtgatcgggggtgtcctcggggtggtgctgttgctgctgctgcttttctacgtggttcggtactgctggctacgcaggcaggcggccctgcagaggaggctcagtgctatggagaaggggaaattgcacaagccaggaaaggacgcgtcgaagcgcgggcggcagacgccagtgctgtatgcaatgctggaccacagcagaagcaccaaagctgtcagtgagaagaaggccaaggggctgggggagtctcgcaaggataagaaatag
[0244]
seq id no.10:早期生长反应2(egr2):ncbi参考序列:nm_000399.5
[0245]
aactgagcgaggagcaattgattaatagctcggcgaggggactcactgactgttataataacactaca
ccagcaactcctggcttcccagcagccggaacacagacaggagagagtcagtggcaaatagacatttttcttatttcttaaaaaacagcaacttgtttgctacttttatttctgttgatttttttttcttggtgtgtgtggtggttgtttttaagtgtggagggcaaaaggagataccatcccaggctcagtccaacccctctccaaaacggcttttctgacactccaggtagcgagggagttgggtctccaggttgtgcgaggagcaaatgatgaccgccaaggccgtagacaaaatcccagtaactctcagtggttttgtgcaccagctgtctgacaacatctacccggtggaggacctcgccgccacgtcggtgaccatctttcccaatgccgaactgggaggcccctttgaccagatgaacggagtggccggagatggcatgatcaacattgacatgactggagagaagaggtcgttggatctcccatatcccagcagctttgctcccgtctctgcacctagaaaccagaccttcacttacatgggcaagttctccattgaccctcagtaccctggtgccagctgctacccagaaggcataatcaatattgtgagtgcaggcatcttgcaaggggtcacttccccagcttcaaccacagcctcatccagcgtcacctctgcctcccccaacccactggccacaggacccctgggtgtgtgcaccatgtcccagacccagcctgacctggaccacctgtactctccgccaccgcctcctcctccttattctggctgtgcaggagacctctaccaggacccttctgcgttcctgtcagcagccaccacctccacctcttcctctctggcctacccaccacctccttcctatccatcccccaagccagccacggacccaggtctcttcccaatgatcccagactatcctggattctttccatctcagtgccagagagacctacatggtacagctggcccagaccgtaagccctttccctgcccactggacaccctgcgggtgccccctccactcactccactctctacaatccgtaactttaccctggggggccccagtgctggggtgaccggaccaggggccagtggaggcagcgagggaccccggctgcctggtagcagctcagcagcagcagcagccgccgccgccgccgcctataacccacaccacctgccactgcggcccattctgaggcctcgcaagtaccccaacagacccagcaagacgccggtgcacgagaggccctacccgtgcccagcagaaggctgcgaccggcggttctcccgctctgacgagctgacacggcacatccgaatccacactgggcataagcccttccagtgtcggatctgcatgcgcaacttcagccgcagtgaccacctcaccacccatatccgcacccacaccggtgagaagcccttcgcctgtgactactgtggccgaaagtttgcccggagtgatgagaggaagcgccacaccaagatccacctgagacagaaagagcggaaaagcagtgccccctctgcatcggtgccagccccctctacagcctcctgctctgggggcgtgcagcctgggggtaccctgtgcagcagtaacagcagcagtcttggcggagggccgctcgccccttgctcctctcggacccggacaccttgagatgagactcaggctgatacaccagctcccaaaggtcccggaggccctttgtccactggagctgcacaacaaacactaccaccctttcctgtccctctctccctttgttgggcaaagggctttggtggagctagcactgccccctttccacctagaagcaggttcttcctaaaacttagcccattctagtctctcttaggtgagttgactatcaacccaaggcaaaggggaggctcagaaggaggtggtgtggggacccctggccaagagggctgaggtctgaccctgctttaaagggttgtttgactaggttttgctaccccacttccccttattttgacccatcacaggtttttgaccctggatgtcagagttgatctaagacgttttctacaataggttgggagatgctgatcccttcaagtggggacagcaaaaagacaagcaaaactgatgtgcactttatggcttgggactgatttgggggacattgtacagtgagtgaagtatagcctttatgccacactctgtggccctaaaatggtgaatcagagcatatctagttgtctcaacccttgaagcaatatgtattataaactcagagaacagaagtgcaatgtgatgggaggaacatagcaatatctgctccttttcgagttgtttgagaaatgtaggctattttttcagtgtatatccactcagattttgtgtatttttgatgtacactgttctctaaattctgaatctttgggaaaaaatgtaaagcatttatgatctcagaggttaacttatttaagggggatgtacatatattctctgaaactaggatgcatgcaattgtgttggaagtgtccttggtgccttgtgtgatgtagacaatgttacaaggtctgcatgtaaatgggttgccttattatggagaaaaaaaatcactccctgagtttagtatggctgtatatttctgcctattaatatttggaattttttttagaaagtatatttttgtatgctttgttttgtgacttaaaagtgttacctttgtagtcaaatttcagataagaatgtacataatgttaccggagctgatttgtttggtcattagctcttaatagttgtgaaaaaataaatctattctaacgcaaaaccactaactgaagttcagataatggatggtttgtgactatagtgtaaataaatacttttcaacaataseq id no.11:神经节苷脂诱导分化相关蛋白1(gdap1):ncbi参
考序列:nm_018972.3
[0246]
atggctgagaggcaggaagagcagagagggagcccgcccttgagggcggaaggcaaggccgacgcggaggttaagctcattctgtaccattggacgcattccttcagctctcaaaaggtgcgcttggtaattgctgaaaaggcattgaagtgcgaggaacatgatgtaagtctgcccttgagtgagcacaatgagccttggtttatgcgtttgaactcaactggagaagtgcctgtccttatccacggggaaaacataatttgtgaggccactcagatcattgattatcttgaacagactttcctggatgaaagaacacccaggttaatgcctgataaagaaagcatgtattacccacgggtacaacattaccgagagctgcttgactccttgccaatggatgcctatacacatggctgcattttacatcctgagttaactgtggactccatgatcccggcttatgcaactacaaggattcgtagccaaattggaaacacagagtctgagctgaagaaacttgctgaagaaaacccagatttacaagaagcatacattgcaaaacagaaacgacttaaatcaaagctgcttgatcatgacaatgtcaagtatttgaagaaaattcttgatgagttggagaaagtcttggatcaggttgaaactgaattgcaaagaagaaatgaagaaaccccagaagagggccagcaaccttggctctgcggtgaatccttcaccctggcagacgtctcactcgctgtcacattgcatcgactgaagttcctggggtttgcaaggagaaactggggaaacggaaagcgaccaaacttggaaacctattacgagcgtgtcttgaagagaaaaacatttaacaaggttttaggacatgtcaacaatatattaatctctgcagtgctgccaacagcattccgggtggccaagaaaagggccccaaaagttcttggcacgacccttgtggttggtttgcttgcaggagtgggatattttgcttttatgcttttcagaaagaggcttggcagcatgatattagcatttagacccagaccaaattatttctag
[0247]
seq id no.12:n-myc下游调节1(ndrg1):ncbi参考序列:nm_001135242.1
[0248]
atgtctcgggagatgcaggatgtagacctcgctgaggtgaagcctttggtggagaaaggggagaccatcaccggcctcctgcaagagtttgatgtccaggagcaggacatcgagactttacatggctctgttcacgtcacgctgtgtgggactcccaagggaaaccggcctgtcatcctcacctaccatgacatcggcatgaaccacaaaacctgctacaaccccctcttcaactacgaggacatgcaggagatcacccagcactttgccgtctgccacgtggacgcccctggccagcaggacggcgcagcctccttccccgcagggtacatgtacccctccatggatcagctggctgaaatgcttcctggagtccttcaacagtttgggctgaaaagcattattggcatgggaacaggagcaggcgcctacatcctaactcgatttgctctaaacaaccctgagatggtggagggccttgtccttatcaacgtgaacccttgtgcggaaggctggatggactgggccgcctccaagatctcaggatggacccaagctctgccggacatggtggtgtcccacctttttgggaaggaagaaatgcagagtaacgtggaagtggtccacacctaccgccagcacattgtgaatgacatgaaccccggcaacctgcacctgttcatcaatgcctacaacagccggcgcgacctggagattgagcgaccaatgccgggaacccacacagtcaccctgcagtgccctgctctgttggtggttggggacagctcgcctgcagtggatgccgtggtggagtgcaactcaaaattggacccaacaaagaccactctcctcaagatggcggactgtggcggcctcccgcagatctcccagccggccaagctcgctgaggccttcaagtacttcgtgcagggcatgggatacatgccctcggctagcatgacccgcctgatgcggtcccgcacagcctctggttccagcgtcacttctctggatggcacccgcagccgctcccacaccagcgagggcacccgaagccgctcccacaccagcgagggcacccgcagccgctcgcacaccagcgagggggcccacctggacatcacccccaactcgggtgctgctgggaacagcgccgggcccaagtccatggaggtctcctgctag
[0249]
seq id no.17:aav-human-mpz-gjb1构建体
[0250]
[0251]
[0252][0253]
粗体=itr序列
[0254]
斜体=人mpz启动子
[0255]
下划线=cx32
[0256]
斜体下划线=wpre序列
[0257]
seq id no.18:人hp0启动子
[0258]
gcctggcataaacttcatttattaaagtttattttgtctttaatctctcatataacttagtcttcctgatattgcagctgtgtgtgcccctcttttgtactcccagcattttgttcattactaaaggaagtgtcatggcttattatacttgattgttgatgggtttgtcctctgatcttcccatctccacctccccaaaccaaattttcaactccttgctggaaggacttaatttttattcctctctctattacctgcattctcatactttacatattgctggcacttaatacaattttgtagccttgaaataaattgaaatggacttaaacagcagcatgaagcactgaaggacttcttgacaaacggaaaggtcaggggcttcttgcctggaaatagtccagtggagaaaaacttctgtctgggaagaatcgcacaggatgaagggaggtgcggggaaaaaaactcccataggacttggtcatctcaagaagtctgtaatgcagcccacattagaggagataacaggggatatcctattttcagagttctctgggggaaacctccctctagttcctagggctgtgaggcagcctctctcaggcaaggaggctgaggagaaatccctttttatggcctttaaattgaggttccatatctatccctcagagaagtgtgtctgtgtccctgtttttgtccctctccctcaccaccccccacaacattccagcctggggcagggggaggccagtggacacaaagccctctgtgtatggggtggtatgtgtccccccacccctccacccagactatacaatgccccttctgctccctgcactctgcccccctccccaccacctctcaactgcacatgccaggctgcaattggttactggctgaggacagccccctcatgctggggccctaggggattttaagcaggttccaggaaccccccgttcagttcctggtcccccact
ttctcaaccccacagatgctccgggcccctgcccctgccccagc
[0259]
seq id no.19:aav-human-mpz-egfp模拟构建体
[0260]
[0261][0262][0263]
粗体=itr序列
[0264]
斜体=人mpz启动子
[0265]
下划线=egfp
[0266]
斜体下划线=wpre序列
[0267]
seq id no.20:用于治疗性sh3tc2基因置换的aav-minmpz-sh3tc2.myc.itr
[0268]
[0269]
[0270][0271]
粗体=itr序列
[0272]
斜体=微型mpz启动子
[0273]
下划线=sh3tc2
[0274]
斜体下划线=合成的最小polya
[0275]
seq id no.21:aav-人-minimpz-sh3tc2
[0276]
[0277]
[0278]
[0279][0280]
粗体=itr序列
[0281]
斜体=微型人hp0启动子
[0282]
下划线=sh3tc2
[0283]
斜体下划线=合成的最小polya
[0284]
seq id no.22:微型人hp0启动子
[0285]
tctctcaggcaaggaggctgaggagaaatccctttttatggcctttaaattgaggttccatatctatccctcagagaagtgtgtctgtgtccctgtttttgtccctctccctcaccaccccccacaacattccagcctggggcagggggaggccagtggacacaaagccctctgtgtatggggtggtatgtgtccccccacccctccacccagactatacaatgccccttctgctccctgcactctgcccccctccccaccacctctcaactgcacatgccaggctgcaattggttactggctgaggacagccccctcatgctggggccctaggggattttaagcaggttccaggaaccccccgttcagttcctggtcccccactttctcaaccccacagatgctccgggcccctgcccctgccccagc
[0286]
seq id no.23:aav-human-minimpz-egfp
[0287]
[0288]
[0289][0290]
粗体=itr序列
[0291]
斜体=微型人hp0启动子
[0292]
下划线=egfp
[0293]
斜体下划线=wpre序列
[0294]
seq id no.24:最小合成poly a序列
[0295]
ggagctctcgagaggcctaataaagagctcagatgcatcgatcagagtgtgttggttttttgtgtgagatct
[0296]
实施例
[0297]
现在将参考以下非限制性实施例描述本发明。
[0298]
实施例1:aav转移质粒克隆
[0299]
aav载体旨在提供cx32(paav-mpz.gjb1,完整载体)或报告基因egfp(paav-mpz.egfp,模拟载体)的雪旺细胞特异性表达,两者均在1.127kb mpz启动子下显示驱动在雪旺细胞中特异性表达(26,32)。使用aav构建体pam/m bp-egfp-wpre-bgh(57)作为起始质粒克隆这些载体,其包含土拨鼠肝炎病毒转录后调控元件(wpre)和两侧为aav2反向末端重复序列(图1和9)的牛生长激素多聚腺苷酸化序列(bghpa)。
[0300]
如何克隆三个构建体aav-mpz.egfp、aav-mpz.gjb1和aav-minimpz.egfp的具体细节如下:
[0301]
264-p0-egfp-wpre(=aav-mpz.egfp
–
seq id no.1)
[0302]
使用包含mpz启动子序列的pbluescript sk+质粒,以便使用xhoi和ecorv限制酶消化掉启动子序列。也使用相同的酶消化aav载体。在连接和转化后,表达盒的正确组装通过限制性消化作图和使用覆盖整个编码序列的引物直接测序来确认。
[0303]
264-mpz(p0)-cx32-wpre(=aav-mpz.gjb1
–
seq id no.2)
[0304]
mpz/cx32 orf是从先前制备的慢病毒构建体中pcr扩增的。用于扩增的引物是p0-cx32-f 5'-aggggtacccttcctgttcagact-3'(seq id no.13)和p0-cx32-r5'-ccgctcgagggatcctc agcag-3'(seq id no.14).pcr产物(2030bp)使用qiagen凝胶提取试剂盒进行凝胶纯化并用kpni和xhoi消化。aav载体也用相同的限制酶消化。通过orf的直接测序确认整个表达盒。
[0305]
264-mpz(p0)min-egfp-wpre(=aav-mini mpz.egfp
–
seq id no.3)
[0306]
aav载体264用hindiii消化并自连接。然后将接头插入到载体中。使用以下引物从大鼠mpz启动子序列pcr扩增mpzmin:kpni-p0-f:5'-ggggtaccgctctcaggcaag-3'(seq id no.15)和agei-p0-r:5'-aaaccggttggcagagcgtctgt-3'(seq id no.16).然后将插入片段(420bp)定向克隆到我们的aav载体264。使用agei和hindiii从另一个构建体中消化egfp并直接连接。
[0307]
实施例2:aav载体生产、纯化和滴定
[0308]
aav9载体的生产是根据公开的方案进行的(58)。将paav-mpz.egfp和paav-mpz.gjb1质粒交叉包装到aav9衣壳中(衣壳质粒由西班牙巴塞罗那大学的a.bosch博士提供,并且最初由美国宾夕法尼亚州宾夕法尼亚大学vector core的james wilson博士开发)。
[0309]
假型9的aav病毒原种如先前所述产生(59)。重组aav(raav)载体是通过用250μgpaav、250μg prepcap和500μg pxx6质粒与聚乙烯亚胺(pei;支链,mw 25,000;sigma)混合三次转染2
×
108hek293细胞产生的。简而言之,在转染后48小时,通过离心(200g,10分钟)收获细胞;重悬于30ml 20mm nacl、2mm mgcl2和50mm tris-hcl(ph 8.5)中,并通过三个冻融循环裂解。细胞裂解液通过离心(2000g,10分钟)澄清,并且raav颗粒通过如下的碘克沙醇梯度从上清液中纯化:澄清的裂解液用50u/ml benzonase(novagen;1小时,37℃)处理并离心(3000g,20分钟)。收集含有载体的上清液,并使用5m储备溶液将其调节为200mm nacl。为了从澄清的细胞裂解物中沉淀病毒,加入聚乙二醇(peg 8000;sigma)至终浓度为8%,并将混合物孵育(3小时,4℃)并离心(8000g,15分钟)。将含有raav的颗粒重新悬浮在20mm nacl、2mm mgcl2和50mm tris-hcl(ph 8.5)中,并在4℃下孵育48小时。raav颗粒将使用如(59)所述的碘克沙醇方法进行纯化。如有必要,使用amicon ultra-15centrifugal filter device(millipore)将raav在pbsmk中浓缩和脱盐。通过picogreen定量(60)评估滴定并计算为每毫升病毒基因组(vg/ml)。
[0310]
实施例3:鞘内载体递送
[0311]
在沿着下腰椎水平切开小皮肤以观察脊柱后,将aav载体以5μl/min的缓慢速率递送到麻醉小鼠的l5-l6椎间隙中。使用连接到26号针头的50μl hamilton注射器(hamilton,giarmata,罗马尼亚)注射20μl的含有aav载体的0.5-1x10
11
载体基因组(vg)的总体积。尾巴的轻弹被认为是成功的鞘内施用的指示。
[0312]
实施例4:aav9介导的雪旺细胞靶向基因表达
[0313]
用上文实施例1和3中描述的aav9-mpz-egfp载体处理2个月大的野生型小鼠。样品通过从pns组织中提取dna并确定病毒dna的存在进行分析,该病毒dna的存在作为注射后4周和6周(表1)的载体拷贝数(vcn)测量,如我们先前所述(33)。在注射后4周和8周也如下所述进行腰椎根切片的免疫荧光染色和腰椎根、股神经和坐骨神经的免疫印迹(表2)。
[0314]
免疫荧光染色:对于免疫染色,根据机构批准的方案用avertin麻醉小鼠,并且然后用生理盐水经心脏灌注,接着在0.1m pb缓冲液中加入新鲜的4%多聚甲醛。解剖附有脊髓根的腰骶脊髓,以及双侧坐骨神经和股骨运动神经。所有组织都被冷冻用于冷冻切片,而坐骨神经和股神经被分离并在立体镜下梳理成纤维。梳理的纤维或切片在冷丙酮中透化并在室温下用含有0.5%triton-x(sigma-aldrich,德国慕尼黑)的5%bsa(sigma-aldrich,德国慕尼黑)封闭溶液孵育1小时。使用的一抗是:针对contactin相关蛋白的小鼠单克隆抗体(caspr,1:50;来自魏茨曼科学研究所elior peles博士的礼物)、针对egfp的兔抗血清(1:1,000;invitrogen,美国)、capr2(1:200,alomone labs,以色列)和cx32(1:50;sigma,德国慕尼黑)都在封闭溶液中稀释,并在4℃下孵育过夜。然后在pbs中洗涤载玻片,并与荧光素和罗丹明缀合的小鼠和兔交叉亲和力纯化的二抗(1:500;jackson immunoresearch,美国)在室温下孵育1小时。用dapi(1μg/ml;sigma,德国慕尼黑)观察细胞核。用荧光封固介质封固载玻片,并使用axiovision软件(carl zeiss microimaging;德国上科亨)在带有数码相机的荧光显微镜下拍摄图像。
[0315]
egfp报告基因的表达率通过计算egfp阳性雪旺细胞的数量占腰椎根和坐骨神经中总雪旺细胞的百分比来量化。cx32的表达通过用轴突结构域标记(包括近旁kv1.2和旁结caspr,用cx32进行双重染色)可视化有髓纤维的节点区域来量化。将cx32免疫反应性阳性的淋巴结区域数量计算为占腰椎根和坐骨神经总淋巴结区域的百分比。
[0316]
免疫印迹分析:使用根和外周神经裂解物的免疫印迹分析检测注射小鼠组织中报告基因egfp或cx32的表达。将注射后4周收集的腰椎根、股骨和坐骨神经裂解物的免疫印迹与兔抗egfp(1:1000;abcam)和抗cx32(克隆918,1:3,000)一抗一起孵育,然后是hrp偶联的抗-兔二抗(jackson immunoresearch,1:3,000稀释)。结合的抗体通过增强的化学发光系统(ge healthcare life sciences)进行可视化。
[0317]
以下图2和表1和2中显示结果。可以检测到报告基因egfp(增强型绿色荧光蛋白)的高表达水平,特别是在schwann细胞、pns的髓鞘细胞,包括腰椎神经根和远端坐骨神经中,并且这显示腰椎根和坐骨神经样品中的egfp报告基因的特异性表达,表明使用该载体递送系统实现雪旺氏细胞中的组织特异性表达。
[0318]
表1:在用aav9-mpz.egfp注射的wt小鼠中检查的所有组织中的载体拷贝数(vcn):
[0319][0320]
表2:在注射后4周和8周aav9-mpz.egfp注射的wt小鼠的腰椎根和坐骨神经中的egfp表达率(%egfp阳性雪旺细胞):
[0321][0322]
实施例5:鞘内递送的aav9-mpz.gjb1载体在2个月cx32 ko和r75wko小鼠中的表达
[0323]
aav9-mpz.gjb1载体如上述实施例1中所述生产(5x10
12
vg/ml),并通过腰椎鞘内(i.th.)注射(5x10
10
vg,20μl)递送到2个月和6个月大的cx32 ko小鼠。对从pns组织中提取的dna中提取的vcn进行分析,如先前所述(33),不同组织中的每个细胞显示广泛的生物分布(图3a),包括在脊髓根和坐骨神经中,并且肝脏中的含量最高(55)。如上所述进行免疫染色和免疫印迹分析。cx32在腰椎根和坐骨神经纤维中超过60-70%的髓鞘施旺细胞中的旁结髓鞘区域表达(图3b-d)。aav9递送的cx32高水平表达也可以通过注射的pns组织裂解物的蛋白质印迹检测到,而不是未注射的cx32 ko小鼠(图3f)。
[0324]
为了阐明允许更高表达水平的aav9-mpz.gjb1病毒载体是否可以克服我们之前研究中用慢病毒载体观察到的高尔基体保留的突变体的干扰作用(29,34),发明人还注射2个月大的r75w基因敲除(r75wko)小鼠。重要的是,在r75w/ko组织中也检测到aav9递送的cx32的偏节点定位,尽管干扰性高尔基体保留的r75w突变体的共表达显示出典型的核周定位(图3e)。因此,aav9显示出提供广泛、高水平和雪旺细胞靶向基因表达的潜力,这也可能克服代表性高尔基体保留的cmt1x突变体的干扰效应。
[0325]
这些结果显示在图3和下面的表3和4中,证明使用载体递送野生型gjb1基因的拷贝导致cx32在cx32敲除小鼠和r75w敲除小鼠中成功表达。尽管在核周区域存在r75wcx32突变蛋白,但r75w高尔基体保留的突变体(图3e)也实现cx32的表达,而这在不使用aav载体的先前工作中是不可能的。
[0326]
表3:在注射aav9-mpz.gjb1的cx32 ko小鼠中检查的所有组织中的载体拷贝数:
[0327] 腰椎根坐骨神经肌肉脊髓vcn0.20
±
0.050.18
±
0.070.05
±
0.030.17
±
0.08n121235
[0328]
表4:在aav9-mpz.gjb1注射的2个月和6个月大的cx32 ko和cx32 ko/r75w转基因小鼠的腰椎根和坐骨神经的cx32蛋白表达率(%cx32蛋白阳性副结髓鞘区域):
[0329][0330]
实施例6:与aav9-mpz.egfp(模拟)治疗的同窝小鼠相比,aav9-mpz.gjb1(完整)注射6个月大的cx32 ko小鼠的行为分析
[0331]
小鼠治疗:使用两组6个月大的cx32敲除(ko)小鼠进行基因治疗试验。对于每个测量的结果,每个治疗组至少8-12只小鼠被认为足以评估基于先前使用类似模型的研究的统计学显著差异(32,33)。动物在病理学开始后(已知在3个月大后开始)在6个月大时接受治
疗。
[0332]
同窝小鼠随机接受aav9-mpz.gjb1(完整)治疗或aav9-mpz.egfp(模拟治疗,作为对照组),并分配一个编码编号以供进一步鉴定。
[0333]
行为测试:然后在治疗前和在8个月和10个月大时,由对治疗条件不知情的检查员通过如下所述的行为测试对小鼠进行评估(图4和表5)。
[0334]
旋转棒测试:如前所述使用加速旋转棒装置(ugo basile,varese,意大利)确定电机平衡和协调(61)。动物训练由每天3次试验组成,试验之间有15分钟的休息时间,连续3天。将小鼠放在杆上,速度从每分钟4转(rpm)逐渐增加到40转。在第四天使用两种不同的速度20和32rpm进行测试。计算每个速度的下降延迟。测试一直持续到老鼠从杆上掉下来或老鼠在杆上停留600秒后被移走。每只小鼠以所使用的每个速度在旋转杆上放置3次,每个速度获得三个不同的值。每只小鼠在两种不同的速度下使用平均值。
[0335]
抓握测试:为了测量抓握,小鼠通过尾巴抓住并朝装置(ugo basile,varese,意大利)下降,直到它们用后爪抓住网格。小鼠被轻轻拉回,直到它们释放网格。在设备上标明以g为单位的力的测量值。每个区段由三个连续的试验组成并且测量值取平均值。在aav9.mpz-gjb1和aav9.mpz-egfp治疗的小鼠之间比较后肢力。
[0336]
与注射aav9-mpz.egfp模拟(非治疗性)载体的同窝小鼠(每组n=20只小鼠)相比,用aav9-mpz.gjb1全治疗载体治疗的年长cx32 ko小鼠在这些测试中表现明显更好。
[0337]
结果显示在下面的图4和表5中,这表明gjb1治疗组的运动性能(通过旋转杆和足部抓握测试测量)在注射后2个月(8个月大时)有所改进,并且这种改进仍然保持稳定直到10个月大。模拟治疗的小鼠没有表现出运动能力的改进。
[0338]
表5:cx32 ko治疗组运动行为表现的纵向比较:
[0339][0340]
实施例7:坐骨神经运动传导研究
[0341]
cx32 ko小鼠在6个月大时,在神经病发作后按上述实施例6所述进行治疗,并且然后在10个月大时如下所述进行运动神经传导研究。
[0342]
运动神经传导速度(mncv):在麻醉动物的坐骨切迹处和脚踝远端经由具有0.05ms的超大方波脉冲(5v)的双极电极刺激后,mncv使用已发表的方法在体内从双侧坐骨神经测量(62)。复合肌肉动作电位(cmap)的潜伏期由插入后爪第2和第3指之间的双极电极记录,并从刺激伪影到负m波偏转开始测量。mncv是通过将刺激和记录电极之间的距离除以从近端延迟减去远端的结果来计算的。
[0343]
在10个月大时进行的mncv研究结果显示在图5和下表6中,这表明与模拟治疗的对照组(n=10只小鼠)相比,在用gjb1治疗的cx32 ko小鼠中在10个月时测量运动神经传导速度得到改进,并接近野生型水平。
[0344]
表6:aav9.mpz.egfp(mock,cx32 ko对照组)、aav9.mpz.gjb1(完整,完整治疗组)和wt的运动神经传导速度和幅度测量值:
[0345][0346]
实施例8:与模拟治疗的小鼠载体相比,鞘内递送aav9-mpz.gjb1后cx32 ko小鼠的前脊髓根、坐骨神经和股神经的形态学分析
[0347]
cx32 ko小鼠在6个月大时如上文实施例6中所述进行治疗,并在4个月后10个月大时进行检查。
[0348]
小鼠经心灌注有0.1m pb缓冲液中的2.5%戊二醛。将附有多个脊髓根的腰脊髓以及股神经和坐骨神经解剖并在4℃下固定过夜,然后渗透、脱水并嵌入爱牢达树脂(均购自agar scientific,essex,uk)。获得具有根部和股骨运动神经和坐骨神经的中间部分的腰脊髓的横向半薄切片(1μm)并用碱性甲苯胺蓝(sigma-aldrich,德国慕尼黑)染色。切片用10倍、20倍和40倍物镜可视化,并用尼康ds-l3相机(尼康日本东京)拍摄。在最终放大倍数为100-200倍时获得整个根部或横向神经切片的图像,并在最终放大倍数为400倍时捕获一系列覆盖根部或神经横截面区域的部分重叠区域。如前所述(22、32、63),这些图像用于检查两组中异常髓鞘形成的程度。简而言之,使用以下标准对所有脱髓鞘、髓鞘再生和正常有髓鞘的轴突进行计数:大于1μm且没有髓鞘的轴突被认为是脱髓鞘的,髓鞘小于轴突直径10%的轴突和/或被“洋葱球”包围的轴突(即周向排列的雪旺氏细胞突和细胞外基质)被认为是髓鞘再生的,而其他有髓鞘的轴突被认为是正常有髓鞘的。
[0349]
此外,计算每个根或神经的整个横截面内存在的泡沫巨噬细胞的数量,作为炎症的指标。巨噬细胞在放大400倍的半薄切片中被鉴定为充满髓鞘碎片的细胞,没有基底膜,并延伸出小的微绒毛状突起,如前所述(64,65)。巨噬细胞计数被计算为每1,000根有髓纤维的比率,以解释不同脊髓根和神经之间的大小差异。所有病理分析均在对每只小鼠的治疗条件不知情的情况下进行。
[0350]
结果显示在图6和表7(针对前脊髓根)、图7和表8(针对坐骨神经)以及图8和表9(针对股骨运动神经)中。这些结果显示,与具有较少脱髓鞘和再髓鞘纤维的模拟处理对照组相比,脊髓根、坐骨神经和股神经的髓鞘形成得到改进,并且异常有髓鞘纤维的比率也得
到改进。所有样品均显示gjb1治疗组泡沫巨噬细胞数量减少,表明治疗组炎症减少。
[0351]
表7:10个月大时鞘内治疗的cx32 ko小鼠前腰椎根的形态计量分析结果:
[0352][0353]
表8:鞘内治疗的cx32 ko小鼠在10个月大时坐骨神经的形态计量分析结果:
[0354][0355]
表9:10个月大时鞘内治疗的cx32 ko小鼠股骨运动神经的形态计量分析结果:
[0356][0357][0358]
实施例9:由最小启动子(minimpz)元件驱动的用于雪旺细胞靶向表达的aav载体的开发
[0359]
上述实施例中描述的基于aav9的方法具有很高的临床转化潜力,可以用于治疗包括cmt4c的其他脱髓鞘cmt类型。然而,需要克服aav载体中较小转基因容量的限制。
[0360]
为了促进aav介导的雪旺细胞靶向基因表达,发明人克隆最小版本的mpz启动子。
从1.127kb全长mpz启动子(seq id no.4)开始并且基于表明全长mpz启动子的功能调节元件(egr2和sox10结合位点)位于起始密码子上游400bp内(56)的增强子/chip-seq数据,发明人选择该策略以使用最小尺寸的启动子在雪旺细胞中实现靶向表达,以保持在aav载体的承载能力范围内。本发明人从起始密码子上游mpz启动子的410bp扩增pcr,然后将该minimpz启动子与下游egfp作为报告基因进一步克隆到aav转移质粒中,并产生aav9-minimpz.egfp载体((seq id no.3和图9)。
[0361]
该aav9-minimpz.egfp载体也在2个月大的野生型(wt)小鼠中使用与实施例3中所述相同的递送方法通过单次腰椎鞘内注射进行体内验证,并显示驱动报告基因egfp在整个pns中高百分比的髓鞘施旺细胞中的表达。这表明载体的广泛表达,其主要限于pns组织中的髓鞘施旺细胞,在腰椎根和周围神经中具有超过50%的表达率和高载体拷贝数(vcn)(图10)。
[0362]
用包括白质和灰质中的神经元neun、星形胶质细胞gfap和少突胶质细胞cc-1的细胞标记物与egfp组合对来自aav9-minimpz-egfp注射的小鼠的脊髓组织进行免疫染色,如实施例4中所述,显示minimpz驱动的构建体仅在cns中约2-3%的神经元和神经胶质细胞的一个非常小的子集中存在,如从n=3-5小鼠中量化的(图11)。
[0363]
结果显示在图10(腰椎根和坐骨神经)和图11(腰脊髓)中,表明egfp表达充分分布在腰椎根和坐骨神经中,并且在腰脊髓中表达极少,显示注射后在周围神经系统的雪旺细胞中存在载体的生物分布和egfp报告蛋白的表达。
[0364]
实施例10:cmt1x模型中基因治疗在神经病变早期发作前治疗的疗效
[0365]
2个月大的cx32敲除(ko)小鼠组,即cmt1x模型(每组n=10只小鼠),在2个月大时注射治疗性(完整)aav9-mpz-gjb1载体或阴性对照(模拟)载体aav9-mpz-egfp。行为分析在治疗前、4个月和6个月大时进行。在6个月大时进行电生理分析,然后对周围神经组织的半薄切片进行形态学分析。除了在2个月大时治疗小鼠外,使用与上述实施例6-8中所述相同的方案。
[0366]
该数据提供在神经病变的早期阶段(2个月大)的小鼠的发作前治疗以及6个月后期发病后治疗的模型(实施例6-8)。
[0367]
治疗与模拟治疗的6个月大cx32 ko小鼠的行为结果
[0368]
使用治疗(完整)或阴性对照(模拟)载体对2个月大的cx32敲除(ko)小鼠(cmt1x模型)进行治疗,并在4个月和6个月大时检查小鼠的运动强度.与模拟治疗组相比,完整治疗组在两个时间点都显示出显著改进的肌肉力量(图12a和b)。完整治疗组在治疗后随着时间的推移也表现出显著改进(图12c),而模拟治疗的小鼠没有表现出任何改进。
[0369]
发作前治疗与模拟治疗的6个月大cx32 ko小鼠的电生理研究
[0370]
电生理研究在治疗(完整)和模拟治疗的6个月大cx32 ko小鼠中,基因治疗后坐骨神经传导速度显著改进,如图13所示。
[0371]
图13显示与模拟载体治疗的cx32 ko小鼠相比,aav9-mpz-gjb1(完整载体)发作前坐骨神经传导速度显著提高。
[0372]
治疗与模拟治疗的6个月大cx32 ko小鼠周围神经组织的形态学研究
[0373]
治疗与模拟治疗的6个月大cx32 ko小鼠周围神经组织的形态学研究。检查腰椎前根(图14)、坐骨中神经(图15)和股骨运动神经(图16)的半薄切片,并与在6个月大时模拟治
疗的cx32ko小鼠相比量化完整治疗的cx32 ko小鼠的组中的异常有髓纤维的比例以及巨噬细胞的数量。
[0374]
如图14、15和16中的每一个所示,与模拟治疗的小鼠相比,在治疗的小鼠中发现较少的脱髓鞘(*)或再髓鞘化(r)纤维和较少的泡沫巨噬细胞。这表明治疗组中髓鞘形成改进和炎症减少。
[0375]
实施例11:开发用于治疗cmt1x的人源化治疗载体
[0376]
实施例1中描述的载体受大鼠mpz启动子控制。为了使该构建体人源化并使其更适合临床应用,本发明人还使用可使用的人hp0启动子(seq id no:18)克隆人-mpz-gjb1构建体(seq id no:17),用于临床前剂量反应测试和非人类灵长类动物(nhp)毒性和生物分布研究。使用引物从基因组dna中pcr扩增人p0序列以引入kpni和agei限制性内切酶。引物是:kpnhp0-f-5'-aggggtaccgcctggcataaac-3'(seq id no.25)和agehp0-r-5'-aatttaccggtgctggggcag-3'(seq id no.26)。在连接hp0后,使用bamhi和xhoi从预先存在的构建体中切下cx32orf。cx32连接到aav转移构建体中,并通过限制性消化图谱和直接测序确认表达盒的正确组装。
[0377]
还产生人源化模拟载体质粒(human-mpz-egfp)用作对照(seq id no:19)。
[0378]
实施例12:治疗cmt4c的治疗载体的开发和表达分析
[0379]
类似于实施例9中描述的那些的mini-mpz-sh3tc2.myc构建体,使用seq id no.5的mini-mpz大鼠衍生的启动子,上面是使用sh3tc2基因插入开发的,并在itr-itr片段中进行进一步修改(包括去除wpre和用最少的合成polya替换polya)(68,69)以保持在大约4700bp的限制内以允许有效地封装到aav9中。该治疗载体的序列显示在seq id no:20中。
[0380]
这种新型治疗载体(mini-mpz-sh3tc2.myc)的表达分析在cmt4c模型小鼠组中进行。这些结果补充以上实施例9中描述的驱动报告基因表达的最小mpz启动子载体的开发。
[0381]
新的aav-minimpz-sh3tc2.myc结构被生产并包装到aav9血清型中,达到5x10
12
vg/ml。通过腰椎鞘内注射将载体(1x10
11
vg,体积为20μl)递送到5个月大的sh3tc2-/-小鼠(n=5),并在注射后5周在固定的腰椎脊髓根中检测表达和双侧坐骨神经切片。
[0382]
在特征性的核周颗粒外观中,并且偶尔沿着雪旺细胞的整个长度在包括根和坐骨神经的整个pns中高百分比的有髓鞘雪旺细胞中检测到sh3tc2的表达(图17a-f)。sh3tc2免疫反应性雪旺氏细胞百分比的量化显示,腰椎根中的平均表达率为54.67%,坐骨神经中的表达率为45.39%(图17g)。
[0383]
这些结果表明该构建体在整个pns的髓鞘施旺细胞中实现了良好的表达水平。
[0384]
实施例13:开发用于治疗cmt4c的人源化治疗载体
[0385]
非常适合临床前测试(由于包含最小版本的大鼠mpz启动子和sh3tc2上的myc标签以促进临床前表达分析)的mini-mpz-sh3tc2.myc(seq id no:20)构建体(如上文实施例12中所述)已被修改以更适合临床应用(seq id no:21)。
[0386]
myc标签已被移除,并且大鼠启动子的最小版本已被最小人mpz启动子的相应序列(seq id no:22)替换。在进入临床应用之前,该载体可以用于最终的临床前剂量反应测试和nhp毒性和生物分布研究。还产生了人源化模拟载体质粒(human-minimpz-egfp)(seq id no:23)。
[0387]
参考文献
[0388]
1.baets j,de jonghe p,timmerman v.recent advances in charcot-marie-tooth disease.curr opin neurol.2014;27(5):532-40.
[0389]
2.kleopa ka,scherer ss.inherited neuropathies.neurol clinics north america.2002;20:679-709.
[0390]
3.kleopa ka,kagiava a,sargiannidou i.gene therapy for cmt inherited neuropathy.in:duan d,mendell j(eds):muscle gene therapy.2019;https://doi.org/10.1007/978-3-030-03095-7_35(springer,cham).
[0391]
4.bergoffen j,scherer ss,wang s,oronzi-scott m,bone l,paul dl,et al.connexin mutations in x-linked charcot-marie-tooth disease.science.1993;262:2039-42.
[0392]
5.kleopa ka,scherer ss.molecular genetics of x-linked charcot-marie-tooth disease.neuromolecular med.2006;8:107-22.
[0393]
6.hahn af,brown wf,koopman wj,feasby te.x-linked dominant hereditary motor and sensory neuropathy.brain.1990;113:1511-25.
[0394]
7.birouk n,le guern e,maisonobe t,rouger h,gouider r,gugenheim m,et al.x-linked charcot-marie-tooth disease with connexin 32 mutations-clinical and electrophysiological study.neurology.1998;50:1074-82.
[0395]
8.shy me,siskind c,swan er,krajewski km,doherty t,fuerst dr,et al.cmt1x phenotypes represent loss of gjb1 gene function.neurology.2007;68:849-55.
[0396]
9.dubourg o,tardieu s,birouk n,gouider r,l
é
ger jm,maisonobe t,et al.clinical,electrophysiological and molecular genetic characteristics of 93 patients with x-linked charcot
–
marie
–
tooth disease.brain.2001;124:1958-67.
[0397]
10.liang gsl,de miguel m,gomez-hernandez jm,glass jd,scherer ss,mintz m,et al.severe neuropathy with leaky connexin32 hemichannels.ann neurol.2005;57:749-54.
[0398]
11.al-mateen m,craig ak,chance pf.the central nervous system phenotype of x-linked charcot-marie-tooth disease:a transient disorder of children and young adults.j child neurol.2014;29:342-8
[0399]
12.hahn af,ainsworth pj,bolton cf,bilbao jm,vallat j-m.pathological findings in the x-linked form of charcot-marie-tooth disease:a morphometric and ultrastructural analysis.acta neuropathol.2001;101:129-39.
[0400]
13.hattori n,yamamoto m,yoshihara t,koike h,nakagawa m,yoshikawa h,et al.demyelinating and axonal features of charcot-marie-tooth disease with mutations of myelin-related proteins(pmp22,mpz and cx32):a clinicopathological study of 205 japanese patients.brain.2003;126:134-51.
[0401]
14.kleopa ka,zamba-papanicolaou e,alevra x,nicolaou p,georgiou d-m,hadjisavvas a,et al.phenotypic and cellular expression of two novel connexin32 mutations causing cmt1x.neurology.2006;66:396-402.
[0402]
15.omori y,mesnil m,yamasaki h.connexin 32 mutations from x-linked charcot-marie-tooth disease patients:functional defects and dominant negative effects.mol biol cell.1996;7(6):907-16.
[0403]
16.yoshimura t,satake m,ohnishi a,tsutsumi y,fujikura y.mutations of connexin32 in charcot-marie-tooth disease type x interfere with cell-to-cell communication but not cell proliferation and myelin-specific gene expression.j neurosci res.1998;51(2):154-61.
[0404]
17.yum sw,kleopa ka,shumas s,scherer ss.diverse trafficking abnormalities of connexin32 mutants causing cmtx.neurobiol dis.2002;11:43-52.
[0405]
18.desch
ê
nes sm,walcott jl,wexler tl,scherer ss,fischbeck kh.altered trafficking of mutant connexin32.j neurosci.1997;17:9077-84.
[0406]
19.oh s,ri y,bennett mvl,trexler eb,verselis vk,bargiello ta.changes in permeability caused by connexin 32 mutations underlie x-linked charcot-marie-tooth disease.neuron.1997;19(4):927-38.
[0407]
20.martin pem,mambetisaeva et,archer da,george ch,evans wh.analysis of gap junctions assembly using mutated connexins detected in charcot-marie-tooth x-linked disease.j neurochem.2000;74:711-20.
[0408]
21.kleopa ka,yum sw,scherer ss.cellular mechanisms of connexin32 mutations associated with cns manifestations.j neurosci res.2002;68:522-34.
[0409]
22.sargiannidou i,vavlitou n,aristodemou s,hadjisavvas a,kyriacou k,scherer ss,et al.connexin32 mutations cause loss of function in schwann cells and oligodendrocytes leading to pns and cns myelination defects.j neurosci.2009;29:4748-61.
[0410]
23.sargiannidou i,kim gh,kyriakoudi s,eun bl,kleopa ka.a start codon cmt1x mutation associated with transient encephalomyelitis causes complete loss of cx32.neurogenetics.2015;16(3):193-200.
[0411]
24.anzini p,neuberg dh-h,schachner m,nelles e,willecke k,zielasek j,et al.structural abnormalities and deficient maintenance of peripheral nerve myelin in mice lacking the gap junction protein connexin32.j neurosci.1997;17:4545-61.
[0412]
25.scherer ss,xu y-t,nelles e,fischbeck k,willecke k,bone lj.connexin32-null mice develop a demyelinating peripheral neuropathy.glia.1998;24:8-20.
[0413]
26.scherer ss,xu yt,messing a,willecke k,fischbeck kh,jeng lj.transgenic expression of human connexin32 in myelinating schwann cells prevents demyelination in connexin32-null mice.j neurosci.2005;25:1550-9.
[0414]
27.abel a,bone lj,messing a,scherer ss,fischbeck kf.studies in transgenic mice indicate a loss of connexin32 function in x-linked charcot-marie-tooth disease.j neuropathol exp neurol.1999;58:702-10.
astrocytes.nat biotechnol.2009;27(1):59-65.
[0439]
52.gurda bl,de guilhem de lataillade a,bell p,zhu y,yu h,wang p,et al.evaluation of aav-mediated gene therapy for central nervous system disease in canine mucopolysaccharidosis vii.mol ther.2016;24(2):206-16.
[0440]
53.calcedo r,wilson jm.humoral immune response to aav.front immunol.2013;4:341.
[0441]
54.jackson kl,dayton rd,klein rl.aav9 supports wide-scale transduction of the cns and tdp-43 disease modeling in adult rats.mol ther methods clin dev.2015;2:15036.
[0442]
55.meyer k,ferraiuolo l,schmelzer l,braun l,mcgovern v,likhite s,et al.improving single injection csf delivery of aav9-mediated gene therapy for sma:a dose-response study in mice and nonhuman primates.mol ther.2015;23(3):477-87.
[0443]
56.jang sw,svaren j.induction of myelin protein zero by early growth response 2 through upstream and intragenic elements.j biol chem.2009;284(30):20111-20.
[0444]
57.von jonquieres g,mersmann n,klugmann cb,harasta ae,lutz b,teahan o,et al.glial promoter selectivity following aav-delivery to the immature brain.plos one.2013;8(6):e65646.
[0445]
58.georgiou e,sidiropoulou k,richter j,papaneophytou c,sargiannidou i,kagiava a,et al.gene therapy targeting oligodendrocytes provides therapeutic benefit in a leukodystrophy model.brain.2017;140(3):599-616.
[0446]
59.zolotukhin s,byrne bj,mason e,zolotukhin i,potter m,chesnut k,et al.recombinant adeno-associated virus purification using novel methods improves infectious titer and yield.gene ther.1999;6(6):973-85.
[0447]
60.piedra j,ontiveros m,miravet s,penalva c,monfar m,chillon m.development of a rapid,robust,and universal picogreen-based method to titer adeno-associated vectors.hum gene ther methods.2015;26(1):35-42.
[0448]
61.savvaki m,panagiotaropoulos t,stamatakis a,sargiannidou i,karatzioula p,watanabe k,et al.impairment of learning and memory in tag-1 deficient mice associated with shorter cns internodes and disrupted juxtaparanodes.mol cell neurosci.2008;39:478-90.
[0449]
62.zielasek j,martini r,toyka kv.functional abnormalities in p0-deficient mice resemble human hereditary neuropathies linked to p0 gene mutations.muscle nerve.1996;19(8):946-52.
[0450]
63.vavlitou n,sargiannidou i,markoullis k,kyriacou k,scherer ss,kleopa ka.axonal pathology precedes demyelination in a mouse model of x-linked demyelinating/type i charcot-marie tooth neuropathy.j neuropathol exp neurol.2010;69:945-58.
[0451]
64.kobsar i,berghoff m,samsam m,wessig c,maurer m,toyka kv,et al.preserved myelin integrity and reduced axonopathy in connexin32-deficient mice lacking the recombination activating gene-1.brain.2003;126:804-13.
[0452]
65.groh j,heinl k,kohl b,wessig c,greeske j,fischer s,et al.attenuation of mcp-1/ccl2 expression ameliorates neuropathy in a mouse model for charcot-marie-tooth 1x.hum mol genet.2010;19:3530-43.
[0453]
66.shevtsova,z.,et al.(2005)."promoters and serotypes:targeting of adeno-associated virus vectors for gene transfer in the rat central nervous system in vitro and in vivo."exp physiol;90(1):53-59
[0454]
67.von jonquieres,g.,et al.(2016)."recombinant human myelin-associated glycoprotein promoter drives selective aav-mediated transgene expression in oligodendrocytes."front mol neurosci;9:13
[0455]
68.levitt,n.,briggs,d.,gil,a.,and proudfoot,n.j.(1989).definition of an efficient synthetic
[0456]
poly(a)site.genes dev.3,1019
–
1025.
[0457]
69.bailey rm,armao d,nagabhushan kalburgi s,gray sj.development of intrathecal aav9 gene therapy for giant axonal neuropathy.mol ther methods clin dev.2018feb15;9:160-171.
[0458]
现在将在以下编号的段落中描述本发明的实施方案:
[0459]
1.一种用于在有需要的受试者中治疗或预防与雪旺细胞相关的疾病的病毒载体,其中所述病毒载体包含可转录为第一多核苷酸的第一核酸序列,并且其中所述病毒载体是aav载体.
[0460]
2.用于段落1的病毒载体,其中所述第一多核苷酸的表达在施旺细胞特异性启动子、任选髓鞘特异性启动子的控制下。
[0461]
3.用于段落1或2的病毒载体,其中所述第一多核苷酸的表达在全长髓鞘蛋白零(mpz)启动子的控制下,其中所述全长启动子是全长大鼠或人髓鞘蛋白零启动子。
[0462]
4.用于段落1-3的病毒载体,其中所述第一多核苷酸的表达是在长度在100bp至1100bp之间的启动子的控制下,任选地其中所述启动子长度范围为200bp至900bp,长度为300bp至800bp,长度为400bp至700bp,任选地,其中所述启动子长度范围为500bp至600bp,任选地,其中所述启动子的长度为410bp。
[0463]
5.用于段落4的病毒载体,其中所述启动子是全长或最小髓鞘特异性启动子,任选最小髓鞘蛋白零(mpz)启动子,任选地其中所述启动子具有与seq id no.5或seq id no.22至少75%序列同源性或序列同一性,任选具有与seq id no.5或seq id no.22至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列。
[0464]
6.用于前述段落中任一段的病毒载体,其中所述载体具有转导雪旺氏细胞的能力。
[0465]
7.用于前述段落中任一段的病毒载体,其中所述载体不整合到宿主细胞的基因组中。
[0466]
8.用于前述段落中任一段的病毒载体,其中所述aav载体选自包括:aav9和aavrh10。
[0467]
9.用于段落8的病毒载体,其中aav载体是aav9。
[0468]
10.用于前述段落中任一段的病毒载体,其中所述第一多核苷酸编码并翻译成第一多肽或蛋白质。
[0469]
11.用于段落10的病毒载体,其中所述第一核酸包含:
[0470]
a)神经病相关基因的野生型或治疗上有益的序列,任选地选自包含以下任何一种基因或由以下任何一种基因组成的组:间隙连接β1(gjb1);sh3结构域和四肽重复序列2(sh3tc2);外周髓鞘蛋白22(pmp22);髓鞘蛋白零(mpz);早期生长反应2(egr2);神经节苷脂诱导分化相关蛋白1(gdap1);n-myc下游调节1(ndrg1)或与脱髓鞘神经病变和雪旺氏细胞功能障碍相关的其他基因;或
[0471]
b)具有与神经病相关基因的野生型序列至少75%序列同源性或序列同一性,任选地至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或具有96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列,例如以下基因之一:间隙连接β1(gjb1);sh3结构域和四肽重复序列2(sh3tc2);外周髓鞘蛋白22(pmp22);髓鞘蛋白零(mpz);早期生长反应2(egr2);神经节苷脂诱导分化相关蛋白1(gdap1);n-myc下游调节1(ndrg1)或与脱髓鞘神经病变和雪旺氏细胞功能障碍相关的其他基因;
[0472]
任选地,其中所述第一核酸包含具有与seq id no 6-12至少75%序列同源性或序列同一性,任选地与seq id no 6-12至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列。
[0473]
12.用于段落10或11的病毒载体,其中所述第一核酸包含野生型开放阅读框(orf)或cdna,其被转录成编码一个或多个多肽的第一多核苷酸,任选地选自包含以下或由以下组成的组:连接蛋白-32(cx32);sh3结构域和四肽重复序列2(sh3tc2);外周髓鞘蛋白22(pmp22);髓鞘蛋白零(mpz);早期生长反应2(egr2);神经节苷脂诱导分化相关蛋白1(gdap1);n-myc下游调节1(ndrg1)。
[0474]
13.用于段落10-11的病毒载体,其中所述第一核酸包含间隙连接β1(gjb1)基因的野生型开放阅读框(orf)。
[0475]
14.段落1-13任一项所述使用的病毒载体,其中所述载体能够驱动第一多核苷酸的表达,任选地驱动第一多肽的表达,任选地其中所述第一多肽是连接蛋白32(cx32)蛋白,任选地野生型cx32。
[0476]
15.段落1-10中任一项所述使用的病毒载体,其中所述第一多核苷酸编码以下的一种或多种:营养因子(例如bdnf、gdnf、nt-3、vegf)、再生因子(例如血管生成素、oct-6、egr2、sox-10)、生长因子(例如igf)。
[0477]
16.用于前述段落中任一段的病毒载体,其中所述病毒载体的施用导致来自所述第一多核苷酸的第一蛋白质的表达,其导致雪旺细胞的功能改进和/或髓鞘的形成增加。
[0478]
17.段落1-9的用途的病毒载体,其中所述第一多核苷酸不编码多肽,任选地其中所述第一多核苷酸是非编码rna。
[0479]
18.用于段落17的病毒载体,其中所述非编码rna是短发夹rna(shrna);微rna(mirna);引导rna(grna)。
[0480]
19.段落17或18中任一项的病毒载体,其中当病毒载体在靶生物体中时,非编码rna的表达导致靶多核苷酸的表达减少,任选地其中所述靶多核苷酸是位于靶生物体中的基因,任选地位于靶生物体的细胞中。
[0481]
20.用于段落19的病毒载体,其中所述靶生物体中靶多核苷酸的表达或过表达被认为与与雪旺细胞相关的疾病相关,任选地其中所述疾病是显性脱髓鞘神经病(cmt1),任选地其中所述靶多核苷酸是髓鞘蛋白零(mpz/p0)的突变等位基因并且与雪旺细胞相关的疾病是cmt1b,或其中靶多核苷酸是与cmt1相关的另一个显性基因。
[0482]
21.用于段落17-20中任一项的病毒载体,其中所述病毒载体的施用导致雪旺细胞功能改进和/或髓鞘形成增加。
[0483]
22.用于前述段落中任一段的病毒载体,其中与雪旺细胞相关的疾病导致雪旺细胞破坏和/或髓鞘形成减少。
[0484]
23.用于前述段落中任一段的病毒载体,其中所述疾病选自:charcot-marie-tooth疾病(cmt);易患压力性麻痹的遗传性神经病(hnpp);糖尿病和其他中毒性周围神经病;运动神经元疾病(mnd)。
[0485]
24.用于前述段落中任一项的病毒载体,其中所述疾病是charcot-marie-tooth疾病(cmt)。
[0486]
25.用于段落24的病毒载体,其中所述疾病选自:charcot-marie-tooth 1x型(cmt1x);charcot-marie-tooth 1a-1f型(cmt1a-1f);charcot-marie-tooth 4a-4h型(cmt4a-4h)。
[0487]
26.用于段落25的病毒载体,其中所述疾病是charcot-marie-tooth 1x型(cmt1x)。
[0488]
27.用于段落25的病毒载体,其中所述疾病是charcot-marie-tooth 4c型(cmt4c)。
[0489]
28.用于段落16或21的病毒载体,其中与治疗前受试者中雪旺氏细胞形成髓鞘时相比,雪旺氏细胞形成的髓鞘增加导致功能改进。
[0490]
29.用于段落28的病毒载体,其中与治疗前的受试者相比,雪旺细胞形成的髓鞘的增加导致以下任一或多个参数的改进:
[0491]
a)肌肉力量;
[0492]
b)坐骨神经传导速度;和/或
[0493]
c)血液生物标志物的反应。
[0494]
30.用于段落28或29的病毒载体,其中雪旺细胞对髓鞘形成的改进导致外周神经的髓鞘形成得到改进。
[0495]
31.前述段落中任一项所述使用的病毒载体,其中所述aav通过鞘内注射或静脉内注射施用到受试者,优选地其中所述aav通过鞘内注射施用。
[0496]
32.用于段落31的病毒载体,其中aav通过以下途径之一施用:腰椎鞘内注射;胸腔鞘内注射;宫颈鞘内注射。
[0497]
33.用于段落32的病毒载体,其中所述病毒载体通过腰椎鞘内注射施用。
[0498]
34.用于段落31-33的病毒载体,其中通过单次鞘内注射施用aav。
[0499]
35.用于前述段落中任一段的病毒载体,其中有需要的受试者是人类受试者。
[0500]
36.前述段落中任一段定义的病毒载体。
[0501]
37.已经用如前述段落中任一段定义的病毒载体转导的细胞,任选地其中所述细胞是雪旺细胞。
[0502]
38.一种最小髓鞘特异性启动子,其中所述最小髓鞘特异性启动子具有与seq id no.5或seq id no.22至少75%序列同源性或序列同一性,任选地与seq id no.5或seq id no.22至少80%,或82%,或84%,或86%,或88%,或90%,或92%,或94%,或96%,或97%,或98%,或99%,或100%序列同一性或序列同源性的序列。
[0503]
39.包含或由seq id no.5或seq id no.22的序列组成的最小髓鞘或由seq id no.5或seq id no.22中定义的序列组成或序列同源性的序列。
[0504]
40.包含第一核酸序列的多核苷酸构建体,所述第一核酸序列是雪旺细胞特异性启动子,任选地为髓鞘特异性启动子,任选地包含如段落38或39中定义的髓鞘蛋白零(mpz)启动子或最小髓鞘特异性启动子,可操作地连接到第二核酸序列,其中所述第二核酸被转录成第一多核苷酸,并且其中所述第二核酸序列:a)是基因的开放阅读框或cdna或其他元件;或b)转录为非编码rna。
[0505]
41.一种病毒载体,其包含根据段落38或39任一项所述的最小髓鞘特异性启动子或段落40所述的多核苷酸构建体。
[0506]
42.段落1-35任一项的病毒载体或段落36或41的病毒载体,其中所述载体具有转导雪旺氏细胞的能力。
[0507]
43.用于前述段落中任一段的病毒载体,其中所述载体不整合到宿主细胞的基因组中。
[0508]
44.根据段落42或43中任一项所述的病毒载体,所述病毒载体包含:
[0509]
a)aav,任选地,其中所述aav载体是aav9;
[0510]
b)包含aav9载体、髓鞘蛋白零(mpz)启动子和egfp报告基因的aav-mpz.egfp载体;
[0511]
c)包含aav9载体、髓鞘蛋白零(mpz)启动子和间隙连接β1(gjb1)基因的开放阅读框(orf)的aav9-mpz-gjb1载体;
[0512]
d)包含aav9载体、最小髓鞘蛋白零(minimpz)启动子和egfp报告基因的aav9-minimpz.egfp载体;
[0513]
e)包含aav9载体、全长人髓鞘蛋白零(hp0)启动子和间隙连接β1(gjb1)基因(seq id no.17)的开放阅读框(orf)的aav9-人mpz-gjb1载体;
[0514]
f)包含aav9载体、全长人髓鞘蛋白零(hp0)启动子和egfp报告基因(seq id no.19)的aav9-人类mpz-egfp载体;
[0515]
g)包含aav9载体、最小大鼠髓鞘蛋白零(mpz)启动子和sh3tc2基因(seq id no.20)的开放阅读框(orf)的aav9-minimpz-sh3tc2.myc.itr载体;
[0516]
h)aav9-human-minimpz-sh3tc2载体,包含aav9载体、人最小髓鞘蛋白零(hp0)启动子和sh3tc2基因(seq id no.21)的开放阅读框(orf);或
[0517]
i)包含aav9载体、人最小髓鞘蛋白零(hp0)启动子和egfp报告基因(seq id no.23)的aav9-human-minimpz-egfp载体。
[0518]
45.一种药物组合物,包含前述段落中任一段的病毒载体。
[0519]
46.段落45的药物组合物,其中所述组合物包含适量的病毒载体并且进一步包含
药学上可接受的载体和/或赋形剂。
[0520]
45.根据前述段落中任一段的病毒载体在制备用于治疗或预防与雪旺细胞相关的疾病的药物的方法中的用途,任选地其中所述疾病导致雪旺细胞破坏和/或减少髓鞘的形成,任选地其中所述疾病是charcot-marie-tooth疾病。
[0521]
46.用于crispr/cas9系统的根据前述段落中任一段的病毒载体或多核苷酸构建体,其中所述病毒载体或多核苷酸包含以下任一种或多种:
[0522]
a)编码靶向目标基因的单一引导rna(sgrna)的多核苷酸;
[0523]
b)编码cas9多肽的多核苷酸;
[0524]
c)编码目标多肽的多核苷酸。
[0525]
47.前述段落中任一段的病毒载体,所述病毒载体用于标记雪旺细胞的方法,例如用荧光蛋白标记,例如绿色荧光蛋白(gfp)或增强型绿色荧光蛋白(egfp),或另一种非荧光蛋白报告基因,任选地其中雪旺细胞的标记可以用于诊断与雪旺细胞相关的疾病的方法中。
[0526]
48.段落1-43任一项的病毒载体,用于其中诱导施旺细胞分化成替代细胞类型(例如少突胶质细胞、星形胶质细胞或神经元)的方法。
[0527]
49.段落1-43任一项的病毒载体,用于刺激雪旺细胞以支持有需要的受试者再生的方法,任选地在受伤或外伤后。
[0528]
50.一种用于预防或治疗与雪旺细胞相关的疾病、标记雪旺细胞或再生雪旺细胞的试剂盒,其中所述试剂盒包含以下的一种或多种:
[0529]
a)任何前述段落中定义的病毒载体;
[0530]
b)段落40定义的多核苷酸构建体;
[0531]
c)病毒载体;
[0532]
d)包含如段落40定义的多核苷酸构建体的病毒载体;
[0533]
e)药学上可接受的载体和/或赋形剂;
[0534]
f)一次性注射器,例如适用于腰椎鞘内注射的一次性注射器;
[0535]
g)使用说明。
[0536]
51.段落50的试剂盒,其中所述试剂盒包含多于一种如前述段落中任一段定义的病毒载体,任选地其中所述试剂盒包含2、3、4、5、6、7、8、9或10种由上述任一段落定义的不同的病毒载体。
[0537]
52.一种用于在有需要的受试者中治疗或预防与雪旺细胞相关的疾病的病毒载体,其中所述病毒载体包含可转录为第一多核苷酸的第一核酸序列,并且其中所述第一多核苷酸的表达在任选地包含或由seq id no.5或seq id no.22中定义的序列组成的最小髓鞘特异性启动子的控制下或由seq id no.5或seq id no.22中定义的序列组成,任选地其中所述病毒载体是aav载体。
[0538]
应当理解,对本文描述的当前优选实施例的各种改变和修改对于本领域技术人员来说将是显而易见的。可以在不脱离本发明的精神和范围且不削弱其预期优点的情况下进行此类改变和修改。因此,这些变化和修改旨在由以下权利要求涵盖。
