1.本发明涉及药物化学技术领域,具体涉及一种酚类衍生物及其制备方法与在制备具有抗炎和/或抗氧化作用的药物中的应用。
背景技术:
2.近些年随着人民居住环境的恶化,哮喘等呼吸道疾病的发病人数不断增加,导致人们的生活、工作受到严重影响。在诱发哮喘的诸因素中,大气污染物不仅能诱发、加重哮喘、鼻炎和急性支气管炎等,对肺功能也会造成严重的损伤。苯并芘(benzopyrene,bap)是多环芳烃化合物,是一种典型的环境污染物。bap来源广泛,包括香烟烟雾、熏烤油炸食品、工业废水以及受污染的大气等。研究显示,城市大气污染状况的加重与呼吸道疾病,尤其是哮喘的发病率有着直接的关系。
3.中药应用于哮喘的临床治疗,具有改善哮喘症状、提高哮喘患者肺功能以及减轻呼吸道炎症的作用。山楂是蔷薇科植物山里红(crataegus pinnatifida bge.var.major n.e.br.)或山楂(crataegus pinnatifida bge.)的成熟果实。目前,从山楂中分离并鉴定的化学成分包括总黄酮类、有机酸类、低聚原花青素类、三萜酸类及固醇和痕量的心脏活性胺等。药理研究结果显示,山楂具有降压、降糖、免疫调节、抗氧化、抗菌抗炎等多种作用。
4.目前鲜见有从山楂中分离出的化合物具有抗氧化以及抗炎作用的报道。因此,以山楂为原料,从中开发出具有抗氧化、抗炎作用的化合物具有重要的意义。
技术实现要素:
5.为了克服现有技术中存在的至少之一的技术问题,本发明提供了一种酚类衍生物;研究表明,所述的酚类衍生物具有抗氧化以及抗炎作用。
6.本发明所要解决的上述技术问题,通过以下技术方案予以解决:
7.本发明提供一种酚类衍生物,其具有式ⅰ、式ⅱ或式ⅲ所示的结构;
[0008][0009]
本发明通过大量实验研究,从山楂中分离得到具有式ⅰ、式ⅱ和式ⅲ所示全新结构
的酚类衍生物;研究表明,所述的酚类衍生物具有抗氧化以及抗炎作用。发明人进一步研究表明,式ⅱ和式ⅲ所示结构的酚类衍生物,其中的一个酚羟基与碳原子其形成了一个六元环,其与不含有六元环的式ⅰ所示结构的酚类衍生物相比,抗氧化以及抗炎作用有着大幅的提高;此外研究还表明,六元环的位置不同,酚类衍生物的抗氧化以及抗炎作用也不相同;研究表明,所述的六元环的位置靠近羰基的式ⅲ所示结构的酚类衍生物,其抗氧化以及抗炎作用要明显高于六元环的位置远离羰基的式ⅱ所示结构的酚类衍生物。
[0010]
本发明还提供上述酚类衍生物的制备方法,其包含如下步骤:
[0011]
(1)取山楂放入乙醇中,然后进行超声提取,将提取液浓缩后得山楂提取物;
[0012]
(2)将山楂提取物上大孔树脂柱;先用水洗脱除杂;再用体积分数为30%~60%的乙醇洗脱,收集体积分数为30%~60%的乙醇洗脱下来的流份,浓缩干燥后得大孔树脂洗脱部位;
[0013]
(3)将大孔树脂洗脱部位上硅胶柱,先用体积比为90~85:10~15的氯仿和甲醇组成的混合溶剂进行洗脱;然后再用体积比80~75:20~25的氯仿和甲醇组成的混合溶剂进行洗脱,收集体积比80~75:20~25的氯仿和甲醇组成的混合溶剂洗脱下来的流份,浓缩干燥后得硅胶洗脱部位;
[0014]
(4)将硅胶洗脱部位采用制备型hplc进行制备得式ⅰ、式ⅱ或式ⅲ所示结构的酚类衍生物。
[0015]
优选地,步骤(1)中所述的乙醇是体积分数为40%~70%的乙醇。
[0016]
最优选地,步骤(1)中所述的乙醇是体积分数为50%的乙醇。
[0017]
所述的乙醇是体积分数为40%~70%的乙醇,在本领域是指乙醇是体积分数为40%~70%的乙醇水溶液;在本文中,提及体积分数的乙醇均是至乙醇水溶液。
[0018]
优选地,步骤(1)中山楂和乙醇的用量比为1g:8~15ml。
[0019]
最优选地,步骤(1)中山楂和乙醇的用量比为1g:10ml。
[0020]
优选地,步骤(2)中,先用5倍柱体积的水洗脱除杂;再用3倍柱体积的体积分数为40%的乙醇洗脱,收集体积分数为40%的乙醇洗脱下来的流份,浓缩干燥后得大孔树脂洗脱部位。
[0021]
优选地,先用3倍柱体积的体积比为88:12的氯仿和甲醇组成的混合溶剂进行洗脱;然后再用3倍柱体积的体积比78:22的氯仿和甲醇组成的混合溶剂进行洗脱,收集体积比78:22的氯仿和甲醇组成的混合溶剂洗脱下来的流份,浓缩干燥后得硅胶洗脱部位。
[0022]
优选地,步骤(4)中制备型hplc的具体制备条件为:
[0023]
采用c18制备型液相色谱柱;以0.1%三氟乙酸水溶液为流动相a,以0.1%三氟乙酸的甲醇溶液为流动相b,流动相a:流动相b=83:17;检测波长为300~330nm,流速为1~3ml/min,进样量为50~300μl;收集9.5min、12.6min以及14.9min处色谱峰对应的流份,浓缩干燥后即得式ⅰ、式ⅱ或式ⅲ所示结构的酚类衍生物。
[0024]
发明人首次提供了一种从山楂中分离制备全新的式ⅰ、式ⅱ或式ⅲ所示结构的酚类衍生物的方法;该方法能够将式ⅰ、式ⅱ和式ⅲ所示结构的酚类衍生物浓缩至同一个洗过部位;然后通过一次hplc制备方法即可以制备得到,可以高效的制备得到式ⅰ、式ⅱ或式ⅲ所示结构的酚类衍生物;且制备得到的式ⅰ、式ⅱ或式ⅲ所示结构的酚类衍生物纯度高。
[0025]
本发明还提供一种提取物或组合物,其含有式ⅰ、式ⅱ和/或式ⅲ所示结构的酚类
衍生物。
[0026]
优选地,所述的提取物或组合物中,式ⅰ、式ⅱ和/或式ⅲ所示结构的酚类衍生物的重量百分比含量为1%~100%;
[0027]
优选地,提取物或组合物中,式ⅰ、式ⅱ和/或式ⅲ所示结构的酚类衍生物的重量百分比含量为10%~90%;如可以为20%、30%、40%、50%、60%、70%以及80%。
[0028]
由于式ⅰ、式ⅱ和/或式ⅲ所示结构的酚类衍生物具有抗炎和/或抗氧化作用;因此,本领域技术人员可以毫无意义的确定,含有式ⅰ、式ⅱ和/或式ⅲ所示结构的酚类衍生物都具有抗炎和/或抗氧化作用。
[0029]
本发明还提供一种上述酚类衍生物、提取物或组合物在制备具有抗炎和/或抗氧化作用的药物或食品或膳食补充剂中的应用。
[0030]
由于式ⅰ、式ⅱ和/或式ⅲ所示结构的酚类衍生物具有抗炎和/或抗氧化作用;因此,可以将由于式ⅰ、式ⅱ和/或式ⅲ所示结构的酚类衍生物用于制备具有抗炎和/或抗氧化作用的药物或食品或膳食补充剂中的应用。
[0031]
本发明还提供一种上述酚类衍生物、提取物或组合物在制备具有抗环境污染物导致的呼吸道上皮细胞氧化和/或炎性损伤作用的药物或食品或膳食补充剂中的应用。
[0032]
优选地,所述的环境污染物为苯并芘(benzopyrene,bap)。
[0033]
发明人进一步研究发现,式ⅰ、式ⅱ和/或式ⅲ所示结构的酚类衍生物尤其是对环境污染物导致的呼吸道上皮细胞氧化和/或炎性损伤具有最佳的抗氧化和/或抗炎作用。
附图说明
[0034]
图1为式ⅰ所示结构的酚类衍生物的hr-esi-ms图。
[0035]
图2为式ⅰ所示结构的酚类衍生物的uv图。
[0036]
图3为式ⅰ所示结构的酚类衍生物的ir图。
[0037]
图4为式ⅰ所示结构的酚类衍生物的1h nmr图。
[0038]
图5为式ⅰ所示结构的酚类衍生物的13c nmr图。
[0039]
图6为式ⅱ所示结构的酚类衍生物的hr-esi-ms图。
[0040]
图7为式ⅱ所示结构的酚类衍生物的uv图。
[0041]
图8为式ⅱ所示结构的酚类衍生物的ir图。
[0042]
图9为式ⅱ所示结构的酚类衍生物的1h nmr图。
[0043]
图10为式ⅱ所示结构的酚类衍生物的13c nmr图。
[0044]
图11为式ⅲ所示结构的酚类衍生物的hr-esi-ms图。
[0045]
图12为式ⅲ所示结构的酚类衍生物的uv图。
[0046]
图13为式ⅲ所示结构的酚类衍生物的ir图。
[0047]
图14为式ⅲ所示结构的酚类衍生物的1h nmr图。
[0048]
图15为式ⅲ所示结构的酚类衍生物的13c nmr图。
[0049]
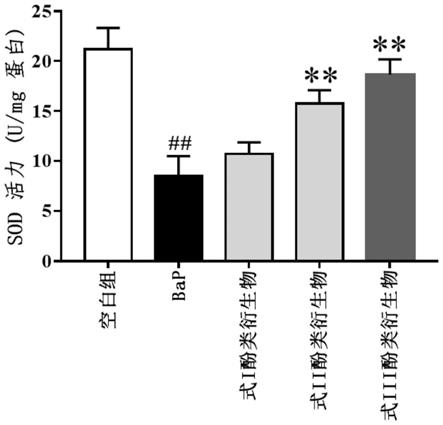
图16为本发明酚类衍生物对16-hbe细胞sod氧化酶活性的影响结果图。
[0050]
图17为本发明酚类衍生物对16hbe细胞中炎症因子tnf-α的影响结果图。
[0051]
图18为本发明酚类衍生物对16hbe细胞中炎症因子il-6的影响结果图。
[0052]
图19为本发明酚类衍生物对16hbe细胞中炎症因子il-1β的影响结果图。
具体实施方式
[0053]
以下结合具体实施例来进一步解释本发明,但实施例对本发明不做任何形式的限定。
[0054]
实施例1化合物的制备
[0055]
(1)取1kg山楂放入10l体积分数为50%的乙醇中,然后进行超声提取60min,将提取液浓缩后得山楂提取物;
[0056]
(2)将山楂提取物上大孔树脂柱;先用5倍柱体积的水洗脱除杂;再用3倍柱体积的体积分数为40%的乙醇洗脱,收集体积分数为40%的乙醇洗脱下来的流份,浓缩干燥后得大孔树脂洗脱部位;
[0057]
(3)将大孔树脂洗脱部位上硅胶柱,先用3倍柱体积的体积比为88:12的氯仿和甲醇组成的混合溶剂进行洗脱;然后再用3倍柱体积的体积比78:22的氯仿和甲醇组成的混合溶剂进行洗脱,收集体积比78:22的氯仿和甲醇组成的混合溶剂洗脱下来的流份,浓缩干燥后得硅胶洗脱部位;
[0058]
(4)将硅胶洗脱部位采用制备型hplc进行制备;制备型hplc的条件为:采用c18制备型液相色谱柱;以0.1%三氟乙酸水溶液为流动相a,以0.1%三氟乙酸的甲醇溶液为流动相b,流动相a:流动相b=83:17;检测波长为310nm,流速为2ml/min,进样量为150μl;收集9.5min、12.6min以及14.9min处色谱峰对应的流份,浓缩干燥后即得式ⅰ、式ⅱ和式ⅲ所示结构的酚类衍生物。
[0059]
式ⅰ所示结构的酚类衍生物:黄色油状物,hr-esi-ms m/z 337.1983[m+h]
+
(calcd for c
19h29
o5,337.2010)。uv(ch3oh)λ
max
:205,291nm。ir(kbr)ν
max
:2954,2871,1614,1585,1441,1369,1283,1159,1119,1092,979,886cm-1
。1h nmr及
13
c nmr数据总结于表1,最终鉴定为式ⅰ所示结构的酚类衍生物,命名为:1-(2,4-dihydroxy-5-(3-hydroxy-3-methylbutyl)-6-methoxy-3-(3-methylbut-2-en-1-yl)phenyl)ethan-1-one。
[0060]
式ⅱ所示结构的酚类衍生物:黄色油状物,hr-esi-ms m/z 341.1729[m+na]
+
(calcd for c
19h26
o4na,341.1723)。uv(ch3oh)λ
max
:206,221,293nm。ir(kbr)ν
max
:3446,2973,2936,1616,1589,1444,1368,1284,1187,1160,1120,1088,980cm-1
。1h nmr及
13
c nmr数据总结于表2,最终鉴定为式ⅱ所示结构的酚类衍生物;命名为:
[0061]
1-(7-hydroxy-8-(3-hydroxy-3-methylbutyl)-5-methoxy-2,2-dimethylchroman-6-yl)ethan-1-one。
[0062]
式ⅲ所示结构的酚类衍生物:黄色油状物,hr-esi-ms m/z 359.1825[m+na]
+
(calcd for c
19h28
o5na,359.1829)。uv(ch3oh)λ
max
:207nm。ir(kbr)ν
max
:3300,2991,2916,1625,1590,1499,1363,1273,1233,1149,1066,834,667cm-1
。1hnmr及
13
c nmr数据总结于表3,最终鉴定为式ⅲ所示结构的酚类衍生物;命名为:
[0063]
1-(5-hydroxy-7-methoxy-2,2-dimethyl-6-(3-methylbut-2-en-1-yl)chroman-8-yl)ethan-1-one。
[0064]
表1.式ⅰ所示结构的酚类衍生物的nmr数据
[0065][0066][0067]
表2.式ⅱ所示结构的酚类衍生物的nmr数据
[0068][0069]
表3.式ⅲ所示结构的酚类衍生物的nmr数据
[0070][0071]
实验例1
[0072]
取16hbe细胞(5
×
105细胞/孔)接种于6孔板,过夜;然后用bap(2.0μm)暴露2.0h,冷pbs清洗2遍,实验组加入含有待测化合物(待测化合物分别为式ⅰ、式ⅱ和式ⅲ所示结构的酚类衍生物,浓度为5μg/ml)的培养基培养12h;同时设置bap对照组(不加任何药物)和正常对照组;采用检测试剂盒,测量细胞内sod的活力。
[0073]
实验结果表明(见图16),bap暴露使16-hbe细胞内sod抗氧化酶的活性降低,相比于正常对照组降低了59.8%(p<0.01);这说明,bap暴露使16-hbe细胞产生了明显的氧化损伤。而实验组经式ⅰ、式ⅱ和式ⅲ所示结构的酚类衍生物处理后的bap暴露的16-hbe细胞,相比bap对照组,sod抗氧化酶的活性分别提高了25.9%(p<0.01)、85.8%(p<0.01)和118.9%(p<0.01)。
[0074]
这说明:本发明式ⅰ、式ⅱ和式ⅲ所示结构的酚类衍生物是通过提高抗氧化酶的活性减轻bap暴露导致的16-hbe细胞氧化损伤,从而起到抗氧化作用。
[0075]
从上述实验还可以看出,式ⅱ和式ⅲ所示结构的酚类衍生物其sod抗氧化酶的活性提高程度要远远高于式ⅰ所示结构的酚类衍生物;这说明:式ⅱ和式ⅲ所示结构的酚类衍生物,其中的一个酚羟基与碳原子其形成了一个六元环,其与不含有六元环的式ⅰ所示结构的酚类衍生物相比,抗氧化作用有着大幅的提高;上述实验结果还表明:六元环的位置不
同,酚类衍生物的抗氧化作用也不相同;研究表明,所述的六元环的位置靠近羰基的式ⅲ所示结构的酚类衍生物,其抗氧化作用要明显高于六元环的位置远离羰基的式ⅱ所示结构的酚类衍生物。
[0076]
实验例2
[0077]
取16hbe细胞(5
×
105细胞/孔)接种于6孔板,过夜;然后用bap(2.0μm)暴露2.0h,冷pbs清洗2遍,实验组加入含有待测化合物(待测化合物分别为式ⅰ、式ⅱ和式ⅲ所示结构的酚类衍生物,浓度为5μg/ml)的培养基培养12h;同时设置bap对照组(不加任何药物)和正常对照组;收集并测试培养液上清中相关炎症因子il-6,il-1β及tnf-α的含量。
[0078]
从图17~19实验数据中可以看出,bap暴露的16hbe细胞培养液上清中相关炎症因子il-6,il-1β及tnf-α的含量显著增加,相比于正常对照组,il-6,il-1β及tnf-α的含量增加218.3%(p<0.01),491.6%(p<0.01),784.0%(p<0.01),说明bap暴露会导致细胞严重的炎性损伤。而经式ⅰ所示结构的酚类衍生物处理的bap暴露的16hbe细胞,其能有效的提高16hbe细胞的存活率抑制bap暴露导致的il-6,il-1β及tnf-α的含量增加;这说明式ⅰ所示结构的酚类衍生物具有抗炎作用。此外,式ⅱ和式ⅲ所示结构的酚类衍生物与式ⅰ所示结构的酚类衍生物的相比,其能够进一步有效抑制bap暴露导致16hbe细胞炎症因子il-6,il-1β及tnf-α的含量显著增加;这说明:式ⅱ和式ⅲ所示结构的酚类衍生物,其中的一个酚羟基与碳原子其形成了一个六元环,其与不含有六元环的式ⅰ所示结构的酚类衍生物相比,抗炎作用有着大幅的提高;上述实验结果还表明:六元环的位置不同,酚类衍生物的抗炎作用也不相同;研究表明,所述的六元环的位置靠近羰基的式ⅲ所示结构的酚类衍生物,其抗炎作用要明显高于六元环的位置远离羰基的式ⅱ所示结构的酚类衍生物。
[0079]
实验例3
[0080]
取16hbe细胞(5
×
105细胞/孔)接种于6孔板,过夜;然后用bap(2.0μm)暴露2.0h,冷pbs清洗2遍,实验组加入含有待测化合物(待测化合物分别为式ⅰ、式ⅱ和式ⅲ所示结构的酚类衍生物,浓度为5μg/ml)的培养基培养12h;同时设置bap对照组(不加任何药物)和正常对照组;收集细胞annexin v-fitc/pi孵育,用流式细胞仪检测细胞存活率;检测结果见表4。
[0081]
表4化合物增强16hbe细胞抗bap暴露导致的炎性损伤活性
[0082][0083]
mean
±
sd(n=3),
#
表示与control组比较,
#
p《0.05,
##
p《0.01;
*
表示与bap组比较,
*
p《0.05,
**
p《0.01。
[0084]
从表4实验数据中可以看出,bap暴露的16hbe细胞其存活率仅仅为70.1%;这说明bap暴露会导致细胞损伤,进而诱发细胞凋亡。
[0085]
而经式ⅰ所示结构的酚类衍生物处理的bap暴露的16hbe细胞,其能有效的提高16hbe细胞的存活率;这说明式ⅰ所示结构的酚类衍生物具有抗炎作用。此外,式ⅱ和式ⅲ所示结构的酚类衍生物与式ⅰ所示结构的酚类衍生物的相比,其能够进一步大幅提高16hbe细胞的存活率。
