用于治疗cd33阳性恶性肿瘤的经cd33靶向性嵌合抗原受体修饰的t细胞
技术领域
1.本公开内容涉及白血病相关的cd33特异性嵌合抗原受体(car)工程化t细胞、配制方法和作为针对cd33阳性细胞有选择性的抗癌剂使用的方法。
2.发明背景
3.急性髓样白血病(aml)是成人中最常见的急性白血病,并具有最高的死亡率(budde et al.(2017)blood 130:811; et al.(2015)n engl j med 373:1136-52;schuster et al.(2017)n engl j med 377:2545-54)。cd33在87-98%的aml病例中的髓样母细胞(blasts)上表达(ehninger et al.(2014)blood cancer 4:e218;andrews rg et al.(1989)j exp med 169:1721-31)。cd33也在髓样衍生抑制细胞(mdsc)、白血病干细胞(lsc)和造血干细胞(hsc)上表达(elliot la et al.(2017)front immunol 8:86;walter rb et al.(2012)blood 119:6198-208)。目前原发性aml的治愈率为35%,并且随着年龄增长而降低;因此,用于aml患者,特别是复发性或难治性(r/r)aml患者的新疗法有迫切的未满足的需要。
4.发明概述
5.本文描述了使用cd33靶向性car t细胞(本文也称为cd33 car t细胞)治疗多种癌症,例如急性髓样白血病(aml)的方法。
6.本文描述的是编码包含嵌合抗原受体(car)的多肽的核酸分子,其中car包含与seq id no:30至少85%、90%、95%、96%、97%、98%、99%或100%相同的或与seq id no:31至少约85%、90%、95%、96%、97%、98%、99%或100%相同的氨基酸序列。还描述的是编码包含嵌合抗原受体(car)的多肽的核酸分子,其中car包含seq id no:30或seq id no:31的具有不超过5个(例如,1、2、3、4或5)单氨基酸变化的氨基酸序列。在某些实施方案中,氨基酸变化完全在以下序列
7.qvqlvqsgaevkkpgssvkvsckasgytftdynmhwvrqapgqglewigyiypynggtgynqkfkskatitadestntaymelsslrsedtavyycargrpamdywgqgtlvtvssggggsggggsggggsdiqmtqspsslsasvgdrvtitcrasesvdnygisfmnwfqqkpgkapklliyaasnqgsgvpsrfsgsgsgtdftltisslqpddfatyycqqskevpwtfgqgtkveik(seq id no:1)或以下序列
8.qvqlvqsgaevkkpgssvkvsckasgytftdynmhwvrqapgqglewigyiypynggtgynqkfkskatitadestntaymelsslrsedtavyycargrpamdywgqgtlvtvss(seq id no:32)或以下序列
9.divmtqspdslavslgeratmsckssqsilyssnqknylawyqqkpgqspklliywastresgvpdrfsgsgsgtdftltisslqaedvavyychqylssytfgqgtkleik(seq id no:33)内。
10.还描述了包含核酸分子的表达载体(例如,病毒载体或慢病毒载体)。还描述了由载体转导的或包含上述核酸分子的人t细胞群或nk细胞群。在各种实施方案中,细胞包含以下项或由以下项组成或基本上由以下项组成:中央记忆t细胞、初始(naive)记忆t细胞、泛t细胞、nk细胞或基本上消减了cd25+细胞和cd14+细胞的pbmc。
11.还描述了在患者中治疗白血病或癌症的方法,其包括施用由包含以上描述的核酸
分子的载体转导的自体或同种异体人t细胞群或nk群或包含本文所述核酸分子的t细胞群或nk细胞群,其中白血病包含表达cd33的细胞。在多个实施方案中:嵌合抗原受体局部或全身施用;表达cd33的细胞是癌性t细胞或t调节细胞;嵌合抗原受体通过单次或重复给药来施用;患者在自体或同种异体人t细胞群之前或与自体或同种异体人t细胞群结合施用低甲基化剂;低甲基化剂是dna甲基转移酶抑制剂;低甲基化剂选自5-氮杂胞苷和地西他滨(decitabine);癌症是选自下组的血液癌症:急性髓样白血病(aml);骨髓增生异常综合征;骨髓增殖性新生物;慢性髓样白血病(cml);和母细胞性浆细胞样树突细胞新生物。
12.还描述了在患有癌症(例如实体瘤)的患者中减少髓样衍生抑制细胞(mdsc)的方法,该方法包括向患者施用包含本文所述的核酸分子的免疫细胞。在一些情况下,mdsc为谱系阴性(lin-)、hla-dr阴性和cd33阳性。在一些情况下,本文所述的cd33 car表达细胞靶向mds母细胞和mdsc。在实施方案中,本文所述的cd33 car表达细胞用于治疗多发性骨髓瘤、慢性淋巴细胞白血病(cll)或实体恶性肿瘤诸如卵巢癌、结肠癌或乳腺癌。
13.还描述了制备cd33 car t细胞的方法,其包括:提供自体或同种异体人t细胞群或nk群并转导t细胞或nk细胞
14.本文描述了包含编码嵌合抗原受体(car)的核苷酸序列的核酸分子,其中嵌合抗原受体包含:靶向cd33的scfv、间隔区、跨膜域、41-bb共刺激域和cd3ζ信号传导域。
15.在各种实施方案中:跨膜域选自:cd4跨膜域或其具有1-5个氨基酸修饰的变体、cd8跨膜域或其具有1-5个氨基酸修饰的变体、cd28跨膜域或其具有1-5个氨基酸修饰的变体;间隔物包含20-150个氨基酸且位于scfv和跨膜域之间;跨膜域是cd4跨膜域或其具有1-5个氨基酸修饰的变体;跨膜域是cd4跨膜域;嵌合抗原受体包含选自以下的跨膜域:cd4跨膜域或其具有1-2个氨基酸修饰的变体、cd8跨膜域或其具有1-2个氨基酸修饰的变体、cd28跨膜域或其具有1-2个氨基酸修饰的变体;间隔区包含选自由seq id no:2-12或其具有1-5个氨基酸修饰的变体组成的组的氨基酸序列;间隔物包含igg铰链区;间隔物包含10-50个氨基酸;4-1bb共刺激域包含seq id no:24的氨基酸序列或其具有1-5个氨基酸修饰的变体;cd3ζ信号传导域包含seq id no:21的氨基酸序列;3至15个氨基酸的接头位于4-1bb共刺激域和cd3ζ信号传导域或其变体之间;car包含seq id no:30或31的氨基酸序列或其具有1-5个氨基酸修饰,例如1-5个单个氨基酸取代的变体;scfv包含seq id no:1的氨基酸序列;权利要求1的核酸分子。
16.本文还公开了:包含本文所述核酸分子的病毒载体;由包含本文所述的核酸分子的载体转导的人t细胞群(例如,包含中央记忆t细胞的群)。
17.本文还描述了在患者中治疗cd33阳性癌症(包括,例如,aml、r/raml、急性淋巴细胞白血病(all)、骨髓增生异常综合征(mds)、骨髓瘤、骨髓增殖性新生物、其他cd33
+
血液系统恶性肿瘤等等)的方法,其包括施用由包含本文所述的核酸分子的载体转导的自体或同种异体人t细胞群,其中癌症(或疾病或病症)包括表达cd33的细胞。在多个实施方案中:嵌合抗原受体局部或全身施用;表达cd33的细胞是癌性t细胞;嵌合抗原受体通过单次或重复给药来施用。
18.在各种实施方案中:嵌合抗原受体包含:cd33 scfv(例如,包含具有多达10个单个氨基酸取代的以下氨基酸序列的scfv:
19.qvqlvqsgaevkkpgssvkvsckasgytftdynmhwvrqapgqglewigyiypynggtgynqkfkska
titadestntaymelsslrsedtavyycargrpamdywgqgtlvtvssggggsggggsggggsdiqmtqspsslsasvgdrvtitcrasesvdnygisfmnwfqqkpgkapklliyaasnqgsgvpsrfsgsgsgtdftltisslqpddfatyycqqskevpwtfgqgtkveik(seq id no:1)。
20.还描述了携带表达cd33 car的载体的t细胞。在各种实施方案中:至少20%、30%或40%的转导的人t细胞是中央记忆t细胞;至少30%的转导的人t细胞是cd4+和cd62l+或cd8+和cd62l+。在各种实施方案中:人t细胞群包含表达嵌合抗原受体的载体,该嵌合抗原受体包含选自seq id no:30或31的氨基酸序列或其具有1-5个氨基酸修饰(例如,1或2)的变体氨基酸修饰(例如,取代);人t细胞群包括中央记忆t细胞(t
cm
细胞),例如至少20%、30%、40%、50%、60%、70%、80%的细胞是t
cm
细胞,或t细胞群包括中央记忆t细胞、初始t细胞和干中央记忆细胞(t
cm/scm/n
细胞)的组合,例如至少20%、30%、40%、50%、60%、70%、80%的细胞是t
cm/scm/n
细胞。在一些实施方案中,t细胞群包括cd4+细胞和cd8+细胞(例如,至少20%的cd3+t细胞是cd4+并且至少3%的cd3+t细胞是cd8+并且至少70、80或90%是cd4+或cd8+;至少15%、20%、25%、30%、35%、40%、50%、60%的细胞cd3+细胞是cd4+并且至少4%、5%、8%、10%、20个cd3+细胞是cd8+细胞)。在一些实施方案中,人t细胞群对患者是自体的。在一些实施方案中,人t细胞群对患者是同种异体的。
21.cd33靶向性car
22.本文所述的cd33靶向性car包括cd33靶向性scfv。在一些实施方案中,scfv包含通过柔性接头连接的以下氨基酸序列:
23.qvqlvqsgaevkkpgssvkvsckasgytftdynmhwvrqapgqglewigyiypynggtgynqkfkskatitadestntaymelsslrsedtavyycargrpamdywgqgtlvtvssggggsggggsggggsdiqmtqspsslsasvgdrvtitcrasesvdnygisfmnwfqqkpgkapklliyaasnqgsgvpsrfsgsgsgtdftltisslqpddfatyycqqskevpwtfgqgtkveik(seq id no:1)或包含以下序列
24.qvqlvqsgaevkkpgssvkvsckasgytftdynmhwvrqapgqglewigyiypynggtgynqkfkskatitadestntaymelsslrsedtavyycargrpamdywgqgtlvtvss(seq id no:32)和以下序列
25.divmtqspdslavslgeratmsckssqsilyssnqknylawyqqkpgqspklliywastresgvpdrfsgsgsgtdftltisslqaedvavyychqylssytfgqgtkleik(seq id no:33)。
26.有用的cd33 car可以由以下项组成或包含以下项:seq id no:30或31的氨基酸序列(缺少信号序列的成熟car),或者cd33 car可以由以下项组成或包含以下项:seq id no:30或31的氨基酸序列,之前是gmcsfra信号序列(seq id no:34)(具有gmcsfra信号序列的未成熟car;(mllllvtslllcelphpafllip;seq id no:34)。可以在具有可用于监测表达的额外序列,例如,t2a跳跃序列和截短的egfrt的情况下表达car。可以在具有可用于监测表达的额外序列,例如,t2a跳跃序列和截短的cd19t表达的情况下car。因此,car可以包含seq id no:30或31的氨基酸序列或由seq id no:30或31的氨基酸序列组成,或者可以包含以下项或由以下项组成:与seq id no:30或31至少95%、96%、97%、98%或99%相同的氨基酸序列。car可以包含以下项或由以下项组成:seq id no:30或31中任一个的具有多达1、2、3、4或5个氨基酸变化(优选保守氨基酸变化)的氨基酸序列。car可以包含靶向cd33的scfv,例如,其包含seq id no:1且具有多达1、2、3、4或5个氨基酸变化(优选保守氨基酸变化)的scfv或如下的scfv,其包含通过柔性接头连接的具有多达1、2、3、4或5个氨基酸变化(优选保守氨基酸变化)的seq id no:32和具有多达1、2、3、4或5个氨基酸变化(优选保守氨基酸
变化)的seq id no:33。
27.在一些实施方案中,编码氨基酸序列seq id no:1-34的核酸经密码子优化。在一些实施方案中,编码氨基酸序列seq id no:1-34的核酸未经密码子优化。
28.间隔物区
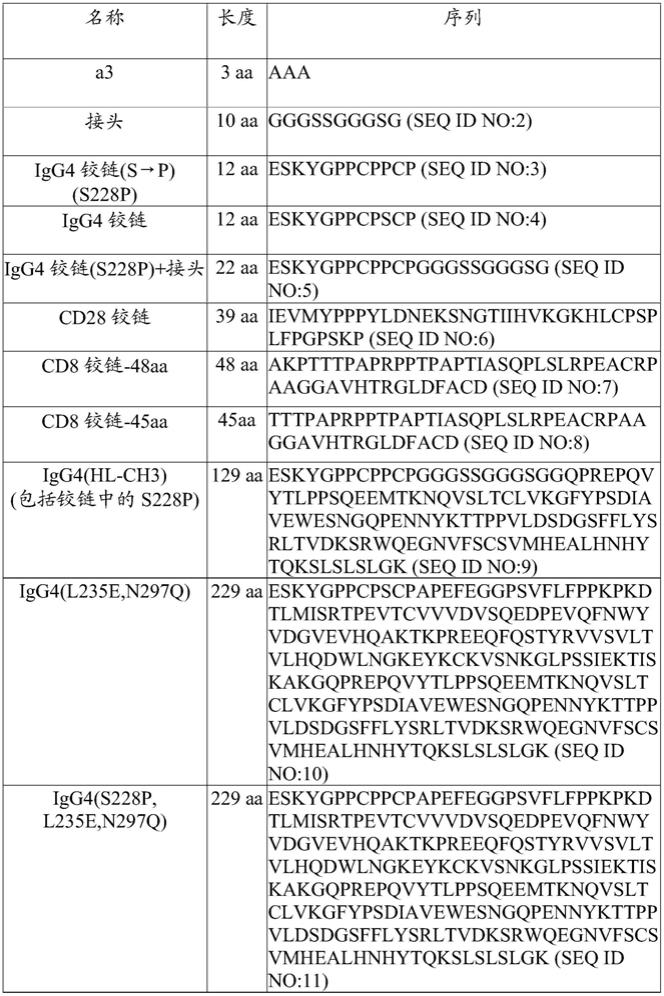
29.本文所述的car可以包括位于cd33靶向域(即,cd33靶向性scfv或其变体)和跨膜域之间的间隔物。可以使用多种不同的间隔物。它们中的一些包括人fc区的至少部分,例如人fc区的铰链部分或ch3域或其变体。下表1提供了可以用于本文所述的car中的各种间隔物。
30.表1:间隔物的示例
[0031][0032]
[0033]
一些间隔物区包括免疫球蛋白(例如,igg1、igg2、igg3、igg4)铰链区的全部或部分,即落入免疫球蛋白的ch1和ch2域之间的序列,例如igg4 fc铰链或cd8铰链。一些间隔物区包括免疫球蛋白ch3域或ch3域和ch2域两者。免疫球蛋白衍生序列可以包括一个或多个氨基酸修饰,例如1、2、3、4或5个取代,例如减少脱靶结合的取代。
[0034]
铰链/接头区还可包含具有序列eskygppcpscp(seq id no:4)或eskygppcppcp(seq id no:3)的igg4铰链区。铰链/接头区还可以包含序列eskygppcppcp(seq id no:3),接着是接头序列gggssgggsg(seq id no:2),接着是igg4 ch3序列gqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seq id no:12)。因此,整个接头/间隔物区可以包含序列:eskygppcppcpgggssgggsggqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seq id no:11)。在一些情况下,与seq id no:11相比,间隔物具有1、2、3、4或5个单氨基酸变化(例如,保守变化)。在一些情况下,igg4 fc铰链/接头区以减少由fc受体(fcr)的结合的方式在两个位置(l235e;n297q)突变。
[0035]
跨膜域
[0036]
多种跨膜域可以用于。表2包括合适的跨膜域的示例。在存在间隔物区的情况中,跨膜域(tm)位于间隔物区的羧基端。
[0037]
表2:跨膜域的示例
[0038][0039][0040]
共刺激域
[0041]
共刺激域可以是任何适合与cd3ζ信号传导域一起使用的域。在一些情况下,共信号传导域是4-1bb共信号传导域,其包括与krgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcel(seq id no:24)至少90%、至少95%、至少98%相同或与krgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcel(seq id no:24)相同的序列。在一些情况下,与seq id no:24相比,4-1bb共信号传导域具有5个氨基酸变化(优选保守)中的1、2、3、4个。
[0042]
共刺激域位于跨膜域和cd3ζ信号传导域之间。表3包括合适的共刺激域的示例以及cd3ζ信号传导域的序列。
[0043]
表3:cd3ζ域和共刺激域的示例
[0044][0045][0046]
在各种实施方案中:共刺激域选自下组:表3中描述的共刺激域或其具有1-5个(例如,1或2)个氨基酸修饰的变体、cd28共刺激域或其具有1-5(例如,1或2)个氨基酸修饰的变体、4-1bb共刺激域或其具有1-5(例如,1或2)个氨基酸修饰的变体和ox40共刺激域或其具有1-5(例如,1或2)个氨基酸修饰的变体。在某些实施方案中,存在4-1bb共刺激域或其具有1-5(例如,1或2)个氨基酸修饰的变体。在一些实施方案中,有两个共刺激域,例如cd28共刺激域或其具有1-5(例如,1或2)个氨基酸修饰(例如,取代)的变体和4-1bb共刺激域或其具有1-5(例如,1或2)个氨基酸修饰(例如,取代)的变体。在各种实施方案中,1-5(例如,1或2)个氨基酸修饰是取代。共刺激域是cd3ζ信号传导域的氨基端并且由2-10个,例如3个氨基酸(例如ggg)组成的短接头可以置于共刺激域和cd3ζ信号传导域之间。
[0047]
cd3ζ信号传导域
[0048]
cd3ζ信号传导域可以是适合与cd3ζ信号传导域一起使用的任何域。在一些情况下,cd3ζ信号传导域包括与以下项至少90%、至少95%、至少98%相同或与以下项相同的序列:
[0049]
rvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr(seq id no:21)。在某些情况下,与seq id no:21相比,cd3ζ信号传导具有5个氨基酸变化(优选保守)中的1、2、3、4个。
[0050]
截短的egfr和截短的cd19
[0051]
cd3ζ信号传导域之后可以是核糖体跳跃序列(例如,legggegrgslltcgdveenpgpr;seq id no:27)和截短的egfr,其具有与以下项至少90%、至少95%、至少98%相同或与以下项相同的序列:
[0052]
lvtslllcelphpaflliprkvcngigigefkdslsinatnikhfknctsisgdlhilpvafrgdsfthtppldpqeldilktvkeitgflliqawpenrtdlhafenleiirgrtkqhgqfslavvslnitslglrslkeisdgdviisgnknlcyantinwkklfgtsgqktkiisnrgensckatgqvchalcspegcwgpeprdcvscrnvsrgrecvdkcnllegeprefvenseciqchpeclpqamnitctgrgpdnciqcahyidgphcvktcpagvmgenntlvwkyadaghvchlchpnctygctgpglegcptngpkipsiatgmvgalllllvvalgiglfm(seq id no:28)。在一些情况下,与seq id no:28相比,截短的egfr具有5个氨基酸变化(优选保守)中的1、2、3、4个。
[0053]
或者,cd3ζ信号传导域之后可以是核糖体跳跃序列(例如,legggegrgslltcgdveenpgpr;seq id no:27)和截短的cd19r,其具有与以下项至少90%、至少95%、至少98%相同或与以下项相同的序列:
[0054]
mppprllffllfltpmevrpeeplvvkveegdnavlqclkgtsdgptqqltwsresplkpflklslglpglgihmrplaiwlfifnvsqqmggfylcqpgppsekawqpgwtvnvegsgelfrwnvsdlgglgcglknrssegpsspsgklmspklyvwakdrpeiwegeppcvpprdslnqslsqdltmapgstlwlscgvppdsvsrgplswthvhpkgpksllslelkddrpardmwvmetglllprataqdagkyychrgnltmsfhleitarpvlwhwllrtggwkvsavtlaylifclcslvgilhlqralvlrrkr(seq id no:26)。
[0055]
氨基酸修饰是指蛋白质或肽序列中的氨基酸取代、插入和/或缺失。“氨基酸取代”或“取代”是指用另一种氨基酸替换亲本肽或蛋白质序列中特定位置处的氨基酸。可以进行取代,从而以非保守方式(即,通过将密码子从属于具有特定大小或特征的氨基酸分组的氨基酸改变为属于另一个分组的氨基酸)或以保守方式(即,通过将密码子从属于具有特定大小或特征的氨基酸分组的氨基酸改变为属于相同分组的氨基酸)改变所得蛋白质中的氨基酸。此类保守变化通常导致所得蛋白质的结构和功能中的较少变化。以下是各种氨基酸分组的实例:1)具有非极性r基团的氨基酸:丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、色氨酸、甲硫氨酸;2)具有不带电荷的极性r基团的氨基酸:甘氨酸、丝氨酸、苏氨酸、半胱氨酸、酪氨酸、天冬酰胺、谷氨酰胺;3)具有带电荷的极性r基团的氨基酸(在ph6.0下带负电荷):天冬氨酸、谷氨酸;4)碱性氨基酸(在ph6.0下带正电荷):赖氨酸、精氨酸、组氨酸(在ph6.0下)。另一分组可以是那些具有苯基的氨基酸:苯丙氨酸、色氨酸和酪氨酸。
[0056]
在某些情况下,cd33 car可以使用载体产生,其中car开放阅读框之后是t2a核糖体跳跃序列和截短的egfr(egfrt),其缺少细胞质信号传导尾。在这种排列中,egfrt的共表达提供了惰性、非免疫原性表面标志物,其容许获得基因修饰细胞的准确测量,并能够进行基因修饰细胞的阳性选择,以及过继转移后体内治疗性t细胞的高效细胞追踪。高效控制增殖以避免细胞因子风暴和脱靶毒性是t细胞免疫治疗成功的重要障碍。在治疗相关毒性的情况下,掺入cd33 car慢病毒载体中的egfrt可以起自杀基因的作用以消融car+t细胞。
[0057]
本文所述的car可以通过本领域已知的任何手段产生,但优选使用重组dna技术产生。可以通过方便的本领域已知的分子克隆标准技术(基因组文库筛选、重叠pcr、引物辅助连接、定点诱变等)制备编码嵌合受体的几个区域的核酸并组装成完整的编码序列。所得编码区优选插入表达载体并用于转化合适的表达宿主细胞系,优选t淋巴细胞,并且最优选自
体t淋巴细胞。
[0058]
从患者分离的各种t细胞亚组可以用用于表达car的载体转导。中央记忆t细胞是一种有用的t细胞亚组。通过使用例如设备免疫磁性选择表达期望受体的细胞来选择cd45ro+/cd62l+细胞,可以从外周血单个核细胞(pbmc)中分离中央记忆t细胞。富含中央记忆t细胞的细胞可以用抗cd3/cd28激活,用例如指导cd33 car以及用于体内检测、消融和潜在的体外选择的非免疫原性表面标志物表达的慢病毒载体转导。活化/遗传修饰的cd33中央记忆t细胞可以在体外用il-2/il-15扩增,然后冷冻保存。制备car t细胞的额外方法可以在pct/us2016/043392中找到。
[0059]
在另一方面,cd33 car表达细胞是免疫效应物细胞,诸如t细胞或nk细胞,该细胞携带外源性rna分子,例如体外转录的rna或合成rna,其包含编码本文所述car分子的核酸分子。
[0060]
除非另有定义,本文使用的所有技术和科学术语与本发明所属领域的普通技术人员通常理解的含义相同。本文描述了用于本发明的方法和材料;也可以使用本领域已知的其他合适的方法和材料。材料、方法和示例仅是说明性的而意图是限制性的。出于任何和所有目的,本文提及的所有出版物、专利申请、专利、序列、数据库条目和其他参考文献均通过引用整体并入。如有冲突,将以本说明书(包括定义)为准。
[0061]
本发明的其他特征和优点将从以下详细描述和附图以及权利要求书中显而易见。
[0062]
附图简述
[0063]
图1显示了描绘代表性cd33 car构建体的示意图。
[0064]
图2a-2c显示了cd33(cd8)car t细胞实验的结果,其中egfrt用作追踪标志物并且其表达贯穿13天培养持续时间是稳定的。通过流式细胞术对模拟物(mock)(未转导;图2a)和cd33 car t细胞(图2b)评估egfr表达以检测car的表达。模拟物和cd33 car t细胞在离体培养期间均展现出稳健的扩增(图2c)。
[0065]
图3显示了人aml细胞系上的cd33表达。人伯基特(burkitt)淋巴瘤细胞系raji用作阴性对照。
[0066]
图4a-4c显示了cd33(cd8)car t细胞针对表达cd33的aml细胞系的效应物功能和杀伤活性。图4a显示了使用2:1的模拟物或cd33 car t细胞相对于aml细胞的e:t比的脱粒测定法的结果。图4b显示了使用1:1的模拟物或cd33 car t细胞相对于aml细胞的e:t比的细胞内ifn-γ染色测定法的结果。图4c显示了使用1:5、1:10和1:20的模拟物或cd33 car t细胞相对于aml细胞的e:t比的再攻击(rechallenge)测定法的结果。raji细胞系用作阴性对照。
[0067]
图5显示了使用具有molm-14-ffluc细胞系(具有高cd33表达水平的aml细胞系)的nod-scid-il2rg
null
(nsg)异种移植物模型的代表性体内研究。
[0068]
图6a-6b显示了cd33(cd8)car t细胞在体内杀死表达cd33的肿瘤系的能力。图6a显示,与3
×
106个模拟t细胞或未处理组相比,3
×
106个cd33 car t细胞在体内显著降低了白血病负荷。图6b显示,与3
×
106个模拟t细胞或未处理组相比,3
×
106个cd33 car t细胞在体内显著延长了总存活。
[0069]
图7显示了在100nm地西他滨或dmso存在下连续2天的aml细胞系上的cd33表达。raji细胞系用作阴性对照。
[0070]
图8显示了描绘地西他滨联合cd33(cd8)car t细胞的体外杀伤活性的示意图。用10nm地西他滨或dmso处理aml细胞系连续2天,然后用cd33(cd8)car或模拟t细胞以1:50的e:t比处理。再48小时后,使用流式细胞术测定各组中的杀伤活性。raji细胞系用作阴性对照。
[0071]
图9a-9b显示了地西他滨或dmso联合cd33(cd8)car或模拟t细胞后,残留aml细胞上程序性死亡配体1(pd-l1)和c型凝集素样分子1(cll-1)表达的平均荧光强度(mfi)。raji细胞系用作阴性对照。
[0072]
图10显示了使用接受了地西他滨联合cd33 car t细胞疗法的具有molm-14-ffluc的nsg异种移植物模型的代表性体内研究。
[0073]
图11a-11b显示了地西他滨和cd33(cd8)car t细胞在体内的组合功效的结果。图11a显示0.5mg/kg/d
×
5d地西他滨,然后1
×
106个cd33 car t细胞,在体内显著降低了白血病负荷。图11b显示0.5mg/kg/d
×
5d地西他滨和1
×
106个cd33 car t细胞的联合处理在体内显著延长了总存活。
[0074]
图12显示幸免于用10nm地西他滨和1:50e:t比的cd33(cd8)car t细胞处理的残留aml细胞显著增加了pd-l1表达水平。
[0075]
图13显示抗pd-1抗体(10μg/ml)显著增强了1:75的e:t比下的cd33(cd8)car t细胞的抗aml功效。
[0076]
图14a-14b显示了cd33 cd8 car(a;seq id no:30)和cd33 eq car(b;seq id no:31)的带注释的氨基酸序列。交替的下划线指示各种组分。
[0077]
图15a-15b显示了以下各项的带注释的核酸和相应氨基酸序列:(a)cd33 cd8 car,之前是gmcsr信号序列以及随后是t2a跳跃序列和egfrt(seq id no:35(核酸)和seq id no:36(氨基酸));和(b)cd33 eq car,之前是gmcsr信号序列以及随后是t2a跳跃序列和egfrt(seq id no:35(核酸)和seq id no:36(氨基酸))。每个核酸序列的密码子优化部分以粗体显示。
[0078]
发明详述
[0079]
在本公开中,描述了具有人源化抗人cd33 scfv抗原结合域和在一些实施方案中,4-1bb胞内共刺激信号传导域的car的产生和抗肿瘤功效。cd33 car t细胞针对表达cd33的人癌系展现出有力的抗原依赖性细胞毒性。cd33 car t细胞在人白血病/淋巴瘤鼠肿瘤模型中的腹膜内或静脉内体内递送赋予了抗原阳性疾病的消除和总存活的延长。
实施例
[0080]
在以下实施例中进一步描述本发明,实施例不限制权利要求书中描述的本发明的范围。
[0081]
实施例1:含有不同接头的cd33 car t细胞的构建
[0082]
以下描述的研究显示cd33 car可以在原代t细胞上稳定表达。
[0083]
设计了多个cd33靶向性car构建体。所有构建体都表达相同的经密码子优化的、人源化的cd33单链可变片段。在一些实施方案中,car构建体还包括cd4跨膜域(tm)、41bb共刺激域、cd3ζ域。在一些实施方案中,car构建体还包括cd8跨膜域(tm)、41bb共刺激域、cd3ζ域。cd33 car的代表性示意图显示在图1中。car与截短的egfr共表达,所述截短的egfr充当
用car构建体成功转导细胞的标志物。在一些实施方案中,cd33 car构建体在它们的接头和跨膜域中不同。不受理论束缚,构建体的细胞外部分的不同长度可以提供car结合抗原和在抗原结合后传递活化信号的能力的差异。这些差异也可导致cd33表达肿瘤细胞的差异杀伤。
[0084]
图14a描绘了cd33 car的氨基酸序列,其包含靶向cd33的scfv、cd8铰链(间隔物)、cd8跨膜域、41-bb共刺激域,通过ggg接头连接至cd3ζ刺激域(seq id no:30)。图14b描绘了cd33 car的氨基酸序列,其包含靶向cd33的scfv、igg4间隔物(igg4(s228p、l235e、n297q))、cd4跨膜域、41-bb共刺激域,通过ggg接头连接至cd3ζ刺激域(seq id no:31)。
[0085]
使用cd33 car慢病毒转导消减了cd14+和cd25+细胞的人健康供体衍生的外周血单个核细胞(dpbmc)、t(n/mem)细胞、泛t细胞的,如先前所述(priceman sj,gerdts ea,tilakawardane d,kennewick kt,murad jp,park ak,jeang b,yamaguchi y,yang x,urak r,weng l,chang wc,wright s,pal s,reiter re,wu am,brown ce,forman sj.co-stimulatory signaling determines tumor antigen sensitivity and persistence of car t cells targeting psca+metastatic prostate cancer.oncoimmunology.2018;7(2):e1380764),以及其他细胞类型,诸如富集的t细胞(easysep human t cell isolation kit.stemcell technologies)。使用egfrt作为追踪标志物,流式细胞术用于显示car表达,如上所述。代表性的cd33 car构建体在t细胞中稳定表达(图2a-2c)。转导细胞后7天,细胞用抗egfr进行染色以标记cd33 car构建体的成功掺入。cd33(cd8)car在转导后第15天稳定表达(图2c)。
[0086]
实施例2:aml细胞系中的cd33表达
[0087]
以下描述的研究检查了各种aml细胞系上的cd33表达。
[0088]
如图3所示,cd33表达在molm-14和thp-1细胞系中最高。kg-1a细胞系展现出中等的cd33表达。cd33表达在raji细胞系中最低。
[0089]
实施例3:cd33 car t细胞在体外展现出有力和特异性的细胞杀伤和效应物功能
[0090]
为了确定cd33 car t细胞是否表现出针对cd33阳性癌细胞的选择性效应物功能和杀伤活性,使cd33 car t细胞在cd33阳性或cd33阴性癌细胞存在的情况下生长。然后,量化cd107a脱粒水平、细胞内ifn-γ染色和杀死的癌性细胞百分比。所用测定法的示意图示于图4中。
[0091]
对于cd107a脱粒测定法,将模拟物或cd33 car t细胞与靶细胞以2:1的e:t比在补充有golgi stop和cd107a抗体的完全x-vivo培养基中共培养6小时,然后进行流式细胞术。cd33阳性aml细胞系是molm-14、thp-1和kg-1a。使用的cd33阴性细胞系是raji(图4a)。对于细胞内ifn-γ染色测定法,将模拟物或cd33 car t细胞与靶细胞以1:1的e:t比在完全x-vivo培养基中共培养4-6小时。然后向培养物补充golgi plug用于过夜温育。接下来,将细胞固定、透化、用ifn-γ抗体染色,并进行流式细胞术(图4b)。对于再攻击测定法,将模拟物或cd33 car t细胞与靶细胞以1:5、1:10和1:20的e:t比共培养48小时。48小时后,我们将额外的肿瘤细胞添加到共培养孔中,达到1:5、1:10或1:20的e:t,重复48小时温育,并将额外的肿瘤细胞添加到共培养孔中,达到1:5、1:10或1:20的e:t。再48小时后,使用流式细胞术测定肿瘤细胞的%特异性裂解(图4c)。
[0092]
与cd33阴性raji细胞系相比,cd33(cd8)car t细胞显示出有力和特异性的cd107a
脱粒水平、细胞内ifn-γ染色和针对cd33阳性aml细胞系的杀伤活性(图4a-4c)。
[0093]
实施例5:验证在小鼠模型中体内递送的cd33 car t细胞展现出有力的抗肿瘤活性并赋予小鼠以延长的寿命
[0094]
为了评估cd33 car t细胞在molm-14模型中选择性靶向cd33阳性细胞的体内功效,递送cd33 car t细胞并随时间评估肿瘤大小和存活。
[0095]
molm-14细胞经慢病毒转导以表达萤火虫萤光素酶(ffluc),从而允许通过非侵入性光学成像追踪肿瘤生长。在肿瘤静脉内注射后6天,通过全身性静脉内注射(i.v.)递送用模拟物或cd33 car t细胞(3x106)处理小鼠(图5)。在经由静脉内递送用cd33(cd8)car t细胞处理的小鼠中观察到迅速的抗肿瘤作用,在处理后1-2周达到最大抗肿瘤响应(图6a)。小鼠中的抗肿瘤响应可持续3-4周。cd33(cd8)car t细胞的递送显著延长了小鼠的存活(图6b)。
[0096]
实施例6:地西他滨在体外增强了cd33 car t细胞介导的aml杀伤
[0097]
地西他滨是常用于aml治疗的低甲基化剂(hma)。我们首先用100nm地西他滨或dmso处理aml细胞系连续2天。raji细胞系用作阴性对照。我们观察到地西他滨处理导致aml细胞上cd33表达的上调(图7)。
[0098]
我们假设地西他滨可以增强cd33 car t细胞介导的aml杀伤。对于体外联合研究,用10nm地西他滨或dmso处理aml细胞系连续2天,然后用cd33(cd8)car或模拟t细胞以1:50的e:t比处理。再48小时后,使用流式细胞术量化每组中的杀伤百分比(%)。在使用aml细胞作为靶标的体外实验中,在用地西他滨然后用cd33 car t细胞处理的组中观察到强健的杀伤(图8)。
[0099]
我们进一步检测了幸免于用地西他滨联合cd33 car t细胞处理的残留aml细胞上pd-l1和cll-1表达的mfi。体外联合处理后,pd-l1(图9a)和cll-1(图9b)的表达水平显著增加。
[0100]
实施例7:地西他滨在体内改善了cd33 car t细胞的抗白血病功效
[0101]
在第0天用1
×
106个molm-14-ffluc细胞i.v.注射nsg小鼠。从第1天到第5天,通过腹膜内(i.p.)注射向它们施用0.5mg/kg/d地西他滨或pbs连续5天。在第6天,通过i.v.注射向小鼠施用1
×
106个cd33(cd8)car(seq id no:30)或模拟t细胞(图10)。
[0102]
与体外发现一致,地西他滨联合cd33 car t细胞在体内显著降低了白血病负荷(图11a)并延长了总存活(图11b)。
[0103]
实施例8:pd-1/pd-l1阻断增强了cd33 car t细胞功效
[0104]
靶向程序性死亡1(pd-1)/pd-l1的检查点阻断参与了对基于免疫的疗法的耐受性机制。幸免于10nm地西他滨和1:50e:t比的cd33(cd8)car(seq id no:30)t细胞处理的残留aml细胞展现出显著升高的pd-l1表达(图12)。发现抗pd-1抗体(10μg/ml)显著增强了1:75的e:t比下的cd33(cd8)car(seq id no:30)t细胞的抗aml功效(图13)。
[0105]
其他实施方案
[0106]
应当理解,虽然本发明已经结合其详细描述进行了描述,但前述描述旨在说明而非限制本发明的范围,本发明的范围由所附权利要求书的范围限定。其他方面、优势和修改在所附权利要求书的范围内。
[0107]
出于任何和所有目的,所有参考文献以其整体并入本文。
