ii-3-1~fr.c-ii-3-10),其中馏分fr.c-ii-3-4再经过半制备型hplc色谱,以乙腈/水洗脱,分离纯化得到化合物1;馏分fr.c-iv洗脱得到的馏分fr.c-iv-4经制备型hplc,以甲醇/水洗脱,得到14个馏分(fr.c-iv-4-1~fr.c-iv-4-14),馏分fr.c-iv-4-10再经过半制备型hplc色谱,以乙腈/水洗脱,分离纯化得到化合物2。
13.上述制备方法,其中:
14.步骤(1)中二氯甲烷-甲醇的梯度为:100:1~1:1(v/v)。
15.步骤(2)中乙醇水的梯度洗脱浓度为:20%,40%,60%,90%。
16.步骤(3)中乙醇水的梯度洗脱浓度为:20%,40%,60%,80%,90%。
17.步骤(4)中石油醚/乙酸乙酯为100:1~1:2(v/v),制备液相甲醇/水的比例为85:15(v/v),半制备液相乙腈/水的比例为70:30(v/v)。
18.所得的化合物1和2经过系统结构鉴定,结果如图1-17及如下内容所示:
19.化合物1,无色晶体(ch3oh);[α]2
d 0-29.1(c 0.10,ch3oh),根据其hresims给出分子离子峰[m+h]
+
m/z 609.2678(calcd for c
34h41o10
,609.2694),确定分子式为c
34h40o10
,不饱和度15。uv光谱给出223nm处有明显吸收峰,uv(ch3oh)λ
max
(logε):225nm。
[0020]1h nmr(600mhz,cdcl3)谱的低场区中存在十个芳香质子信号δ8.01(1h,m),7.92(2h,m),7.55(1h,m),7.49(1h,m),7.43(2h,t,j=7.8hz),7.38(2h,t,j=7.8hz),提示该化合物存在两个单取代的苯环;一组末端双键上的质子信号δ5.16(1h,s),5.17(1h,s);4个连氧次甲基质子信号δ6.02(1h,dd,j=3.0hz),4.57(1h,d,j=5.1hz),4.09(1h,dd,j=9.9,2.1hz),3.56(1h,s);1对连在季碳上的羟甲基质子信号4.74(1h,d,j=12.7hz),δ4.31(1h,d,j=12.7hz)。高场区存在1个连在季碳上的甲基δ1.88(3h,s),2个连在叔碳上的甲基δ1.01(3h,d,j=6.5hz),0.95(3h,d,j=7.2hz)。
13
c nmr(150mhz,cdcl3)谱中显示有34个碳信号,其中两个苯甲酰氧基上的羰基碳信号δ167.1,166.4;一对末端双键碳信号δ145.1,114.2;两组单取代苯环上的碳信号δ133.4,133.2,130.0
×
3,129.9
×
2,129.5,128.6
×
2,128.5
×
2。同时,瑞香烷型二萜原酸酯δ117左右的特征季碳信号消失,说明该化合物的原酸酯的氧环开裂。在高场区,存在3个甲基碳信号δ19.2,15.6,15.8。通过以上核磁数据判断该化合物为具有两个苯甲酰基取代的瑞香烷型二萜类化合物。根据在该化合物的hmbc谱中存在δ6.02(h-14)到δ167.1(c-1')以及δ4.74和4.31(h
2-20)到δ167.1(c-1”)的相关,确定了两个苯甲酰基基团分别连接在该化合物的c-14和c-20位。综上分析可确定该化合物的平面结构。
[0021]
在noesy光谱中,h-10/h-2、h-10/h-3和h-10/h-5的相关表明h-2、h-3、h-5和h-10是在β平面上,而h-7和h-20的相关也表明h-7也位于β面。此外,h-16a/h-8和h-16b/h-14的相关证实h-8和h-14也是位于β平面上。以此确定了化合物1的相对构型。化合物1的绝对构型确定是通过计算和实测ecd比较的方法进行确定。最终将其确定为2s,3s,4r,5s,6r,7s,8s,9r,10s,11r,13r,14r。同时对化合物1进行单晶培养,并通过x单晶衍射进一步证实了1的绝对构型。经scifinder数据库检索,化合物1为未见报道的新化合物,命名为yuanhuakine a。
[0022]
化合物2,白色无定形粉末(ch3oh);[α]2
d 0-7.2(c 0.10,ch3oh);uv(ch3oh)λ
max
(logε):265nm;其分子式为c
30h46
o9,hresims给出m/z 551.3211[m+h]
+
(calcd for c
30h47
o9,551.3215)。1h nmr(600mhz,cdcl3)谱中低场区存在一组末端双键上的质子信号δ5.11(1h,
s),5.14(1h,s)。4个连氧次甲基质子信号δ5.22(1h,d,j=9.5hz),5.05(1h,d,j=7.5hz),4.13(1h,s),3.67(1h,d,j=3.4hz);1对连在季碳上的羟甲基质子信号δ4.10(1h,d,j=11.4hz),3.52(1h,d,j=11.4hz)。在高场区存在3甲基氢信号δ1.82(3h,s),0.89(3h,m),0.96(3h,d,j=7.0hz)。
13
c nmr(150mhz,cdcl3)谱中显示一个羰基碳信号δ168.1(c-1
′
);一对末端双键碳信号δ144.7(c-15),115.1(c-16)。结合该化合物1h,
13
c nmr谱,判断其存在一个(2e,4e)-decatrienoyl基团。在高场区中存在3个甲基碳信号为δ19.2(c-17),15.5(c-19),14.1(c-18)。通过
13
c nmr中显示一个δ91.9的连氧碳信号,表明化合物2应为4,7位成氧环的瑞香烷型二萜类化合物。通过hmbc谱中存在δ5.22(h-3)与δ168.1的相关,证明(2e,4e)-decatrienoyl基团连接在c-3位。经以上分析可确定该化合物的平面结构。
[0023]
根据noesy谱中显示的h-10与h-2,h-3,和h-5的相关以及h-7与h-8,h
2-20,和h-14的相关,确定了化合物2的相对构型。同时,通过对比计算与实测的ecd数据,化合物2的绝对构型被确定为2s,3s,4s,5r,6r,7r,8s,9r,10s,11r,13r,14r。经scifinder数据库检索,化合物2为未见报道的新化合物,命名为yuanhuakined。
[0024]
表1化合物1的核磁数据
[0025][0026][0027]
表2化合物2的核磁数据
[0028]
[0029][0030]
对本发明涉及的2个瑞香烷型二萜类化合物1和2进行抑制肿瘤细胞系生长活性评价。结果表示化合物1和2显示出与阳性药相近的对a549,hep3b,和mcf-7细胞系的肿瘤细胞抑制活性。因此,本发明所述的瑞香烷型二萜类化合物1和2具有作为抗肿瘤细胞的药物的潜力。
[0031]
本发明还提供一种药物组合物,包含所述的芫花花蕾中瑞香烷型二萜类化合物1和/或2,以及药学上可接受的载体或赋形剂。
[0032]
本发明的优点在于,所述化合物1和2均为新化合物,且均为立体构型确定的光学纯化合物,同时有较好的抗肿瘤细胞生长活性,具有进一步开发的价值。
附图说明
[0033]
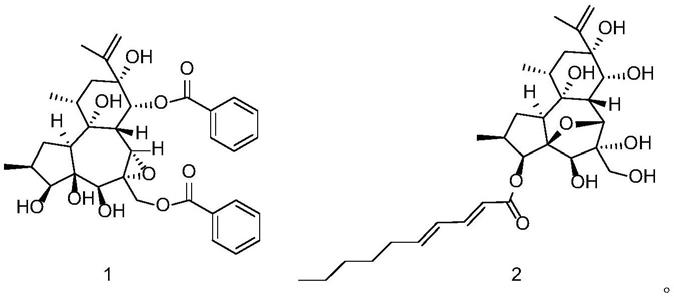
图1化合物1和2的结构;
[0034]
图2化合物1的质谱;
[0035]
图3化合物1的1h-nmr谱(600mhz,cdcl3);
[0036]
图4化合物1的
13
c-nmr谱(150mhz,cdcl3);
[0037]
图5化合物1的hsqc谱(600mhz,cdcl3);
[0038]
图6化合物1的hmbc谱(600mhz,cdcl3);
[0039]
图7化合物1的1h-1
h cosy谱;
[0040]
图8化合物1的noesy谱(600mhz,cdcl3);
[0041]
图9化合物1的单晶图;
[0042]
图10化合物2的质谱;
[0043]
图11化合物2的1h-nmr谱(600mhz,cdcl3);
[0044]
图12化合物2的
13
c-nmr谱(150mhz,cdcl3);
[0045]
图13化合物2的hsqc谱(600mhz,cdcl3);
[0046]
图14化合物2的hmbc谱(600mhz,cdcl3);
[0047]
图15化合物2的1h-1
h cosy谱;
[0048]
图16化合物2的noesy谱(600mhz,cdcl3);
[0049]
图17化合物1和2的实验和计算ecd谱图;
[0050]
图18化合物1和2对a549,hep3b,和mcf-7细胞系的肿瘤细胞抑制活性;所有数据以means
±
sd表示(三次独立实验);cisplatina,sorafeniba,doxorubicina为阳性药。
具体实施方式
[0051]
下面所列实施例有助于本领域技术人员更好地理解本发明,但不以任何方式限制本发明。
[0052]
实施例1
[0053]
芫花花蕾中瑞香烷型二萜类化合物1-2的制备,具体包括以下操作:
[0054]
(1)取干燥的瑞香科瑞香属植物芫花花蕾(60kg)以70%工业乙醇回流提取3次,合并提取液浓缩得到浸膏。所得浸膏先后采用二氯甲烷,乙酸乙酯萃取。二氯甲醇层部分(2400g)和乙酸乙酯层部分(1300g)经减压硅胶柱色谱,以二氯甲烷-甲醇系统(100:1,50:1,30:1,20:1,10:1,5:1,3:1,1:1)进行梯度洗脱,共收集到4个馏分(fr.a~fr.d)。
[0055]
(2)馏分fr.c(230g)经hp20柱色谱,以乙醇水梯度洗脱(20%,40%,60%,90%),共收集到4个馏分(fr.c-1~fr.c-4)。
[0056]
(3)4个馏分fr.c-1(25g),fr.c-2(32g),fr.c-3(35g),fr.c-4(43g)分别经ods柱色谱,交叉合并,以乙醇水梯度洗脱(20%,40%,60%,80%,90%),收集得到新的4个馏分(fr.c-i,fr.c-ii,fr.c-iii,fr.c-iv)。
[0057]
(4)馏分fr.c-ii(15.5g)和fr.c-iv(18.2g)分别经硅胶柱,经石油醚/乙酸乙酯(100:1,50:1,30:1,20:1,10:1,5:1,3:1,1:1,1:2)梯度洗脱;其中馏分fr.c-ii洗脱得到的馏分fr.c-ii-3经制备型hplc,以甲醇/水体积比(85:15)洗脱,得到10个馏分(fr.c-ii-3-1~fr.c-ii-3-10),fr.c-ii-3-4再经过半制备型hplc色谱,以乙腈/水体积比(70:30)洗脱,
分离纯化得到化合物1(38.1mg);馏分fr.c-iv洗脱得到的馏分fr.c-iv-4经制备型hplc,以甲醇/水体积比(85:15)洗脱,得到14个馏分(fr.c-iv-4-1~fr.c-iv-4-14),fr.c-iv-4-10再经过半制备型hplc色谱,以乙腈/水体积比(70:30)洗脱,分别分离纯化得到化合物2(2.5mg)。
[0058]
实施例2
[0059]
芫花花蕾中瑞香烷型二萜类化合物1-2的抗肿瘤细胞活性检验。
[0060]
使用mtt法测试实施例1中制得的化合物1-2对肿瘤细胞系a549,hep3b,和mcf-7的生长抑制活性。取对数生长的细胞以6
×
104个/m l,以每孔100μl接种于96孔板中,设置3个复孔并置于37℃、5%co2培养箱中孵育24h。然后用不同浓度的测试化合物1和2(0.1,1,10,50μm),加药处理48h。
[0061]
药物作用48h后,将细胞与mtt溶液(0.5mg/ml)在37℃下再孵育4小时。吸除培养液后每孔加入dmso将其完全溶解,并采用酶标仪于490nm处测定吸光度。所有实验都平行进行并重复三次,设置空白组及阳性对照组结果如图18所示。该发明中描述的两个化合物1和2,均表现出较好的对a549,hep3b,mcf-7细胞系的抑制活性。
