1.本发明涉及动物模型技术领域的一种生物工具的构建方法和应用,具体涉及一种角朊蛋白(hornerin)基因修饰小鼠动物模型的构建方法和应用。
背景技术:
2.人类存在许多复杂疾病,其遗传模式复杂,有众多因素参与疾病的进程,如单个基因的多个突变、多个基因的突变以及与环境因素的交互影响。特应性皮炎(atopic dermatitis,简称ad;mim603165)是人皮肤常见的一种复杂疾病,临床表现为慢性、易复发性、炎症性、瘙痒性等特点,常伴发哮喘和过敏性鼻炎。据统计,在发达国家ad好发于儿童(患病率高达20%),成人患病率也达3%,且呈逐年上升趋势。我国ad发病率为3%。目前,国际上对ad发病机制的了解很有限,也缺乏特效的治疗手段,这给患者个人、家庭和社会带来了沉重的负担,逐步成为一个严重的社会问题。
3.长期以来,ad被认为是一种免疫系统功能障碍性疾病,表现在ad患者血清ige比正常人高1倍~10倍,从而介导过敏反应和炎症的发生。近年来随着复杂疾病全基因组关联研究技术的快速发展,科学家们发现了许多同ad关联的易感基因/位点,如1q21.3(flg)、5q22.1(tmem232/slc25a46)、 11q13.5(c11orf30)和20q13.33等,其中filaggrin(flg)基因的功能缺失突变最具有代表性(参见文献:common loss-of-function variants of the epidermal barrierprotein filaggrin are a major predisposing factor for atopic dermatitis.nat genet. 38(4):441-446.2006)。由于flg是构成表皮机械性屏障的角质层的角质包膜的主要结构蛋白,flg基因突变会导致表皮屏障的缺陷,使得皮肤在应对过敏原或细菌产物时,全身和皮肤免疫功能低下,可能还会并发某些过敏性疾病,如食物过敏、哮喘和过敏性鼻炎等(参见文献:synergy of understanding dermatologicdisease and epidermal biology.j clin invest.122(2):436-439.2012)。这项里程碑式的研究,极大地提高了人类对皮肤复杂疾病发病机制的认识,并突出了表皮屏障功能在复杂疾病特定替代疗法中的关键作用。当前在全球范围内兴起的对 flg基因的snp分析就是对其潜在重要性的一个理性的肯定。
4.但是,基于ad病理机制的复杂性,flg基因突变并不一个充分必要条件,甚至也已有证据表明flg的基因剔除并不一定会对皮肤表皮角质层屏障功能造成很大的影响(参见文献:knock-down of filaggrin does not affect lipidorganization and composition in stratum corneum of reconstructed human skinequivalents.exp dermatol.22(12):807-812.2013)。另外,在皮肤角质层还存在两个新的flg同源姐妹蛋白hornerin(hornerin)和filaggrin-2(flg-2),二者对表皮屏障形成所起的作用可能与flg重叠(参见文献:highly complexpeptide aggregates of the s100 fused-type protein hornerin are present in human skin. j invest dermatol.129(6):1446-1458.2009;参见文献:molecular identification andexpression analysis of filaggrin-2,a member of the s100 fused-type protein family. plos one.4(4):
e5227.2009)。在分子水平上,上述三个姐妹基因flg、hornerin 和flg-2都编码大分子前提蛋白(氨基酸序列长度》2000),在角质形成细胞分化过程中经过酶切而形成成熟的小分子功能单元。因此,维护皮肤表皮健康的屏障功能,不仅需要相关结构蛋白基因的正常表达,还需要正常的蛋白修饰与成熟过程。由于参与表皮屏障构建的结构蛋白种类繁多,又有功能上的相互协同作用,不同皮肤疾病的发生决定于表皮屏障的缺陷类别与总体缺陷程度。
5.人类疾病的动物模型是疾病机理研究的重要基础,小鼠动物模型的建立使得对皮肤屏障功能异常疾病发病机制的研究更有可操作性、重复性和可比性,有助于认识该类疾病的发生发展机制。在对皮肤复杂疾病的研究中,对hornerin 基因的全敲除研究曾有报道(参见文献:transient epidermal barrier deficiency andlowered allergic threshold in filaggrin-hornerin(flg/hornerin)double-deficient mice. allergy,74(9):1327
–
1339.2019),但结果不理想,其原因在于hornerin基因的结构特点。hornerin基因包含3个外显子,基因功能主要通过超大的第三外显子编码hornerin蛋白重复功能单元而实现,因而很难通过通常的基因敲除方式实现基因生物学功能的验证。
技术实现要素:
6.为了解决背景技术中存在的问题,本发明首先提供了一种角朊蛋白hornerin 基因修饰小鼠动物模型,同时提供基因修饰小鼠动物模型的构建方法,以及在表皮屏障功能异常疾病发病发展机理研究和筛选预防治疗药物中的应用。
7.本发明所采用的技术方案是:
8.一、一种制备角朊蛋白hornerin基因修饰动物模型的方法:
9.所述方法是hornerin基因中的第三外显子中插入一段荧光蛋白编码基因 tdtomato和一段终止子序列wpre,使得hornerin基因不表达主要蛋白功能单元,而表达tdtomato,从而完成修饰,达到hornerin基因功能缺失的效果。
10.所述动物为小鼠。
11.方法包括以下步骤:
12.c1,按照a1-a3步骤,根据sgrna靶序列制备获得sgrna载体;
13.c2,采用sgrna载体进行体外转录,转录产物与cas9/crispr的rna混合,得到进行显微注射的rna混合液;
14.c3,制备获得带有荧光蛋白编码基因tdtomato和终止子序列wpre的打靶载体;
15.c4,将打靶载体和rna混合液通过显微注射到小鼠受精卵中,取注射后存活的受精卵移植到假孕母鼠体的输卵管中发育,产出小鼠,获得f0代小鼠;
16.c5,利用pcr技术对f0代小鼠进行检测,验证细胞中hornerin基因第三外显子靶位点区插入的荧光蛋白编码基因tdtomato和终止子序列wpre,获得 hornerin基因修饰阳性小鼠;
17.所述c5中使用的pcr检测引物对序列如seq id no∶22-25所示。
18.c6,将上述获得的hornerin基因修饰阳性小鼠通过自交和杂交的方式繁殖,扩大种群数量,并用pcr技术进行检测,筛选并建立稳定的hornerin-/-纯合子小鼠;
19.所述c6中使用的pcr检测引物对序列如seq id no∶2629-所示。
20.所述c1中的sgrna载体按照以下方法制备获得:
21.a1,按照seq id no:3-10任一项所示序列的任一项sgrna靶序列,制备获得正向寡核苷酸序列和反向寡核苷酸序列;
22.优选的,所述sgrna靶序列为seq id no:5,制备的正向寡核苷酸序列为seq id no:11;反向寡核苷酸序列为seq id no:12。
23.a2,合成上述所述的正向寡核苷酸和反向寡核苷酸,经变性、退火处理,形成可连接的双链sgrna寡核苷酸;
24.a3,将双链sgrna寡核苷酸连接至百奥塞图的t7-sgrna载体,筛选获得 sgrna载体。
25.所述c3中的靶向载体,包括:
26.seq id no:3-10任一项的sgrna靶序列作为hornerin基因靶位点区域序列;优选的sgrna(seq id no:5)靶序列作为hornerin基因靶位点区域序列;
27.期望的供体dna序列,包含荧光蛋白编码基因tdtomato和终止子序列 wpre;
28.与sgrna靶序列5’端同源的dna片段lr(5’臂),长度为1301个核苷酸;
29.与sgrna靶序列3’端同源的第二个dna片段rr(3’臂),长度为991个核苷酸。
30.二、一种用于制备朊蛋白hornerin基因修饰动物模型的sgrna靶序列:
31.所述sgrna靶序列如seq id no:3-10任一项所示。
32.所述sgrna靶序列如seq id no:5所示。
33.三、一种sgrna载体,由所述sgrna靶序列通过正反向寡核苷酸序列制备获得。
34.四、所述方法产生的动物或其后代在制备动物模型应用。
35.五、所述的方法产生的动物或其后代在研究hornerin基因功能、病原学研究、针对人hornerin靶位点的药物研究以及相关疾病药物方面的用途。
36.本发明的所述小鼠模型是把报告基因tdtomato蛋白编码序列和wpre序列敲入小鼠hornerin基因第三个外显子的前端,在hornerin基因表达的组织中表达tdtomato蛋白并发出红色荧光,而不表达hornerin蛋白的功能单元,达到 hornerin基因敲除的效果。
37.本发明的有益效果是:
38.本发明按照独特的方法(主要是打靶方式和sgrna设计)并把ko小鼠动物模型建成功了(应用),实现了生物工具的制备,具有很好的应用价值。
39.本发明构建的小鼠模型可以用于研究hornerin基因缺失后表皮屏障异常疾病相关的表型变化,用于阐明发病机制及药物筛选。具体可应用于hornerin基因缺失后动物表皮屏障功能异常相关疾病的发病机制和药物筛选。
附图说明
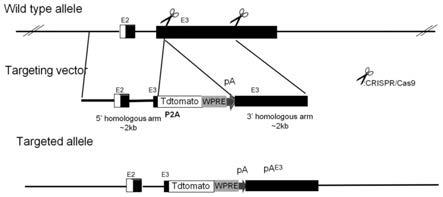
40.图1为本发明实施例1中hornerin基因敲除策略示意图;
41.图2为本发明实施例1中cas9/sgrna的活性检测结果图;
42.图3为本发明实施例1中hornerin-sgrna3的rna电泳图;
43.图4为本发明实施例2中打靶载体pclone-4g-hornerin质粒图谱示意图;
44.图5为本发明实施例2中打靶载体酶切鉴定结果电泳图;
45.图6为本发明实施例2中打f0小鼠基因型鉴定引物设计原则示意图;
46.图7为本发明实施例2中f0代基因型检测结果图;
47.图8为本发明实施例2中f1代基因型检测结果图;
48.图9为本发明实施例2中f1代阳性小鼠southern blot筛选策略的示意图;
49.图10为本发明实施例2中f1代阳性小鼠southern blot检测结果图;
50.图11为本发明实施例3中基因工程小鼠纯合子基因型鉴定引物设计原则示意图;
51.图12为本发明实施例3中基因工程小鼠纯合子基因型鉴定检测结果图。
具体实施方式
52.下面结合具体实施方式对本发明做进一步阐述和说明。本发明中各个实施方式的技术特征在没有相互冲突的前提下,均可进行相应组合。实施案列中所用材料、试剂或仪器等,如无特别说明,均可通过商业途径获得。
53.实施例1
54.(一)
55.1、打靶策略的设计:
56.hornerin基因在3号染色体正链上,全长约13.82kb(ncbi id:68723)。分析hornerin基因结构,共包含3个外显子,其中第三外显子编码hornerin蛋白的主要蛋白功能单元。
57.由于所述hornerin基因结构的特殊性,传统的敲除整个编码区或蛋白功能单元编码区的打靶策略很难实现对hornerin基因生物学功能的全面鉴定,本发明却采用敲进方式代替敲除方式来实现hornerin基因功能缺失的效果。
58.具体是选择在hornerin基因的第三外显子前端序列中敲进荧光蛋白编码基因 tdtomato和一个终止子wpre,使得角朊蛋白基因不表达主要蛋白功能单元,而替代表达惰性的指示荧光蛋白tdtomato,从而达到hornerin基因功能缺失的效果。
59.具体敲进策略如图1所示。
60.2、hornerin基因修饰模式小鼠的制备
61.采用百奥赛图公司基于crispr/cas9开发的ege系统制备模式小鼠。实施步骤如下:
62.2.1靶序列的确认:
63.为了保证所设计cas9/sgrna的效率,对以制备所用的c57bl/6鼠尾靶位点序列进行pcr扩增并测序,并与ncbi/ensembl数据库序列比对。以测序结果为准设计sgrna。
64.所用pcr酶采用天根公司的taq dna polymerase(2.5u/μl,货号et101-02-01), pcr引物如下所示:
65.表1用于靶序列的确认的pcr引物
[0066][0067]
对c57bl/6鼠尾dna进行pcr及测序,结果证明:c57bl/6鼠尾靶序列与genebank和ensembl所给序列完全一致。
[0068]
2.2 sgrna的设计
[0069]
基于sgrna的设计原则,在靶位点区域共设计8条sgrna靶序列,如下:
[0070]
表2 sgrna靶序列
[0071][0072]
2.3 cas9/sgrna质粒的构建
[0073]
按照表2设计的sgrna靶序列合成引物,即在其5'端加上caccg且在3' 端除去agg得到正向寡核苷酸得到正向寡核苷酸,其互补链5'端加上aaac 并3'端加上c在得到反向寡核苷酸,退火后以酶切连接(bbsi)的方式,将酶切产物分别连接至bbsi酶切的pcs质粒,连接产物转化后送样测序验证正确。
[0074]
2.4 sgrna的活性检测
[0075]
采用百奥赛图的crispr/cas9活性检测方法-uca
tm
方式以uca试剂盒检测 sgrna的活性,检测结果参见图2,结果可见向导sgrna具有不同活性,综合选择hornerin-sgrna3进行后续实验。
[0076]
2.5 sgrna的制备
[0077]
按照表2设计的hornerin-sgrna3序列合成相应引物(如表3),将sgrna 靶序列hornerin-sgrna3连入带t7启动子质粒载体pt7-sgrna上并进行体外转录,得到进行显微注射的rna。rna电泳图如图3所示。
[0078]
表3用于sgrna制备的序列表
[0079][0080]
(二)
[0081]
1、打靶载体的构建
[0082]
根据打靶方案(如图1),通过aio
tm
cloning将lr片段seq id no:15 (1306kb)、rr片段seq id no:20(991kb)和p2a
–
tdtomato(2382kb) 构建成tv-4g-hornerin载体。lr片段、rr片段和p2a
–
tdtomato引物序列如下表)并通过酶切鉴定和测序,确认打靶载体构建完成。酶切鉴定结果如图5所示。
[0083][0084][0085]
表4用于打靶载体的构建的序列表
[0086]
2、受精卵显微注射
[0087]
将上述制备的打靶载体和hornerin-sgrna3通过显微注射到c57bl/6n小鼠受精卵中,分4次注射,共注射760个,注射后f0小鼠出生158只。
[0088]
3、f0小鼠基因型鉴定
[0089]
本发明使用cas9/sgrna注射受精卵的方法制备基因敲入小鼠。
[0090]
f0小鼠基因型鉴定引物设计原则如图6所示,图中箭头代表引物设计的位置及方向。合成两对引物hornerin-l-gt-f/hornerin-l-gt-r和 hornerin-r-gt-f/hornerin-r-gt-r(如表4所示),分别对hornerin基因敲进小鼠进行pcr鉴定及测序检测。
[0091]
pcr条件(touchdown)如下表为:
[0092][0093]
得到的pcr产物检测结果如图7所示。根据图6和测序结果,表明ec9-127 (雄鼠)和ec9-137(鼠雌)为f0阳性鼠。
[0094]
由于胚胎早期卵裂速度很快,因此得到的f0小鼠为嵌合体。因此,以f0小鼠鼠尾进行基因型鉴定得到的f0基因型仅供参考,不一定为可遗传的基因突变型,可遗传的基因型需待f1小鼠基因型鉴定后确定。
[0095]
表5用于f0小鼠基因型鉴定的pcr引物
[0096][0097][0098]
4、f1代小鼠基因型鉴定
[0099]
4.1 f1代小鼠基因型初步鉴定
[0100]
将上述f0代阳性小鼠ec9-127和ec9-137与野生型小鼠交配以得到获得具有稳定基因型的f1代小鼠。交配后,亲本为ec9-127雄鼠的共出生f1代小鼠 25只,而和亲本为ec9-137鼠雌的未有子代出生。
[0101]
采用与f0小鼠基因型鉴定一致的方法,对上述25只f1代小鼠基因型进行初步鉴定。得到的pcr产物检测结果如图7所示。根据图8和测序结果,表明通过pcr及测序结果,表明1ec9-5,1ec9-7,1ec9-11,1ec9-12和1ec9-13 为5只阳性小鼠(其中2只为雄鼠,3只为雌鼠)。
[0102]
4.2 f1代阳性小鼠southern blot检测
[0103]
为了筛选到发生正确重组的基因打靶小鼠,需要进一步采用southern blot 方法验证。
[0104]
4.2.1 southern blot筛选策略
[0105]
southern blot筛选策略的示意图如图9所示,利用scai作为southern blot 酶切位点,3’探针用于检测是否发生正确重组,若发生正确重组,将会出现野生型(15.7kb)和突变型(11.5kb)两个条带;若未正确重组,将只会出现野生型条带(15.7kb)。wpre探针用于检测是否含有随机插入,若发生正确重组,将只会出现目的条带(6.5kb);若存在随机插入,将会出现多条带。
[0106]
4.2.2 f1代阳性小鼠southern blot检测
[0107]
经过pcr鉴定1ec9-5,1ec9-7,1ec9-11,1ec9-12和1ec9-13为阳性小鼠(如图8)。提取上述小鼠鼠尾dna进行southern blot检测,检测结果如图 10,表明f1代小鼠1ec9-5,1ec9-7,1ec9-11,1ec9-12和1ec9-13均为两端正确重组,且没有随机插入。
[0108]
上述表明使用本方法能构建出可稳定传代、且无随机插入的hornerin基因功能缺失的基因工程小鼠。
[0109]
(三)
[0110]
1、基因工程小鼠纯合子的鉴定
[0111]
将鉴定为阳性的f1代小鼠互相交配,可得到hornerin基因功能缺失基因工程小鼠纯合子。采用pcr方法鉴定纯合子,引物设计如图11所示,引物对msd-f 和msd-r设计在野生基因序列中,野生型等位基因的pcr产物比较短,容易扩增出来;突变型等位基因的pcr产物比较长,可能不能扩增出来。所以msd-f 和msd-r这对引物主要用于鉴定野生型等位基因的存在,并结合wpre-f和 msd-r这对引物的pcr结果判断动物的具体基因型:纯合/杂合/野生型。合成的引物序列如5。
[0112]
表6用于基因工程小鼠纯合子鉴定的pcr引物
[0113][0114]
提取小鼠鼠尾dna进行pcr检测,pcr条件为:
[0115][0116]
pcr检测结果如图12。同时出现野生型条带和突变型条带,为杂合子。
[0117]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
[0118]
seqidno.1:
[0119]
名称:c57bl/6鼠尾靶序列的pcr引物hornerin-msd-f
[0120]
来源:人工序列(artificialsequence)
[0121]
gccttcccccaaatgcttaactagc
[0122]
seqidno.2:
[0123]
名称:c57bl/6鼠尾靶序列的pcr引物hornerin-msd-r
[0124]
来源:人工序列(artificialsequence)
[0125]
aggtgttagagtgacctgagccaga
[0126]
seqidno.3:
[0127]
名称:sgrna靶序列hornerin-sgrna1
[0128]
来源:人工序列(artificialsequence)
[0129]
gccttcccccaaatgcttaactagc
[0130]
seqidno.4:
[0131]
名称:sgrna靶序列hornerin-sgrna2
[0132]
来源:人工序列(artificialsequence)
[0133]
tctggcgaatgttattcttctgg
[0134]
seqidno.5:
[0135]
名称:sgrna靶序列hornerin-sgrna3
[0136]
来源:人工序列(artificialsequence)
[0137]
gatgatactcaagctgactaagg
[0138]
seqidno.6:
[0139]
名称:sgrna靶序列hornerin-sgrna4
[0140]
来源:人工序列(artificialsequence)
[0141]
ggctctttaagttctagtgcagg
[0142]
seqidno.7:
[0143]
名称:sgrna靶序列hornerin-sgrna5
[0144]
来源:人工序列(artificialsequence)
[0145]
agctccagtacaaaaggatctgg
[0146]
seqidno.8:
[0147]
名称:sgrna靶序列hornerin-sgrna6
[0148]
来源:人工序列(artificialsequence)
[0149]
ggaaaacatggttcatcatcagg
[0150]
seqidno.9:
[0151]
名称:sgrna靶序列hornerin-sgrna7
[0152]
来源:人工序列(artificialsequence)
[0153]
aagtgatcacgaaaatagtgagg
[0154]
seqidno.10:
[0155]
名称:sgrna靶序列hornerin-sgrna8
[0156]
来源:人工序列(artificialsequence)
[0157]
gagagaatgactcttattccagg
[0158]
seqidno.11:
[0159]
名称:sgrna靶序列hornerin-sgrna3的正向寡核苷酸
[0160]
来源:人工序列(artificialsequence)
[0161]
caccggatgatactcaagctgacta
[0162]
seqidno.12:
[0163]
名称:sgrna靶序列hornerin-sgrna3的反向寡核苷酸
[0164]
来源:人工序列(artificialsequence)
[0165]
aaactagtcagcttgagtatcatcc
[0166]
seqidno.13:
[0167]
名称:载体克隆引物hornerin-lr-f
[0168]
来源:人工序列(artificialsequence)
[0169]
aagaaggagatatacatggaattctcctccagtgaaccacatcagct ctt
[0170]
seqidno.14:
[0171]
名称:载体克隆引物hornerin-lr-r
[0172]
来源:人工序列(artificialsequence)
[0173]
aattagtagctccgcttccgagctccagcttgagtatcatcagaaga tac
[0174]
seqidno.15:
[0175]
名称:lr片段基因序列
[0176]
来源:人工序列(artificialsequence)
[0177]
aagaaggagatatacatggaattctcctccagtgaaccacatcagctctt aatataaaactcaaaat
tccccaacacgatttaagaattatgatccagtc tatattaatctcactagcacaatgtccttactgcttgtactaaatttagc agtcatgaatttctgtcaattccttaaataaactatacttctcttttctttc atactgtgttcatatcatcacatctatctgcatcttctctgtgttcctccta cctttcttcctttagctagttctaatccatccttcaatgaataacatatcct ctcattaaactttcttgaatcacaactggctcccttttgatgtgctcatat ttgatataaaattataaatttgtatatcaaaccataaggcttcacttttaa tattttatctatttactcatttactattaaaacaatatctcctgtaatata gtctggccttaaacttgctatgtacctgagaatgaccttgaactcctgatc ttagtgcctctacctcctgagtgacaggattacaggcatgcatcatcagg ccaagcaaaaaacttaaatcattcactgctttagaccctccataacatag tgctaggcatactacagctctgaccccaagattactgttttaaaatctgta attagcaaataaacagactgggcaaagaaaatttatatataattaagta gacatctacaattattatttataaattatctaaccatccttgattaaccat tgcccgtctttcattctttccttctttctttccttgcttccttctttctttct ttgacaagattttgcttctaattccaaggatgccaggaacttcctatgca acacacactgcaaagtcaagatcatatttccttggcctgcaaaatattat tcacagctactaactttacaaagctaacaggccaacttgctcctctctctc tctctctctctctctctctctctccccctccctcactcttcctcgctatctca ctctctatcccttttacctttctagcccaaacaactatgtggtcaatttca accaaaatgtattaaatattcatatttctacagccttcccccaaatgctta actagctttatattaaatagttacagaaccttcacttatactttattcctt gacagaatccagatgatccagacaccgtagatatcatcatgcaaaatctg gatcgagatcataaccacaaagtggattttactgaaattagtagctccgc ttccgagctccagcttgagtatcatcagaagatac
[0178]
seqidno.16:
[0179]
名称:载体克隆引物hornerin-p2a-td-f
[0180]
来源:人工序列(artificialsequence)
[0181]
gtatcttctgatgatactcaagctggagctcggaagcggagctact
[0182]
seqidno.17:
[0183]
名称:载体克隆引物hornerin-p2a-td-r
[0184]
来源:人工序列(artificialsequence)
[0185]
ttacaagccttagtagtactggatcctccccagcatgcctg
[0186]
seqidno.18:
[0187]
名称:载体克隆引物hornerin-rr-f
[0188]
来源:人工序列(artificialsequence)
[0189]
caggcatgctggggaggatccagtactactaaggcttgtaataaaat tattggc
[0190]
seqidno.19:
[0191]
名称:载体克隆引物hornerin-rr-r
[0192]
来源:人工序列(artificialsequence)
[0193]
gcagccggatctcaggcggccgcgaagacttgccttgtccgcaacct tg
[0194]
seqidno.20:
[0195]
名称:rr片段基因序列
[0196]
来源:人工序列(artificialsequence)
[0197]
caggcatgctggggaggatccagtactactaaggcttgtaataaaattat tggcaaagattactgccaagcttcagggtcaaagcagaaaaatcacagt caccagcaccaagaggaacagagtaaaaaagaaacagaaaacaaggag caaaaaggctctttaagttctagtgcaggagagaatgactcttattccag gggctcaagaggaagcaat
aaaagcaaatccaaaaaactaagaaaagg gaaggagcaaagttctaaacaaacaacaaaatcaaattcaagtgatcac gaaaatagtgaggattatgaacaaggccagcatgaatcaggattttcta actcatctggcaacgggagacctagctcaaggaaagcttctggcttccct caacctggttcagaaccaggacaatcttctagctccagtacaaaaggatc tggcgaatgttattcttctggtaatggaaaacatggttcatcatcaggag gatcagcagtttctggctcaggtcactctaacacctatggtaaacaagga acaggatcaaggcattcatcaagcaacaggagaagcaggtctacctcaa gggaatcttctggctcccaagaatatagctctggatcatcagaagaacct ggctttacacatggatctggtcgaaaaaactcttctacttgtggaaaaaa cggttcctactctggacagtcaacaggcagacatcaacaaggatttggat ctagtcatgaattagaatccggtcaatcaatcacctctgctaaccatggc tctcattctaatcagtcatcatgcagtggcacaagagagtgtgggtctag cgagtcttccatgaagaagacccatgtttctggttcaggacactcttcaa gtacaggtaaatatacatccacttcaggacaaaattataactccactaga gcagccggatctcaggcggccgcgaagacttgccttgtccgcaaccttg
[0198]
seqidno.21:
[0199]
名称:f0小鼠基因型鉴定的pcr引物hornerin-l-gt-f
[0200]
来源:人工序列(artificialsequence)
[0201]
tcccagggtaggtactgatttcctcaat
[0202]
seqidno.22:
[0203]
名称:f0小鼠基因型鉴定的pcr引物hornerin-l-gt-r
[0204]
来源:人工序列(artificialsequence)
[0205]
aagcttgattacttgtacagctcgtcca
[0206]
seqidno.23:
[0207]
名称:f0小鼠基因型鉴定的pcr引物hornerin-r-gt-f
[0208]
来源:人工序列(artificialsequence)
[0209]
gaggacaacaacatggccgtcatca
[0210]
seqidno.24:
[0211]
名称:f0小鼠基因型鉴定的pcr引物hornerin-r-gt-r
[0212]
来源:人工序列(artificialsequence)
[0213]
gactgacctgacgaacagcctgaag
[0214]
seqidno.25:
[0215]
名称:基因工程小鼠纯合子鉴定的pcr引物msd-f
[0216]
来源:人工序列(artificialsequence)
[0217]
gccttcccccaaatgcttaactagc
[0218]
seqidno.26:
[0219]
名称:基因工程小鼠纯合子鉴定的pcr引物msd-r
[0220]
来源:人工序列(artificialsequence)
[0221]
cctcttgagcccctggaataagagtc
[0222]
seqidno.27:
[0223]
名称:基因工程小鼠纯合子鉴定的pcr引物wpre-f
[0224]
来源:人工序列(artificialsequence)
[0225]
cctcttgagcccctggaataagagtc
[0226]
seqidno.28:
[0227]
名称:基因工程小鼠纯合子鉴定的pcr引物wt-r2
[0228]
来源:人工序列(artificialsequence)
[0229]
cctcttggtgctggtgactgtgatt 。
