一种靶向泛素化诱导bcr-abl蛋白降解的化合物及其应用
技术领域
1.本发明属于化学领域,具体涉及一种靶向泛素化诱导bcr-abl蛋白降解的化合物、制备方法及应用。
背景技术:
2.蛋白降解靶向嵌合体(proteolytic targeting chimera,protac)技术是一种化学诱导靶蛋白多聚泛素化,并通过泛素-蛋白酶体系统降解靶蛋白的新兴技术。protac是由靶蛋白配体和e3连接酶配体通过适当的连接链连接而成的双功能分子,能够同时招募靶蛋白和e3连接酶诱导靶蛋白泛素化降解,具有广泛的应用前景和发展空间。从protac的特殊作用机制来看,protac分子泛素化标记poi并促使蛋白降解后可与poi解离并在细胞内可以循环利用,起到亚化学计量催化的效果,减少药物的使用剂量从而减少体内药物暴露量,降低毒副作用;由于其短暂的结合,因此并不需要配体与受体较高的亲和力,对低亲和力或不可成药靶点具有一定的应用价值;与传统的小分子抑制剂的“占据驱动”作用机制不同,protac是以“事件驱动”作用模式实现生物活性的,从根本上可逆、快速敲低致病蛋白,可以同时影响激酶依赖性和非依赖性的生物学功能,理论上可以推迟甚至是消除耐药性的发生。
3.由于protac新技术的独特优势加之bcr-abl激酶抑制剂的发展瓶颈以及不可避免地耐药性发生。
4.慢性粒细胞白血病(chronic myeloid leukemia,cml)是一种起源于造血干细胞(hematopoietic stem cells,hscs)的多系骨髓增生恶性肿瘤,其典型特征是造血干细胞不受控制的增殖,特别是骨髓中会产生过多的粒性白细胞。据统计,cml约占所有癌症的0.3%,占成人白血病的20%,全世界每10万成年人中就有1-2人患有cml,任何年龄的人群都可发病,50岁以上人群较为常见且发病率随着年龄的增加而增加,通常男性患者多于女性患者。cml的细胞遗传学标志是长臂染色体9和22之间的相互异位(9号染色体上的bcr基因与22号染色体上的c-abl基因融合形成新的bcr-abl序列基因),t(9;22)(q34;q11)形成费城染色体(philadelphia chromosome,ph),95%的cml患者具有费城染色体。ph染色体上的bcr-abl融合基因编码致病蛋白(p210bcr-abl)不断增加酪氨酸激酶活性,激活多条下游信号通路促进cml的发生发展,从而导致造血干细胞不受控制的增殖,细胞黏附的修饰以及细胞凋亡的抑制。cml的进展分为三个阶段:慢性期(chronic phase,cp),占确诊时的85-90%;加速期(accelerated phase,ap)以及髓细胞或淋巴细胞的急变期(blast crisis)。随着bcr-abl酪氨酸激酶抑制剂(tyrosine kinase inhibitors,tkis)的不断发展,现已大大延长了处于慢性期的cml患者的总生存期,特别是在伊马替尼(imatinib)已成为黄金标准的一线用药的今天。然而,经过服用马替尼一段时间后会产生不同程度的的获得性耐药,严重阻碍了临床应用。
技术实现要素:
5.本发明针对以上问题,提供一种靶向泛素化诱导bcr-abl蛋白降解的化合物、制备方法及应用。
6.发明目的通过以下方案实现:一种式(i)所示的靶向泛素化诱导bcr-abl蛋白降解的化合物:
[0007][0008]
式(i)中,n为5或6或10或11。
[0009]
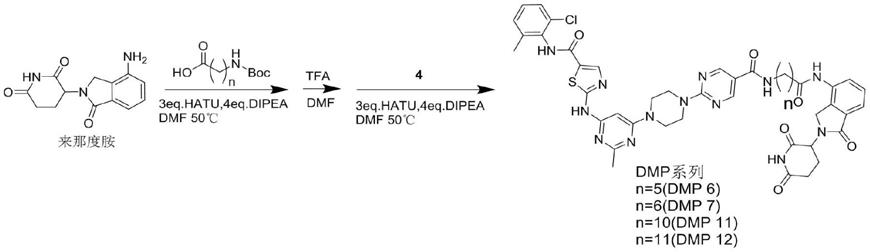
一种靶向泛素化诱导bcr-abl蛋白降解的化合物的合成方法,合成路线如下:
[0010][0011]
n为5或6或10或11。
[0012]
进一步的,化合物4合成路线如下:
[0013][0014]
一种药物组合物,包括靶向泛素化诱导bcr-abl蛋白降解的化合物或其药学上可接受的盐和水合物,和药学上可接受的赋形剂。
[0015]
一种药物组合物,包括靶向泛素化诱导bcr-abl蛋白降解的化合物,在药物组合物中加入药学上可接受的辅料制成临床上可接受的剂型。
[0016]
一种靶向泛素化诱导bcr-abl蛋白降解的化合物在制备预防或/和治疗癌症的药物中应用。
[0017]
进一步的,所述的癌症为慢性粒细胞性白血病、急性粒细胞性白血病、慢性淋巴性白血病、急性淋巴性白血病。
[0018]
一种式(ⅱ)所示的靶向泛素化诱导bcr-abl蛋白降解的化合物:
[0019][0020]
一种式(ⅲ)所示的靶向泛素化诱导bcr-abl蛋白降解的化合物:
[0021][0022]
进一步的,式(ⅲ)所示的靶向泛素化诱导bcr-abl蛋白降解的化合物:其特征在于linker的8种结构如下
[0023][0024]
本发明优点在于:该化合物不仅具有优异的bcr-abl蛋白降解作用和抗肿瘤活性,对人体毒副作用小,可用于制备抗肿瘤药物。
附图说明
[0025]
附图1是(i)化合物对k562细胞中bcr-abl蛋白的降解作用(6h)。
[0026]
附图2是(i)化合物dmp-011孵育6h对bcr-abl蛋白降解的量效关系图。
[0027]
附图3是大鼠尾静脉给予5mg/kg dmp-011后药动学参数及血药浓度曲线。
具体实施方式
[0028]
实施例1结合附图1-3;一种式(i)所示的靶向泛素化诱导bcr-abl蛋白降解的化合物:
[0029][0030]
式(i)中,n为5或6或10或11。
[0031]
一种靶向泛素化诱导bcr-abl蛋白降解的化合物的合成方法,合成路线如下:
[0032][0033]
n为5或6或10或11。
[0034]
一种靶向泛素化诱导bcr-abl蛋白降解的化合物的合成方法,化合物4合成路线如下:
[0035][0036]
化合物4的制备过程:2-氯嘧啶-5-羧酸乙酯(化合物1)2号位在碱性条件下受boc哌嗪进攻,同理化合物2和3在碱性条件下亲核取代,在naoh溶液中水解酯健得到化合物4。
[0037]
称取1.9g化合物1(10mmol,1eq)、5.6g1-boc-哌嗪(30mmol,3eq)、4.1g碳酸钾(30mmol,3eq)溶解于dmf中,缓慢加热到80℃,tlc薄层色谱监控反应,反应3h;反应结束冷却至室温,加入300ml的纯水,用盐酸调节ph,加入300ml
×
3的乙酸乙酯萃取,收集有机相,300ml
×
3饱和食盐水洗涤,加入无水硫酸钠脱水;收集有机相,减压蒸馏得粗品;硅胶层析柱分离(dcm:meoh=5:1),烘干得化合物2白色粉末2.2g,产率94%;
[0038]
称取2.0g化合物2(8.5mmol,1eq)、3.3g化合物3(8.5mmol,1eq)、3.5g碳酸钾(25.5mmol,3eq)溶解于dmf中,缓慢加热到80℃,tlc薄层色谱监控反应,反应3h;反应结束冷却至室温,加入0.5g氢氧化钠(12.75mmol,1.5eq),缓慢加热到50℃,tlc薄层色谱监控反
应,反应3h;反应结束冷却至室温,加入300ml的纯水,加入300ml
×
3的乙酸乙酯萃取,收集有机相,300ml
×
3饱和食盐水洗涤,加入无水硫酸钠脱水;收集有机相,减压蒸馏得粗品;硅胶层析柱分离(dcm:meoh=5:1),烘干得化合物4白色粉末4.0g,产率83%。
[0039]
一种药物组合物,包括靶向泛素化诱导bcr-abl蛋白降解的化合物或其药学上可接受的盐和水合物,和药学上可接受的赋形剂。
[0040]
一种药物组合物,包括靶向泛素化诱导bcr-abl蛋白降解的化合物,在药物组合物中加入药学上可接受的辅料制成临床上可接受的剂型。
[0041]
一种靶向泛素化诱导bcr-abl蛋白降解的化合物在制备预防或/和治疗癌症的药物中应用。
[0042]
一种靶向泛素化诱导bcr-abl蛋白降解的化合物的应用,所述的癌症为慢性粒细胞性白血病、急性粒细胞性白血病、慢性淋巴性白血病、急性淋巴性白血病。
[0043]
所述药物上可接受的赋形剂是指任何可用于药物领域的稀释剂、辅助剂和/或载体。
[0044]
一种式(i)所示的靶向泛素化诱导bcr-abl蛋白降解的化合物;
[0045][0046]
称取3.31g化合物38(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物46白色粉末2.83g,产率60%;
[0047]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.339g化合物46(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物47白色粉末0.31g,产率50%。
[0048][0049]
称取3.86g化合物40(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物48白色粉末3.16g,产率60%;
[0050]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea
(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.379g化合物48(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物49白色粉末0.32g,产率50%。
[0051][0052]
称取4.14g化合物42(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物50白色粉末3.33g,产率60%;
[0053]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.400g化合物50(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物51白色粉末0.33g,产率50%。
[0054][0055]
称取3.86g化合物45(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物52白色粉末3.16g,产率60%;
[0056]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.379g化合物52(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物53白色粉末0.32g,产率50%。
[0057]
本发明还公开了上述药物组合物制成的制剂,包括:在药物组合物中加入药学上可接受的辅料制成临床上可接受的剂型。所述临床上可接受的剂型为口服制剂、注射制剂或局部制剂。
[0058]
其中,口服制剂可为片剂、胶囊剂、溶液或混悬液;注射制剂可为注射溶液或混悬剂或可注射的干燥粉末,在注射前加入注射用水可立即使用;局部制剂可为软膏或溶液。
[0059]
其中,药学上可接受的辅料包括:口服制剂用的粘合剂、润滑剂、崩解剂、助溶剂、
稀释剂、稳定剂、悬浮剂、色素或矫味剂;注射制剂用的防腐剂、加溶剂或稳定剂;局部制剂用的基质、稀释剂、润滑剂、防腐剂等。药物制剂可以经口服或胃肠外方式(如静脉内、皮下、腹膜内或局部)给药,如果某些药物在胃部条件下是不稳定的,可将其配制成肠衣片剂。
[0060]
已经合成dmp系列连接链长度不同的四个化合物,纯度均大于96%;理化性质表明四个化合物在室温存放48h后未发生明显的降解,稳定性良好;目前已经完成了初步的降解活性实验以及考察了降解活性较好的dmp-011在大鼠体内药动学行为。
[0061]
体外细胞活率实验表明,dmp系列化合物ic50较弹头达沙替尼有较明显的下降且dmp系列中个化合物的ic50相差200-400倍不等,表明连接链对细胞抑制活性有明显的影响。实验表明在dmp系列中化合物dmp-11抑制肿瘤细胞活性的效果较好,其对达沙替尼敏感的慢性粒细胞性白血病细胞系k562的ic50=0.49nm,对达沙替尼耐药的慢性粒细胞性白血病细胞系ka的ic50=6.35nm,对肿瘤细胞(包括耐药与非耐药株)活性的抑制率明显优于弹头达沙替尼,结果见表1。
[0062]
表1.dmp系列及弹头的ic
50
值
[0063]
ic
50
(nm)72hk562kawarhead2.71973dmp-06126.30978024dmp-0784.70272169dmp-110.496.35dmp-12192.05336
[0064]
附图1中(i)化合物在100nm对k526细胞中的bcr-abl降解表明化合物dmp11表现出较好的活性。
[0065]
附图2中(i)化合物在对bcr-abl的降解活性表现出剂量依赖性,且在125nm表现出明显的降解活性
[0066]
附图3中(i)化合物在由于protac化合物分子结构复杂,分子量庞大,为考察(i)化合物是否具有良好的药代动力学行为,我们分别进行了灌胃(10mg/kg)和尾静脉注射(5mg/kg)给予大鼠dmp-011考察药动学行为。实验结果表明,化合物dmp-011灌胃给药不吸收,静脉注射给药后药动学行为良好。
[0067]
实施例2一种式(ⅱ)所示的靶向泛素化诱导bcr-abl蛋白降解的化合物:
[0068][0069]
一种式(ⅱ)所示靶向泛素化诱导bcr-abl蛋白降解的化合物的合成方法;合成路线如下:
[0070][0071]
称取2.83g化合物4(5mmol,1eq)溶解在10ml亚硫酰氯和3滴dmf中。将混合物加热至回流温度3小时,然后真空除去过量的亚硫酰氯,用20ml乙醚溶解固体,冰浴环境加入0.63g重氮甲烷(15mmol,3eq)反应15分钟,移除冰浴并将溶液在室温下搅拌3小时。用氮气流除去溶剂和过量的重氮甲烷。硅胶层析柱分离(甲苯:乙酸乙酯=1:1),烘干得化合物5黄色粉末2.23g,产率76%。
[0072][0073]
称取1.20g化合物61(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物7白色粉末2.16g,产率60%;
[0074]
称取0.36g化合物7(1mmol,1eq)、1.2g化合物5(2mmol,2eq.),溶于100ml乙醚中,加入5滴bf3·
et2o,室温静置2天,水性后处理得到油状残余物,硅胶层析柱分离(甲苯:乙酸乙酯=1:1),得到化合物8白色固体0.55g,产率58%。
[0075][0076]
称取1.64g化合物62(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物9白色粉末2.36g,产率60%;
[0077]
称取0.38g化合物9(1mmol,1eq)、1.2g化合物5(2mmol,2eq.),溶于100ml乙醚中,加入5滴bf3·
et2o,室温静置2天,水性后处理得到油状残余物,硅胶层析柱分离(甲苯:乙酸乙酯=1:1),得到化合物10白色固体0.56g,产率58%。
[0078][0079]
称取2.08g化合物63(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物11白色粉末2.56g,产率60%;
[0080]
称取0.40g化合物11(1mmol,1eq)、1.2g化合物5(2mmol,2eq.),溶于100ml乙醚中,加入5滴bf3·
et2o,室温静置2天,水性后处理得到油状残余物,硅胶层析柱分离(甲苯:乙酸乙酯=1:1),得到化合物12白色固体0.57g,产率58%。
[0081][0082]
称取2.52g化合物64(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物13白色粉末2.72g,产率60%;
[0083]
称取0.42g化合物13(1mmol,1eq)、1.2g化合物5(2mmol,2eq.),溶于100ml乙醚中,加入5滴bf3·
et2o,室温静置2天,水性后处理得到油状残余物,硅胶层析柱分离(甲苯:乙酸乙酯=1:1),得到化合物14白色固体0.58g,产率58%。
[0084]
一种药物组合物,(ⅱ)所示靶向泛素化诱导bcr-abl蛋白降解的化合物或其药学上可接受的盐和水合物,和药学上可接受的赋形剂。
[0085]
一种药物组合物,(ⅱ)所示靶向泛素化诱导bcr-abl蛋白降解的化合物,在药物组合物中加入药学上可接受的辅料制成临床上可接受的剂型。
[0086]
一种(ⅱ)所示靶向泛素化诱导bcr-abl蛋白降解的化合物在制备预防或/和治疗癌症的药物中应用。
[0087]
癌症为慢性粒细胞性白血病、急性粒细胞性白血病、慢性淋巴性白血病、急性淋巴性白血病。
[0088]
实施例3一种式(ⅲ)所示的靶向泛素化诱导bcr-abl蛋白降解的化合物:
[0089][0090]
其中linker为如下8种结构:
[0091][0092]
一种式(iii)所示靶向泛素化诱导bcr-abl蛋白降解的化合物的合成方法:8种式(iii)所示靶向泛素化诱导bcr-abl蛋白降解的化合物的合成方法
[0093][0094]
称取3.06g化合物15(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物16白色粉末2.73g,产率60%;
[0095]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.335g化合物16(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄
色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物17白色粉末0.30g,产率50%。
[0096][0097]
称取3.46g化合物18(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物19白色粉末2.93g,产率60%;
[0098]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.352g化合物19(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物20白色粉末0.31g,产率50%。
[0099][0100]
称取3.56g化合物21(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物22白色粉末2.99g,产率60%;
[0101]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.362g化合物22(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物23白色粉末0.32g,产率50%。
[0102][0103]
取3.46g化合物24(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物325白色粉末2.93g,产率60%;
[0104]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加
入0.352g化合物25(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物26白色粉末0.31g,产率50%。
[0105][0106]
称取2.83g n-boc 6氨基酸(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物27白色粉末3.18g,产率60%;
[0107]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.318g化合物27(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物28白色粉末0.28g,产率50%。
[0108][0109]
称取2.88g n-boc 7氨基酸(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物29白色粉末3.18g,产率60%;
[0110]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.318g化合物29(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物30白色粉末0.28g,产率50%。
[0111][0112]
称取2.88g n-boc 10氨基酸(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物31白色粉末3.18g,产率60%;
[0113]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea
(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.318g化合物31(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物32白色粉末0.28g,产率50%。
[0114][0115]
称取3.08g n-boc 12氨基酸(10mmol,1eq.),加入100ml thf溶解,加入3.87g dipea(30mmol,3eq),室温搅拌10min,加入5.70g hatu(15mmol,1.5eq.),40℃搅拌30min,加入3.10g化合物6(12mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物33白色粉末3.18g,产率60%;
[0116]
称取0.3g化合物4(0.60mmol,1eq.),加入50mlthf溶解,加入0.232g dipea(1.80mmol,3eq),室温搅拌10min,加入0.34g hatu(0.9mmol,1.5eq.),40℃搅拌30min,加入0.318g化合物33(0.72mmol,1.2eq.),40℃反应5h,反应结束冷却至室温,减压旋蒸的黄色油状,硅胶层析柱分离(dcm:meoh=15:1),烘干得化合物34白色粉末0.28g,产率50%。
[0117][0118]
称取2.09g化合物35(10mmol,1eq.)、3.72g化合物36(20mmol,2eq.)、1.9g cui(10mmol,1eq.)、0.7g pdcl2(pph3)2(1mmol,0.1eq.)加入100ml dmf溶解,100℃搅拌4h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物37白色粉末,溶于dcm,加入适量氢氧化钠(20mmol,2eq),常温水解反应3h,减压旋干,水相中加入过量的柠檬酸,析出白色絮状沉淀,减压过滤烘干得化合物38白色粉末2.65g,产率80%;
[0119][0120]
称取2.09g化合物35(10mmol,1eq.)、3.72g化合物36(20mmol,2eq.)、1.9g cui(10mmol,1eq.)、0.7g pdcl2(pph3)2(1mmol,0.1eq.)加入100ml dmf溶解,100℃搅拌4h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物34白色粉末;
[0121]
称取2.59g化合物37(10mmol,1eq.)、1.71g化合物39(10mmol,1eq.)、0.93gnabh3cn(15mmol,1.5eq.)、5mlacoh、加入50ml meoh溶解,50℃搅拌4h,反应结束冷却至室温,减压旋蒸的淡黄色油状,溶于dcm,加入适量氢氧化钠(20mmol,2eq),常温水解反应3h,减压旋干,水相中加入过量的柠檬酸,析出白色絮状沉淀,减压过滤烘干得化合物40白色粉末3.08g,产率80%;
[0122][0123]
称取2.09g化合物35(10mmol,1eq.)、3.72g化合物36(20mmol,2eq.)、1.9g cui
(10mmol,1eq.)、0.7g pdcl2(pph3)2(1mmol,0.1eq.)加入100ml dmf溶解,100℃搅拌4h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物37白色粉末;
[0124]
称取2.59g化合物37(10mmol,1eq.)、1.71g化合物41(10mmol,1eq.)、0.93gnabh3cn(15mmol,1.5eq.)、5mlacoh、加入50ml meoh溶解,50℃搅拌4h,反应结束冷却至室温,减压旋蒸的淡黄色油状,溶于dcm,加入适量氢氧化钠(20mmol,2eq),常温水解反应3h,减压旋干,水相中加入过量的柠檬酸,析出白色絮状沉淀,减压过滤烘干得化合物42白色粉末3.20g,产率80%
[0125][0126]
称取1.81g化合物43(10mmol,1eq.)、3.72g化合物36(20mmol,2eq.)、1.9g cui(10mmol,1eq.)、0.7g pdcl2(pph3)2(1mmol,0.1eq.)加入100ml dmf溶解,100℃搅拌4h,反应结束冷却至室温,减压旋蒸的淡黄色油状,加入200ml dcm溶解,加入10ml过量的tfa,室温反应2h,减压旋蒸得粗品,硅胶层析柱分离(dcm:meoh=3:1),烘干得化合物44白色粉末;
[0127]
称取2.31g化合物44(10mmol,1eq.)、1.71g化合物41(10mmol,1eq.)、0.93gnabh3cn(15mmol,1.5eq.)、5mlacoh、加入50ml meoh溶解,50℃搅拌4h,反应结束冷却至室温,减压旋蒸的淡黄色油状,溶于dcm,加入适量氢氧化钠(20mmol,2eq),常温水解反应3h,减压旋干,水相中加入过量的柠檬酸,析出白色絮状沉淀,减压过滤烘干得化合物45白色粉末3.08g,产率80%。
[0128]
一种药物组合物,(ⅲ)所示靶向泛素化诱导bcr-abl蛋白降解的化合物或其药学上可接受的盐和水合物,和药学上可接受的赋形剂。
[0129]
一种药物组合物,(ⅲ)所示靶向泛素化诱导bcr-abl蛋白降解的化合物,在药物组合物中加入药学上可接受的辅料制成临床上可接受的剂型。
[0130]
一种(ⅲ)所示靶向泛素化诱导bcr-abl蛋白降解的化合物在制备预防或/和治疗癌症的药物中应用。
[0131]
癌症为慢性粒细胞性白血病、急性粒细胞性白血病、慢性淋巴性白血病、急性淋巴性白血病。
[0132]
实施例4
[0133]
本发明所述的(i)(ⅱ)(ⅲ)化合物为一种蛋白水解靶向嵌合分子(protacs),其包括可以与bcr-abl蛋白底物相结合的部分、可以与e3结合的部分以及连接链,利用这种双功能小分子可以将目标蛋白和细胞内的e3拉近,从而使本来不能与e3结合的bcr-abl靶蛋白泛素化,进而被蛋白酶体识别并降解。
[0134]
n为liner的不同长度,首次引入“privileged scaffold”——嘧啶环,考察不同组成linker是否会对bcr-abl融合蛋白降解作用产生影响。
[0135]
(i)中n=11,优选的化合物降解bcr-abl蛋白效果更好,其抗肿瘤活性也更强。
[0136]
本发明还公开了一种药物组合物,包括上述化合物或其药学上可接受的盐,与药学上可接受的赋形剂。
[0137]
所述药物上可接受的赋形剂是指任何可用于药物领域的稀释剂、辅助剂和/或载体。
[0138]
本发明还公开了上述药物组合物制成的制剂,包括:在药物组合物中加入药学上可接受的辅料制成临床上可接受的剂型。所述临床上可接受的剂型为口服制剂、注射制剂或局部制剂。
[0139]
其中,口服制剂可为片剂、胶囊剂、溶液或混悬液;注射制剂可为注射溶液或混悬剂或可注射的干燥粉末,在注射前加入注射用水可立即使用;局部制剂可为软膏或溶液。
[0140]
其中,药学上可接受的辅料包括:口服制剂用的粘合剂、润滑剂、崩解剂、助溶剂、稀释剂、稳定剂、悬浮剂、色素或矫味剂;注射制剂用的防腐剂、加溶剂或稳定剂;局部制剂用的基质、稀释剂、润滑剂、防腐剂等。药物制剂可以经口服或胃肠外方式(如静脉内、皮下、腹膜内或局部)给药,如果某些药物在胃部条件下是不稳定的,可将其配制成肠衣片剂。
[0141]
实施例5实施例1-3所述(i)(ⅱ)(ⅲ)化合物的氢谱预测,
[0142]
dmp系列
[0143]
dmp6
[0144][0145]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.41(s,1h),8.47(s,1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.22(s,2h),4.44(m,1h),3.28(m,8h),3.06(m,2h),2.35(m,2h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.63(m,2h),1.50(m,2h),1.33(m,2h);
[0146]
dmp7
[0147][0148]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.41(s,1h),8.47(s,1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.22(s,2h),4.44(m,1h),3.28(m,8h),3.06(m,2h),2.35(m,2h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.63(m,2h),1.52(m,2h),1.33(m,2h),1.29(m,2h);
[0149]
dmp11
[0150][0151]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.41(s,1h),8.47(s,1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.22(s,2h),4.44(m,1h),3.28(m,8h),3.06(m,2h),2.35(m,2h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.63(m,2h),1.57(m,2h),1.52(m,2h),1.30(m,2h),1.30(m,2h),1.30(m,2h),1.29(m,2h),1.28(m,2h),1.27(m,2h);
[0152]
dmp12
[0153][0154]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.41(s,1h),8.47(s,1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.22(s,2h),4.44(m,1h),3.28(m,8h),3.06(m,2h),2.35(m,2h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.63(m,2h),1.57(m,2h),1.52(m,2h),1.30(m,2h),1.30(m,2h),1.30(m,2h),1.29(m,2h),1.28(m,2h),1.27(m,2h),1.26(m,2h);
[0155]
peg(n=1)
[0156][0157]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),10.02(s,1h),8.47(s,1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.48(m,2h),4.44(m,1h),4.31(m,2h),4.22(s,2h),3.52(m,4h),3.28(m,8h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),;
[0158]
peg(n=2)
[0159][0160]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),10.02(s,1h),8.47(s,1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.48(m,2h),4.44(m,1h),4.31(m,2h),4.22(s,2h),3.52(m,8h),3.28(m,8h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h);
[0161]
peg(n=3)
[0162][0163]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),10.02(s,1h),8.47(s,1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.48(m,2h),4.44(m,1h),4.31(m,2h),4.22(s,2h),3.52(m,12h),3.28(m,8h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h);
[0164]
peg(n=4)
[0165][0166]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),10.02(s,1h),8.47(s,1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.48(m,2h),4.44(m,1h),4.31(m,2h),4.22(s,2h),3.52(m,16h),3.28(m,8h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h);
[0167]
zsx系列
[0168][0169]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.79(s,1h),8.73(s,2h),8.47(s,
1h),8.61(s,2h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.44(m,1h),4.22(s,2h),3.58(s,2h),3.28(m,8h),3.15(m,4h),2.55(m,4h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h);
[0170][0171]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.79(s,1h),8.80(s,1h),8.67(s,1h),8.69(s,1h),8.53(s,1h),8.47(s,1h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.44(m,1h),4.22(s,2h),3.77(s,2h),3.58(s,2h),3.42(s,2h),3.28(m,8h),2.45(m,4h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.38(m,4h);
[0172][0173]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.79(s,1h),8.80(s,1h),8.67(s,1h),8.69(s,1h),8.53(s,1h),8.47(s,1h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.44(m,1h),4.22(s,2h),3.71(m,4h),3.58(s,2h),3.42(s,2h),3.28(m,8h),3.02(s,2h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.38(m,4h);
[0174][0175]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.79(s,1h),8.80(s,1h),8.67(s,1h),8.69(s,1h),8.53(s,1h),8.47(s,1h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.44(m,1h),4.22(s,2h),3.71(m,4h),3.58(s,2h),3.28(m,8h),2.45(m,4h),2.29(s,3h),2.23-1.98(m,2h),
2.21-2.11(m,2h),2.12(s,3h),1.38(m,8h);
[0176][0177]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.79(s,1h),8.98(s,1h),8.97(s,1h),8.80(s,1h),8.67(s,1h),8.47(s,1h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.44(m,1h),4.22(s,2h),3.58(s,2h),3.28(m,8h),2.54(m,1h),2.51-2.41(m,4h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.75-1.50(m,4h);
[0178][0179]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.79(s,1h),8.98(s,1h),8.97(s,1h),8.80(s,1h),8.67(s,1h),8.47(s,1h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.44(m,1h),4.22(s,2h),3.73-3.48(m,2h),3.36(m,1h),3.58(s,2h),3.33-3.08(m,2h),3.28(m,8h),2.54(m,1h),2.51-2.41(m,4h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.75-1.50(m,4h);
[0180][0181]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.79(s,1h),8.98(s,1h),8.97(s,1h),8.80(s,1h),8.67(s,1h),8.47(s,1h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.44(m,1h),4.22(s,2h),3.79-3.54(m,2h),3.27(m,1h),3.58(s,2h),3.40-3.15(m,2h),3.28(m,8h),2.63(m,1h),2.51-2.41(m,4h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.69-1.44(m,4h);
[0182][0183]1h nmr(d
6-dmso)δ11.06(s,1h),10.21(s,1h),9.79(s,1h),8.98(s,1h),8.97(s,1h),8.80(s,1h),8.67(s,1h),8.47(s,1h),8.34(m,1h),8.19(s,1h),7.68(m,1h),7.57(m,1h),7.53(m,1h),7.51(m,1h),7.17(m,1h),7.11(m,1h),5.28(s,1h),4.44(m,1h),4.22(s,2h),3.58(s,2h),3.28(m,8h),2.63(m,1h),2.54(m,1h),2.51-2.41(m,8h),2.29(s,3h),2.23-1.98(m,2h),2.21-2.11(m,2h),2.12(s,3h),1.75-1.50(m,4h),1.69-1.44(m,4h)。
[0184]
虽然本发明已通过参考优选的实施例进行了描述,但是本领域技术人员应当了解,在权利要求书的范围内可作出形式和细节上的各种变化。
