1.本发明涉及再利用包含有机成分、甚至有机和金属成分的废料的领域。对于汽车粉碎残余物(asr)的再利用而言,它具有特别有利的应用。
背景技术:
2.塑料在废料中占越来越大的比重,但其回收或再利用率仍然很低。
3.已为普通废料设立分类设施,以方便其再利用。然而,这些分类模式不适用于包含有机成分的废料,特别是由汽车产生的废料,更特别是报废车辆产生的粉碎残余物和/或混合物。
4.例如,汽车粉碎残余物难以再利用,因为它们是异质的,而且可能还含有对环境有害的流体残余物,例如但不限于制动液、防冻剂、机油的残余物。此外,这些汽车粉碎残余物可能含有例如来自安全气囊的弹出装置的爆炸性物质。大约90%的汽车粉碎残余物被送往垃圾填埋场或在焚烧厂处理。通过这些方法,这些残余物的有机成分、甚至有机成分和金属成分都很少或者甚至根本没有再利用。
5.即便如此,仍然存在允许再利用包含有机成分甚至有机和金属成分的废料的方法,例如物理分离方法、“高温”方法和湿法冶金方法。
6.混合物中废料的物理分离方法,例如通过浮选,使得废料的有机成分和金属成分得以分离。然而,回收率相对较低并且需要使用大量的水,其后这些水作为废水而不得不进行处理。
[0007]“高温”方法,诸如通过燃烧,例如通过焚烧,排放大量二氧化碳以及有毒气体,例如二恶英或氢卤酸。这些方法还需要约1200℃的高温,从而产生温度介于850℃和1100℃之间的烟气,因此从能源的角度来看是昂贵的。
[0008]
关于湿法冶金方法,它们需要大量的酸或碱溶液,或氰化物,因此产生在其实施的下游待处理的大量废水。此外,这些方法仅涉及金属成分的再利用。
[0009]
因此,上述方法显示出局限性。特别地,它们中没有一个允许通过限制其对环境的影响来再利用包含有机成分、甚至有机和金属成分的废料。
[0010]
在现有的解决方案中,熔盐浴中的氧化是一种例如用于处理有害废料和诸如废轮胎的废料的方法,这种情况下直接焚烧和废水处理是困难的。该方法基于使用盐或包含碳酸盐的盐混合物或这些化合物与氢氧化钠的混合物。将所述盐或盐混合物加热至超过其熔化温度以形成反应介质并引起所述废料的有机成分的氧化。
[0011]
熔盐具有大范围的电化学稳定性,允许有机成分发生氧化反应。它们的高离子电导率在反应介质中引起高交换动力学。此外,它们在环境层面上没有实质性的危险。
[0012]
尤其是从flandinet等人的文献《metals recovering from waste printed circuit boards(wpcbs)using molten salts(使用熔融盐从废印刷电路板(wpcb)中回收金属)》,journal of hazardous materials(有害材料学报),213-214,2012,485-490中已知一种使用包含氢氧化钠共晶混合物和氢氧化钾共晶混合物的熔盐处理来自电子产品的
废料的方法。所述共晶混合物具有170℃的熔化温度,允许在低温下特别是从250℃起氧化所述废料的有机成分。因此,降低了能源成本并降低了该方法对环境的影响。
[0013]
在这个背景下,本发明提出了一种在盐浴中氧化的替代方法,该方法可以克服上述缺点中的至少一个。
[0014]
更具体地,根据本发明的方法旨在能够以降低的能量成本再利用包含有机成分、甚至有机和金属成分的废料。有利地,根据本发明的方法还旨在在所述废料的处理过程中限制有害化合物的排放。
[0015]
本发明的其他目的、特征和优点将在阅读以下描述和附图时显现出来。应当理解,可以并入其他优点。
技术实现要素:
[0016]
为了实现该目的,根据本发明的一个实施方案提供了一种在熔盐浴中再利用包含有机成分的废料的方法,包括以下步骤:
[0017]
向反应器提供至少一种盐或盐混合物,其中至少一种盐,优选每种盐包含至少一种碱金属氢氧化物或此类氢氧化物的混合物;
[0018]
向反应器提供所述废料;
[0019]
在高于所述盐或盐混合物的熔点的温度下加热反应器以熔化所提供的所述盐或盐混合物,从而形成液体反应介质,然后引起所提供废料的有机成分的至少部分氧化、更优选完全氧化;和
[0020]
回收由所述有机化合物氧化产生的至少一种化合物;
[0021]
所述至少一种碱金属氢氧化物,优选每种碱金属氢氧化物包含结晶水作为反应介质中有机化合物的氧化剂,以引起氢气的产生,后者作为氧化反应产生的化合物被回收,用于其再利用。
[0022]
根据本发明的方法允许特别是通过回收能够在该方法的下游用作可燃气体或化学原料的氢气而再利用包含有机成分的废料。此外,由于所述废料的有机成分的氧化是在液体介质中进行的,因此根据本发明的方法可以限制有害化合物的排放并因此减少所述方法对环境的影响。
[0023]
可选地,本发明还可具有以下特征中的至少任何一个。
[0024]
向反应器提供的废料还可以包含金属成分,反应器在低于所述金属成分的沸点温度的温度下加热。优选地,将反应器加热到低于至少一部分金属成分的熔化温度的温度。所述方法还可包括通过过滤反应介质的金属成分的回收步骤。根据该特征的方法构成本发明的一个优选实施方案。根据上述特征的盐或盐混合物对金属没有腐蚀性,即在废料处理期间金属成分不会发生显著的氧化。因此,根据该特征的方法允许这些金属的后续再利用。此外,由于加热温度可以低于至少一部分金属成分的熔化温度,所以防止了至少一部分所述成分的熔化。金属成分可以保持固态并且因此可以在反应器的加热温度下与反应介质物理分离。
[0025]
可以以防止所述废料的有机成分热解的方式加热反应器。优选地,反应器可以在低于有机成分的热解温度的温度下加热。更优选地,反应器可以在低于至少一部分有机成分的沸点的温度下加热。因此,反应介质的温度可以限制在盐的熔化温度和所述成分的沸
点温度之间。因此,有机成分的至少部分、优选完全氧化可以在液体介质中进行。这有几个优点。首先,有机物在液体介质中氧化导致产生碳酸盐,这些碳酸盐被限制在熔盐中。因此,诸如所述的方法可大量减少二氧化碳的排放并防止二恶英的排放。其次,卤代化合物也被限制在熔盐中。因此,该方法可防止氢卤酸(如盐酸、氢氟酸或氢溴酸)的排放,其中溴化物通常用作阻燃剂,如多溴二苯醚(pbde)、六溴环十二烷(hbcdd)、四溴双酚a(tbbpa)和多溴联苯(pbb)。
[0026]
在该方法的实施要素中,至少反应器可以处于大气压下。诸如所述的熔盐具有低蒸气压且氧化反应在液体介质中进行,该方法实际上可以在大气压下进行。
[0027]
对于所述至少一种碱金属氢氧化物,优选每种碱金属氢氧化物或此类氢氧化物的混合物可以形成具有低熔点的化合物。例如,对于所述至少一种碱金属氢氧化物,优选每种碱金属氢氧化物或此类氢氧化物的混合物可以形成其熔化温度在50℃至300℃之间的化合物。使用具有低熔点的化合物可以限制形成反应介质所需的能量。因此,该方法的能量成本被最小化。对于所述至少一种碱金属氢氧化物,优选每种碱金属氢氧化物或此类氢氧化物的混合物可以是定义的或未定义的化合物。此外,对于所述至少一种碱金属氢氧化物,优选每种碱金属氢氧化物或此类氢氧化物的混合物可与结晶水形成共晶。使用所述至少一种碱金属氢氧化物和水之间的共晶能够降低盐或盐混合物的熔化温度。
[0028]
根据一个具体的实施方案,所述至少一种碱金属氢氧化物是氢氧化钾。更具体地,氢氧化钾与一水合物部分形成分子式为koh+koh
·
h2o(1:1)的共晶。因此,式koh+koh
·
h2o的共晶的熔化温度基本上等于100℃。
[0029]
根据本发明的方法的加热步骤可以配置为使得反应介质的温度为100℃至450℃,优选地170℃至350℃,甚至更优选地170℃至250℃。
[0030]
根据具体的实施方案,废料可以包括汽车粉碎残余物。优选地,废料可以由汽车粉碎残余物构成。
[0031]
根据具体的实施方案,废料可以包括固体回收燃料。优选地,废料可以由固体回收燃料构成。
[0032]
在该方法的实施要素中,反应器至少可以保持在包含惰性处理气体如氩气或氮气的气氛中。优选地,处理气体是氮气。因此,在气相中产生的氢气与所述气氛的反应受到限制,甚至被抑制,这使爆炸的风险最小化。
[0033]
在该方法的实施要素中,反应器至少可以由耐受所述液体反应介质的材料制成。优选地,反应器由不锈钢制成,例如选自碳钢、304和316型不锈钢,或具有钴合金基体(如司太立)或镍合金基体(如和)。实际上,使用对金属几乎没有腐蚀性或甚至根本没有腐蚀性的反应介质以及减少氢卤酸的排放有利地使得可以使用不锈钢来形成该方法的至少一些实施要素。具体地,反应器可以由不锈钢制成,在废料处理期间反应器壁没有任何显著腐蚀。
[0034]
根据一个具体的实施方案,该方法免除了在反应器中加入除水之外的氧化剂的步骤。结晶水用作有机化合物的氧化剂,其后不必向反应器中加入另一种氧化剂,例如氧气。由于避免了添加氧气,与氧气的存在加之所产生的氢气相关的爆炸风险被最小化。此外,结晶水的存在使得可以限制在该方法中加入水,从而减少水的消耗并减少该方法下游待处理的废水的体积。优选地,该方法免除了在反应器中加入除最初包含在碱金属氢氧化物中的
结晶水之外的氧化剂的步骤。
[0035]
回收由所述有机化合物氧化产生的所述至少一种化合物的步骤还可包括回收包含所产生的氢气的气体部分。除了产生的氢气之外,所述气体部分可还以包含多种无害气体,例如甲烷、氮气以及挥发性有机化合物。此外,这些气体可以通过本领域技术人员已知的技术分离,任选地进行再利用。
[0036]
该方法还可以包括添加选自加氢催化剂的至少一种催化剂的步骤。向反应介质中加入加氢催化剂可以通过多相催化提高氧化还原反应动力学以及产生的氢气的量。所述至少一种催化剂可包含金属颗粒,例如镍或铁基的金属颗粒,或此类颗粒的混合物。
附图说明
[0037]
通过以下附图所例示的本发明实施方案的详细描述,本发明的意图、目的以及特征和优点将更加清楚。
[0038]
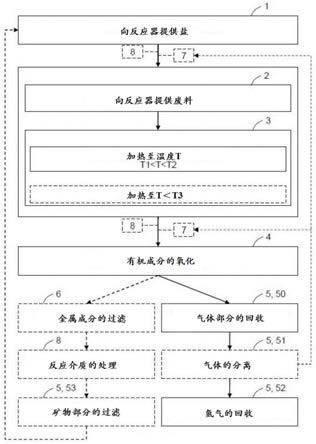
图1显示了根据本发明的一个实施方案的在熔盐浴中再利用包含有机成分的废料的方法的步骤。
[0039]
图2示出了根据本发明的另一个实施方案的在熔盐浴中再利用包含有机成分的废料的方法的步骤。
[0040]
附图作为示例给出,并不限制本发明。它们构成旨在促进对本发明的理解的示意图。
具体实施方式
[0041]
在开始详细论述本发明的实施方案之前,在下文中提及该方法的一般方面以及可能组合使用或替代地使用的可选特征。
[0042]
根据本发明的再利用废料的方法涉及包含有机成分的所有类型的废料。更具体地,该方法涉及再利用异质废料,异质废料包括有机成分,可能具有不同的性质,甚至还与金属成分混合。例如,所述废料可以是来自电气和电子设备的废料;汽车粉碎残余物,特别是报废车辆粉碎产生的残余物(asr);或由生活垃圾产生的固体回收燃料(srf)。
[0043]
所述方法可以进一步涉及被均匀分类以包含相似性质的有机成分的废料的再利用。例如,此类废料源自诸如聚对苯二甲酸乙二醇酯或聚乙二醇等材料,或源自聚酯纺织品。根据另一个实施例,该废料还可以是或者包括油,例如来自车辆的废油。
[0044]
所述方法还用使用过的有机分子,例如合成的或购买的,例如草酸钠、乙二醇或纤维素进行测试。由于熔盐是离子介质,具有极性键的分子通常是可溶的,并且在下文所述的温度下容易氧化。
[0045]
在废料为固体的情况下,所述废料通常在方法的上游、特别是在其在分类设施中的回收期间,通过机械作用例如通过切削、粉碎或压碎来成形。在该方法的上游不进行所述成形的情况下,根据本发明的再利用方法可以包括允许在步骤2中将所述废料提供给反应器之前对其进行成形的步骤。如此粉粹的废料具有对熔盐浴中的其有机成分的氧化作用更大的可及表面。在适用的情况下,除了在该方法的上游进行的成形之外,所述方法还可以包括该成形步骤以增加所述废料的可及表面。例如,废料的机械成形导致尺寸小于5毫米的碎片。
[0046]
根据上述特征,该方法涉及的废料是固体甚至液体。然而,在步骤2中,不排除气态废料,所述废料能够通过鼓泡提供至反应介质。
[0047]
为了使所述废料的有机成分氧化,根据本发明的方法包括使用盐或盐混合物,其中至少一种盐(优选是每种盐)包含至少一种碱金属氢氧化物或这些氢氧化物的混合物。所述至少一种碱金属氢氧化物(优选是每种碱金属氢氧化物)包含结晶水,用作反应介质中有机化合物的氧化剂。此外,结晶水可以降低盐或盐混合物的熔点。
[0048]
明确指出,一般地,在本发明的框架内,术语“结晶水”是指处于盐的晶体结构中的水分子。
[0049]
一般地,在本发明的框架内,术语“氧化剂”是指在氧化还原反应期间接受另一种化学物质的至少一个电子的化合物。
[0050]
结晶水包含在盐的晶体结构中,通过静电相互作用稳定。因此,在加热反应器的步骤期间,更具体地在为形成液体反应介质而使提供的所述盐或盐混合物的熔化期间,其蒸发受到限制。结晶水因此允许在有机成分液相中的氧化,特别是通过避免额外添加氧化剂。
[0051]
此外,结晶水引起氢气的产生,这一优势在阅读下文所展示的实施例时会更清楚地体现出来。更具体地,产生的氢气至少部分地、甚至大部分地、甚至全部地由废料还原结晶水产生。
[0052]
至少一种盐(优选是每种盐)包含至少一种碱金属氢氧化物或此类氢氧化物的混合物。事实上,根据要再利用的废料类型使用不同的碱金属氢氧化物可能是有利的,例如以这种方式调整方法的成本。此外,因此可以改变所述氢氧化物与有机成分、甚至有机和金属成分,以及与由所述有机成分氧化产生的化合物的相互作用特性。
[0053]
至少一种碱金属氢氧化物(优选是每种碱金属氢氧化物)包含结晶水。例如,氢氧化物是共晶或确定相形式的氢氧化钠,或优选氢氧化钾。
[0054]
至少一种碱金属氢氧化物优选与结晶水形成共晶。因此,使用共晶引起盐的熔化温度低于纯碱金属氢氧化物的熔化温度,这可以限制反应器的加热温度。因此,获得了该方法的较低能量影响。
[0055]
举例来说,碱金属氢氧化物与结晶水确定的主要相在下表中给出,总结了用碱金属氢氧化物定义的主要化合物(p.pascal,nouveau trait
é
de chimie min
é
rale(矿物化学新条约),masson and cie,volume ii(1and 2),paris,1963;f.-z.roki,m.-n.ohnet,s.fillet,c.chatillon,i.nuta,j.chem.thermodynamics(化学热力学杂志),80,2015,147-160)。
[0056]
表1
[0057][0058]
举例来说,下表给出了碱金属氢氧化物与结晶水的主要共晶及其熔化温度。然而,相并不总是被识别出来,如符号(?)所示。
[0059]
表2
[0060][0061]
包含在所述至少一种盐中的碱金属氢氧化物的混合物还可以形成共晶。建立了无水碱金属氢氧化物的二元相图,但没有碱金属氢氧化物与水的三元图,具体地是由于根据水的摩尔分数和根据混合物的碱金属的水分子的共享可能的相数。然而,在水性介质中存在具有确定相的化合物,例如naoh-lioh-h2o(a.lach,l.andre,a.lassin,m.azaroual,j.-p.serin,p.c
é
zac,j.solution chem.(溶液化学杂志),44,2015,1424-1451)。下表给出了可与水一起用作熔盐的无水氢氧化物的二元体系的共晶熔化温度。
[0062]
表3
[0063]
[0064][0065]
在140℃至200℃使用碱金属氢氧化物moh(m=k、na、rb或cs)对熔融介质中的水的瞬态的测量表明,氢氧化钾是保留水最好的氢氧化物,而氢氧化钠最容易释放水((w.m.vogel,k.j.routsis,v.j.kehrer,d.a.landsman,j.g.tschinkel,journal of chemical and engineering data(化学与工程数据杂志),12(4),1967,465-472)。此外,已知一水氢氧化锂在500℃下熔化一天,每摩尔lioh还可以保留0.05摩尔h2o(p.pascal,nouveau trait
é
de chimie min
é
rale(矿物化学新条约),masson and cie,volume ii(fascicule 1),paris,1963)。
[0066]
基于经济性以及其保留结晶水的能力的考虑,优选选择氢氧化钠以在根据本发明的方法中至少部分地形成熔盐浴。
[0067]
更优选地,盐因此包含具有式koh+koh.h2o的氢氧化钾,其熔点为100℃(p.pascal,nouveau trait
é
de chimie min
é
rale(矿物化学新条约),masson and cie,volume ii(fascicule 2),paris,1963)。也可以提供使用氢氧化钠和氢氧化钾的混合物。例如,氢氧化钠和氢氧化钾的混合物的分子式为naoh-(koh+koh.h2o)。
[0068]
用氢氧化钠和氢氧化钾之间的不同摩尔比的naoh-(koh+koh.h2o)混合物进行实验。此外使用混合物naoh-(koh+koh.h2o)的非完美确定的相。在任何情况下,氢氧化钾的结晶水都会引起有机材料的氧化。
[0069]
此外,可以提供使用包含至少一种碱金属氢氧化物m的化合物,其具有式moh-h2o-x,其中x可以是例如醇(甲醇、乙醇)或氨,其中醇或水构成溶剂。x也可以是碱金属盐或过渡金属。
[0070]
有机成分的整体氧化反应根据熔盐氧化机制展开。该反应包括通过溶剂分解对有机成分进行溶液处理。溶剂分解,一般地,在本发明的框架内,对应于有机成分与包含在反应介质中的化学物质之间的反应,以溶解全部或部分所述成分。溶剂分解后,在均质液相中氧化有机成分被结晶水溶剂分解所产生的产物。然而,溶剂分解和氧化可以同时发生。此外,有机成分的全部或部分溶解可以直接由所述成分的氧化引起。
[0071]
通过阻止二恶英的排放,废料的有机成分的氧化尤其会引起碳酸盐的产生。这些碳酸盐保持溶解在反应介质中,减少甚至防止碳氧化物,特别是一氧化碳或二氧化碳的排放。实际上,在反应介质所产生的气体部分中没有测量到超过20ppm的二氧化碳排放,20ppm是用来进行测量的设备的检测极限。此外,废料产生的任何卤化部分都会转化为卤离子。卤离子通过静电相互作用被限制在反应介质中,从而限制了氢卤酸如盐酸、氢溴酸或氢氟酸的排放。然而,根据在浴中的停留时间,并考虑到这些氢卤酸的低沸点温度,可以在反应器的出口处实施高温气体的洗涤,以防止任何痕量氢卤酸的排放。
[0072]
废料中有机成分的氧化也会引起氢气的产生。通过使用草酸钠作为待再利用的废料实施根据本发明的方法,揭示了结晶水作为氧化剂用于生产氢气的作用。草酸钠是一种不含任何氢原子的有机分子。在根据该方法氧化该分子期间,在反应器中观察到氢气的产
生。产生的氢气的量对应于草酸钠氧化所需的摩尔数。因此,氢气来自对草酸钠起氧化剂作用并包含氢原子的物质,其指向结晶水。
[0073]
同样地,使用聚对苯二甲酸乙二醇酯瓶作为待再利用的废料实施根据本发明的方法引起氢气的产生,氢气的量大于聚对苯二甲酸乙二醇酯单体中所含氢的摩尔数。在这种情况下,产生的氢气共同来自有机材料和结晶水的还原。使用粉状纤维素也验证了该结论。
[0074]
根据一个具体实施方案,将加氢催化剂加入液体反应介质中。添加这些催化剂会使有机成分的氧化重新定位在催化剂表面而不是均质的液相中。然后通过多相催化产生氧化反应,实际上需要水分子和有机成分之间较少的接触。因此提高结晶水的还原反应动力学以及因此产生的氢气的量。加氢催化剂包含金属颗粒,优选具有镍或铁基的金属颗粒,甚至这些颗粒的混合物。
[0075]
举例来说,该方法在图1和图2中示出,其中该方法的替代方案由平行路径指示并且可选步骤由虚线指示。如图1所示,该方法包括:步骤1,在其期间,根据上文所述特征,将至少一种盐或盐混合物提供至反应器;步骤2,在其期间,将废料提供给反应器;以及步骤3,在高于盐或盐混合物的熔化温度t1的温度t下加热反应器。优选地,温度t介于温度t1和温度t2之间,温度t2选自废料的有机成分的热解温度,并且优选选自这些成分的至少一部分的沸点温度。在废料包含金属成分的情况下,温度t还低于金属成分的沸腾温度,优选低于其熔化温度。根据一个具体实施方案,反应介质的温度介于100℃和450℃之间,优选介于170℃和350℃之间。在高于100℃的温度下工作确实是有利的,以便一方面为氧化反应提供热能。另一方面,可以获得低粘度的熔盐,以有利于熔盐溶液更好地润湿废料表面以及反应介质的有效混合。根据一个具体实施方案,反应介质的温度介于170℃和250℃之间,特别是当有机成分可以在低温下被结晶水氧化时。
[0076]
通过上文所述的三个步骤获得液体反应介质,其包含盐或熔盐的混合物以及废料,由此在步骤4引起废料的有机成分的整体氧化反应。这三个步骤的相对顺序可以根据方法的实施方案进行修改。特别地,如图1所示,步骤1、2可以将盐或盐混合物与废料依次或作为混合物引入反应器中。然后可以在步骤3中在温度t下加热反应器。或者,可以在步骤1将包含盐或盐混合物和废料的混合物一次性或优选逐渐引入到预先在温度t下加热的反应器3中。替代方案如图2所示。因此,盐的逐渐熔化可以使废料进行溶剂分解和氧化反应,并防止废料的热解。此外,逐渐加入该混合物可以防止反应介质的温度下降。在将盐和废料引入反应器之前,还可以将盐熔化并加热废料。因此,根据该具体实施方案的方法可以防止在步骤3加热反应器期间由反应器内部温度升高引起的延时。该实施方案还允许连续实施该方法,根据该方法将盐或盐混合物与废料连续引入反应器,同时还允许连续排空反应器。
[0077]
如图1和2所示,在步骤1引入盐或盐混合物期间或之后,可以进一步在步骤8将催化剂添加到反应器中。优选地,催化剂与盐混合。还可以规定,步骤8的催化剂添加稍后进行,例如,可以当形成液体反应介质时引入催化剂。
[0078]
有机成分的整体氧化反应(步骤4)以上述方式发生。在步骤4的该氧化期间,反应器保持在温度t,即使调节温度t,仍然保持在介于t1和t2之间,甚至介于t1和t3之间,t3是可以与有机成分混合的至少一部分金属成分的沸腾温度。优选地,t3是可以与有机成分混合的大多数金属成分的熔化温度。特别地,可以提高温度t以提供热能从而加速有机成分的氧化反应。此外,有利地形成反应介质的混合物以促进反应。
[0079]
用于实施根据本发明的方法的反应器可以具有通过传导(例如通过电阻器加热)、通过对流(例如通过在反应器中循环的高温气流)或通过发光或电磁辐射(感应、微波)的加热模式。根据待处理的固相、液相或气相有机废料的体积或质量,包括构建其所需材料的熔炉的性质会有所不同;加热方法也可以根据本领域技术人员已知的技术进行调整。此外,加热模式导致对反应器中熔融物料的搅拌模式的选择。例如,为了确保反应介质的混合,由电阻器加热的反应器包括至少一种能够混合所述介质的元件,例如旋转壁、转子或叶片。
[0080]
由于根据本发明的步骤3反应介质在加热温度的范围内本质上对金属没有腐蚀性,并且避免了氢卤酸的排放,所以反应器可以由金属制成,优选由不锈钢制成,在该方法的实施期间反应器壁没有任何显著的腐蚀。还可以规定,反应器具有钴合金基体(例如司太立),或镍合金(例如和)。注意,也可以使用不属于金属类别的其他材料,例如碳或氮化硼。实际上,在不存在氧气和二氧化碳的情况下,例如碳石墨或玻璃碳在高达450℃的加热温度下不会被水氧化。
[0081]
在有机成分的氧化反应(步骤4)期间,获得两种甚至三种部分:液体部分,包含反应介质和氧化产物如碳酸盐;气体部分,包含有机成分由步骤4的氧化所产生的多种气体,尤其是氢气;固体部分,例如在废料包含金属成分的情况下。
[0082]
如图1和2所示,根据本发明的方法包括回收由有机成分被氧化(步骤4)产生的至少一种化合物的步骤5。该方法尤其包括从反应介质释放的气体部分的回收(步骤50)。氧化所产生的一种或多种气体可以被载气带走。优选地,向反应器供应连续流的载气(步骤7)以携带由氧化步骤4所产生的一种或多种气体。因此在有机成分的氧化步骤4的上游的该方法的任何步骤之间向反应器供应载气。更优选地,载气是中性气体,例如氩气或氮气,以防止产生的氢气发生爆炸的任何风险。优选地,载气是氮气以限制该方法的成本。
[0083]
此外,通过热重热差分析(由缩写tga-tda表示)进行的测量表明,氢氧化钾中所含的结晶水在高于300℃时可以至少部分释放。为了补偿氧化反应所需的结晶水,可以将载气水合,特别是对于反应器的高温加热(步骤3),例如对于介于350℃和450℃之间的温度范围。由此,在液体反应介质和液体上方的气相之间保持蒸汽形式的水平衡。尽管载气的这种水合在高达350℃(对应于易氧化分子的温度区)似乎没有任何重要性,但在高于350℃的温度下氧化导致气体产量似乎有所增加。
[0084]
步骤50回收的气体部分由多种气体组成,例如氢气、甲烷和氮气,以及挥发性有机化合物。这些不同的成分可以通过本领域技术人员已知的技术分离(步骤51)。例如,通过将气体部分的温度降低到低于80℃来冷凝挥发性有机化合物。分离气体的目的是再利用它们。特别地,回收氢气(步骤52)以再利用作可燃燃料或化学原料。甲烷可以回收作为可燃气体再利用。此外,可以回收氮气以用作载气以向反应器供应(步骤7)。
[0085]
包含废料的金属成分的固体部分可以通过过滤步骤6来回收。使用至少一个筛网从反应介质中进行过滤,优选过滤尺寸小于金属成分尺寸例如基本上等于0.8mm的不锈钢筛网。当反应介质处于反应器被加热步骤3的温度时,特别是在至少一部分金属成分的熔化温度高于反应器的被加热步骤3的温度的情况下,可以进行该过滤步骤6。此外,该过滤步骤6可以在盐或盐混合物的熔化温度与废料可包含的所有金属成分的熔化温度之间的温度下进行。例如,该温度可以对应于反应器的加热步骤3的温度或在反应介质冷却之后达到。反应介质可以进一步冷却至低于盐或盐混合物的熔化温度的温度。在使用至少一个筛网进行
步骤6的过滤之前,可以将直接来自固相的反应介质溶解在一定体积的水中。根据该示例,筛网的尺寸可以小于当盐或盐的混合物熔化时所使用的尺寸。
[0086]
可以对包含反应介质和步骤4的氧化的产物例如碳酸盐的液体部分进行处理(步骤8),以再生盐或盐混合物,以在该方法中重复使用。例如,溶解在一定体积水中的反应介质用生石灰或具有化学式ca(oh)2的熟石灰处理(步骤8),优选在室温下。添加石灰会引起碳酸钙的冷沉淀,并产生可用于混凝土的caco3样品,例如方解石,甚至是方解石和文石的混合物。
[0087]
此外,处理步骤8可以为碱金属氢氧化物的再生提供氢氧根离子。盐或盐混合物因此可以在该方法中重复使用。
[0088]
与气体、液体和固体部分的管理或回收有关的方法的实施利用的单元操作,例如混合器、过滤,其实施元件在市场上存在。
[0089]
该方法可以通过使用“分批”类型的常规反应器(即包括小室(cellule))不连续地进行。盐或盐混合物以及废料被引入小室。根据该方法的步骤,由此引入的废料被再利用。新的废料,甚至是一批新的盐或盐混合物,会被引入小室进行再利用。因此,该方法是不连续的并且依次处理不同批次的废料。或者,该方法还可以通过使用包括至少一个入口和一个出口的反应器连续进行,该至少一个入口和一个出口配置为使得废料的供应,甚至由有机成分氧化产生的至少一种化合物例如氢气的回收是连续进行的。为此,考虑了包括蜗杆的反应器,同时仍考虑所产生气体的爆炸性。
[0090]
本发明不限于上述实施例,而是扩展到权利要求所涵盖的所有实施例。
[0091]
特别地,可以规定,该方法在从大气压到更高压力的压力范围内进行。由于盐或熔盐混合物具有低蒸气压且氧化反应在液体介质中进行,该方法实际上可以在大气压下进行。最大压力是出于安全方面的考虑而选择的,因此取决于反应器和方法的实施要素。优选地,该方法可以在小于8巴的压力下进行。
