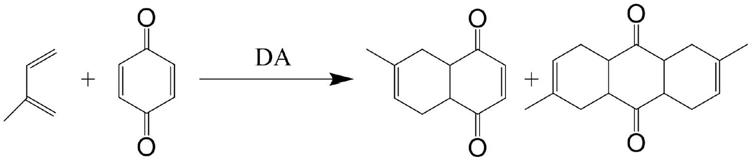
1.本发明涉及由生物质c5、c6共轭二烯烃和对苯醌制备烷基十氢化萘航空煤油的方法。
背景技术:
2.19世纪以前,未发现化石燃料的社会依靠植物生物质来满足其能源需求。如今,全球范 围内的能源危机和相关的环境影响再度引发了有关生物质转化的广泛研究与开发计划。在 2012年“国际人人享有可持续能源年”的背景下,国际可再生能源署发起了全球路线图“remap 2030”,力争到2030年将可再生能源的份额提高一倍。美国能源部还设定到到2030年,美国 有20%的运输燃料、25%的化学品将由生物质生产。shell、uop、petrobras、conoco
‑
phillips、 dupont、dow和bp等传统石油和化工公司已经开发了生物燃料和生化产品生产技术和基础设 施。根据经济法则,随着石油储量的减少,石油产品的价格将上涨,生物燃料最终将具有成 本竞争力,甚至比石油衍生的燃料更便宜。
3.生物质原料的高碳含量(40%)可以满足运输燃料的碳需求,包括汽油、柴油和航空煤油。 利用生物质和生物质衍生的化学品生产长链柴油(c
12
‑
c
22
)和航空煤油(c8‑
c
16
)极具吸引力。 目前国际上大部分的生物质通过加氢脱氧合成航空煤油范围烷烃的工作都以支链或直链烷烃 为主,若能合成存在环张力环烷烃,将显著提高航空煤油的密度,使其性能更加优越;此外 开发由生物质制备航空煤油的反应新路线并对反应过程进行优化整合,将更有利于生物质航 空煤油技术的工业化。
4.多环烷烃十氢萘和烷基十氢萘的密度在0.86
‑
0.89g/ml之间,十六烷值在37
‑
48之间, 是一种理想的高密度燃料,在汽轮机以及柴油发动机中燃烧性能良好。目前十氢萘主要由煤 路线获得,而生物质路线获得十氢萘却鲜有报道。本课题组先后以糠醛衍生物环戊醇和半纤 维素衍生物环戊酮为原料合成十氢萘:环戊醇在温和条件下通过脱水、低聚/重排及加氢反应 获得多环烷烃,其中十氢萘的选择性为77%(acs sustainable chemistry&engineering, 2016,4,6160
‑
6166);环戊酮经自身羟醛缩合、加氢脱氧、异构化获得十氢萘,总碳收率达 74%(acs sustainable chemistry&engineering,2019,7,17354
‑
17361)。此外,利用更 多的生物质平台化合物作为反应底物,开拓由生物质制备航空煤油的反应路线,将更有利于 生物质航空煤油技术的应用。
5.异戊二烯作为工业上重要的共轭二烯烃,其年产量达80万吨。此外,异戊二烯也可以由 生物质通过改良的大肠杆菌生产,经济分析表明,该生物路线的能源效率和相对成本可代替 化石基异戊二烯的生产途径。2,3
‑
二甲基
‑
1,3
‑
丁二烯是另一种简单的生物质衍生1,3
‑
二烯, 在离子液体中可由生物质频哪醇通过酸催化脱水简单制备。重要化工原料环戊二烯除了石油 裂解生产外,还可由生物质平台化合物糠醇脱水制备。纤维素基3
‑
甲基
‑2‑
环戊烯酮可直接 加氢脱氧到甲基环戊二烯。生物质平台化合物异己二醇经酸脱水可高效制备2
‑
甲基
‑
1,3
‑
戊 二烯和4
‑
甲基
‑
1,3
‑
戊二烯。高活性亲双烯体对苯醌也可由木质素经过解聚、氢解、氧化得 到。因此,本发明的原料均可通过可再生生物质资源获取,并在温和
条件下通过一锅内狄尔 斯
‑
阿尔德反应和加氢脱氧反应以高收率直接获得高热稳定性和高能量密度烷基十氢化萘航 空煤油。
技术实现要素:
6.本发明目的在于提供一条以生物质c5或c6共轭二烯烃和对苯醌为原料一锅直接合成高密 度烷基十氢化萘航空煤油的新路线。该过程在一锅内通过两步完成,首先,c5、c6共轭二烯烃 和对苯醌在热催化下发生狄尔斯
‑
阿尔德反应,进一步在双功能催化剂作用下加氢脱氧合成烷 基十氢化萘。本发明中所用原料c5、c6共轭二烯烃和对苯醌可从化石资源获得,亦可由廉价 易得的木质纤维素转化获得,因此原料具有可再生的特点。此外,本发明涉及的催化剂制备 方便,反应工艺简单,目标产物收率高,一锅方式简化了反应步骤、节约了能源成本,提供 了由生物质平台化合物直接合成高热稳定性(分解温度≥482.22℃)和高能量密度(41.14 mj
·
l
‑1)烷基十氢化萘航空煤油的新方法。
7.为实现上述目的,本发明采用的技术方案为:
8.一种由共轭二烯烃和对苯醌一锅合成航空煤油的方法,以生物质c5或c6共轭二烯烃和对 苯醌为原料制备烷基十氢化萘航空煤油分为一锅两步反应:
9.第一步,反应底物c5或c6的共轭二烯烃和对苯醌在加热条件下进行狄尔斯
‑
阿尔德反应 合成中间产物环加成化合物;
10.第二步,中间产物环加合物在氢气气氛下经双功能催化剂催化进行加氢脱氧反应,生成 烷基十氢化萘烷烃化合物。
11.基于以上技术方案,优选的,反应底物生物质c5或c6共轭二烯烃为异戊二烯、2,3
‑
二甲 基
‑
1,3
‑
丁二烯、环戊二烯、甲基环戊二烯、2
‑
甲基
‑
1,3
‑
戊二烯、4
‑
甲基
‑
1,3
‑
戊二烯中的 一种或两种以上。
12.基于以上技术方案,优选的,c5或c6的共轭二烯烃和对苯醌的摩尔比在1:5
‑
20:1之间, 优选为1:1
‑
5:1;双功能催化剂与对苯醌的质量比在0.01
‑
0.30之间,优选为0.1
‑
0.3。
13.基于以上技术方案,优选的,第一步,所述狄尔斯
‑
阿尔德反应中,反应温度为20
‑
120℃; 反应时间为0.5
‑
12小时;
14.第二步,所述加氢脱氧反应中,氢气压力为0.1
‑
20mpa;反应温度为140
‑
220℃,优选 为180
‑
220℃;反应时间为8
‑
24小时,优选为10
‑
24小时。
15.基于以上技术方案,优选的,第一步的狄尔斯
‑
阿尔德反应和第二步的加氢脱氧反应在釜 式反应器中进行;具体地,在釜式反应器中分别投入反应底物c5或c6的共轭二烯烃和对苯醌、 溶剂、双功能催化剂,共轭二烯烃和对苯醌在20
‑
120℃下发生狄尔斯
‑
阿尔德反应,反应 0.5
‑
12小时生成环加合物后,向釜内通入氢气,氢气压力在0.1
‑
20mpa之间,反应釜升温 至140
‑
220℃,环加合物在氢气气氛下经双功能催化剂催化加氢脱氧反应,反应时间8
‑
24 小时。
16.基于以上技术方案,优选的,加氢脱氧反应采用的双功能催化剂具体为a/x负载型双功 能催化剂,包括活性金属a和载体x两部分;活性金属a为钯、铂、钌、铑、铱、铜、镍、 钼、铁、铼中的一种或两种以上,活性金属负载量为0.1
‑
20wt%,优选为5
‑
20%;所述载体x 为氧化锆、氧化钛、氧化锌、氧化镁、氧化铝、氧化硅、h
‑
y型分子筛、h
‑
β型分子筛、h
‑
usy 型分子筛(如从南开大学催化剂厂购买,si/al=5.5)、h
‑
zsm
‑
5型分子筛、活性炭中的一种 或两
种以上。
17.基于以上技术方案,优选的,上述双功能催化剂采用等体积浸渍法制备:配制质量浓度 0.1
‑
20wt%的金属前驱体(如pdcl2、ptcl2、rucl3、rhcl3等)水溶液,加入上述载体进行 等体积浸渍,负载后催化剂中金属负载量为0.1
‑
20wt%,之后室温下静置2小时以上,在 60
‑
150℃下干燥5小时以上,再在300
‑
800℃空气氛围下焙烧1
‑
6小时,200℃
‑
600℃氢气 还原1
‑
10小时,最后待温度降低至室温后通入含体积浓度1
‑
3%氧气的氮气钝化0.5
‑
4小时。
18.基于以上技术方案,优选的,第一步的狄尔斯
‑
阿尔德反应和第二步的加氢脱氧反应在同 一釜内无溶剂或同一溶剂下进行,采用溶剂为甲醇、乙醇、丙醇、异丙醇、丁醇、异丁醇、 环己烷、十三烷、正己烷、二氯甲烷、1,4
‑
二氧六环、乙酸乙酯、二甲基亚砜、n
‑
甲基吡咯 烷酮、四氢呋喃、乙腈、甲苯的一种或多种,底物对苯醌的质量浓度为0.02%
‑
100%,优选为 20
‑
80%。
19.本发明具有如下优点:
20.本发明所提供的航空煤油范围烷基十氢萘烷烃化合物合成路线是以木质纤维素平台化合 物对苯醌和生物质基c5或c6共轭二烯烃作为起始原料,为直接由生物质平台化合物制备热稳 定的航空燃料十氢化萘开辟了新思路,减少了对化石能源的依赖的同时规避了传统化石能源 生产的纯度低、产量小的难点。
21.本发明利用狄尔斯
‑
阿尔德反应高效构建存在环张力多环烷烃,显著提高了航空煤油的密 度;采用狄尔斯
‑
阿尔德和加氢脱氧两步反应一锅方式省去中间产物的分离和纯化步骤,进一 步降低能耗、缩短反应路线,从而达到降低产品损失、能源成本和废物输出的目的;双功能 催化剂由较为常见的金属和固体酸催化剂合成,制备方便,成本较低,催化性能优异。
22.本发明的原料来源广、反应路线短、工序操作简单、反应条件温和、目标产物选择性高, 因此本发明的方法是一种较为实用的制备高密度航空煤油的方法。
附图说明
23.图1.实施例103异戊二烯和对苯醌热催化狄尔斯
‑
阿尔德反应的gc谱图;
24.图2.实施例103异戊二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化合物甲基四氢萘 醌的1h
‑
nmr谱图;
25.图3.实施例103异戊二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化合物甲基四氢萘 醌的
13
c
‑
nmr谱图;
26.图4.实施例103异戊二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化合物二甲基十氢 蒽二酮的1h
‑
nmr谱图;
27.图5.实施例103异戊二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化合物二甲基十氢 蒽二酮的
13
c
‑
nmr谱图;
28.图6.实施例103异戊二烯和对苯醌一锅实现狄尔斯
‑
阿尔德和加氢脱氧反应的gc谱图;
29.图7.实施例103加氢脱氧产物甲基十氢化萘的ms谱图;
30.图8.实施例1042,3
‑
二甲基
‑
1,3
‑
丁二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化 合物二甲基四氢萘醌的1h
‑
nmr谱图;
31.图9.实施例1042,3
‑
二甲基
‑
1,3
‑
丁二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化 合物二甲基四氢萘醌的
13
c
‑
nmr谱图;
32.图10.实施例1042,3
‑
二甲基
‑
1,3
‑
丁二烯和对苯醌一锅实现狄尔斯
‑
阿尔德和加氢脱氧 反应的gc谱图;
33.图11.实施例104加氢脱氧产物二甲基十氢化萘的ms谱图;
34.图12.实施例105环戊二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化合物的1h
‑
nmr 谱图;
35.图13.实施例105环戊二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化合物的
13
c
‑
nmr 谱图;
36.图14.实施例105环戊二烯和对苯醌一锅实现狄尔斯
‑
阿尔德和加氢脱氧反应的gc谱图;
37.图15.实施例105加氢脱氧产物十氢
‑
1,4
‑
甲烷萘的ms谱图;
38.图16.实施例106甲基环戊二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化合物的1h
ꢀ‑
nmr谱图;
39.图17.实施例106甲基环戊二烯和对苯醌经狄尔斯
‑
阿尔德反应所得环加成化合物的 13
c
‑
nmr谱图;
40.图18.实施例106甲基环戊二烯和对苯醌一锅实现狄尔斯
‑
阿尔德和加氢脱氧反应的gc 谱图;
41.图19.实施例106加氢脱氧产物1
‑
甲基三环[6.2.1.0
2,7
]十一烷的ms谱图。
具体实施方式
[0042]
下面将以具体的实施例来对本发明加以说明,但本发明的保护范围不局限于这些实施例。
[0043]
下述实施例中双功能催化剂以金属负载量为5%的pd/h
‑
β为例,制备方法如下:配制质 量浓度10wt%的pdcl2水溶液2g,加入2g h
‑
β分子筛,补加适量水进行等体积浸渍,负载 后催化剂中金属负载量为5wt%,之后室温下静置12小时,在100℃下干燥10小时以上, 再在550℃空气氛围下焙烧4小时,300℃氢气(体积浓度60%)还原4小时,最后待温度降 低至室温后通入含体积浓度1%氧气的氮气钝化4小时。参照上述方法可以调整pd的负载量、 活性金属成分、载体种类,制备出a/x负载型双功能催化剂。
[0044]
1.生物质共轭二烯烃异戊二烯和对苯醌热催化狄尔斯
‑
阿尔德反应(反应物比例、温度、 时间影响)
[0045]
在30ml间歇式的耐压反应釜中加入一定量的异戊二烯,对苯醌(10mmol),加入溶剂 甲苯(5.0g),在一定的温度下反应特定的时间。
[0046]
表1.热催化狄尔斯
‑
阿尔德的反应结果
[0047][0048][0049]
表1结果表明,反应温度、反应时间和反应物比例对产物分布影响较大,随着温度提高, 甲基四氢萘醌收率提高,但继续升高温度,甲基四氢萘醌选择性下降,二甲基十氢蒽二酮收 率上升;随着反应时间延长,甲基四氢萘醌收率提高,继续延长反应时间,甲基四氢萘醌进 一步转化为二甲基十氢蒽二酮,二甲基十氢蒽二酮选择性提高,甲基四氢萘醌收率下降;异 戊二烯比例增加,甲基四氢萘醌选择性降低,二甲基十氢蒽二酮选择性提高。因此在较为温 和的实验条件下,即异戊二烯和对苯醌摩尔比在1
‑
5,80℃
‑
100℃的温度区间反应6
‑
10小时, 可获得甲基四氢萘醌大于80%的收率。
[0050]
2.生物质共轭二烯烃异戊二烯和对苯醌热催化狄尔斯
‑
阿尔德反应(溶剂影响)
[0051]
在30ml间歇式的耐压反应釜中加入异戊二烯(10mmol),对苯醌(10mmol),加入一 定量溶剂,在80℃下反应6小时。
[0052]
表2.不同溶剂对狄尔斯
‑
阿尔德反应活性的影响
[0053][0054][0055]
由表2结果可以看出,所使用的溶剂对狄尔斯
‑
阿尔德影响不大,其中四氢呋喃、甲苯、 1,4
‑
二氧六环对该反应具有相对较好的效果。以1,4
‑
二氧六环为溶剂考察底物浓度对反应 的影响。结果发现,底物浓度对狄尔斯
‑
阿尔德反应存在明显的影响,甲基十氢化萘收率随着 底物浓度的增加而提高,但无溶剂条件下的甲基十氢化萘产率较低。因此,该反应需要在一 定溶剂条件下进行。
[0056]
3.生物质共轭二烯烃异戊二烯和对苯醌一锅实现狄尔斯
‑
阿尔德和加氢脱氧反应(催化 剂的影响)
[0057]
在30ml间歇式的耐压反应釜中加入异戊二烯(10mmol)、对苯醌(10mmol,1.08g), 加入1,4
‑
二氧六环(5.0g),加入一定量双功能催化剂,80℃反应6小时后通入4mpa氢 气,升
温至180℃反应10小时。
[0058][0059]
表3.不同双功能催化剂的加氢脱氧反应活性
[0060]
[0061][0062]
从表3中的数据可以看出,常见的加氢金属催化剂负载分子筛对甲基四氢萘醌的加氢脱 氧均有一定的效果。其中,以pd/h
‑
β和pd/h
‑
y表现的活性凸显。金属负载量和催化剂用量 对甲基十氢萘烷烃化合物的产率存在一定的影响,甲基十氢萘烷烃化合物的产率随金属负载 量和催化剂用量增加而提高,在pd/h
‑
β催化作用下金属负载量在5
‑
20%之间,催化剂质量为 对苯醌质量的0.1
‑
0.3范围内,可获得大于90%的甲基十氢萘烷烃化合物收率。
[0063]
4.生物质共轭二烯烃异戊二烯和对苯醌一锅实现狄尔斯
‑
阿尔德和加氢脱氧反应(反应 温度、反应时间、氢气压力的影响)
[0064]
在30ml间歇式的耐压反应釜中加入异戊二烯(10mmol)、对苯醌(10mmol,1.08g), 加入1,4
‑
二氧六环(5.0g),加入双功能催化剂5wt%pd/h
‑
y(20wt%对苯醌,0.216g), 80℃反应6小时后通入一定压力氢气,升温至一定温度反应一定时间。
[0065]
表4.不同条件下加氢脱氧反应活性
[0066]
[0067][0068]
从表4中的数据可以看出,反应温度、反应时间、氢气压力对甲基十氢萘烷烃化合物的 产率来说影响较大。甲基十氢萘烷烃收率随氢气压力增大而增加,随反应时间的延长而增加, 随反应温度升高而升高。以pd/h
‑
y为催化剂在180
‑
220℃的温度区间,高于4mpa的氢气 压力下反应10小时以上,均获得大于85%的收率。
[0069]
5.生物质共轭二烯烃和对苯醌一锅实现狄尔斯
‑
阿尔德和加氢脱氧反应(反应底物共轭 二烯烃的影响)
[0070]
在30ml间歇式的耐压反应釜中加入共轭二烯烃(10mmol)、对苯醌(10mmol),加入 1,4
‑
二氧六环(5.0g),加入双功能催化剂5wt%pd/h
‑
y(10wt%对苯醌,0.108g),80℃ 反应6小时后通入4mpa氢气,升温至200℃反应12小时。
[0071]
表5.不同共轭二烯烃与对苯醌的狄尔斯
‑
阿尔德/加氢脱氧反应结果
[0072]
[0073][0074]
根据表5结果,生物质c5、c6共轭二烯烃均可与对苯醌一锅实现狄尔斯
‑
阿尔德/加氢脱 氧反应,高收率获得产物单一的烷基十氢化萘烷烃化合物。
