1.本技术涉及兽药技术领域,特别涉及一种盐酸沙拉沙星水溶性颗粒剂及其制备方法。
背景技术:
2.盐酸沙拉沙星(sarafloxacin hydrochloride)是动物专用的第三代氟喹诺酮类抗菌药物,具有抗菌谱广,抗菌活性强,对革兰氏阴性菌、革兰氏阳性菌及霉形体均表现出良好的抗菌作用,尤其是大肠杆菌、沙门氏菌、克雷伯氏菌、变形杆菌、多杀性巴氏杆菌、弯曲杆菌等肠杆菌。盐酸沙拉沙星吸收迅速,代谢快,几乎无残留,与许多抗菌药物无交叉耐药现象,主要用于敏感菌引起的畜禽消化系统、呼吸系统、泌尿道感染和霉形体病的治疗。
3.盐酸沙拉沙星为浓度依赖型药物,在动物体内需要达到一定浓度后方可发挥药效作用。而盐酸沙拉沙星进入动物体内渗透性强,吸收代谢快,现有产品做成缓释制剂,但是没有考虑盐酸沙拉沙星属于浓度依赖性药物,常规的脂质体及包衣材料会降低药物的血药浓度,起不到好的治疗效果,还会导致该药物的休药期延长,药残问题严重,存在24h后仍存在药物残留情况。
技术实现要素:
4.本发明的目的是为了解决上述技术的不足,提供一种盐酸沙拉沙星水溶性颗粒剂及其制备方法,在起到良好的治疗效果的同时,无药物残留问题,不影响药物休药期。
5.为此,本发明提供一种盐酸沙拉沙星水溶性颗粒剂,是由以下重量份的原料组成的:二乙烯二胺15~45份,环糊精-甲基乙烯基醚/马来酸酐共聚物150~220份,盐酸沙拉沙星100份,无水葡萄糖635~735份,水适量。
6.优选的,是由以下重量份的原料组成的:二乙烯二胺15份,环糊精-甲基乙烯基醚/马来酸酐共聚物150份,盐酸沙拉沙星100份,无水葡萄糖735份,水适量。
7.优选的,是由以下重量份的原料组成的:二乙烯二胺30份,环糊精-甲基乙烯基醚/马来酸酐共聚物200份,盐酸沙拉沙星100份,无水葡萄糖670份,水适量。
8.优选的,是由以下重量份的原料组成的:二乙烯二胺45份,环糊精-甲基乙烯基醚/马来酸酐共聚物220份,盐酸沙拉沙星100份,无水葡萄糖635份,水适量。
9.优选的,无水葡萄糖需过80目筛处理。
10.制备上述的一种盐酸沙拉沙星水溶性颗粒剂的方法,包括如下步骤:(1)按照重量份分别称量二乙烯二胺、环糊精-甲基乙烯基醚/马来酸酐共聚物,加入55~60 ℃的热水中进行搅拌混合均匀,得到混合物一;(2)按照重量份分别称量盐酸沙拉沙星、无水葡萄糖,并搅拌混合均匀,得到混合物二;(3)将步骤(2)得到的混合物二投至立体流化床中,将步骤(1)得到的混合物一作为粘合剂进行流化床造粒;期间控制进风温度、进风风量、雾化压力,最终获得盐酸沙拉沙
星颗粒。
11.优选的,步骤(1)中的搅拌速度为150 r/min,搅拌时间为30 min。
12.优选的,步骤(3)中的进风温度为65 ℃,进风风量50立方,雾化压力150 kpa。
13.本发明的有益效果是:本发明提供一种盐酸沙拉沙星水溶性颗粒剂及其制备方法,采用立式流化床制粒工艺,将环糊精-甲基乙烯基醚/马来酸酐共聚物作为药物的载体,该载体具有强大的载药量,使盐酸沙拉沙星在肠道中持续稳定的释放,一定时间内维持较高血药浓度,并且在12h后可基本消除。与现有产品相比,在起到良好治疗效果的同时,不影响药物休药期。
附图说明
14.为了更清楚地说明本技术实施例中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本技术的实施例。
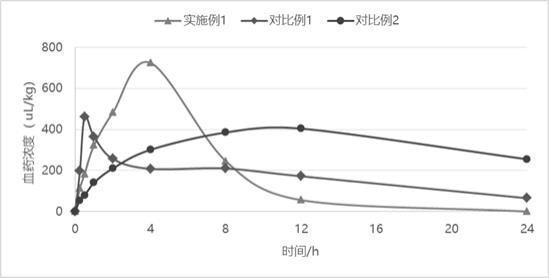
15.图1为鸡口服实施例1、对比例1、对比例2盐酸沙拉沙星制剂药-时曲线;图2为鸡口服实施例2、对比例1、对比例2盐酸沙拉沙星制剂药-时曲线;图3为鸡口服实施例3、对比例1、对比例2盐酸沙拉沙星制剂药-时曲线。
具体实施方式
16.为了使本技术所要解决的技术问题、技术方案及有益效果更加清楚明白,以下结合附图及实施例,对本技术进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本技术,并不用于限定本技术。本发明中所使用的方法如无特殊规定,均为常规的方法;所使用的原料和装置,如无特殊规定,均为常规的市售产品。
17.实施例1:本实施例提出了一种盐酸沙拉沙星水溶性颗粒剂的方法,包括如下步骤:(1)分别称量二乙烯二胺15 g、环糊精-甲基乙烯基醚/马来酸酐共聚物150 g,加入55℃热水中进行搅拌混合均匀,得到混合物一;(2)分别称量盐酸沙拉沙星100 g、无水葡萄糖735 g,并搅拌混合均匀,得到混合物二;(3)将所述步骤(2)得到的混合物二投至立体流化床中,将所述步骤(1)得到的混合物一作为粘合剂进行流化床造粒;期间控制进风温度、进风风量、雾化压力,最终获得盐酸沙拉沙星颗粒。
18.实施例2:本实施例提出了一种盐酸沙拉沙星水溶性颗粒剂的方法,包括如下步骤:(1)分别称量二乙烯二胺30g、环糊精-甲基乙烯基醚/马来酸酐共聚物200 g,加入58℃热水中进行搅拌混合均匀,得到混合物一;(2)分别称量盐酸沙拉沙星100 g、无水葡萄糖670 g,并搅拌混合均匀,得到混合物二;(3)将所述步骤(2)得到的混合物二投至立体流化床中,将所述步骤(1)得到的混合物一作为粘合剂进行流化床造粒;期间控制进风温度、进风风量、雾化压力,最终获得盐
酸沙拉沙星颗粒。
19.实施例3:本实施例提出了一种盐酸沙拉沙星水溶性颗粒剂的方法,包括如下步骤:(1)分别称量二乙烯二胺45g、环糊精-甲基乙烯基醚/马来酸酐共聚物220 g,加入60℃热水中进行搅拌混合均匀,得到混合物一;(2)分别称量盐酸沙拉沙星100 g、无水葡萄糖635 g,并搅拌混合均匀,得到混合物二;(3)将所述步骤(2)得到的混合物二投至立体流化床中,将所述步骤(1)得到的混合物一作为粘合剂进行流化床造粒;期间控制进风温度、进风风量、雾化压力,最终获得盐酸沙拉沙星颗粒。
20.上述实施例1~实施例3,为了便于对比分析,步骤(1)中的搅拌速度为150 r/min,搅拌时间为30 min;步骤(2)中使用过80目筛处理后的无水葡萄糖;步骤(3)立体流化床的进风温度为65 ℃,进风风量50立方,雾化压力150 kpa,主要工艺过程为,使用加热器将进风空气加热,将混合均匀的含有盐酸沙拉沙星的混合物二物料加入到立体流化床中,加热后的空气使立体流化床混合物二物料呈流化状态;使用蠕动泵将作为粘合剂水溶液的混合物一送入喷枪管,由压缩空气将粘合剂混合物一喷成雾状,散布在混合物二物料表面,使混合物二物料相互碰撞凝集成颗粒,制粒完成后,干燥,最终得到盐酸沙拉沙星颗粒。
21.下面分别对实施例1~实施例3制得的盐酸沙拉沙星颗粒、以及对比例1、对比例2市售产品进行药代动力学比对试验、水溶性比对试验、稳定性比对试验。其中,对比例1 为市售10%盐酸沙拉沙星可溶性粉,河南某厂家生产,批号20210502;对比例2 为市售10%盐酸沙拉沙星可溶性粉,江苏某厂家生产,批号20210710。
22.药代动力学比对试验对实施例1~实施例3制得的盐酸沙拉沙星可溶性颗粒及对比例1、对比例2市售产品分别进行药代动力学检测。
23.实验材料:精神状态良好的三黄鸡20只(公母各半,体重2kg
±
0.2)、给药器、高效液相色谱仪等。
24.实验步骤:将三黄鸡随机平均分成五组,每组一公一母,将药品以10mg/kg体重灌服给药,给药后分别在0min、15min、30min、1h、2h、4h、8h、12h、24h分别静脉采血,分离血清,-20℃保存待用。将血清处理完毕后取上清hplc检测盐酸沙拉沙星含量。检测结果见表1及图1~图3。
25.表1 药代动力学比对试验检测结果
采血时间(h)实施例1平均血药浓度(ug/l)实施例2平均血药浓度(ug/l)实施例3平均血药浓度(ug/l)对比例1平均血药浓度(ug/l)对比例2平均血药浓度(ug/l)0000000.2511290121197550.518321020546178132234231336414024825204992562104724691682208301824623030221038512565039172404
24未检出未检出未检出65255
从表1及图1~图3中可以看出:本发明实施例1~实施例3制备的盐酸沙拉沙星水溶性颗粒剂相比对比例1、对比例2市售药物,能够持续稳定的释放并吸收,在一定时间内维持较高血药浓度,作为浓度依赖型药物能够起到良好的治疗效果;同时本发明的颗粒剂代谢较快,无药物残留问题,不影响药物休药期。
26.一方面,本发明将环糊精-甲基乙烯基醚/马来酸酐共聚物作为药物的载体,该载体具有强大的载药量,使盐酸沙拉沙星在肠道中持续稳定的释放,一定时间内维持较高血药浓度,并且在12h后可基本消除。与现有产品相比,在起到良好治疗效果的同时,不影响药物休药期;另一方面,二乙烯二胺是药物的医药中间体,可以作为盐酸沙拉沙星的抗菌增效剂,提高抗菌效果,更好发挥用药效果。
27.水溶性比对试验对实施例1~实施例3制得的盐酸沙拉沙星水溶性颗粒剂及对比例1~对比例4市售药物分别以不同浓度在25℃自来水中溶解,比较溶解状态。
28.对比例3:本实施例提出了一种盐酸沙拉沙星颗粒剂的方法,包括如下步骤:(1)称量二乙烯二胺30g加入58℃热水中进行搅拌混合均匀,得到混合物一;(2)分别称量盐酸沙拉沙星100 g、无水葡萄糖870 g,并搅拌混合均匀,得到混合物二;(3)将所述步骤(2)得到的混合物二投至立体流化床中,将所述步骤(1)得到的混合物一作为粘合剂进行流化床造粒;期间控制进风温度、进风风量、雾化压力,最终获得盐酸沙拉沙星颗粒。
29.对比例4:本实施例提出了一种盐酸沙拉沙星颗粒剂的方法,包括如下步骤:(1)称量环糊精-甲基乙烯基醚/马来酸酐共聚物200 g,加入58℃热水中进行搅拌混合均匀,得到混合物一;(2)分别称量盐酸沙拉沙星100 g、无水葡萄糖700 g,并搅拌混合均匀,得到混合物二;(3)将所述步骤(2)得到的混合物二投至立体流化床中,将所述步骤(1)得到的混合物一作为粘合剂进行流化床造粒;期间控制进风温度、进风风量、雾化压力,最终获得盐酸沙拉沙星颗粒。
30.试验材料为:烧杯、玻璃杯、自来水。
31.实验步骤:每个烧杯中放置100ml自来水,分别称取0.5g、1.0g、3.0g、5.0g样品加入烧杯中,然后玻璃棒搅拌2min,观察每个烧杯中样品的溶解情况,检测浊度,并做好记录。监测结果如表2所示。
32.表2 水溶性比对试验检测结果
样品/加入量0.5g1.0g3.0g5.0g实施例1完全溶解,浊度5.4ntu完全溶解,浊度10.3ntu完全溶解,浊度15.6ntu完全溶解,浊度21.5ntu
实施例2完全溶解,浊度5.2ntu完全溶解,浊度8.2ntu完全溶解,浊度11.3ntu完全溶解,浊度19.6ntu实施例3完全溶解,浊度3.2ntu完全溶解,浊度5.1ntu完全溶解,浊度6.2ntu完全溶解,浊度9.8ntu对比例1完全溶解,浊度20.5ntu底部少量不溶颗粒,浊度35.9ntu底部较多不溶颗粒,浊度60.3ntu底部大量不溶颗粒,浊度220.7ntu对比例2溶液浑浊,浊度120.5ntu溶液浑浊,浊度300.2ntu溶液严重浑浊溶液严重浑浊对比例3完全溶解,浊度7.8ntu完全溶解,浊度10.1ntu完全溶解,浊度13.3ntu完全溶解,浊度21.3ntu对比例4溶液浑浊,浊度125.3ntu溶液浑浊,浊度378.5ntu溶液严重浑浊溶液严重浑浊
盐酸沙拉沙星在水中几乎微溶,为了提高盐酸沙拉沙星的溶解度,目前市场上的大多数产品在生产工艺上多采用一些常规的助溶剂,但是盐酸沙拉沙星的溶解度并无明显提高,无法满足实际生产需求,存在动物饮水给药过程中管道阻塞,给药不均匀等问题,起不到治疗和预防效果,且造成药物的浪费。
33.从表1结果表明,本发明中实施例1~3制备的盐酸沙拉沙星水溶性颗粒剂溶解度比对比例1、对比例2市售药物高10倍左右,完全满足临床用药需求。通过实施例2、对比例3、对比例4的对比分析,表明二乙烯二胺作为助溶剂,显著增加盐酸沙拉沙星的溶解度。
34.稳定性比对试验对实施例1~实施例3制得的盐酸沙拉沙星水溶性颗粒及对比例1、对比例2市售药物分别进行药物稳定性中的加速试验验证。
35.实验步骤:将样品在加速试验箱(40℃、75%湿度)中放置六个月,在放置后第1、3、6个月分别取样检测盐酸沙拉沙星制剂的外观性状、含量、干燥失重等。加速试验第6个月的检查结果如表3所示。
36.表3稳定性比对试验检测结果
项目实施例1实施例2实施例3对比例1对比例2性状淡黄色颗粒,无性状变化淡黄色颗粒,无性状变化淡黄色颗粒,无性状变化红褐色块状,严重变性淡黄色粉末,无性状变化干燥失重2.53%3.68%3.99%8.13%5.15%含量99.2%97.5%98.7%92.5%87.3%是否合格合格合格合格不合格不合格
从表3中可以看出:本发明实施例1~实施例3制备的盐酸沙拉沙星颗粒剂各项指标均优于对比例1、对比例2市售药物。市售药物稳定性较差,对比例1易结块变色,对比例2含量明显下降。而本发明性状及含量非常稳定,在加速试验箱中放置6个月含量比对比例高出5%以上,且不易吸潮,更易于储存、使用。
37.以上所述仅为本技术的较佳实施例而已,并不用以限制本技术,凡在本技术的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本技术的保护范围之内。
