n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物及其药物组合物和其应用
技术领域
1.本发明属于医药技术领域,具体涉及一类n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物,其制备方法,以该类化合物作为活性成分的药物组合物,及其在制备新型强效镇痛药物中的应用。
背景技术:
2.阿片类药物在体内的靶点为阿片受体,由于强效镇痛的能力在临床医学和公共卫生领域受到广泛关注。阿片类药物往往伴随着如欣快症、身体依赖性、呼吸抑制和便秘等副作用,因此寻找更安全,更有效的止痛药是阿片类药物研究领域的重要课题。
3.阿片受体属于g蛋白偶联受体(g protein-coupled receptors,gpcrs)a类家族。至今,四种阿片受体亚型被克隆,分别为μ-阿片受体(mu opioid receptor,mor),κ-阿片受体(kappa opioid receptor,kor),δ-阿片受体(delta opioid receptor,dor),痛敏肽受体(nociceptin opioid receptor,nop)。
4.mor激动剂如吗啡对剧烈疼痛如癌痛是强效的镇痛药,但是因为其严重的副作用如欣快症、身体依赖性、呼吸抑制和便秘而受到使用限制。kor激动剂在体内激活可能会产生强大的镇痛作用,而不会产生滥用可能性,但是在非人类灵长类动物中会产生严重的不良副作用如烦躁不安、水利尿、流涎、呕吐和镇静。dor激动剂镇痛活性弱,仅针对于炎症疼痛,主要副作用是惊厥,但尚未有针对性的dor激动剂获得临床批准。大量药理证据说明第四种亚型nop基因与其他阿片受体存在显著差异。动物模型和临床试验结果表明,不同亚型的阿片受体激动剂联合用药可以减少体内副作用的引发。因此阿片受体多重激动剂能同时激活dor/mor/kor来抵消其中一种亚型独自被激活而产生的的副作用,能够保持镇痛作用且具有较高的呼吸安全性和较少的滥用倾向。
5.目前,现有技术中,未见有新型的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物的报道,也没有其具备药理活性的报道。
技术实现要素:
6.本发明基于阿片受体dor、mor、kor的晶体结构,进行dor、mor、kor三重激动剂的设计及合成,得到新型的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物,提高了强效镇痛的能力。其目的是提供通式(1)n,n-(4-哌啶基、芳基)-3-氨基苯酚类化合物及其制备方法,以及以其为活性成分的药物组合物,及其在制备强效镇痛药物中的应用。
7.为了实现本发明的上述目的,本发明提供了如下的技术方案:
8.下述通式(1)所示n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物,
[0009][0010]
式中,n=0,1,2;
[0011]
ar可为如下基团之一:
[0012][0013]
其中,w可以为h,me,et,f,cl,br,i,cf3,ph等基团
[0014]
r可为如下基团之一:
[0015][0016]
其中,r1,r2,r3为相互独立的基团,可以为h,me,et,f,cl,br,i,cf3,ph等,x,y,z可以为相互独立的c,n原子;n’值为0~4;
[0017]
所述的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物在制备阿片受体激动剂的药物中的应用。
[0018]
所述的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物在制备强效镇痛药物中的应用。
[0019]
制备所述的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物方法如下:
[0020][0021]
(1)step1:以1,2-二氯乙烷为溶剂,3-氨基苯胺与n-叔丁氧羰基-4-哌啶酮在三乙酰氧基硼氢化钠和冰乙酸的存在下通过还原胺化得到化合物31;
[0022]
(2)step2:以二氯甲烷为溶剂,化合物31在4-甲基苯磺酸吡啶的催化和3,4-二氢-2h-吡喃的保护下反应得到化合物32;
[0023]
(3)step3:以甲苯为溶剂,在叔丁醇钠和三叔丁基膦的存在下,化合物32与ari经双(二亚芐基丙酮)钯催化的偶联反应得到化合物33;
[0024]
其中,ar的定义同上;
[0025]
(4)step4:以二氯甲烷为溶剂,化合物33使用三氟乙酸脱去保护基得到化合物34;
[0026]
(5)step 5:以n,n-二甲基甲酰胺为溶剂,化合物34与在三乙酰氧基硼氢化钠和冰乙酸的存在下通过还原胺化得到化合物1;
[0027]
其中,r的定义同上。
[0028]
本发明通式1化合物都可以用上述或类似上述的制备方法制备得到,根据取代基的不同和取代基位置的不同选用相应的起始原料即可。本领域技术人员应当认识到,上述路线有助于理解本发明,但并不限制本发明的内容,除非另有规定,变量如同通式1中提及的一样定义。
[0029]
本发明同时提供了一种药物组合物,其包含本发明的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物任其一或任意组合和至少一种药学上可接受的载体。
[0030]
所述的药物组合物在制备阿片受体激动剂的药物中的应用。
[0031]
所述的药物组合物在制备镇痛药物中的应用。
[0032]
本发明的制备药物组合物的方法,是先依照上述制备化合物的方法得到化合物,最后,将上述制备得到的化合物其中一种或任意组合加入药学上可接受的载体制成药物组合物。
[0033]
本发明药物组合物包括通式1的化合物或其药学上可接受的盐、前药、晶型、立体异构体、互变异构体、水合物或溶剂合物以及药学上可接受的载体或赋形剂。
[0034]
本发明发现并通过阿片受体(mor、dor、kor)的激动活性测试,验证了本发明通式1的n,n-(4-哌啶基、芳基)-3-氨基苯酚类化合物具有良好的阿片受体(mor、dor、kor)三重激动活性,这类化合物可以制备强效镇痛药物。
[0035]
与现有技术相比,本发明具备如下的优益性:
[0036]
1.首次合成了新型的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物,提供了现有技术中未有的具有较好药用价值的新化合物,填补了技术空白。
[0037]
2.本发明提供的新型的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物的制备方法简单易行,得率高,环保节料。
[0038]
3.本发明提供的新型的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物具有较好对三种阿片受体显示出较高的三重激动活性,尤其是对mor、dor激动活性可高达nm水平。
[0039]
4.本发明提供了新型的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物的一个全新的药物应用,提供了本发明所涉及的化合物用于制备强效镇痛药物。
[0040]
5.本发明提供了新型的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物的一个全新的药物应用,提供了新型的n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物在制备阿片受体激动剂的药物中的应用。
附图说明:
[0041]
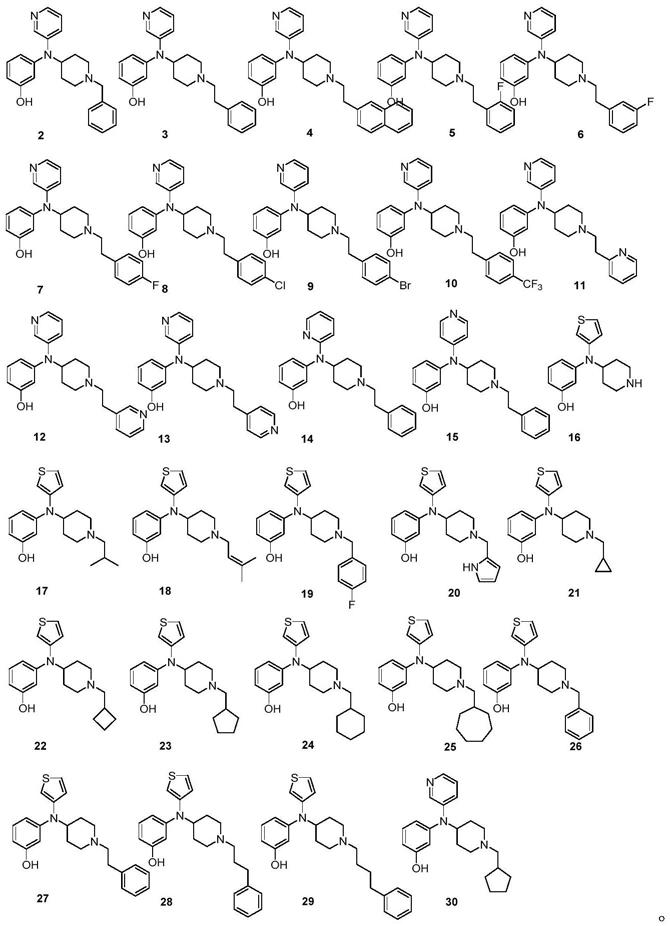
图1为本发明n,n-(4-哌啶基、芳基)-3-氨基苯酚类化合物的结构示意图:
[0042]
图2为本发明合成路线流程图。
具体实施方式
[0043]
本发明人经过广泛而深入的研究,发现一批结构全新的化合物,这些衍生物能激活mor、dor、kor阿片受体,其中一些化合物的激动活性的ec
50
值达到nm级别。在此基础上完成了本发明。
[0044]
本发明人合成了具有mor、dor、kor阿片受体激动活性的一系列候选化合物。通过对得到的候选化合物进行结构优化设计,发现了一批新型对mor、dor、kor阿片受体具有激
动活性的n,n-(4-哌啶基、芳基)-3-氨基苯酚类化合物,并对这类化合物进行了细胞水平活性评价,多个化合物对mor、dor、kor阿片受体激动活性ec
50
值达到nm级别。下面将用本发明的实施例来进一步说明本发明的实质性内容,但并不以此来限定本发明。
[0045]
下面结合附图,用本发明的实施例来进一步说明本发明的实质性内容,但并不以此来限定本发明。
[0046]
下面结合具体实施例描述本发明通式1化合物的制备方法,但这些具体方法不对本发明构成任何限制。本发明化合物还可以任选将在本说明书中描述的或本领域已知的各种合成方法组合起来而方便地制得,这样的组合可由本发明所属领域的技术人员容易地进行。
[0047]
实施例1:
[0048]
合成通式:
[0049][0050]
中间体31合成:
[0051]
于无水无氧处理的反应瓶中加入3-氨基苯酚(5.0g,45.9mmol,1.0eq)溶于室温搅拌下的1,2-二氯乙烷(150ml),依次加入n-叔丁氧羰基-4-哌啶酮(9.2g,45.8mmol,1.0eq),三乙酰氧基硼氢化钠(14.6g,68.7mmol,1.5eq)和冰乙酸(4.1ml,68.7mmol,1.5eq)。24h后,加入1n氢氧化钠溶液(76.1ml,76.1mmol)淬灭,实验后处理按通用实验操作,经柱层析纯化得到中间体31(9.9g,74.7%)。
[0052]
中间体32合成:
[0053]
于无水无氧处理的耐压瓶中加入化合物31(5.0g,17.1mmol,1.0eq)溶于室温搅拌下的超干二氯甲烷(35ml),随后加入4-甲基苯磺酸吡啶(640.0mg,1.7mmol,0.1eq)和dhp(4.3g,51.0mmol,3.0eq)。氩气保护下密封耐压瓶,加热至40℃,24h后,冷却至室温,通过碳酸氢钠溶液淬灭,实验后处理按通用实验操作,经柱层析纯化得到中间体32(3.0g,46.6%)。
[0054]
中间体33的合成:
[0055]
于无氧处理的反应管中加入中间体32(1.0eq)溶于室温搅拌下的甲苯,依次加入叔丁醇钠(4.0eq),双(二亚芐基丙酮)钯(0.1eq),三叔丁基膦(428,0.1eq)和芳基碘ari(1.4eq),在氩气保护下密封反应管加热至140℃,监测反应完全后,冷却至室温,硅藻土过滤并浓缩,经柱层析纯化得到中间体33。
[0056]
中间体34的合成:
[0057]
于反应管中加入在上述中间体33(1.0eq),溶于二氯乙烷中并冷却至0℃,缓慢滴加三氟乙酸(60.0eq),移至常温,监测反应完成后,冰浴下加入碳酸氢钠淬灭,实验后处理
按通用实验操作进行,经柱层析纯化得到中间体34。
[0058]
终产物1的合成:
[0059]
无水无氧处理的反应瓶中加入上述中间体34(1.0eq)及n,n-二甲基甲酰胺,依次加入异丁醛(1.0eq),三乙酰氧基硼氢化钠(1.5eq)和冰乙酸(1.5eq)。24h后,监测反应完成后,加入饱和碳酸氢钠淬灭,实验后处理按通用实验操作进行,经柱层析纯化得到产物1。
[0060]
具体化合物的制备如下:
[0061]
1、3-((1-苄基哌啶-4-基)(吡啶-3-基)氨基)苯酚(化合物2):参照以上合成通式step1~5,step 3中使用3-碘吡啶替代ari,step 5中使用苯甲醛。1h nmr(400mhz,cdcl3)δ7.92(q,j=10.04hz,2h),7.26(m,5h),7.09(m,j=5.00hz,2h),6.94(d,j=7.47hz,1h),6.57(d,j=7.96hz,1h),6.41(d,j=7.73hz,1h),6.21(s,1h),3.74(m,1h),3.53(s,2h),2.98(d,j=11.31hz,2h),2.14(t,j=11.55hz,2h),1.83(d,j=12.05hz,2h),1.54(q,j=11.18hz,2h).
[0062]
2、3-((1-苯乙基哌啶-4-基)(吡啶-3-基)氨基)苯酚(化合物3):参照以上合成通式step1~5,step 3中使用3-碘吡啶替代ari,step 5中使用苯乙醛。1h nmr(400mhz,cdcl3)δ7.95(q,j=5.91hz,2h),7.24(m,2h),7.12(m,5h),6.97(d,j=7.36hz,1h),6.58(d,j=8.03hz,1h),6.43(d,j=7.80hz,1h),6.31(s,1h),3.80(m,1h),3.12(d,j=11.35hz,2h),2.79(m,2h),2.63(m,2h),2.23(t,j=11.56hz,2h),1.92(d,j=12.23hz,2h),1.63(q,j=11.42,2h).
[0063]
3、3-((1-(2-(萘-2-基)乙基)哌啶-4-基)(吡啶-3-基)氨基)苯酚(化合物4):参照以上合成通式step1~5,step 3中使用3-碘吡啶替代ari,step 5中使用2-萘乙醛。1h nmr(400mhz,cdcl3)δ8.02(d,j=13.91hz,3h),7.83(d,j=10.56hz,1h),7.71(d,j=8.07hz,1h),7.46(m,2h),7.37(t,j=6.36hz,1h),7.31(d,j=5.45hz,1h),7.17(t,j=7.95hz,1h),7.09(m,1h),7.00(d,j=7.95hz,1h),6.68(d,j=7.83hz,1h),6.47(d,j=7.70hz,1h),6.43(s,1h),3.88(m,1h),3.31(m,2h),3.25(d,j=11.13hz,2h),2.79(t,j=8.07hz,2h),2.37(t,j=12.54hz,2h),1.98(d,j=11.86hz,2h),1.74(m,j=9.35hz,2h).
[0064]
4、3-((1-(2-氟苯乙基)哌啶-4-基)(吡啶-3-基)氨基)苯酚(化合物5):参照以上合成通式step1~5,step 3中使用3-碘吡啶替代ari,step 5中使用2-氟苯乙醛。1h nmr(400mhz,cdcl3)δ7.98(q,j=5.46hz,2h),7.14(m,4h),7.02(m,3h),6.64(d,j=7.58hz,1h),6.45(d,j=7.80hz,1h),6.37(s,1h),3.85(m,1h),3.19(d,j=10.88hz,2h),2.88(m,2h),2.69(m,2h),2.34(t,j=13.32hz,2h),1.97(m,2h),1.70(m,2h).
[0065]
5、3-((1-(3-氟苯乙基)哌啶-4-基)(吡啶-3-基)氨基)苯酚(化合物6):参照以上合成通式step1~5,step 3中使用3-碘吡啶替代ari,step 5中使用3-氟苯乙醛。1h nmr(400mhz,cdcl3)δ7.97(q,j=7.22hz,2h),7.22(q,j=7.67hz,1h),7.12(m,2h),7.01(d,j=7.20hz,1h),6.94(d,j=7.24hz,1h),6.88(q,j=5.34hz,2h),6.63(d,j=7.70hz,1h),6.45(d,j=7.70hz,1h),6.35(s,1h),3.83(m,1h),3.14(d,j=11.13hz,2h),2.82(q,j=5.34hz,2h),2.66(q,j=5.34hz,2h),2.28(t,j=11.13hz,2h),1.95(d,j=11.92hz,2h),1.65(q,j=11.37hz,2h).
[0066]
6、3-((1-(4-氟苯乙基)哌啶-4-基)(吡啶-3-基)氨基)苯酚(化合物7):参照以上合成通式step1~5,step 3中使用3-碘吡啶替代ari,step 5中使用4-氟苯乙醛。1h nmr
nmr(400mhz,cdcl3)δ8.47(d,j=4.89hz,2h),8.01(d,j=11.76hz,2h),7.14(m,4h),7.04(d,j=8.19hz,1h),6.66(d,j=6.97hz,1h),6.44(d,j=7.83hz,1h),6.39(s,1h),3.85(m,1h),3.14(d,j=13.33hz,2h),2.83(q,j=5.54hz,2h),2.71(q,j=5.09hz,2h),2.32(t,j=12.17hz,2h),1.97(d,j=12.47hz,2h),1.64(q,j=11.21hz,2h).
[0073]
13、3-((1-苯乙基哌啶-4-基)(吡啶-2-基)氨基)苯酚(化合物14):参照以上合成通式step1~5,step 3中使用2-碘吡啶替代ari,step 5中使用苯乙醛。1h nmr(400mhz,cdcl3)δ8.11(d,j=4.16hz,1h),7.23(d,j=7.08hz,2h),7.17(m,5h),6.66(d,j=7.70hz,1h),6.52(m,2h),6.44(s,1h),6.02(d,j=8.56hz,1h),4.97(m,1h),3.22(d,j=10.64hz,2h),2.88(q,j=5.05hz,2h),2.75(q,j=5.38hz,2h),2.47(t,j=11.43hz,2h),1.93(d,j=11.62hz,2h),1.78(q,j=10.69hz,2h).
[0074]
14、3-((1-苯乙基哌啶-4-基)(吡啶-4-基)氨基)苯酚(化合物15):参照以上合成通式step1~5,step 3中使用4-碘吡啶替代ari,step 5中使用苯乙醛。1h nmr(400mhz,cdcl3)δ8.02(d,j=5.99hz,2h),7.22(m,5h),7.14(d,j=7.83hz,1h),6.83(d,j=8.44hz,1h),6.49(d,j=8.44hz,1h),6.39(d,j=5.75hz,2h),3.85(m,1h),3.08(d,j=11.00hz,2h),2.76(q,j=5.42hz,2h),2.59(q,j=5.30hz,2h),2.18(t,j=11.49hz,2h),1.89(d,j=11.74hz,2h),1.63(q,j=11.13hz,2h).
[0075]
15、3-(哌啶-4-基(噻吩-3-基)氨基)苯酚(化合物16):参照以上合成通式,step 3中使用3-噻吩碘替代ari,经step 4即可得到16。1h nmr(400mhz,meod-d4)δ7.36(dd,j1=5.1,j2=3.1hz,1h),6.96(t,j=8.2hz,2h),6.84(dd,j1=3.1,j2=1.4hz,1h),6.71(dd,j1=5.2,j2=1.4hz,1h),6.26(ddd,j1=7.9,j2=5.0,j3=2.2hz,2h),6.19(t,j=2.3hz,1h),3.88(tt,j1=11.9,j2=3.7hz,1h),3.07(dt,j1=13.5,j2=2.9hz,2h),2.72(td,j1=12.6,j2=2.4hz,2h),1.97(dd,j1=12.9,j2=3.2hz,2h),1.42(qd,j1=12.5,j2=4.0hz,2h).
[0076]
16、3-((1-异丁基哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物17):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用异丁醛。1h nmr(400mhz,cdcl3)δ7.20(dd,j1=4.7,j2=3.5hz,1h),7.02(t,j=8.2hz,1h),6.66(d,j=4.9hz,2h),6.27(ddd,j1=10.1,j2=7.9,j3=2.2hz,2h),6.10(t,j=2.4hz,1h),3.69(tt,j1=11.9,j2=3.8hz,1h),2.96(dt,j1=12.7,j2=3.2hz,2h),2.10(d,j=7.1hz,2h),2.03(td,j1=12.1,j2=2.3hz,2h),1.89(dt,j1=12.6,j2=3.1hz,3h),1.75(m,1h),1.60(qd,j1=12.5,j2=3.6hz,2h),0.89(d,j=6.8hz,6h).
[0077]
17、3-((1-(3-甲基-2-烯-1-基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物18):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用3-甲基-2-烯醛。1h nmr(400mhz,cdcl3)δ7.17(dd,j1=5.0,j2=3.1hz,1h),7.04(t,j=8.2hz,1h),6.63(d,j=5.1hz,1h),6.61(dd,j1=3.4,j2=1.8hz,1h),6.30(ddd,j1=13.1,j2=8.0,j3=2.2hz,2h),6.13(d,j=2.3hz,1h),5.22(t,j=7.3hz,1h),3.70(tt,j1=11.9,j2=3.8hz,1h),3.02(d,j=11.5hz,2h),2.96
–
2.94(m,2h),2.09(t,j=11.6hz,2h),1.92(d,j=12.2hz,2h),1.68(s,3h),1.63(s,3h),1.57(td,j1=13.2,j2=12.7,4.0hz,2h).
[0078]
18、3-((1-(4-氟苄基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物19):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用4-氟苯甲醛。1h nmr
(400mhz,cdcl3)δ7.30
–
7.19(m,3h),6.98(dt,j1=16.9,j2=8.3hz,3h),6.64(dd,j1=7.3,j2=4.0hz,2h),6.24(ddd,j1=18.3,j2=8.1,j3=2.3hz,2h),6.04(t,j=2.2hz,1h),3.68(tt,j1=11.8,j2=3.9hz,1h),3.45(s,2h),2.91(d,j=11.5hz,2h),2.07(t,j=11.2hz,2h),1.87(dt,j1=12.9,j2=2.9hz,2h),1.53(qd,j1=12.4,j2=3.7hz,2h).
[0079]
19、3-((1-((1h-吡咯-2-基)甲基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物20):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step5中使用2-吡咯甲醛。1h nmr(400mhz,cdcl3)δ8.78(s,1h),7.23(dd,j1=5.1,j2=3.2hz,1h),7.03(t,j=8.2hz,1h),6.71(q,j=2.4hz,1h),6.64(d,j=5.0hz,2h),6.28(td,j1=8.2,j2=2.1hz,2h),6.13(d,j=2.3hz,1h),6.10(d,j=2.9hz,1h),6.05(d,j=3.2hz,1h),3.73(ddt,j1=12.0,j2=7.9,j3=3.9hz,1h),3.54(s,2h),2.98(d,j=11.8hz,2h),2.15(t,j=12.0hz,2h),1.93(d,j=12.8hz,3h),1.54(qd,j1=12.7,j2=3.4hz,2h).
[0080]
20、3-((1-(环丙基甲基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物21):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用环丙基甲醛。1h nmr(400mhz,cdcl3)δ7.12(dd,j1=5.2,j2=3.1hz,1h),7.03(t,j=8.1hz,1h)6.52(dd,j1=5.2,j2=1.4hz,1h),6.40(d,j=3.0hz,1h),6.35(ddd,j1=14.0,j2=8.1,j3=2.1hz,2h),6.15(t,j=2.3hz,1h),3.69(tt,j1=12.0,j2=3.9hz,1h),3.17(d,j=11.6hz,2h),2.23(d,j=6.8hz,2h),2.10(t,j=11.6hz,2h),1.95(d,j=3.6hz,2h),1.63(qd,j1=12.5,j2=3.8hz,2h),0.81(dtt,j1=12.0,j2=7.0,j3=3.5hz,1h),0.47
–
0.42(m,2h),0.08(t,j=5.0hz,2h).
[0081]
21、3-((1-(环丁基甲基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物22):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用环丁基甲醛。1h nmr(400mhz,cdcl3)δ7.16(q,j=2.67hz,1h),7.01(t,j=8.06hz,1h),6.57(d,j=4.64hz,1h),6.48(d,j=1.36hz,1h),6.31(t,j=7.86hz,2h),6.16(s,1h),3.70(m,1h),3.01(d,j=11.36hz,2h),2.48(d,j=6.25hz,2h),2.22(t,j=11.44hz,2h),2.01(q,j=8.32hz,2h),1.91(d,j=12.28hz,2h),1.84(m,1h),1.73(m,2h),1.67(m,2h),1.63(m,2h).
[0082]
22、3-((1-(环戊基甲基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物23):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用环戊基甲醛。1h nmr(400mhz,cdcl3)δ7.16(dd,j1=5.1,j2=3.1hz,1h),7.03(t,j=8.2hz,1h),6.59(d,j=5.1hz,1h),6.51(d,j=3.1hz,1h),6.30(ddd,j1=19.5,j2=8.1,j3=2.2hz,2h),6.08(s,1h),3.68(tt,j=11.8,3.8hz,1h),3.02(d,j=11.5hz,2h),2.29(d,j=6.9hz,2h),2.06(t,j=11.8hz,2h),1.98(m,1h),1.89(d,j=11.5hz,2h),1.75(dd,j1=12.0,j2=6.6hz,2h),1.60(m,2h),1.55(m,2h),1.45(m,2h),1.11(m,2h).
[0083]
23、3-((1-(环己基甲基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物24):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用环己基甲醛。1h nmr(400mhz,cdcl3)δ7.27(m,1h),7.02(t,j=8.2hz,1h),6.72(d,j=3.2hz,1h),6.69(d,j=5.1hz,1h),6.27(td,j1=8.3,j2=2.3hz,2h),6.13(d,j=2.5hz,1h),3.69(tt,j1=11.6,j2=3.9hz,1h),2.96(d,j=11.5hz,2h),2.11(d,j=6.8hz,2h),2.00(t,j=11.8hz,2h),1.89(d,j=12.2hz,2h),1.73
–
1.61(m,4h),1.60
–
1.50(m,2h),1.45
–
1.40(m,1h),1.19
–
1.09(m,4h),0.88
–
0.80(m,2h).
[0084]
24、3-((1-(环庚基甲基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物25):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用环庚基甲醛。1h nmr(400mhz,cdcl3)δ7.21(m,1h),7.00(t,j=7.98hz,1h),6.65(d,j=4.88hz,2h),6.31(d,j=7.64hz,1h),6.25(d,j=8.08hz,1h),6.20(s,1h),3.71(m,1h),3.02(d,j=10.88hz,2h),2.20(d,j=6.32hz,2h),2.13(t,j=11.34hz,2h),1.90(d,j=12.04hz,2h),1.70(m,2h),1.61(m,2h),1.56(m,1h),1.52(m,2h),1.46(m,2h),1.35(m,2h),1.27(m,2h),1.11(q,j=10.03hz,2h).
[0085]
25、3-((1-苄基哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物26):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用苯甲醛。1h nmr(400mhz,cdcl3)δ7.24
–
7.20(m,5h),7.18(t,j=4.1hz,1h),6.98(t,j=8.2hz,1h),6.61(d,j=4.2hz,2h),6.23(ddd,j1=16.3,j2=8.1,j3=2.2hz,2h),6.02(d,j=2.5hz,1h),3.65(tt,j1=11.9,j2=3.8hz,1h),3.47(s,2h),2.93(dd,j1=9.0,j2=6.1hz,2h),2.07(t,j=11.6hz,2h),1.84(d,12.2hz,2h),1.54(qd,j1=12.5,j2=3.7hz,2h).
[0086]
26、3-((1-苯乙基哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物27):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用苯乙醛。1h nmr(400mhz,cdcl3)δ7.23(d,j=7.24hz,2h),7.17(m,2h),7.13(d,j=7.65hz,2h),7.00(t,j=8.09hz,1h),6.62(d,j=4.09hz,2h),6.28(m,j=4.01hz,2h),6.17(s,1h),3.73(m,1h),3.12(d,j=11.47hz,2h),2.79(m,2h),2.63(m,2h),2.23(t,j=11.61hz,2h),1.94(d,j=11.95hz,2h),1.67(q,j=11.25hz,2h).
[0087]
27、3-((1-(3-苯基丙基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物28):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用苯丙醛。1h nmr(400mhz,cdcl3)δ7.25(d,j=3.7hz,1h),7.23(d,j=7.4hz,1h),7.19
–
7.09(m,4h),6.96(t,j=8.1hz,1h),6.61(dd,j1=6.9,j2=4.1hz,2h),6.42(s,1h),6.38(dd,j1=8.1,j2=2.2hz,1h),6.18(dd,j1=8.2,j2=2.1hz,1h),3.82(t,j=4.0hz,1h),3.18(d,j=11.6hz,2h),2.62
–
2.55(m,4h),2.50(t,j=12.2hz,2h),1.95
–
1.88(m,4h),1.82(t,j=12.7hz,2h).
[0088]
28、3-((1-(4-苯基丁基)哌啶-4-基)(噻吩-3-基)氨基)苯酚(化合物29):参照以上合成通式step1~5,step 3中使用3-噻吩碘替代ari,step 5中使用4-苯基丁醛。1h nmr(400mhz,cdcl3)δ7.23(d,j=7.44hz,2h),7.16(m,2h),7.12(d,j=8.32hz,2h),7.01(t,j=8.06hz,1h),6.58(d,j=4.36hz,1h),6.52(d,j=1.64hz,1h),6.29(t,j=6.68hz,2h),6.12(s,1h),3.70(m,1h),3.02(d,j=11.24hz,2h),2.57(m,2h),2.38(m,2h),2.13(t,j=11.60hz,2h),1.91(d,j=12.00hz,2h),1.63(m,2h),1.56(m,2h),1.52(m,2h).
[0089]
29、3-((1-(环戊基甲基)哌啶-4-基)(吡啶-3-基)氨基)苯酚(化合物30):参照以上合成通式step1~5,step 3中使用3-碘吡啶替代ari,step 5中使用环戊基甲醛。1h nmr(400mhz,cdcl3)δ7.97(q,j=4.14hz,2h),7.13(m,1h),7.08(t,j=4.12hz,1h),6.97(d,j=7.68hz,1h),6.60(d,j=7.32hz,1h),6.43(d,j=7.84hz,1h),6.34(s,1h),3.82(m,1h),3.12(d,j=11.16hz,2h),2.41(d,j=6.72hz,2h),2.24(t,j=10.80hz,2h),2.05(m,1h),1.91(d,j=12.08hz,2h),1.75(m,1h),1.69(m,1h),1.55(m,1h),1.49(m,1h),1.14(m,1h).
[0090]
实施例2:
[0091]
生物学活性。本发明化合物对阿片受体(mor、dor、kor)的激动活性的评价。
[0092]
为评价本发明化合物对阿片受体(mor、dor、kor)的激动作用,本发明以药物dago(mor激动剂)、dpdpe(dor激动剂)、u50488(kor激动剂)为阳性对照。化合物的ec
50
值通过浓度效应生成曲线计算确定。
[0093]
1.实验原理和方法
[0094]
实验原理:通过建立了共转目标受体和gα16的细胞系,使得受体被激活后能引起gα16蛋白的活化,进而激活磷脂酶c(plc)产生ip3和dag,ip3可与细胞内内质网和线粒体上的ip3受体结合,从而引起胞内钙的释放。因此,测定胞内钙的变化可以作为检测目标受体活化状态的方法。fluo-4/am是一种钙荧光探针指示剂用来测量钙离子,作为非极性脂溶性的化合物,进入细胞后在细胞脂解酶的作用下,am基团解离,释出fluo-4;由于fluo-4是极性分子,不易通过脂质双分子膜,它可使fluo-4长时间保留在细胞内。最终可以通过测量被激发的荧光强度来反映gα蛋白被激活的水平。如果筛选的化合物能够激动目标受体,则可以使钙流反应大大升高。反之,如果筛选的化合物能够拮抗目标受体,则可以使钙流反应大大降低。
[0095]
2.实验结果
[0096]
本发明中n,n-(4-哌啶基、芳基)-3-氨基苯酚类化合物对阿片受体的三个亚型mor、dor、kor的激动活性如下表1所示。
[0097]
表1.本发明化合物对阿片受体(mor、dor、kor)的激动活性的ec
50
值
[0098]
[0099][0100]
从表1的活性数据可以发现本发明n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物对三种阿片受体显示出较高的三重激动活性,尤其是对mor、dor激动活性可高达nm水平,本发明所涉化合物可用于制备强效镇痛药物。
[0101]
实施例3:
[0102]
片剂的制备:
[0103]
取n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物(化合物2-30任其一或任意组合)、其多晶型物,按其与赋形剂重量比为1:5-1:10的比例加入赋形剂,制粒压片。
[0104]
实施例4:
[0105]
口服液制剂的制备:
[0106]
取n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物(化合物2-30任其一或任意组合)、其多晶型物,按常规口服液制法制成口服液。
[0107]
实施例5:
[0108]
胶囊剂、颗粒剂、或冲剂的制备:
[0109]
取n,n-(4-哌啶基、芳基)-3-氨基苯酚类衍生物(化合物2-30任其一或任意组合)、其多晶型物,按其与赋形剂重量比为5:1的比例加入赋形剂,制成胶囊或颗粒剂或冲剂。
