1.本发明属于天然产物提取与分离技术领域,具体涉及一种利用深度共熔溶剂结合大孔树脂层析柱技术,从藤茶中得到二氢杨梅素的方法。
背景技术:
2.藤茶是葡萄科vitaceae michx蛇葡萄属ampelopsis野生木质落叶藤本植物显齿蛇葡萄ampelopsis grossedentata(hand-mazz)w.t.,原产于中国江南山区各地,作为茶类饮品在民间已有数百年的饮用历史,2013年被卫计委批准为新资源食品原料。近年来的研究表明,藤茶富含黄酮类功能活性成分,包括二氢杨梅素、杨梅素、杨梅苷等,其中二氢杨梅素在藤茶中的含量可高达30
–
40%;它具有抗肿瘤、抗炎、抗病毒、抗老年痴呆症等多种生物活性。因此,开发藤茶中二氢杨梅素的提取方法具有很大的实用价值。
3.二氢杨梅素传统的提取方法主要有有机溶剂提取法、碱性提取法、酶提取法和水提取法,其中有机溶剂提取目前最常用,然而,有机溶剂有许多缺点,如不环保、易燃、限制某些食品的使用等。因此,尝试新型绿色溶剂替代有机溶剂提取藤茶中二氢杨梅素的绿色方法是亟需解决的问题。
4.深度共熔溶剂(deep eutectic solvents,des),于2001年首次提出,它将两种具有较高熔点的固体物质混合加热一段时间,合成了均匀的混合溶液,且发现其物理状态由固态变成液体,混合物的熔点远低于合成所用的两种固体组成物。它作为一种新型溶剂还具有低毒性、不易挥发的显著优点。中国专利申请号201610209945.3的发明专利中,公开了一种利用氢键受体为季铵盐的深度共熔溶剂提取花青素的方法,季铵盐与氢供体的摩尔比为1:5。中国专利申请号202010351893.x的发明专利中,公开了一种深度共熔溶剂提取辣木总黄酮的方法,氢键受体为氯化胆碱,供体为丙三醇、尿素、乳酸。虽然深度共熔溶剂运用于天然活性物质的提取有诸多报道,但是针对藤茶中含量丰富的二氢杨梅素的提取制备目前还没有报道。
5.此外,大孔吸附树脂是常用于与天然产物分离的材料,具有吸附选择好、成本低、操作简便等多方面优点。中国专利申请号cn201811393143.8的发明专利中,公开了一种从藤茶水提液中使用大孔树脂进行吸附分离二氢杨梅素的方法。中国专利申请号cn200710026288.x中,公开了一种从枳椇子中提取二氢杨梅素的方法。因而大孔树脂应用于des提取后二氢杨梅素的富集与des的回收具有可行性。
技术实现要素:
6.针对现有技术存在的问题,本发明的目的在于设计提供一种应用des和大孔树脂从藤茶中提取高纯度二氢杨梅素的方法的技术方案。该方法首先通过优选的深度共熔溶剂与提取条件优化,高效获得二氢杨梅素;然后采用大孔树脂进行吸附分离,从二氢杨梅素提取物中分离获得高纯度的二氢杨梅素。该方法充分发挥了des和大孔树脂的特点,能够有效获得二氢杨梅素。
7.本发明具体通过以下技术方案实现:
8.所述的一种从藤茶中提取二氢杨梅素的方法,其特征在于包括以下步骤:
9.1)制备des:将氢键受体与氢键供体共熔,得到des,静置过夜;
10.2)des提取:取步骤1)得到的des与水配成提取溶剂,再将藤茶粉末与提取溶剂混合均匀,震荡提取,得到二氢杨梅素的提取液;
11.3)大孔树脂吸附分离:取步骤2)得到的二氢杨梅素的提取液,上样于大孔树脂,依次用蒸馏水、80%的乙醇、95%乙醇洗脱,收集获得80%乙醇洗脱液a,浓缩洗脱液a获得浓缩物b,即为二氢杨梅素单体成分。
12.进一步,所述步骤1)中所述氢键受体为四丁基溴化铵;所述氢键供体为丙酮酸;所述四丁基溴化铵与丙酮酸的摩尔比为1:2。
13.进一步,所述步骤1)中共熔处理条件为:80℃摇床中200rpm震荡3-4小时。
14.进一步,所述步骤2)中des与水配成体积浓度为60%-80%的提取溶剂。
15.进一步,所述步骤2)中藤茶粉末的粒径小于1mm,藤茶粉末的含水率为10%~12%。
16.进一步,所述步骤2)中藤茶粉末与提取溶剂按料液比为10-40g/ml。
17.进一步,所述步骤2)中震荡提取条件为:35-55℃,转速150-230rpm的摇床中震荡2-3h。
18.进一步,所述步骤3)中大孔吸附树脂型号为ab-8、dm301或xad-7hp。
19.进一步,所述步骤3)中大孔树脂吸附分离条件为:固液比为1-2g/ml,初始上样浓度25-100μg/ml,吸附温度为20-30℃。
20.本发明能够简便、高效地从藤茶中获得二氢杨梅素化合物,提取的二氢杨梅素得率高,比传统有机溶剂提取率高10-20%。本发明提供的提取方法,利用的des是由两种或者几种廉价且安全的化合物通过彼此之间氢键作用相互结合形成的混合盐溶液。des极性较大,物理化学性质接近于离子液体,但比离子液体更便宜、更安全、更容易制备,提取程序简单、提取效率高、分析时间短。相比传统有机溶剂,des有着原料价格低廉、具有良好的生物相容性、不易挥发、过程操作简单、提取过程无副产物产生的优点,充分体现了绿色化学的特点。其次,本发明中所采用的大孔树脂可以反复利用至少6次以上,且操作过程简便,适用于小规模或工业化的应用,具有较好的应用前景。
附图说明
21.图1为藤茶二氢杨梅素对照品的hplc谱图;
22.图2为深度共熔溶剂(des)提取藤茶样品hplc图;
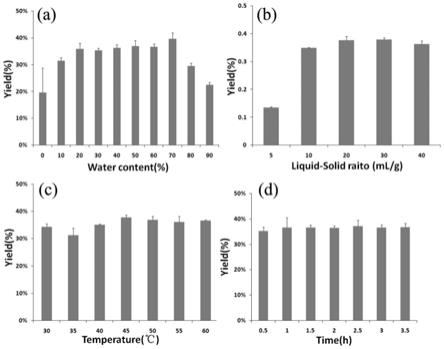
23.图3为深度共熔溶剂(des)含水率(a)、液料比(b)、提取温度(c)和提取时间(d)对藤茶二氢杨梅素提取得率的影响;
24.图4为响应面优化交互作用对藤茶中二氢杨梅素提取效率的影响;
25.图5为不同大孔树脂吸附二氢杨梅素回收率;
26.图6为考察dm301大孔树脂在料液比(a)、上样品初始浓度(b)、吸附温度(c)对二氢杨梅素的吸附率的影响;
27.图7为实施例3中dm301大孔树脂回收des提取样品hplc图。
具体实施方式
28.以下结合具体实施例来进一步说明本发明。
29.本实施例所采用分析藤茶提取液中二氢杨梅素的hplc条件为:以十八烷基硅烷键合硅胶(c18)色谱柱(岛津wondacract ods-2 4.6mm
×
250mm,5μm)为填充剂,以甲醇-0.1%甲酸(30:70)为流动相;检测波长为292nm。流速1.0ml/分钟,柱温35℃,进样量10μl。二氢杨梅素标准品hplc检测图谱见图1。
30.实施例1:des的选择以及des提取条件的选择
31.(1)制备深度共熔溶剂:将氢键受体与氢键供体按按一定摩尔比混合均匀,具体采用的氢键受体与氢键供体及摩尔比见表1,放入密封的玻璃瓶中,200rpm,80℃摇床中震荡3小时,得到纯净均匀液体,随后30℃静置过夜。本实施共制备了32种深度共熔溶剂供试。
32.(2)深度共熔溶剂提取:将(1)中所得溶液与水配成30%(体积比)的提取溶剂a,将藤茶粉末与提取溶剂a按料液比1:20g/ml混合均匀,在45℃,转速200rpm的摇床中震荡2h,得到二氢杨梅素的提取液,经液相检测该提取液中二氢杨梅素的得率;32种des提取溶剂提取所得二氢杨梅素得率见表1,发现四丁基溴化铵为氢键受体所得des提取效率较高,其中以12号四丁基溴化铵:丙酮酸(1:2)得率最高为388.481(mg/g藤茶干重),hplc检测图谱见图2。因此,本发明选择12号des作为提取剂。
33.表1不同des组成及其二氢杨梅素提取率
[0034][0035]
(a)深度共熔溶剂(des)含水率的选择
[0036]
按照上述提取条件,其他实验相同,分别考察des含水率为10,20,30,40,50,60,70,80,90%对目标化合物提取效率的影响。如图3(a)所示,当含水率为70%时,提取效率到达最大值,继续增大含水率,提取效率反而下降。综合,本技术选择des含水率为60-80%。
[0037]
(b)液料比的选择
[0038]
按照上述提取条件,其他实验相同,分别考察不同液料比5,10,20,30,40ml/g对目标化合物提取效率的影响。如图3(b)所示,当液料比达到20ml/g时,提取效率到达最大值,继续增大固液比,提取效率反而下降。这可能是因为des自身结果和物理特性的原因。综合,
本技术选择液料比为10-40ml/g。
[0039]
(c)提取温度的选择
[0040]
按照上述提取条件,其他实验相同,分别考察了不同提取温度20℃,35℃,40℃,45℃,50℃,55℃,60℃,对目标化合物提取效率的影响。如图3(c)所示,当提取温度从30℃增加到50℃时,二氢杨梅素的提取效率逐渐增大,而当温度进一步升高时,二氢杨梅素的提取效率反而微微下降,可能是因为高温下化合物降解的原因。综合,本技术选择提取温度为35-55℃。
[0041]
(d)提取时间的选择
[0042]
按照上述提取条件,其他实验相同,分别考察了不同提取时间0.5,1,1.5,2,2.5,3,3.5h对目标化合物提取效率的影响。如图3(d)所示,当提取时间为2.5h时,目标化合物的提取效率最大,进一步延长提取时间后,目标化合物的提取效率变化不显著,提示提取过程已经到达了平衡。综合,本技术选择提取时间为2-3h。
[0043]
(e)通过响应曲面实验优化最佳提取条件
[0044]
根据box-behnken的中心组合实验设计原理,以二氢杨梅素提取效率为响应值(y),固定液料比为20ml/g,选取des含水率(a)、提取温度(b)、时间(c)为优化因素,采用三因素三水平的响应曲面分析方法。实验因素与水平设计见表2。
[0045]
表2响应面因素设计水平表
[0046][0047]
为考察各因素及其交互作用对提取效率的影响,本发明利用design-expert软件对表2中的四因素三水平进行多元回归拟合,得到总提取效率的计算方程y=2.960a-0.482b+6.531c+0.014ab-0.060ac+0.294bc-0.024a
2-0.014b
2-2.837c
2-63.463。拟合该二次多项式模型的方差分析见表3,模型p《0.0001(极显著),表明该模型可用来进行响应值的预测。模型失拟项不显著,说明回归方程在整个回归空间内的拟合度较好。
[0048]
表3模型方差分析
[0049][0050][0051]
依据该回归方程得到的响应曲面图如图4所示,表明了各因素的作用和交互作用与提取效率之间的关系。通过分析得出藤茶中二氢杨梅素最佳提取条件为:含水率为71.18%,提取时间2.80h,提取温度46.40℃。依此条件测得二氢杨梅素得率为40.1%,与模型的计算值39.82%相近,表明采用该响应曲面法得到的最优提取条件准确可靠,具有实际应用价值。
[0052]
实施例2:大孔树脂的选择以及上样条件的选择
[0053]
大孔树脂分离:取实施例1中12号des作为提取剂得到的二氢杨梅素提取液1ml,上样于大孔树脂依次用大量蒸馏水、80%的乙醇洗脱(10ml),将上样后乙醇洗脱部分收集获得洗脱液a,浓缩洗脱液获得浓缩物b,测定纯度的得率。
[0054]
(a)大孔树脂的筛选
[0055]
选择xad1600n,xad16,xad1180,xad7hp,d101,s-8,ab-8,dm301,x-5九种大孔树脂,进行二氢杨梅素提取液的吸附回收实验,结果ab-8、dm301或xad-7hp对二氢杨梅素效果较好(图5a)。对dm301重复使用6次,回收率结果良好(图5b)。
[0056]
(b)上样条件的影响研究
[0057]
具体按照上述吸附洗脱步骤,其他条件相同,分别考察固液比(2,1,0.5,0.5,0.33,0.25,0.2g/ml),上样浓度(306.52,234.19,98.11,47.58,25.93μg/ml),吸附温度(20,30,40,50,60℃)对二氢杨梅素吸附率的影响,如图6所示,随着固液比、吸附温度的增加吸附率下降,而吸附初始浓度的减少吸附率增加。因此选择合适的固液比,吸附浓度和吸附温度,可以增加二氢杨梅素的回收率。
[0058]
实施例3:一种从藤茶中提取二氢杨梅素的方法
[0059]
1)制备des:将氢键受体四丁基溴化铵与氢键供体丙酮酸按摩尔比为1:2共熔,共熔条件为:80℃摇床中200rpm震荡3.5小时,得到des,静置过夜;
[0060]
2)des提取:取步骤1)得到的des与水配成浓度为70%的提取溶剂,再将藤茶粉末与提取溶剂按液料比20ml/g,混合均匀,藤茶粉末的粒径小于1mm,藤茶粉末的含水率为
11%,45℃,转速200rpm的摇床中震荡2.5h,得到二氢杨梅素的提取液;经hplc检测该提取液中二氢杨梅素的得率达到40.09%;
[0061]
3)大孔树脂吸附分离:取步骤2)得到的二氢杨梅素的提取液1ml,上样于大孔树脂,大孔吸附树脂型号为dm301,大孔树脂吸附分离条件为:固液比为2g/ml,初始上样浓度25.93μg/ml,吸附温度为20℃,依次用蒸馏水、80%的乙醇、95%乙醇洗脱,收集获得80%乙醇洗脱液a,浓缩洗脱液a获得浓缩物b,即为二氢杨梅素单体成分,得到纯度为92.1%二氢杨梅素23.34mg(图7)。
[0062]
实施例4:一种从藤茶中提取二氢杨梅素的方法
[0063]
1)制备des:将氢键受体四丁基溴化铵与氢键供体丙酮酸按摩尔比为1:2共熔,共熔条件为:80℃摇床中200rpm震荡3小时,得到des,静置过夜;
[0064]
2)des提取:取步骤1)得到的des与水配成浓度为60%的提取溶剂,再将藤茶粉末与提取溶剂按液料比40ml/g,混合均匀,藤茶粉末的粒径小于1mm,藤茶粉末的含水率为10.5%,55℃,转速230rpm的摇床中震荡3h,得到二氢杨梅素的提取液;经hplc检测该提取液中二氢杨梅素的得率达到39.64%;
[0065]
3)大孔树脂吸附分离:取步骤2)得到的二氢杨梅素的提取液2ml,上样于大孔树脂,大孔吸附树脂型号为ab-8,大孔树脂吸附分离条件为:固液比为1.5g/ml,初始上样浓度40μg/ml,吸附温度为30℃,依次用蒸馏水、80%的乙醇、95%乙醇洗脱,收集获得80%乙醇洗脱液a,浓缩洗脱液a获得浓缩物b,即为二氢杨梅素单体成分,得到纯度为91.6%二氢杨梅素21.24mg。
[0066]
实施例5:一种从藤茶中提取二氢杨梅素的方法
[0067]
1)制备des:将氢键受体四丁基溴化铵与氢键供体丙酮酸按摩尔比为1:2共熔,共熔条件为:80℃摇床中200rpm震荡4小时,得到des,静置过夜;
[0068]
2)des提取:取步骤1)得到的des与水配成浓度为80%的提取溶剂,再将藤茶粉末与提取溶剂按液料比10ml/g,混合均匀,藤茶粉末的粒径小于1mm,藤茶粉末的含水率为11.5%,35℃,转速150rpm的摇床中震荡2h,得到二氢杨梅素的提取液;经hplc检测该提取液中二氢杨梅素的得率达到39.40%;
[0069]
3)大孔树脂吸附分离:取步骤2)得到的二氢杨梅素的提取液1ml,上样于大孔树脂,大孔吸附树脂型号为xad-7hp,大孔树脂吸附分离条件为:固液比为1.5g/ml,初始上样浓度40μg/ml,吸附温度为30℃,依次用蒸馏水、80%的乙醇、95%乙醇洗脱,收集获得80%乙醇洗脱液a,浓缩洗脱液a获得浓缩物b,即为二氢杨梅素单体成分,得到纯度为90.9%二氢杨梅素44.62mg。
