用于检测食道癌的组合物及其用途
1.本技术是中国申请号为201810989986.8、发明名称为“用于检测食道癌的组合物及其用途”且申请日为2018年8月28日的专利申请的分案申请。
技术领域
2.本发明属于生物技术领域,涉及一种组合物及其在疾病检测中的用途,具体地涉及一种用于检测食管癌的组合物及其相应的试剂盒和用途。
背景技术:
3.食管癌是一种常见消化道肿瘤。全国肿瘤防治办公室数据显示:2015年,中国食管癌发病率为478例/10万人,死亡率为375例/万人,分别位居常见癌症中的第四位和第三位。食管癌的病死率接近80%,是一种恶性程度很高的癌症。全球每年约有30万人死于食管癌,其中一半来自中国。
4.导致食管癌高死亡率的重要因素是早期食管癌的确诊率低。早期食管癌的治愈率远高于中晚期,但是由于早期食管癌缺乏明显和特异的症状,绝大部分受试者确诊时已经发展进入中晚期。临床研究发现,癌症从病灶开始形成到受试者出现临床症状的过程平均需要数年时间;这为发现早期食管癌、提高早期食管癌的确诊率提供了一个有效的窗口期。充分利用这个窗口期,有望提高食管癌治疗效果、降低食道癌死亡率。
5.目前临床上应用于食管癌诊断的技术在早期食道癌的检测和筛查方面的应用有限,主要因为:1)组织活检侵入性强,不适于早癌筛查;2)影像学检测技术(如:食管造影检查和内镜检查)在设备成本、操作技术、和侵入性等方面上的限制,也难以作为癌症筛查技术而大范围推广;3)传统血清肿瘤标识物(如:afp、cea、ca125、和ca199等)对食管癌检测的灵敏度较低,无法充分满足早癌筛查的要求。
技术实现要素:
6.基于此,针对现有食管癌检测技术存在的检测不便、灵敏度低、和成本高的问题,本发明提供了一种用于检测食道癌的组合物。本发明提供的组合物能够灵敏和特异地检测食管癌,本发明还提供了包含所述组合物的试剂盒以及其在检测食管癌中的用途。本发明提供的试剂盒具有良好的食管癌检测灵敏性,能够方便、快捷、有效地检测食管癌。
7.本发明提供了一种用于体外检测食管癌的组合物、试剂盒及其用途,以及基于该试剂盒来执行检测的方法。
8.具体来说,本发明涉及以下内容:
9.1.一种用于体外检测食管癌的组合物,所述组合物包括:
10.用于检测目标基因靶序列甲基化状态的核酸,以及
11.用于检测目标蛋白浓度的抗体,
12.其中,所述目标基因为mt1a基因和epo基因中的一种或两种,
13.所述目标蛋白为sncg,即γ突触核蛋白(γ-synuclein)。
14.2.根据项1所述的组合物,其中,所述mt1a基因的靶序列如seq id no:1所示。
15.3.根据项1所述的组合物,其中,所述epo基因的靶序列如seq id no:3所示。
16.4.根据项1~3中任一项所述的组合物,其中,所述用于检测目标基因靶序列甲基化状态的核酸包括:
17.所述目标基因靶序列中至少9个核苷酸的片段,
18.所述片段包含至少一个cpg二核苷酸序列。
19.5.根据项1~4中任一项所述的组合物,其中,所述用于检测目标基因甲基化状态的核酸包括还包括:
20.在中等严紧或严紧条件下杂交于所述目标基因靶序列中至少15个核苷酸的片段,
21.所述片段包含至少一个cpg二核苷酸序列。
22.6.根据项1~5中任一项所述的组合物,其还包括:
23.将目标基因靶序列的5位未甲基化胞嘧啶碱基转化为尿嘧啶的试剂。
24.7.根据项1~6中任一项所述的组合物,其中,所述用于检测目标基因甲基化状态的核酸还包括:
25.优先与处于非甲基化状态的靶序列结合的阻断剂。
26.8.根据项7所述的组合物,其中,
27.所述至少9个核苷酸的片段,其为seq id no:5和seq id no:6的序列,或者其为seq id no:9和seq id no:10的序列,
28.所述至少15个核苷酸的片段,其为seq id no:7的序列或seq id no:11的序列,
29.阻断剂,其为seq id no:8的序列或seq id no:12的序列。
30.9.根据项1~8中任一项所述的组合物,所述组合物还包括:
31.用于检测目标蛋白浓度的试剂,所述试剂为酶联免疫吸附测定试剂,例如,所述试剂包括用于检测目标蛋白浓度的抗体包被的反应板,sncg蛋白酶结合物,底物液,洗液和终止液。
32.10.一种用于体外检测食管癌的寡核苷酸,其包括:
33.所述seq id no:1或其互补序列中的至少9个核苷酸且包含至少一个cpg二核苷酸序列的片段;和/或
34.所述seq id no:3或其互补序列中的至少9个核苷酸且包含至少一个cpg二核苷酸序列的片段。
35.11.根据项10所述的寡核苷酸,其还包括:
36.在中等严紧或严紧条件下杂交于所述seq id no:1或其互补序列中的至少15个核苷酸且包含至少一个cpg二核苷酸序列的片段;和/或
37.在中等严紧或严紧条件下杂交于所述seq id no:3或其互补序列中的至少15个核苷酸且包含至少一个cpg二核苷酸序列的片段。
38.12.根据项11所述的寡核苷酸,其还包括:
39.优先与处于非甲基化状态的靶序列结合的阻断剂。
40.13.一种用于体外检测食管癌的寡核苷酸,其包括:
41.seq id no:5和seq id no:6的序列。
42.14.根据项13所述的寡核苷酸,其还包括:
43.seq id no:7的序列。
44.15.根据项14所述的寡核苷酸,其还包括:
45.seq id no:8的序列。
46.16.一种用于体外检测食管癌的寡核苷酸,其包括:
47.seq id no:9和seq id no:10的序列。
48.17.根据项16所述的寡核苷酸,其还包括:
49.seq id no:11的序列。
50.18.根据项17所述的寡核苷酸,其还包括:
51.seq id no:12的序列。
52.19.mt1a基因在制备用于体外检测食管癌的试剂盒中的用途。
53.20.epo基因在制备用于体外检测食管癌的试剂盒中的用途。
54.21.一种试剂盒,其包括项1~9中任一项所述的组合物或包括项10~18中任一项所述的寡核苷酸。
55.22.根据项21所述的试剂盒,其还包含选自下述的至少一种其它组分:
56.三磷酸核苷、dna聚合酶和所述dna聚合酶功能所需的缓冲液,以及
57.用于检测目标蛋白浓度的抗体包被的反应板,sncg蛋白酶结合物,底物液,洗液和终止液。
58.23.根据项21或22所述的试剂盒,其还包含:说明书。
59.24.根据项1~9中任一项所述的组合物或项10~项18中任一项所述的寡核苷酸在用于制备用于体外检测食管癌的试剂盒中的用途。
60.25.根据项19、20以及24中任一项所述的用途,其中,所述用于体外检测食管癌的试剂盒通过包括如下步骤的方法来检测食管癌:
61.1)确定受试者生物样品中所述目标基因靶序列的甲基化状态;
62.2)确定受试者生物样品中所述目标蛋白的浓度;
63.3)通过所述目标基因靶序列甲基化状态和目标蛋白浓度的检测结果联合判断受试者是否患有食管癌,从而实现对食管癌的体外检测。
64.26.根据项25所述的用途,其中,所述方法包括如下步骤:
65.抽取受试者的外周血,分离血浆或血清;
66.提取血浆或血清中的游离dna;
67.使用试剂处理提取的游离dna,使5位未甲基化的胞嘧啶碱基转化为尿嘧啶或其它碱基;
68.将试剂处理过的dna样品与dna聚合酶和目标基因靶序列的引物接触,并在优先与处于非甲基化状态的靶序列结合的阻断剂的存在下进行dna聚合反应;
69.用探针检测扩增产物;
70.基于所述扩增产物是否存在,确定所述目标基因靶序列的至少一个cpg二核苷酸的甲基化状态;以及
71.使用sncg抗体,利用免疫反应确定血浆或血清中sncg的浓度。
72.27.根据项26所述的用途,其中,所述试剂为亚硫酸氢盐试剂。
73.28.一种检测食管癌的方法,其包括如下步骤:
74.抽取受试者的生物样品;
75.确定受试者生物样品中的所述目标基因靶序列的甲基化状态;
76.确定受试者生物样品中的所述目标蛋白的浓度;以及
77.通过所述目标基因靶序列甲基化状态和目标蛋白浓度的检测结果联合判断受试者是否患有食管癌,从而实现对食管癌的体外检测。
78.29.一种检测食管癌的方法,其包括如下步骤:
79.抽取受试者外周血,分离血浆或血清;
80.提取血浆或血清中的游离dna;
81.使5位未甲基化的胞嘧啶碱基转化为尿嘧啶或其它碱基;
82.将试剂处理过的dna样品与dna聚合酶和目标基因靶序列的引物接触,并在优先与处于非甲基化状态的靶序列结合的阻断剂的存在下进行dna聚合反应;
83.用探针检测扩增产物;
84.基于所述扩增产物是否存在,确定所述目标基因靶序列的至少一个cpg二核苷酸的甲基化状态;以及
85.使用sncg抗体,利用免疫反应确定血浆或血清中sncg的浓度。
86.30.根据项28或29所述的方法,其中,
87.所述目标基因为mt1a基因和epo基因中的一种或两种,以及
88.所述目标蛋白为sncg。
89.31.根据项30所述的方法,其中,所述mt1a基因的靶序列如seq id no:1所示。
90.32.根据项30所述的方法,其中,所述epo基因的靶序列如seq id no:3所示。
91.33.根据项29所述的方法,其中,所述试剂为亚硫酸氢盐试剂。
92.34.根据项29所述的方法,其中,所述引物为:
93.所述seq id no:1或其互补序列中的至少9个核苷酸且包含至少一个cpg二核苷酸序列的片段;和/或
94.所述seq id no:3或其互补序列中的至少9个核苷酸且包含至少一个cpg二核苷酸序列的片段。
95.35.根据项29所述的方法,其中,所述阻断剂为优先与处于非甲基化状态的靶序列结合的阻断剂。
96.36.根据项29所述的方法,其中,所述探针为:
97.在中等严紧或严紧条件下杂交于所述seq id no:1或其互补序列中的至少15个核苷酸且包含至少一个cpg二核苷酸序列的片段;和/或
98.在中等严紧或严紧条件下杂交于所述seq id no:3或其互补序列中的至少15个核苷酸且包含至少一个cpg二核苷酸序列的片段。
99.37.根据项34所述的方法,其中,所述引物为seq id no:5和seq id no:6的序列,或者其为seq id no:9和seq id no:10的序列。
100.38.根据项35所述的方法,其中,所述阻断剂为seq id no:8的序列或seq id no:12的序列
101.39.根据项36所述的方法,其中,所述探针为seq id no:7的序列或seq id no:11的序列。
102.本发明的发明人利用表观基因组学和生物信息学技术,通过分析食管癌组织和癌旁对照组织的全基因组甲基化数据,发现两个与食管癌相关的甲基化基因,并确定了这两个食管癌甲基化基因发生甲基化异常的靶序列;进一步,本发明的发明人发现,通过这两个食管癌甲基化基因的靶序列,能够灵敏和特异地检测这两个基因的甲基化状态,从而可以用于对外周血游离dna的检测。通过对食管癌受试者和正常对照个体的外周血样本的检测显示:本发明描述的组合物和检测方法能够灵敏和特异地检测食管癌;进一步,本发明的发明人发现,在众多肿瘤蛋白标识物中,sncg蛋白与所述目标基因甲基化的联合检测能够显著提高对食管癌的检出。因此,本发明提供了一种可用于体外检测食管癌的组合物和检测方法,具有重要的临床应用价值。
103.本发明的其他特点和优势将由下面的具体说明和权利要求书作详细的描述。
附图说明
104.本发明的上述及其它特征将通过下面结合附图及其详细描述作进一步说明。应当理解的是,这些附图仅示出了根据本发明的若干示例性的实施方式,因此不应被视为是对本发明保护范围的限制。除非特别说明,附图不必是成比例的,并且其中类似的标号表示类似的部件。
105.图1显示筛选本发明的目标基因的结果图。
106.图2为使用本发明提供的组合物和检测方法对白细胞基因组dna(目标基因靶序列甲基化状态的阴性参考品)和dna甲基转移酶处理后的白细胞基因组dna(目标基因靶序列甲基化状态的阳性参考品)的检测。结果显示:本发明提供的组合物和检测方法对白细胞基因组dna的检测结果为阴性,对dna甲基转移酶处理后的白细胞基因组dna的检测结果为阳性。
107.图3为利用所述的组合物和检测方法,通过检测目标基因靶序列的甲基化状态和目标蛋白的浓度,实现对食管癌的体外无创检测的结果图。
具体实施方式
108.一方面,本发明提供了一种用于体外检测食管癌的组合物,所述组合物包括用于检测目标基因靶序列内甲基化状态的核酸,和用于检测目标蛋白浓度的抗体;其中,所述目标基因为mt1a基因和epo基因中的一种或两种,所述目标蛋白为sncg。
109.本发明提供了一组在食管癌中发出异常甲基化的目标基因靶序列,包括mt1a基因和epo基因的靶序列,mt1a基因的靶序列如seq id no:1-2所示,epo基因的靶序列如seq id no:3-4所示。
110.mt1a基因的靶序列如seq id no:1所示。
111.seq id no:1
112.cacccaggggagctcagtggactgtgcgccttgcctttctgctgcgcaaagcccagtccaggtcatcacctcgggcggggcggactcggctgggcggactcagcggggcgggcgcaggcgcagggcgggtcctttgcgtccggccctctttcccctgaccataaaagcagc
113.seq id no:1的互补序列如seq id no:2所示。
114.seq id no:2
115.gctgcttttatggtcaggggaaagagggccggacgcaaaggacccgccctgcgcctgcgcccgccccgctgagtccgcccagccgagtccgccccgcccgaggtgatgacctggactgggctttgcgcagcagaaaggcaaggcgcacagtccactgagctcccctgggtg
116.优选地,epo基因的靶序列的序列如seq id no:3所示。
117.seq id no:3
118.cgcgcacgcacacatgcagataacagccccgacccccggccagagccgcagagtccctgggccaccccggccgctcgctgcgctgcgccgcaccgcgctgtcctcccggagccggaccggggccaccgcgcccgctctgctccgacaccgcgccccctggacagccgccctctcctccaggcccgtggggctggccctgcaccgccgagcttcccgggatgagggcccccggtgtggtcacccggcgcgccccaggtcg
119.seq id no:3的互补序列如seq id no:4所示。
120.cgacctggggcgcgccgggtgaccacaccgggggccctcatcccgggaagctcggcggtgcagggccagccccacgggcctggaggagagggcggctgtccagggggcgcggtgtcggagcagagcgggcgcggtggccccggtccggctccgggaggacagcgcggtgcggcgcagcgcagcgagcggccggggtggcccagggactctgcggctctggccgggggtcggggctgttatctgcatgtgtgcgtgcgcg
121.优选地,用于检测目标基因甲基化状态的核酸包括目标基因靶序列中的至少9个核苷酸的片段,其中所述片段包含至少一个cpg二核苷酸序列。在某些优选实施方式中,如使用亚硫酸氢盐对待测样本dna进行转化,用于检测目标基因甲基化状态的核酸包括对目标基因靶序列进行亚硫酸氢盐转化后的序列中的至少9个核苷酸的片段,其中所述核苷酸的片段包含至少一个cpg二核苷酸序列。
122.更优选地,用于检测目标基因甲基化状态的核酸包括在中等严紧或严紧条件下杂交于所述目标基因靶序列中的至少15个核苷酸的片段,其中所述核苷酸的片段包含至少一个cpg二核苷酸序列。在某些优选实施方式中,如:使用亚硫酸氢盐对待测样本dna进行转化,用于检测目标基因甲基化状态的核酸包括在中等严紧或严紧条件下,杂交于目标基因靶序列进行亚硫酸氢盐转化后序列中的至少15个核苷酸的片段,其中所述核苷酸的片段包含至少一个cpg二核苷酸序列。
123.优选地,所述组合物还包括将目标基因靶序列的5位未甲基化胞嘧啶碱基转化为尿嘧啶的试剂。更优选地,所述试剂为亚硫酸氢盐。
124.优选地,用于检测目标基因甲基化状态的核酸还包括优先与处于非甲基化状态的dna结合的阻断剂。
125.优选地,所述组合物包括如下的引物、探针和/或阻断剂中的一种或多种:
126.mt1a引物f
127.seq id no:5
128.cggacgtaaaggattc
129.mt1a引物r
130.seq id no:6
131.gaaacgaactcgactaaacg
132.mt1a探针
133.seq id no:7
134.tgcgtttgcgttcgtttcg
135.mt1a阻断剂
136.seq id no:8
137.caaactcaactaaacaaactcaacaaaacaaac
138.epo引物f
139.seq id no:9
140.agtcgtagagtttttgggtt
141.epo引物r
142.seq id no:10
143.caacgcgatacgacg
144.epo探针
145.seq id no:11
146.cgcaacgaacgaccga
147.epo阻断剂
148.seq id no:12
149.gagtttttgggttattttggttgtttgttg
150.另一方面,本发明提供用于体外检测食管癌的寡核苷酸,其包括:seq id no:1或其互补序列中的至少9个核苷酸且包含至少一个cpg二核苷酸序列的片段;和/或seq id no:3或其互补序列中的至少9个核苷酸且包含至少一个cpg二核苷酸序列的片段。
151.优选地该用于体外检测食管癌的寡核苷酸包括:对seq id no:1或其互补序列进行亚硫酸氢盐转化后的序列中的至少9个核苷酸的片段;和/或对seq id no:3或其互补序列进行亚硫酸氢盐转化后的序列中的至少9个核苷酸且包含至少一个cpg二核苷酸序列的片段。
152.本发明的用于体外检测食管癌的寡核苷酸,其还包括:在中等严紧或严紧条件下杂交于所述seq id no:1或其互补序列中的至少15个核苷酸且包含至少一个cpg二核苷酸序列的片段;和/或在中等严紧或严紧条件下杂交于所述seq id no:3或其互补序列中的至少15个核苷酸且包含至少一个cpg二核苷酸序列的片段。
153.优选地该用于体外检测食管癌的寡核苷酸包括:在中等严紧或严紧条件下杂交于对seq id no:1或其互补序列进行亚硫酸氢盐转化后的序列中的至少15个核苷酸且包含至少一个cpg二核苷酸序列的片段;和/或在中等严紧或严紧条件下杂交于对seq id no:3或其互补序列进行亚硫酸氢盐转化后的序列中的至少15个核苷酸且包含至少一个cpg二核苷酸序列的片段。
154.本发明的用于体外检测食管癌的寡核苷酸,其还包括:优先与处于非甲基化状态的dna结合的阻断剂。
155.在一个具体的实施方式中,用于体外检测食管癌的寡核苷酸,其包括:seq id no:5和seq id no:6的序列。其还包括:seq id no:7的序列。其还包括:seq id no:8的序列。
156.在另一个具体的实施方式中,用于体外检测食管癌的寡核苷酸,其包括:seq id no:9和seq id no:10的序列。其还包括:seq id no:11的序列。其还包括:seq id no:12的序列。
157.另一方面,本发明提供了包括所述组合物的试剂盒。该试剂盒还包含选自下述的
至少一种其它组分:三磷酸核苷、dna聚合酶和所述dna聚合酶功能所需的缓冲液。
158.本发明的用于体外检测食管癌的组合物,所述还包括用于检测目标蛋白浓度的抗体,所述目标蛋白为γ突触核蛋白(sncg)。
159.本发明还涉及mt1a基因、epo基因、sncg蛋白在制备用于体外检测食管癌的试剂盒中的用途。
160.其中,所述mt1a为金属硫蛋白1a,英文名称metallothionein 1a,位于人类的第16号染色体的q13区域,属于金属硫蛋白基因家族。金属硫蛋白是一种小分子蛋白,富含半胱氨酸,缺乏含有芳香基的氨基酸,能够结合二价重金属离子。金属硫蛋白是一种抗氧化剂,能够保护细胞免受含有羟基的自由基损害,维持细胞内金属离子的平衡,同时发挥去除重离子毒性的作用。金属硫蛋白基因功能的丧失会导致癌症的发生等病理现象。
161.所述epo基因为红细胞生成素基因,英文名称erythropoietin,位于人类的第7号染色体的q22.1区域。该基因所编码的蛋白是一种由细胞分泌的糖基化的细胞活素(cytokine)。当红细胞生成素与相应受体结合后,能够促进红细胞的合成。
162.所述sncg蛋白为突触核蛋白-γ,是sncg基因的产物。sncg基因的英文名称为synuclein gamma,位于人类的第10号染色体的q23.2区域。该基因是突触核蛋白基因家族的一员,其蛋白序列如下:)。
163.sncg基因所编码蛋白的氨基酸序列为:
164.mdvfkkgfsiakegvvgavektkqgvteaaektkegvmyvgaktkenvvqsvtsvaektkeqanavseavvssvntvatktveeaeniavtsgvvrkedlrpsapqqegeaskekeevaeeaqsggd
165.再一方面,本发明提供了一种体外检测食管癌的方法,所述方法包括以下步骤:
166.1)确定受试者生物样品中所述目标基因靶序列的甲基化状态;
167.2)确定受试者生物样品中所述目标蛋白的浓度;
168.3)通过所述目标基因靶序列甲基化状态和目标蛋白浓度的检测结果联合判断受试者是否患有食管癌,从而实现对食管癌的体外检测。
169.其中,生物样品是由受试者的外周血中分离的血浆或血清。
170.根据某些优选实施方式,所述方法还包括以下步骤:
171.1)抽取受试者外周血,分离血浆或血清;
172.2)提取血浆或血清中的游离dna;
173.3)使用试剂处理步骤2)得到的游离dna,使5位未甲基化的胞嘧啶碱基转化为尿嘧啶或其它碱基,即目标基因靶序列的5位未甲基化的胞嘧啶碱基转化为尿嘧啶或其它碱基,转化后的碱基在杂交性能方面不同于5位未甲基化的胞嘧啶碱基,并且是可检测的;
174.4)将经步骤3)处理过的游离dna与dna聚合酶和所述目标基因靶序列的引物接触,使得所述经处理的目标基因靶序列被扩增以产生扩增产物或不被扩增;所述经处理的目标基因靶序列如果发生dna聚合反应,会产生扩增产物;所述经处理的目标基因靶序列如果不发生dna聚合反应,则不被扩增;
175.5)用探针检测扩增产物;
176.6)基于所述扩增产物是否存在,确定所述目标基因靶序列的至少一个cpg二核苷酸的甲基化状态。
177.7)使用sncg抗体,利用免疫反应确定血浆或血清中sncg的浓度。
178.优选地,典型的引物包括所述目标基因靶序列的片段,所述目标基因靶序列的片段包含分别等同于、互补于或在中等严紧或严紧条件下杂交于选自seq id no:1-2和seq id no:3-4中的至少9个核苷酸的片段。
179.优选地,所述引物、探针和/或阻断剂中的一种或多种如下所示:
180.mt1a引物f
181.seq id no:5
182.cggacgtaaaggattc
183.mt1a引物r
184.seq id no:6
185.gaaacgaactcgactaaacg
186.mt1a探针
187.seq id no:7
188.tgcgtttgcgttcgtttcg
189.mt1a阻断剂
190.seq id no:8
191.caaactcaactaaacaaactcaacaaaacaaac
192.epo引物f
193.seq id no:9
194.agtcgtagagtttttgggtt
195.epo引物r
196.seq id no:10
197.caacgcgatacgacg
198.epo探针
199.seq id no:11
200.cgcaacgaacgaccga
201.epo阻断剂
202.seq id no:12
203.gagtttttgggttattttggttgtttgttg
204.并且,所述接触或扩增包括使用至少一种如下的方法:使用耐热dna聚合酶作为所述扩增酶、使用缺乏5-3’外切酶活性的聚合酶、使用聚合酶链式反应(pcr)、产生带有可检测标记的扩增产物核酸分子。
205.据某些优选实施方式,所述目标基因靶序列中至少一个cpg二核苷酸的甲基化状态是由pcr反应的循环阈值ct值确定的。通过利用pcr反应分析生物样本中dna的方法,能方便地实现针对目标基因靶序列甲基化状态的检测,并且能根据pcr反应的循环阈值来快速、便捷地判断受检样本是否呈阳性,因而提供了一种无创、快速的食管癌体外检测方法。
206.所述的生物样品选自外周血全血、血浆、或血清。
207.本发明还提供了包括所述组合物的试剂盒。典型地,所述的试剂盒包括用于容纳受试者生物样品的容器。并且,所述的试剂盒也包括使用和解释检测结果的说明。
208.本发明提供了一种通过检测目标基因靶序列甲基化状态和目标蛋白浓度,体外无
创检测食管癌的方法。本发明人发现,在食管癌组织中mt1a基因和epo基因靶序列的甲基化状态和正常食管组织的所述基因靶序列的甲基化状态存在显著性差异:在食管癌组织中,mt1a基因和epo基因靶序列发生甲基化,而在正常食管组织中,mt1a基因和epo基因靶序列不发生甲基化。本发明人进一步发现,与单独检测目标基因靶序列甲基化状态相比,联合检测目标基因靶序列甲基化状态和目标蛋白浓度能够显著提高对食管癌的检出率,同时对检测的特异性没有显著影响。因此本技术提供了一种通过检测样本中的mt1a基因和epo基因靶序列甲基化状态和sncg蛋白浓度,对食管癌进行体外检测的方法,本发明提供的方法能够无创、快速地检测食管癌。
209.除非另外定义,本说明书中有关技术的和科学的术语与本领域内的技术人员所通常理解的意思相同。虽然在实验或实际应用中可以应用与此间所述相似或相同的方法和材料,本文还是在下文中对材料和方法做了描述。在相冲突的情况下,以本说明书包括其中定义为准,另外,材料、方法和例子仅供说明,而不具限制性。
210.本发明还提供一种能够灵敏和特异地检测目标基因靶序列甲基化状态和目标蛋白浓度的组合物;以及一种可用于体外无创检测食管癌的方法和试剂盒。
211.下述描述为本发明的组合物、试剂盒、核酸序列以及检测方法的实施例。第一组实施方案公开了目标基因和目标基因靶序列;第二组实施方案公开了用于检测目标基因靶序列甲基化状态的组合物,包括用于检测目标基因靶序列甲基化状态的核酸;第三组实施方案公开了一种通过检测目标基因靶序列甲基化状态和目标蛋白浓度进行体外无创检测食管癌的方法。
212.优选地,所述核酸检测的序列包括所述目标基因靶序列中的至少9个核苷酸的片段,其中所述核苷酸的片段包含至少一个cpg二核苷酸序列;在某些优选实施方式中,如:使用亚硫酸氢盐对待测样本dna进行转化,所述核酸检测的序列包括对目标基因靶序列进行亚硫酸氢盐转化后的序列中的至少9个核苷酸的片段,其中所述核苷酸的片段包含至少一个cpg二核苷酸序列;
213.更优选地,所述核酸检测的序列分别包括在中等严紧或严紧条件下杂交于所述目标基因靶序列中的至少15个核苷酸的片段,其中所述核苷酸的片段包含至少一个cpg二核苷酸序列;在某些优选实施方式中,如:使用亚硫酸氢盐对待测样本dna进行转化,所述核酸检测的序列包括在中等严紧或严紧条件下,杂交于目标基因靶序列进行亚硫酸氢盐转化后序列中的至少15个核苷酸的片段,其中所述核苷酸的片段包含至少一个cpg二核苷酸序列。
214.在某些实施方式中,所述组合物还包括将基因的5位未甲基化的胞嘧啶碱基转化为尿嘧啶的试剂。优选地,该试剂是亚硫酸氢盐。dna的亚硫酸氢盐修饰为已知的用于评估cpg甲基化状态的工具。在真核细胞的dna中,5-甲基胞嘧啶是最常见的共价碱基修饰。5-甲基胞嘧啶不能通过测序来鉴定,因为5-甲基胞嘧啶与胞嘧啶有相同的碱基配对行为。此外,在pcr扩增过程中,5-甲基胞嘧啶携带的表观遗传信息则完全丢失。最常用于分析dna中5-甲基胞嘧啶存在的方法是基于亚硫酸氢盐与胞嘧啶的特异反应;在随后的碱性水解后,没有甲基化的胞嘧啶被转变为在配对行为上对应胸腺嘧啶的尿嘧啶;但在这些条件下5-甲基胞嘧啶保持不被修饰。由此原始的dna以此方式被转变,使得原来在其杂交行为上不能与胞嘧啶区分开的5-甲基胞嘧啶现在可作为仅剩的胞嘧啶被常规的已知分子生物学技术检测到,例如通过扩增和杂交。所有这些技术都基于不同的碱基配对特性,现在可被充分利用
了。因此,典型地,本技术提供了亚硫酸氢盐技术与一种或多种甲基化测定的联合使用,用于确定目标基因靶序列内的cpg二核苷酸序列的甲基化状态。此外,本发明的方法适于分析异质的生物样品,例如血液或粪便中的低浓度肿瘤细胞。因此,当分析这种样品中cpg二核苷酸序列的甲基化状态时,本领域技术人员可以使用定量测定法来确定特定cpg二核苷酸序列的甲基化水平(例如百分比、份数、比率、比例或程度),而不是甲基化状态。相应地,术语甲基化状况或甲基化状态还应被认为是指反映cpg二核苷酸序列甲基化状态的值。
215.在某些实施方式中,本技术的方法具体包括:1)抽取受试者外周血;2)提取血浆或血清中的游离dna;3)使用试剂处理步骤2)得到的游离dna,使5位未甲基化的胞嘧啶碱基转化为尿嘧啶或其它碱基,即目标基因靶序列的5位未甲基化的胞嘧啶碱基转化为尿嘧啶或其它碱基,转化后的碱基在杂交性能方面不同于5位未甲基化的胞嘧啶碱基,并且是可检测的;4)将经步骤3)处理过的dna样品与dna聚合酶和所述目标基因靶序列的引物接触,使得所述经处理的目标基因靶序列被扩增以产生扩增产物或不被扩增;所述经处理的目标基因靶序列如果发生dna聚合反应,会产生扩增产物;所述经处理的目标基因靶序列如果不发生dna聚合反应,则不被扩增;5)用探针检测扩增产物;6)基于所述扩增产物是否存在,确定所述目标基因靶序列的至少一个cpg二核苷酸的甲基化状态;7)利用sncg抗体,通过免疫反应(优选地,酶联免疫吸附试验,elisa),检测血浆或血清中目标蛋白的浓度。
216.典型地,所述接触或扩增包括使用至少一种如下的方法:使用耐热dna聚合酶作为所述扩增酶;使用缺乏5-3’外切酶活性的聚合酶;使用pcr;产生带有可检测标记的扩增产物核酸分子。优选地,用pcr方式来测定甲基化状态,诸如“基于荧光的实时pcr技术”、甲基化敏感的单核苷酸引物延伸反应(ms-snupe)、甲基化特异性pcr(msp)、和甲基化cpg岛扩增(mca)等测定方法被用于测定目标基因靶序列的至少一个cpg二核苷酸的甲基化状态。其中,“基于荧光的实时pcr”测定为高通量定量甲基化测定,其使用基于荧光的实时pcr(taqman)技术,在pcr步骤后不需要进一步的操作。简言之,“基于荧光的实时pcr”方法以基因组dna的混合样品开始,该混合样品根据标准操作在亚硫酸氢钠反应中被转变为甲基化依赖的序列差异的混合池。随后在“偏移的(biased)”反应(采用重叠已知cpg二核苷酸的pcr引物)中进行基于荧光的pcr。可在扩增水平以及在荧光检测扩增水平上产生序列差别。“基于荧光的实时pcr”测定可以用作基因组dna样品中甲基化状态的定量测试,其中序列区分发生在探针杂交水平上。在该定量方式中,在重叠特定的cpg二核苷酸的荧光探针存在下,pcr反应提供了甲基化特异的扩增。用于起始dna量的无偏移对照由以下反应提供:其中引物和探针都不覆盖任何cpg二核苷酸。“基于荧光的实时pcr”方法可与任何适合的探针一起使用,如“taqman”、“lightcycler”等。taqman探针为荧光报道物(reporter)和淬灭分子(quencher)双标记的,并被设计为特异于相对高gc含量区,以至于其在pcr循环中以比正向或反向引物高约10℃的温度熔解。这使得taqman探针在pcr退火/延伸步骤中保持充分杂交。当taq聚合酶在pcr中酶合成新链时,其最终会遇到退火的taqman探针。taq聚合酶5至3’内切酶活性随后将通过消化taqman探针而顶替它,从而释放荧光报道物分子用于采用实时荧光检测系统定量检测其现在未被淬灭的信号。用于“基于荧光的实时pcr”分析的典型试剂可以包括,但不限于:用于目标基因靶序列pcr引物;非特异扩增阻断剂;taqman或lightcycler探针;优化的pcr缓冲液以及脱氧核苷酸;以及taq聚合酶等。
217.其中利用sncg抗体,利用免疫反应确定血浆或血清中sncg的浓度是通过酶联免疫
吸附法(elisa)检测sncg蛋白在血清中的表达水平;
218.优选地,所述elisa为“三明治法”,具体来说该方法包括以下步骤:
219.1)使用sncg单克隆抗体(鼠)对96孔板进行包被;
220.2)加入10倍稀释的临床血清样本或血浆样本和系列稀释的人源sncg蛋白溶液;
221.3)在每孔中加入辣根过氧化酶(horseradish peroxidase,hrp)标记的鼠抗人源sncg的多抗(igg);
222.4)装有以上混合物的免疫反应板在室温、震荡条件下,孵育,用洗液清洗个反应孔后,加入显色底物;
223.5)加入终止液终止显色反应后,使用读板仪对各反应孔的光谱进行检测;
224.6)利用系列稀释的人源sncg蛋白溶液的检测值建立标准曲线,并基于标准曲线对临床血清样本进行定量。
225.在本发明的具体事实方式中,基于一定数量的食管癌样本和正常样本的sncg基因的血清或血浆蛋白水平,确定相对于sncg基因血清或血浆蛋白水平的食管癌和正常的临界值。
226.实施例
227.实施例1
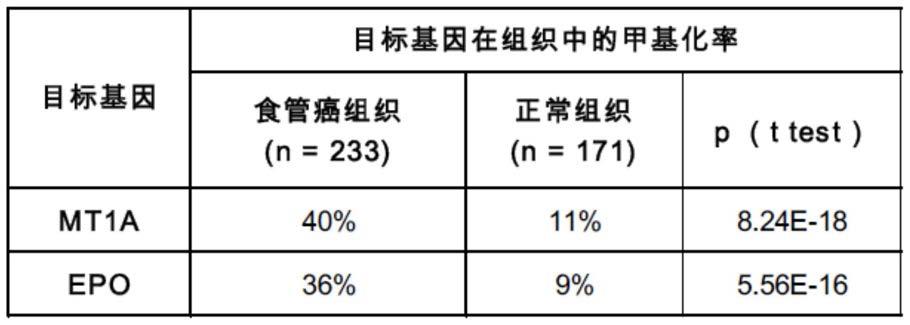
228.通过分析233例食管癌组织及171例正常食道组织的全基因组甲基化芯片(illumina公司的humanmethylation450k芯片)数据,本发明人发现mt1a基因和epo基因在食道癌组织中的甲基化水平显著高于正常食道组织(分析结果如图1所示)。进一步地,本发明人通过分析mt1a基因和epo基因在全基因组甲基化芯片上的探针序列及相应的甲基化率数据,发现了这两个目标基因在食道癌组织和正常食道组织中甲基化差异最明显的序列片段,从而确定为这两个目标基因的靶序列。
229.mt1a基因的靶序列如seq id no:1所示。
230.seq id no:1
231.cacccaggggagctcagtggactgtgcgccttgcctttctgctgcgcaaagcccagtccaggtcatcacctcgggcggggcggactcggctgggcggactcagcggggcgggcgcaggcgcagggcgggtcctttgcgtccggccctctttcccctgaccataaaagcagc
232.mt1a基因的靶序列的互补序列如seq id no:2所示。
233.seq id no:2
234.gctgcttttatggtcaggggaaagagggccggacgcaaaggacccgccctgcgcctgcgcccgccccgctgagtccgcccagccgagtccgccccgcccgaggtgatgacctggactgggctttgcgcagcagaaaggcaaggcgcacagtccactgagctcccctgggtg
235.epo基因的靶序列如seq id no:3所示。
236.seq id no:3
237.cgcgcacgcacacatgcagataacagccccgacccccggccagagccgcagagtccctgggccaccccggccgctcgctgcgctgcgccgcaccgcgctgtcctcccggagccggaccggggccaccgcgcccgctctgctccgacaccgcgccccctggacagccgccctctcctccaggcccgtggggctggccctgcaccgccgagcttcccgggatgagggcccccggtgtggtcacccggcgcgccccaggtcg
238.epo基因的靶序列的互补序列如seq id no:4所示。
239.seq id no:4
240.cgacctggggcgcgccgggtgaccacaccgggggccctcatcccgggaagctcggcggtgcagggccagccccacgggcctggaggagagggcggctgtccagggggcgcggtgtcggagcagagcgggcgcggtggccccggtccggctccgggaggacagcgcggtgcggcgcagcgcagcgagcggccggggtggcccagggactctgcggctctggccgggggtcggggctgttatctgcatgtgtgcgtgcgcg
241.实施例2
242.第一步:获得待分析的生物样品的dna。该来源可以是任何适合的来源,例如细胞系、组织学切片、活检组织、石蜡包埋的组织、体液、粪便、尿、血浆、血清、全血、分离的血细胞、从血液分离的细胞及其所有可能的组合。然后通过现有技术中的任何标准手段来分离,从所述样品分离dna。简言之,当dna被包裹在细胞膜中时,该生物样品必须被破碎并通过酶、化学或机械手段被裂解。随后例如通过蛋白激酶k的消化而清除蛋白和其它的污染物。接着从溶液回收dna。这可以通过各种方法来实现,包括盐析、有机提取或将dna结合到固相支持物。对方法的选择会受到多种因素的影响,包括时间、费用和所需的dna的量。当所述样品dna未被包裹在细胞膜中时(例如来自血液样品的循环dna),可以使用现有技术中分离和/或纯化dna的标准方法。这些方法包括使用蛋白质降解试剂,例如离液盐,如盐酸胍或脲;或去污剂,如十二烷基磺酸钠(sds)、溴化氰。其它方法包括但不限于乙醇沉淀或丙醇沉淀、通过离心的真空浓缩等。本领域技术人员也可以利用装置,例如诸如超滤的滤器,硅表面或膜,磁性颗粒,聚苯乙烯颗粒,聚苯乙烯表面,带正电荷的表面以及带阳性电荷的膜,带电膜,带电表面,带电转换膜,带电转换表面。一旦核酸被提取,就将dna用于分析。
243.在本实施方案中,生物样本dna为白细胞基因组dna和dna甲基转移酶处理后的白细胞基因组dna。白细胞基因组dna的目标基因靶序列的为非甲基化状态,因此白细胞基因组dna是目标基因靶序列甲基化状态的阴性参考品。dna甲基转移酶处理后的白细胞基因组dna的目标基因靶序列为甲基化状态,因此dna甲基转移酶处理后的白细胞基因组dna是目标基因靶序列甲基化状态的阳性参考品。
244.第二步:将上述两种dna样品分别处理,以使得在5位未甲基化的胞嘧啶碱基被转变为尿嘧啶、胸腺嘧啶或在杂交行为上不用于胞嘧啶的另一碱基。优选地,通过亚硫酸氢盐试剂处理来实现。术语“亚硫酸氢盐试剂”指包括亚硫酸氢盐、酸式亚硫酸盐或其组合的试剂,如这里所公开的可用于区分甲基化和未甲基化的cpg二核苷酸序列。优选地,该亚硫酸氢盐处理在变性溶剂存在下进行,所述变性溶剂诸如但不限于正烷基二醇,尤其是二乙二醇二甲基醚(dme),或者在二噁烷或二噁烷衍生物存在下进行。在优选的实施方案中,所述变性溶剂以1%至35%(v/v)的浓度使用。还优选该亚硫酸氢盐反应在清除剂存在下进行,例如但不限于色原烷衍生物,如6-羟基-2,5,7,8,-四甲基色原烷2-羧酸或三羟基苯甲酸及其衍生物,例如没食子酸。该亚硫酸氢盐转变优选在30℃至70℃的反应温度下进行,其中在反应期间温度短时间地增加至超过85℃。经亚硫酸氢盐处理的dna优选在定量之前进行纯化。这可通过任何现有技术中已知的方法来进行,例如但不限于超滤。
245.第三步:采用本发明的引物以及扩增酶扩增经处理的dna的片段。可在同一个反应容器中同时进行几种dna片段的扩增。优选地,所述扩增产物的长度为100至2,000个碱基对。当所要检测的生物样本的基因组dna是处于甲基化和非甲基化状态的混合物时,尤其是在处于甲基化状态的dna远远少于处于非甲基化状态的dna的情况下,如:癌症受试者外周
血中游离dna,为了提高pcr扩增引物的扩增特异性,本发明采用了在pcr反应体系中使用目标基因靶序列特异的阻断剂。阻断剂核苷酸序列的5端与正向(f)或者反向(r)引物的3’端核苷酸序列有大于或等于5个核苷酸的重叠区域;阻断剂与正向(f)或者反向(r)引物互补于目标基因靶序列dna的同一条链;阻断剂的解链温度高于正向(f)或者反向(r)引物超过(包括)5℃;阻断剂的核苷酸序列包含至少一个cpg二核苷酸序列,并与亚硫酸氢盐转化后的未发生甲基化的目标基因靶序列dna的序列互补。因此,当所要检测的生物样本的基因组dna是处于甲基化和非甲基化状态的混合物时,尤其是在处于甲基化状态的dna远远少于处于非甲基化状态的dna的情况下,处于非甲基化状态的dna经亚硫酸氢盐转化后,会优先与阻断剂相结合,从而抑制dna模板与pcr引物结合,因而不发生pcr扩增,而处于甲基化状态的dna不与阻断剂相结合,因而与引物结合,发生pcr扩增。之后,直接或间接地检测通过扩增获得的片段。优选的是标记物为荧光标记物、放射性核素或可附着的分子片段的形式。
246.根据目标基因靶序列seq id no:1-2和seq id no:3-4,在本发明中设计了用于检测mt1a和epo这两个目标基因靶序列甲基化状态的引物、探针和阻断剂序列(seq id no:5-12):
247.优选地,所述引物、探针和/或阻断剂中的一种或多种如下所示:
248.mt1a引物f
249.seq id no:5
250.cggacgtaaaggattc
251.mt1a引物r
252.seq id no:6
253.gaaacgaactcgactaaacg
254.mt1a探针
255.seq id no:7
256.tgcgtttgcgttcgtttcg
257.mt1a阻断剂
258.seq id no:8
259.caaactcaactaaacaaactcaacaaaacaaac
260.epo引物f
261.seq id no:9
262.agtcgtagagtttttgggtt
263.epo引物r
264.seq id no:10
265.caacgcgatacgacg
266.epo探针
267.seq id no:11
268.cgcaacgaacgaccga
269.epo阻断剂
270.seq id no:12
271.gagtttttgggttattttggttgtttgttg
272.在本发明中,可以利用各种商业用实时pcr仪器设备上根据现有技术的标准操作进行实时pcr的检测。根据某些具体实施方式,在lifetechnologies仪器(7500fast)上进行实时pcr的检测。pcr反应混合物由经亚硫酸氢盐转化的dna模板25-40ng和300-600nm引物和阻断剂、150-300nm探针、1utaq聚合酶、50-400μm的各个dntp、1至10mm的mgcl2和2xpcr缓冲至最终的2μl至100μl的体积。在85至99℃持续3-60分钟,以用预循环扩增样品,紧接着在50至72℃进行1至30秒的35-55个循环的退火,在45至80℃下退火及延伸5至90秒,在85至99℃下变性5至90秒。通过仅仅在甲基化的目标基因靶序列上观测扩增,用与含5-甲基胞嘧啶的目标基因靶序列的cpg岛区域的特异性的探针检测所述基因片段。并且,在某些具体实施方式中,可以以β肌动蛋白基因(actb)作为pcr的内参,通过使用与β肌动蛋白基因序列互补的引物来创建β肌动蛋白基因扩增子,并且用特定的探针检测β肌动蛋白基因扩增子。每个样品进行至少一次的实时pcr,在某些具体实施方式中,进行两次或三次实时pcr检测。
273.实验结果显示如图2所述:使用本发明提供的组合物和检测方法对白细胞基因组dna(目标基因靶序列甲基化状态的阴性参考品)的检测没有发生pcr扩增,检测结果为阴性,即:受检dna样本的目标基因靶序列没有发生甲基化;使用本发明提供的组合物和检测方法对dna甲基转移酶处理后的白细胞基因组dna(目标基因靶序列甲基化状态的阳性参考品)的检测发生pcr扩增,检测结果为阳性,即:受检dna样本的目标基因靶序列发生甲基化。由此判断,本发明提供的组合物和检测方法能够特异性地检测目标基因靶序列的甲基化状态。
274.实施例3
275.根据本技术的具体实施方式,基于一定数量的食管癌样本和正常样本的检测结果的平均ct值,确定能够有效区分食管癌和正常的目标基因的ct值,即:临界值。目标基因靶序列的至少一个cpg二核苷酸的甲基化状态是由聚合酶链式反应的循环阈值ct值确定,通过比较所测样本的ct值与预先设定的临界值,确定基于目标基因的分析结果是阴性(正常)、还是阳性(食管癌)。
276.本实施例包括以下步骤:
277.首先,得到20例食管癌患者和22例正常人的血浆样本。所有样品来源于博尔诚公司。然后提取受测样本的外周血游离dna,并对所述dna样品预处理以使得在5位未甲基化的胞嘧啶碱基被转变为尿嘧啶、胸腺嘧啶或在杂交行为上不用于胞嘧啶的另一碱基。在本实施例中,通过亚硫酸氢盐试剂处理来实现该预处理。所述dna的提取和处理可以采用现有技术中的任何标准手段来进行,具体而言,在本实施例中,所有的样品dna的提取和亚硫酸氢盐dna修饰是通过使用博尔诚公司的血浆处理试剂盒提取的。
278.然后,上述经过处理的20例食道癌患者和22例正常人的dna样本中加入上述的目标基因引物、探针和阻断剂组合,通过pcr检测目标基因靶序列的甲基化状态。其中,本实验例中采取的pcr在life technologies仪器(7500)上进行。pcr反应混合物由经亚硫酸氢盐转化的dna模板35ng、450nm引物和阻断剂、225nm探针、1utaq聚合酶、200μm的各个dntp、4.5mm的mgcl2和2xpcr缓冲至最终的50μl的体积。在94℃持续20分钟,以用预循环扩增样品,紧接着在62℃进行5秒的45个循环的退火,在55.5℃下退火及延伸35秒,在93℃下变性30秒。
279.最后,分别测得20例食道癌患者和22例正常人的dna样本对于目标基因靶序列的
实时pcr的ct值,选用特定的临界值,优选地临界值ct=37。
280.然后,针对另外得到63例食道癌受试者的血浆样本。然后提取血浆中的游离dna,并对所述基因组dna样品预处理以使得在5’位未甲基化的胞嘧啶碱基被转变为尿嘧啶、胸腺嘧啶或在杂交行为上不用于胞嘧啶的另一碱基。在本实施例中,通过亚硫酸氢盐试剂处理来实现该预处理。所述dna的提取和处理可以采用现有技术中的任何标准手段来进行,具体而言,在本实施例中,所有的样品dna的提取和亚硫酸氢盐dna修饰是通过使用博尔诚公司的血浆处理试剂盒提取的。然后,上述经过处理的63例食道癌受试者的dna样本中加入上述的mt1a和epo基因引物、探针组合和内参基因actb基因引物、探针组合,通过pcr检测mt1a和epo基因的甲基化状态。其中,本实验例中采取的pcr扩增条件为:在life technologies仪器(7500)上进行实时pcr。pcr反应混合物由经亚硫酸氢盐转化的dna模板35ng和450nm引物、225nm探针、1utaq聚合酶、200uμm的各个dntp、4.5mm的mgcl2和2xpcr缓冲液组成至最终的30uμl的体积。在94℃保持20分钟用预循环扩增样品,紧接着在62℃进行5秒的45个循环的退火,在55.5℃下退火35秒,在93℃下变性30秒。
281.同时,对这63例食道癌受试者的血浆样本进行sncg基因血清蛋白水平的检测。通过酶联免疫吸附剂测定技术(elisa)检测sncg基因的血清蛋白水平。此elisa检测技术是通过“三明治法”实现对sncg基因的血清蛋白水平的检测:首先以sncg单克隆抗体(鼠)(来源博尔诚公司)对96孔板进行包被(1μg/孔);之后加入10倍稀释的临床血清样本和系列稀释(2.5ng/ml~0.04ng/ml)的人源sncg蛋白溶液(50μl/孔);然后在每管中加入50μl的0.47μg/ml的辣根过氧化酶(horseradish peroxidase,hrp)标记的鼠抗人源sncg的多抗(igg)(来源博尔诚公司)。装有以上混合物的免疫反应板在室温、震荡条件下,孵育3小时;用洗液清洗个反应孔后,加入显色底物。通过加入2m硫酸终止显色反应后,使用读板仪(如:bio-rad 550)在450nm光谱波段对各反应孔进行检测。最后,利用系列稀释的人源sncg蛋白溶液的检测值建立标准曲线,并基于标准曲线对临床血清样本进行定量。sncg基因血清水平在食道癌和正常个体中的临界值为2.0ng/ml。
282.最后,利用罗氏公司(roche)的电化学发光免疫检测系统分别测得63例食道癌受试者样本中的常用癌症标识物的水平,包括:cea、ca199、ca125、和afp。
283.检测结果显示(图3):食道癌受试者中mt1a和epo基因甲基化检测和sncg蛋白检测食道癌的阳性率显著高于常用癌症标识物(如:cea、ca199、ca125、和afp)。同时,mt1a和epo基因dna甲基化和sncg蛋白联合检测对食道癌的检测具有突出的互补性,二者联检大大提高了食道癌的检出率。另外,mt1a和epo基因dna甲基化检测和sncg蛋白检测的互补性是独特的,常用癌症标识物(如:cea、ca199、ca125、和afp)并不具备这种特性。
284.上述实验结果表明了目标基因靶序列甲基化状态和目标蛋白浓度的联合检测能够灵敏、特异地检测食管癌。通过本发明的目标基因靶序列甲基化dna检测,可以实现体外无创检测食管癌,并能够提高食管癌的检出率。
285.综上所述,本技术利用以上所述的组合物、核酸序列、试剂盒及其用途,以及上述检测方法,通过检测目标基因靶序列甲基化状态和目标蛋白浓度,实现了利用目标基因靶序列甲基化状态和目标蛋白浓度来对食管癌进行体外检测,从而有效提高了食管癌体外检测的灵敏度和特异性。通过利用实时pcr分析血浆样本游离dna的方法和elisa方法分析血浆中目标蛋白浓度,能够方便地实现针对目标基因靶序列甲基化状态和目标蛋白浓度的联
合检测,并且能够根据实时pcr的ct值和elisa的检测浓度来快速、便捷地判断样本是否呈阳性,提供了一种无创、便捷的食管癌体外检测方法。
286.尽管在此公开了本发明的各个方面和实施例,但其他方面和实施例对于本领域技术人员而言也是显而易见的。在此公开的各个方面和实施例仅用于说明目的,而非限制目的。本发明的保护范围和主旨仅通过后附的权利要求书来确定。
