植物乳杆菌ai-66在制备降低胆固醇含量的制剂中的应用
技术领域
1.本发明属于益生菌技术领域,具体涉及植物乳杆菌ai-66在制备降低胆固醇含量的制剂中的应用。
背景技术:
2.近年来,人们逐渐从人体中分离出益生菌菌株,从益生菌的菌种定位至菌株水平,开发安全菌株的功能方向,比如干酪乳杆菌、lgg和bb12这些明星菌株,在多种疾病(肥胖、2型糖尿病、非酒精性脂肪肝和心脑血管等)中发挥了重要的作用,其中,明星菌株植物乳杆菌299v具有较明显的降胆固醇的功能,创造了巨大的经济价值。
3.高胆固醇血症是引起冠心病、高血压、动脉粥样硬化等心血管疾病的重大因素之一,已成为威胁人类健康的首要因素,患病率和死亡率呈逐年上升的趋势。目前,临床上主要是靠药物降解血清胆固醇,虽然快速有效,但具有副作用,且价格昂贵。因此,筛选出具有降胆固醇的益生菌菌株对于开发新型微生态制剂和功能性健康食品具有重要意义。
技术实现要素:
4.有鉴于此,本发明的目的在于提供植物乳杆菌ai-66在制备降低胆固醇含量的制剂中的应用,所述植物乳杆菌ai-66能够显著降低胆固醇水平,从而大大降低心血管疾病的发生风险,相关益生菌产品可应用于肥胖、高血脂的辅助治疗。
5.为了实现上述发明目的,本发明提供以下技术方案:
6.本发明提供了植物乳杆菌(lactobacillus plantarum)ai-66在制备降低胆固醇含量的制剂中的应用。
7.优选的,所述植物乳杆菌ai-66的保藏编号为cgmcc no.21741。
8.优选的,所述制剂包括食品和/或膳食补充剂。
9.优选的,所述食品包括固体饮料、益生菌粉、发酵乳制品、含乳饮料或奶酪。
10.本发明还提供了植物乳杆菌ai-66在制备瘦身减肥组合物中的应用。
11.优选的,所述组合物包括食品组合物、饲料组合物或药物组合物。
12.本发明还提供了一种以植物乳杆菌ai-66为唯一有效成分的降低胆固醇含量的制剂。
13.本发明还提供了一种以植物乳杆菌ai-66为唯一有效成分的瘦身减肥组合物。
14.有益效果:本发明提供了植物乳杆菌ai-66在制备降低胆固醇含量的制剂中的应用,所述植物乳杆菌ai-66具有良好的耐受胃肠液性能,能够通过胃液到达肠道并在肠道中定植。本发明所述植物乳杆菌ai-66可降低胆固醇:降低高胆固醇肥胖模型小鼠的体重;改善和缓解高胆固醇模型小鼠肝脏的病变程度;明显改善高胆固醇模型小鼠血清胆固醇水平。在本发明实施例中,所述植物乳杆菌ai-66经发酵培养后,具有明显优于植物乳杆菌299v的胆固醇利用率,可应用于食品、功能食品及膳食补充剂中,以降低由血清胆固醇及高胆固醇引发的高血脂、动脉粥样硬化等风险。
15.生物保藏信息
16.植物乳杆菌(lactobacillus plantarum)ai-66,于2021年01月26日保藏于中国微生物菌种保藏管理委员会普通微生物中心(cgmcc),具体保藏地址为北京市朝阳区北辰西路1号院3号中国科学院微生物研究所,保藏编号为cgmcc no.21741。
附图说明
17.图1为植物乳杆菌ai-66的革兰氏染色后菌体形态图;
18.图2为4组小鼠体重图;
19.图3为植物乳杆菌ai-66对高胆固醇模型鼠肝脏的he图(400x);
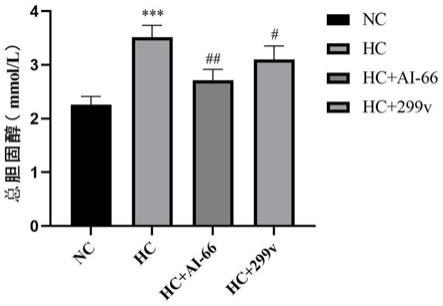
20.图4为4组老鼠血清总胆固醇含量的测定,其中:***,与nc比较,p<0.001;#,与hc比较,p<0.05;##,与hc比较,p<0.01。
具体实施方式
21.本发明提供了植物乳杆菌(lactobacillus plantarum)ai-66在制备降低胆固醇含量的制剂中的应用。
22.本发明所述植物乳杆菌ai-66的保藏编号优选为cgmcc no.21741。在本发明中,所述植物乳杆菌ai-66优选包括所述菌株的厌氧发酵液,所述厌氧发酵液的制备方法,优选包括将所述植物乳杆菌ai-66接种于mrs肉汤培养基中,于37℃厌氧发酵24h,得所述厌氧发酵液。本发明所述植物乳杆菌ai-66的接种体积优选为所述mrs肉汤培养基体积的1%。
23.本发明可直接以所述厌氧发酵液作为所述制剂,也可将所述厌氧发酵液进一步浓缩后作为液态菌制剂,也可将发酵液干燥后制备菌粉,或是从发酵液中分离出菌体制备菌粉。本发明的液态菌制剂优选还包括将菌体重悬于培养液、缓冲液或去离子水等溶剂后的液态制剂。本发明的植物乳杆菌液态菌制剂或固态菌制剂(菌粉)在保藏期具有较好的稳定性;所述的菌制剂可以用于食品、饲料或药品的生产。
24.本发明所述制剂的种类优选包括食品和/或膳食补充剂,且所述食品优选包括固体饮料、益生菌粉、发酵乳制品、含乳饮料或奶酪。
25.本发明还提供了植物乳杆菌ai-66在制备瘦身减肥组合物中的应用。
26.本发明所述组合物优选包括食品组合物、饲料组合物或药物组合物。本发明所述食品组合物、饲料组合物或药物组合物的种类或剂型优选与上述相同,在此不再赘述。
27.本发明还提供了一种以植物乳杆菌ai-66为唯一有效成分的降低胆固醇含量的制剂。
28.本发明所述植物乳杆菌ai-66具有良好的耐受胃肠液性能,能够通过胃液到达肠道并在肠道中定植,并表现出降低高胆固醇肥胖模型小鼠的体重、改善和缓解高胆固醇模型小鼠肝脏的病变程度以及明显改善高胆固醇模型小鼠血清胆固醇水平,从而体现出所述植物乳杆菌ai-66具有对心血管疾病的辅助治疗作用,可应用于制备降低胆固醇含量的制剂。本发明所述制剂优选与上述相同,在此不再赘述。
29.本发明还提供了一种以植物乳杆菌ai-66为唯一有效成分的瘦身减肥组合物。
30.本发明所述植物乳杆菌ai-66,较明星君主植物乳杆菌299v的胆固醇利用率更高,可应用于食品、功能食品及膳食补充剂中,以降低由血清胆固醇及高胆固醇引发的高血脂、
动脉粥样硬化和肥胖等的风险。
31.下面结合实施例对本发明提供的植物乳杆菌ai-66在制备降低胆固醇含量的制剂中的应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
32.本发明的各实施例中,实验数据表示为mean
±
s.e.m.数据采用prism version 5.0(graphpad,san diego,ca,usa)进行统计。组间差异采用one-way anova跟随tukery’s multiple comparison test的方法进行统计。p《0.05时具有显著的统计学差异。
33.实施例1
34.菌株的筛选与鉴定
35.采用选择性培养基(mrs琼脂培养基)从健康青年人和儿童肠道分离得到菌株,具体方法如下:用无菌竹棒挑取自然排出的粪便2~3克,置于无菌采集管中,1小时内加入50ml无菌水,振荡制成匀浆。用无菌水连续稀释10倍浓度到10-5;取不同稀释度的样品0.1ml涂布于两种选择性培养基上,37℃厌氧培养48h;取出培养皿,挑不同形态特征的单菌落,转接至液体mrs肉汤培养基,37℃厌氧培养24h后送测序公司检测鉴别菌种,将确定的菌株连续传代3次后可冷冻保藏。
36.筛选得到的植物乳杆菌ai-66的单菌落形态为白色,表面凸起,边缘规则呈圆形;菌株形态为粗短直杆,排列规则(图1)。经过16s rdna分子鉴定,发现ai-66菌株的16s rdna序列(seq id no.1)同源性最高的为植物乳杆菌属(lactobacillus plantarum),序列相似性高达100%。因此结合形态和分子鉴定,确定ai-66菌株属于植物乳杆菌(lactobacillus plantarum)。
37.吸取静置培养20~24h的菌混悬液按1%接种量接种至mrs肉汤培养基中,放置37℃培养箱静置培养20~24h,作传代操作,重复传代3次;于无菌冻存管中加入40%甘油与传代2次的益生菌菌液,体积比例为1:1。放置-20℃储存。
38.实施例2
39.菌株的安全性评价
40.将实施例1得到的-20℃冻存的甘油管植物乳杆菌菌株ai-66,接种复苏于正常mrs肉汤培养基中,进行3次转接活化培养(37℃厌氧培养24h),活化后的培养液用于抗生素敏感性实验。
41.将活化后的植物乳杆菌ai-66取0.5ml,均匀涂布于mrs琼脂平皿表面,待吹干,将庆大霉素、万古霉素、卡那霉素、克林霉素、链霉素、氨苄西林、青霉素、红霉素、氯霉素的药敏纸片贴在琼脂表面,置于37℃培养箱培养24h,观察琼脂表面菌株的生长情况。若抗生素纸片周围出现明显的透明圈,则用直尺测量透明圈的直径以判断供试菌株是否具有药敏性。同时选用金黄色葡萄球菌作为药敏实验的质控菌株。供试菌株是否具有对各种抗生素的抗性依据美国临床和实验室标准化协会(clinical and laboratory standards institute,clsi)制定的相关标准(见表1)判断。
42.表1药敏纸片含量及抗药性判断标准
[0043][0044]
表2k-b纸片扩散的实验结果
[0045][0046][0047]
注:表中“s”表示益生菌对抗生素表现出敏感s效果,“i”表示益生菌对抗生素表现出中介i效果,“r”表示益生菌对抗生素表现出耐药r效果,“/”表示益生菌无需进行此抗生素的安全性评估。
[0048]
k-b纸片扩散实验结果显示,植物乳杆菌ai-66对九种抗生素的敏感性都很高,因此具有良好的安全性。
[0049]
实施例3
[0050]
植物乳杆菌对胃酸液的耐受性实验
[0051]
将实施例1得到的-20℃冻存的甘油管菌株,接种复苏于正常mrs肉汤培养基中,进行3次转接活化培养,活化后的培养液按1%接种量接种于ph分别为1.5、2.5、3.5、4.5的mrs肉汤培养基中,放置37℃培养箱,分别在接种后的第0h、1h、2h取样作计数处理。
[0052]
结果如表3所示,植物乳杆菌ai-66可耐受ph2.5及以上的酸性环境,在ph 2.5中3h,植物乳杆菌ai-66仍可100%存活,具有较好的耐受能力。
[0053]
表3植物乳杆菌ai-66耐酸能力评估(单位:cfu/ml)
[0054][0055]
实施例4
[0056]
单菌株体外胆汁盐耐受性实验
[0057]
将实施例1得到的-20℃冻存的甘油管菌株,接种复苏于正常mrs肉汤培养基中,进行3次转接活化培养,活化后的培养液按1%接种量接种于含胆盐的mrs肉汤培养基中,放置37℃培养箱,分别在接种后的第0h、1h、2h取样作计数处理。
[0058]
结果如表4所示,植物乳杆菌ai-66可耐受0.1%及以下浓度胆汁盐,在0.1%浓度胆汁盐环境下2h,植物乳杆菌ai-66的活菌存活率保有73%,具有较好的胆汁盐耐受性。
[0059]
表4植物乳杆菌ai-62耐牛胆汁盐能力评估(单位:cfu/ml)
[0060][0061]
实施例5
[0062]
植物乳杆菌ai-66在体外对胆固醇利用率的优势
[0063]
将实施例1得到的-20℃冻存的甘油管菌株,接种复苏于正常mrs肉汤培养基中,进行3次转接活化培养,活化后的培养液按1%接种量接种于含100μg/ml胆固醇的胆盐mrs(含2.8μmol/ml甘氨胆酸钠、1.2μmol/ml牛磺胆酸钠)培养基中,37℃厌氧培养24h,离心收集上清,备用。取1ml上清于洁净试管中,每管加入1ml 30%koh、2ml无水乙醇,涡旋1min,37℃水浴15min;冷却后每管加入2ml蒸馏水、3ml正己烷,涡旋1min,室温放置15min,静置分层;小心吸取2ml正己烷层转移至洁净试管中,60℃水浴,小心通氮气流将正己烷蒸干;然后每管加入1ml无水乙醇、4ml opa试剂(每ml冰醋酸加入0.5mg opa),室温放置10min后,缓慢加入
2ml 98%浓硫酸,立即涡旋20s混匀,再室温放置10min,检测550nm处吸光度a550,以空白试验较零,对应标准曲线,结果用μg/ml表示。
[0064]
标准曲线测定方法同样品(预先配制胆固醇标准液1000μg/ml,用无水乙醇稀释至0、20、40、60、80、100μg/ml,按上述方法测定吸光度后绘制标准曲线)。结果如表5所示,植物乳杆菌ai-66对胆固醇的去除率为35.33%,较明星菌株鼠李糖乳杆菌gg和植物乳杆菌299v有优势。
[0065]
表5植物乳杆菌ai-66在体外降胆固醇中的优势
[0066][0067]
实施例6
[0068]
高胆固醇小鼠模型和益生菌干预
[0069]
将植物乳杆菌ai-66菌株于mrs肉汤培养基中37℃培养16小时后,于4℃、2500rpm下离心10min,收集菌体,磷酸盐缓冲液(pbs)洗涤后4℃以下保存。用于本发明实施例6至实施例9的实验研究。
[0070]
32只5周龄,体重17~18g的雄性c57bl/6小鼠,进行1周的适应性培养之后(动物培养环境条件:室温(25
±
1℃)光照12h黑暗12h循环。),随机分为4组,每组8只。分组如下:
[0071]
①
空白组:喂食普通饲料,灌胃生理盐水;
[0072]
②
模型组:喂食高胆固醇饲料(1.25%胆固醇,0.5%胆汁盐),灌胃生理盐水;
[0073]
③
喂食高胆固醇饲料,灌胃植物乳杆菌ai-66;
[0074]
④
喂食高胆固醇饲料,灌胃植物乳杆菌299v;
[0075]
连续灌胃8周,每天0.3ml(1
×
109cfu/ml菌株悬浮液)。
[0076]
实施例7
[0077]
植物乳杆菌ai-66显著降低高胆固醇肥胖模型小鼠的体重
[0078]
如图2小鼠体重曲线,发现喂饲高胆固醇模型组(hc)7周后体重增加到28.75g,显著高于正常饲料组的小鼠体重(24.69g)(p<0.05)。而灌胃植物乳杆菌ai-66组和植物乳杆菌299v的小鼠体重显著低于模型组(p<0.05)。且植物乳杆菌ai-66组的体重(25.82g)低于植物乳杆菌299v的小鼠体重(26.84g)(p<0.05)。
[0079]
实施例8
[0080]
植物乳杆菌ai-66显著改善高胆固醇肥胖模型小鼠肝脏的病变
[0081]
迅速取小鼠肝脏并用4%多聚甲醛固定,乙醇梯度脱水,然后常规处理石蜡包埋。取约4μm厚的石蜡切片进行hematoxylin&eosin(h&e)染色,在400倍显微镜下进行形态学观察。
[0082]
如图3小鼠肝脏he染色,可发现喂饲高胆固醇模型组(hc)7周后肝脏的细胞核边缘
化和重度脂肪空泡变性,灌胃植物乳杆菌ai-66组和植物乳杆菌299v的小鼠肝脏病理染色显示改善了脂肪空泡化变性。且植物乳杆菌ai-66组的肝脏细胞脂质沉积和脂肪空泡化程度较植物乳杆菌299v组有所改善。
[0083]
实施例9
[0084]
植物乳杆菌ai-66显著改善高胆固醇肥胖模型小鼠血清胆固醇水平
[0085]
将血液样品(3500g,4℃)离心3min,分离血清。然后血清总胆固醇水平通过市售试剂盒(南京建成生物工程研究所,中国南京)进行检测。
[0086]
如图4小鼠血清总胆固醇含量测定结果,可发现喂饲高胆固醇模型组(hc)7周后总胆固醇含量达到3.54mmol/l,显著高于正常组老鼠的血清胆固醇水平2.26mmol/l(p<0.05),灌胃植物乳杆菌ai-66组和植物乳杆菌299v的小鼠的血清胆固醇水平分别为2.71mmol/l和3.1mmol/l。较模型hc组血清胆固醇水平显著降低(p<0.05)。且灌胃植物乳杆菌ai-66组血清胆固醇水平较灌胃植物乳杆菌299v的小鼠的血清胆固醇水平低。
[0087]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
