1.本发明涉及医疗器械技术领域,尤其涉及一种用于检测骨质疏松治疗效果的装置及其制备方法。
背景技术:
2.骨质疏松症是一种进展缓慢的代谢性骨骼疾病,主要特征是骨量低下以及骨组织的微结构破坏性改变,导致骨的脆性与骨折的风险增加。随着全球人口老龄化的发展,骨质疏松症已成为全世界公共卫生问题,该疾病的脆性骨折可导致病人致残甚至死亡,病人的生活品质受到严重的影响,由于骨质疏松症的疾病进程缓慢,通常很难察觉,大多数病人都是在骨折发生后才得知患有此病,这时病情已达到较为严重的程度,同时再骨折发生率高,所以早期诊断、治疗及预防骨质疏松症与骨质疏松性骨折意义重大,如何以便捷的检查手段来达到早期诊断与治疗监测是应对骨质疏松症未来的发展方向。
3.当前双能x射线检测单位骨面积的骨密度值是骨质疏松症诊断的金标准,但由于骨结构改变缓慢,骨密度检测无法反馈骨质疏松患者短期治疗效果,因此单独采用骨密度检测来诊断骨质疏松的治疗效果是不够全面的。同时,由于射线安全的问题,骨密度不适用于大范围普查和反复检查。其他骨质疏松检测的手段还有定量ct、微量ct和超声等,这些手段虽然能检测骨密度与骨微结构,但由于其诊断阈值未定,射线辐照量相对较多,价格昂贵等原因,目前不作为常规临床诊断方法,较合适应用于科学研究。
技术实现要素:
4.有鉴于此,本发明实施例的目的是提供一种用于检测骨质疏松治疗效果的装置及其制备方法,能够安全地对骨质疏松症治疗效果进行检测、价格便宜且普适性高。
5.第一方面,本发明实施例提供了一种用于检测骨质疏松治疗效果的装置,包括中空微针阵列单元、负压盖、负压泵及吸水性物质;其中,所述中空微针阵列单元包括一体成型的中空微针阵列与底座,所述负压盖包括外槽、内槽和负压接口,所述外槽与所述底座可拆卸连接,所述吸水性物质设置于所述内槽,所述负压接口与所述负压泵连接;
6.所述中空微针阵列,用于穿透皮肤及作为骨转换标志物的传输通道;
7.所述负压盖,用于传递负压泵的负压,便于血液中的所述骨转换标志物外渗且富集于组织液中;
8.所述吸水性物质,用于存储所述骨转换标志物。
9.可选地,所述中空微针阵列的微针长度范围包括1100um~1300um。
10.可选地,所述中空微针阵列的微针孔径范围包括150~250mm。
11.可选地,所述外槽与所述底座嵌套连接。
12.可选地,所述负压接口与所述负压泵通过胶管连接。
13.可选地,所述吸水性物质包括滤纸或纱布中的任一种。
14.第二方面,本发明实施例提供了一种用于检测骨质疏松治疗效果的装置的制备方
法,包括:
15.制备中空微针阵列单元的模具;所述中空微针阵列单元包括一体成型的中空微针阵列与底座;
16.将制备中空微针阵列单元的流体材料注入所述模具,并剥离固化后的流体材料得到中空微针阵列单元;
17.制备负压盖,所述负压盖包括外槽、内槽和负压接口,所述外槽的尺寸与所述底座的尺寸匹配;
18.提供负压泵和吸水性物质;
19.将所述中空微针阵列单元、所述负压盖、所述负压泵及所述吸水性物质组装,所述吸水性物质设置于所述内槽,所述负压接口与所述负压泵连接。
20.可选地,所述模具通过以下方法制备:
21.将聚二甲基硅氧烷及固化剂以预设比例混合并充分搅拌;
22.将未固化的混合溶液置于预设真空环境放置预设时间;
23.将所述混合溶液浇铸到预设的su-8模板上干燥形成所述模具。
24.可选地,所述将制备中空微针阵列单元的流体材料注入所述模具,并剥离固化后的流体材料得到中空微针阵列单元,具体包括:
25.将聚甲基丙烯酸甲酯粉末在预设温度下加热至熔融状态;
26.将熔融状态的材料浇铸到所述模具中,并放置若干时间使熔融状态的材料固化;
27.将固化物质剥离所述模具,并通过激光在每个微针的中间段位置打一个通孔。
28.实施本发明实施例包括以下有益效果:本实施例中的装置包括中空微针阵列单元、负压盖、负压泵及吸水性物质,通过中空微针阵列单元穿透皮肤,通过负压泵使皮下形成负压状态以使骨转换标志物在组织液富集便于快速提取,骨转换标志物经过中空微针阵列通道存储在吸水性物质中用于检测,从而实现安全地对骨质疏松症治疗效果进行检测、价格便宜且普适性高。
附图说明
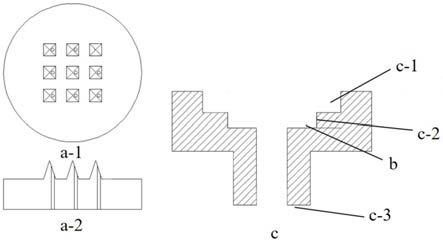
29.图1是本发明实施例提供的一种用于检测骨质疏松治疗效果的装置中的中空微针阵列单元及负压盖的结构示意图;
30.图2是本发明实施例提供的一种用于检测骨质疏松治疗效果的装置的实物图;
31.图3是本发明实施例提供的一种利用非负压法及负压法提取组织液中三种不同大小荧光模拟物和血浆中三种不同大小荧光模拟物的荧光强度的结果示意图;
32.图4是本发明实施例提供的一种利用非负压法及负压法提取组织液三种不同大小荧光模拟物与血浆中三种不同大小荧光模拟物的相关性图;
33.图5是本发明实施例提供的一种利用非负压法及负压法提取的骨转换标志物与血浆中的骨转换标志物的浓度对比图;
34.图6是本发明实施例提供的一种利用非负压法及负压法提取的骨转换标志物与血浆中的骨转换标志物的相关性图;
35.图7是本发明实施例提供的一种用于检测骨质疏松治疗效果的装置的制备方法的步骤流程示意图。
具体实施方式
36.下面结合附图和具体实施例对本发明做进一步的详细说明。对于以下实施例中的步骤编号,其仅为了便于阐述说明而设置,对步骤之间的顺序不做任何限定,实施例中的各步骤的执行顺序均可根据本领域技术人员的理解来进行适应性调整。
37.生物分子信息检测能够为解析生命活动的机制提供强而有力的方法,其检测对象可以从细胞、组织、器官到生物体等各层面,涵盖了各类的生物分子,包括dna、蛋白质、激素等大分子物质。其中,生物标志物是一种可以在生理状态和疾病发生过程中进行判断的指示物,可应用于疾病的诊断、对疾病进程的梳理与判断、评价治疗方案和新药在临床上的有效性和安全性,将生物标志物和临床医学上的检测方法进行协同运用,可以对疾病病情更准确快速地诊断和判断。骨代谢是一个旧骨吸收和新骨重塑的过程,骨转换标志物可以实时反映了这一过程。骨转换标志物分为骨形成标记物(i型前胶原氨基端前肽(pinp)、骨特异性碱性磷酸酶、骨保护蛋白等)和骨吸收标记物(i型胶原交联羧基末端肽(ctx-i)、抗酒石酸酸性磷酸酶等)。因为其在血清中的高灵敏度和特异性,pinp和ctx-i已被国际骨质疏松基金会 (iof)和国际临床化学联合会(ifcc)推荐作为监测骨代谢的参考指标。在pinp和ctx-i 的帮助下,医生可以有效地监测骨质疏松治疗的早期效果,并及时调整治疗方案,以防止未来可能发生的骨质疏松性骨折。
38.人体的皮下组织液(interstitial fluid,isf)中小分子生物标志物的含量与血液中相应的小分子生物标志物的浓度存在紧密的相关性。基于此关联性,通过检测皮下组织液中小分子生物标志物的浓度,能推断血液中相应的生物标志物浓度。大分子生物标志物通常只存在于血管中,难以穿越血管壁外渗至组织液中。另一方面,微针由于其针头的微型化设计,避免穿刺血管导致疼痛或出血,这也限制了微针直接从血液中检测大分子生物标志物的可行性。而如果增长微针针头长度以穿破皮下血管,则类似于普通金属针头,容易造成疼痛、流血、感染风险。因此大分子生物标志物仍然难以使用微针阵列技术进行提取和检测。然而,许多重要的生物标记物具有较大的分子量以及不同的化学性质,例如骨转换标志物中的pinp(分子量约35kda),它们可能会与血浆蛋白结合,并且难以穿透毛细血管壁。
39.如图1所示,本发明实施例提供了一种用于检测骨质疏松治疗效果的装置,包括中空微针阵列单元(a-1为俯视图,a-2为侧视图)、负压盖c、负压泵及吸水性物质b;其中,所述中空微针阵列单元包括一体成型的中空微针阵列与底座,所述负压盖c包括外槽c-1、内槽 c-2和负压接口c-3,所述外槽c-1与所述底座可拆卸连接,所述吸水性物质b设置于所述内槽c-2,所述负压接口c-3与所述负压泵连接;
40.所述中空微针阵列,用于穿透皮肤及作为骨转换标志物的传输通道;
41.所述负压盖c,用于传递负压泵的负压,便于血液中的所述骨转换标志物外渗且富集于组织液中;
42.所述吸水性物质b,用于存储所述骨转换标志物。
43.参阅图2,图2为用于检测骨质疏松治疗效果的装置的实物图,其中,图2-a表示中空微针阵列单元,图2-b及图2-c表示负压盖,图2-d表示中空微针阵列单元与负压盖组装后的模块,图2-e及图2-f分别表示微针在扫描电镜下的俯视图和侧视图,图2-a至图2-d的标尺2000um,图2-e至2-f的标尺200um。图2-b及图2-c中,黑色方形代表连接负压泵的负压接口,黑色圆形代表放置微针阵列的外槽,黑色三角形代表储存吸收性物质的内槽。
dextran(非负压法:r2=0.65,r=0.80,p=0.002;负压法:r2=0.73,r=0.85,p<0.001)和fitc-dextran(非负压法:r2=0.36,r=0.60,p=0.038;负压法:r2=0.64,r=0.80,p=0.002)。
60.由图3及图4可知,负压协同微针诊断装置相比非负压微针装置,能够有效促进血液中的大分子物质透过毛细血管壁进入组织液中,提高组织液中大分子物质的浓度。
61.实施例二
62.本实施例验证带负压单元的装置在检测骨质疏松松治疗效果中的应用。
63.在骨质疏松小鼠模型中分别应用非负压法和负压法进行组织液中骨转换标志物pinp和 ctx-i的连续提取监测,并将其与血浆中的pinp和ctx-i进行浓度对比及相关性分析,实现在组织液中实时监测骨质疏松的治疗效果。
64.具体实施方式:选取12周龄的c57bl/6小鼠,将小鼠模型分为对照组(非骨质疏松组) 及骨质疏松组(8只/组);两组小鼠分别进行假手术及卵巢切除术,在0周、6周、9周及12 周分别检测组织液和血浆中的pinp(分子量约35kda)和ctx-i(分子量约1000da)的相关浓度,并分析它们之间的相关性。在第6周时给予骨质疏松组静脉注射抗骨质疏松的唑来膦酸治疗,对照组给予相同剂量的生理盐水。实验结果如图5至图6所示。
65.小鼠模型中组织液(非负压法和负压法提取)和血浆中的pinp和ctx-i的浓度对比。如图5所示,在小分子ctx-i的结果中,非负压法和负压法在对照组和骨质疏松组的浓度变化趋势与血浆均相同;而在大分子pinp中,只有负压法在对照组和骨质疏松组中产生的浓度变化趋势与血浆一致。数据以平均值
±
标准差表示,n=8次重复试验。统计学显著性通过非配对t检验计算,*p《0.05,**p《0.01,***p《0.001。
66.组织液中ctx-i和pinp(非负压法和负压法提取)与血浆浓度之间的相关性。由图6 可知,a和b配对血浆和组织液之间的相关性:ctx-i(非负压法:r2=0.72,r=0.85,p《0.001;负压法:r2=0.91,r=0.95,p《0.001,皮尔森相关系数检验)和pinp(非负压法:r2=0.53, r=0.73,p《0.001;负压法:r2=0.85,r=0.92,p《0.001),n=64。
67.由图5及图6可知,虽然pinp和ctx-i可以通过非负压法在组织液中监测,但负压法显著增加了组织液中pinp和ctx-i的浓度,并提高了它们与血浆的相关性,特别是在大分子中,这表明负压协同微针诊断装置的应用可以获得更准确的监测结果。
68.如图7所示,本发明实施例提供了一种用于检测骨质疏松治疗效果的装置的制备方法,包括:
69.s100、制备中空微针阵列单元的模具;所述中空微针阵列单元包括一体成型的中空微针阵列与底座。
70.可选地,所述模具通过以下方法制备:
71.s110、将聚二甲基硅氧烷及固化剂以预设比例混合并充分搅拌;
72.s120、将未固化的混合溶液置于预设真空环境放置预设时间;
73.s130、将所述混合溶液浇铸到预设的su-8模板上干燥形成所述模具。
74.具体地,将聚二甲基硅氧烷(pdms)及固化剂以10:1的比例混合并充分搅拌;将未固化的混合溶液置于4.5pa的真空环境中30分钟以去除气泡;将pdms溶液浇铸到光刻技术定制的su-8模板上,然后在60℃下过夜干燥,形成pdms模具。
75.s200、将制备中空微针阵列单元的流体材料注入所述模具,并剥离固化后的流体
材料得到中空微针阵列单元。
76.可选地,所述将制备中空微针阵列单元的流体材料注入所述模具,并剥离固化后的流体材料得到中空微针阵列单元,具体包括:
77.s210、将聚甲基丙烯酸甲酯粉末在预设温度下加热至熔融状态;
78.s220、将熔融状态的材料浇铸到所述模具中,并放置若干时间使熔融状态的材料固化;
79.s230、将固化物质剥离所述模具,并通过激光在每个微针的中间段位置打一个通孔。
80.具体地,将聚甲基丙烯酸甲酯(pmma)粉末(分子量=75000da)在200℃下加热至熔融状态,然后将其浇铸到pdms模具中;真空放置5小时后,微针阵列在pdms模具中固化,然后从模具上剥离;激光打孔机输入800w功率和0.25秒/孔的工作时长,每个微针打一个 200mm的通孔。
81.s300、制备负压盖,所述负压盖包括外槽、内槽和负压接口,所述外槽的尺寸与所述底座的尺寸匹配。
82.具体地,负压盖是根据与中空微针阵列相匹配的尺寸设计,使用精密雕刻机在pmma板材上加工制成;其中,铣刀直径1mm,转速8000rpm,加工精度20um。
83.s400、提供负压泵和吸水性物质。
84.具体地,吸水性物质可以是普通的滤纸或纱布。
85.s500、将所述中空微针阵列单元、所述负压盖、所述负压泵及所述吸水性物质组装,所述吸水性物质设置于所述内槽,所述负压接口与所述负压泵连接。
86.具体地,首先将吸水性物质放在负压盖的内槽中,然后将中空微针阵列单元与负压盖的外槽嵌套连接,最后通过胶管将负压接口和负压泵连接。
87.实施本发明实施例包括以下有益效果:本实施例中的装置包括中空微针阵列单元、负压盖、负压泵及吸水性物质,通过中空微针阵列单元穿透皮肤,通过负压泵使皮下形成负压状态以使骨转换标志物在组织液富集便于快速提取,骨转换标志物经过中空微针阵列通道存储在吸水性物质中用于检测,从而实现安全地对骨质疏松症治疗效果进行检测、价格便宜且普适性高。另外,本实施例中用于检测骨质疏松治疗效果的装置结构紧凑、使用方便、创伤小、无痛且组织液提取效率高。
88.以上是对本发明的较佳实施进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明精神的前提下还可做作出种种的等同变形或替换,这些等同的变形或替换均包含在本技术权利要求所限定的范围内。
