1.本发明属于无机和材料化学技术领域,尤其涉及一种金属有机骨架材料及其制备方法和应用。
背景技术:
2.乙炔是石油化工领域应用最广泛的原料之一。然而,由于生产工艺的限制,乙炔通常含有二氧化碳、氢气、一氧化碳等杂质。在这些杂质中,二氧化碳与乙炔具有相似的沸点、分子尺寸/形状、动力学直径。因此从二氧化碳中选择性地分离乙炔是一项特别重要但极其困难的工业步骤。
3.传统的提纯乙炔的方法都是不环保的能源密集型产业。因此,开发绿色节能的替代方法迫在眉睫。利用晶态多孔材料的物理吸附分离被认为是一种很有前途的分离技术。
技术实现要素:
4.本发明提供一种金属有机骨架材料及其制备方法和应用,解决了现有技术中分离二氧化碳/乙炔混合物存在的高能耗、多步骤等问题。
5.为了达到上述目的,本发明的技术方案如下:
6.一种金属有机骨架材料,该材料的化学式为[zn(atz)(bdc-cl4)
0.5
]n,式中atz为脱质子的3-氨基-1,2,4-三氮唑,bdc-cl4为脱质子的四氯对苯二甲酸。
[0007]
进一步的,该多孔材料的zn
2+
离子同三个3-氨基-1,2,4-三氮唑配体的三个氮原子和一个四氯对苯二甲酸配体的一个羧基氧原子配位,形成扭曲的四面体几何构型;zn
2+
离子与配体连接形成具有直径的一维孔道的三维柱层结构,该多孔材料的空隙率为25.2%。
[0008]
上述金属有机骨架材料的制备方法,包括如下步骤:
[0009]
s1、将六水合硝酸锌、3-氨基-1,2,4-三氮唑、四氯对苯二甲酸、n,n-二甲基甲酰胺和水混合并搅拌均匀得到混合物;
[0010]
s2、将上述混合物密闭在容器中,加热到100~110℃并恒温24~48h,然后缓慢冷却到室温;
[0011]
s3、过滤容器中的反应物,得到无色块状的反应产物;
[0012]
s4、将上述反应产物用二氯甲烷交换,然后在真空以及60~80℃下活化,得到所述多孔材料。
[0013]
上述金属有机骨架材料应用于从二氧化碳和乙炔混合气体中选择性吸附分离乙炔。
[0014]
与现有技术相比,本发明的有益效果如下:
[0015]
1.本发明金属有机骨架材料用于从二氧化碳和乙炔混合气体中对乙炔的选择性吸附分离;所述材料在285k和1个大气压下,对二氧化碳和乙炔的吸附量分别为34.6cm
3 cm-3
和18.0cm
3 cm-3
。在100kpa下,对于组成比例为1:1的二氧化碳和乙炔混合物,所述金属有
机骨架材料的二氧化碳/乙炔的吸附选择性比值为2.4,表现出优良的乙炔选择性吸附分离性能,具有潜在的应用价值,可应用于乙炔净化领域。
[0016]
2.与现有技术相比,本发明的金属有机骨架材料制备工艺简单、操作简便、反应条件温和,合成的金属有机骨架材料具备很高的二氧化碳/乙炔分离选择性,可一步净化乙炔气体。
附图说明
[0017]
图1是本发明制备得到的金属有机骨架材料中的zn
2+
的配位环境图;
[0018]
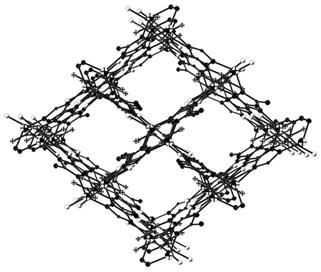
图2是本发明制备得到的金属有机骨架材料的三维骨架结构图。
[0019]
图3本发明制备得到的金属有机骨架材料在285k温度下对二氧化碳和乙炔的吸附等温线图;
[0020]
图4是通过理想吸附溶液理论计算的对于等摩尔二氧化碳/乙炔,本发明制备得到的金属有机骨架材料在285k温度下的吸附选择性图。
具体实施方式
[0021]
为了使本发明的目的、技术方案和优点更加清楚,下面将结合实施例对本发明作进一步地详细描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
[0022]
金属有机骨架材料作为一种晶态多孔材料,因其孔径可调、易于功能化而受到研究者的高度重视。大多数金属有机骨架材料因为其官能团可以与酸性更强和高极化的乙炔形成氢键和π络合作用,对乙炔吸附量更大,而具有高乙炔/二氧化碳选择性。但是这种乙炔/二氧化碳选择性分离需要解吸过程才能得到纯净的乙炔产物,而二氧化碳/乙炔选择性吸附剂只需一次吸附就可以直接生产纯净的乙炔,这意味着能耗更低,操作更简单。因此制备能够反向分离二氧化碳/乙炔混合物的金属有机骨架材料具有重要的实际意义。
[0023]
本发明的金属有机骨架材料,化学式为[zn(atz)(bdc-cl4)
0.5
]n,式中atz为脱质子的3-氨基-1,2,4-三氮唑,bdc-cl4为脱质子的四氯对苯二甲酸。
[0024]
该金属有机骨架材料的不对称单元由一个zn
2+
离子、一个3-氨基-1,2,4-三氮唑配体和半个四氯对苯二甲酸配体组成。zn
2+
同三个3-氨基-1,2,4-三氮唑配体的三个氮原子和一个四氯对苯二甲酸配体的一个羧基氧原子配位,形成扭曲的四面体几何构型。
[0025]
下面介绍采用溶剂热法制备上述金属有机骨架材料的两个实施例:
[0026]
实施例1:
[0027]
s1、将0.1mmol六水合硝酸锌、0.1mmol 3-氨基-1,2,4-三氮唑、0.1mmol四氯对苯二甲酸、2ml n,n-二甲基甲酰胺和0.5ml水混合,搅拌均匀,得到混合物。
[0028]
s2、将上述混合物密闭在10ml玻璃瓶中,加热到105℃并恒温48h,然后以0.5℃/min的速度冷却到室温,之后过滤玻璃瓶中的反应物,得到无色块状的反应产物。
[0029]
s3、将上述反应产物用二氯甲烷交换72h,然后在真空以及80℃下活化12h。
[0030]
实施例2:
[0031]
s1、将0.2mmol六水合硝酸锌、0.2mmol 3-氨基-1,2,4-三氮唑、0.2mmol四氯对苯
二甲酸、6ml n,n-二甲基甲酰胺和2ml水混合,搅拌均匀,得到混合物。
[0032]
s2、将上述混合物密闭在15ml玻璃瓶中,加热到95℃并恒温48h,然后以0.5℃/min的速度冷却到室温,之后过滤玻璃瓶中的反应物,得到无色块状的反应产物。
[0033]
s3、将上述反应产物用二氯甲烷交换72h,然后在真空以及60℃下活化24h。
[0034]
对上述制备的金属有机骨架材料的结构进行表征:
[0035]
取实施例1制备得到的无色块状晶体,在室温下通过x射线单晶衍射仪收集该无色块状晶体的x射线单晶衍射数据。
[0036]
通过对该无色块状晶体的x射线单晶衍射数据进行解析,我们得到如下结论:
[0037]
如图1所示,该金属有机骨架材料的不对称单元由一个zn
2+
离子、一个3-氨基-1,2,4-三氮唑配体和半个四氯对苯二甲酸配体组成。zn
2+
同三个3-氨基-1,2,4-三氮唑配体的三个氮原子和一个四氯对苯二甲酸配体的一个羧基氧原子配位,形成扭曲的四面体几何构型。如图2所示,zn
2+
离子与配体连接形成具有直径约的一维孔道的三维柱层结构,材料的空隙率为25.2%。
[0038]
采用相同的方法对实施例2制备得到的无色块状晶体也进行了x射线单晶衍射,通过对x射线单晶衍射数据的解析,我们得到如下结论:
[0039]
实施例2制备得到的无色块状晶体与实施例1制备得到的无色块状晶体具有完全相同的结构。
[0040]
使用美国康塔公司的autosorb-iq mp物理吸附仪测试在285k温度下实施例1制备得到的金属有机骨架材料对二氧化碳和乙炔的吸附等温线,得到的吸附等温线如图3所示。
[0041]
在760mmhg和285k下,该金属有机骨架材料对二氧化碳的吸附量为34.6cm
3 cm-3
。相反,在760mmhg和285k下,对乙炔的吸附量很低,为18.0cm
3 cm-3
。
[0042]
可见,该金属有机骨架材料对二氧化碳的吸附最大,对乙炔的吸附量很少,其对乙炔具有明显的吸附分离选择性,在吸附分离二氧化碳/乙炔方面具有潜在的应用前景。
[0043]
利用理想吸附溶液理论方法能够计算出该金属有机骨架材料对二氧化碳/乙炔的分离选择性。
[0044]
通过理想吸附溶液理论计算的实施例1制备得到的金属有机骨架材料对等摩尔二氧化碳/乙炔在285k温度下的吸附选择性如图4所示。
[0045]
由图4可知:
[0046]
在100kpa压力下,对于等摩尔的二氧化碳/乙炔混合物,该金属有机骨架材料的选择性为2.4;
[0047]
这种高选择性表明:本发明制备得到的金属有机骨架材料具有优异的从其二氧化碳中分离乙炔的性能。
[0048]
本发明制备得到的金属有机骨架材料之所以对乙炔具有优异的选择性,是由于:该金属有机骨架材料的孔道中存在电负性氯原子,使得孔道的电荷与二氧化碳的电荷更加匹配,但是却排斥乙炔,所以促进了二氧化碳的扩散,抑制了乙炔的扩散,导致了良好的二氧化碳/乙炔分离性能。
[0049]
以上为本发明的具体实施例,但本发明的结构特征并不局限于此,本发明可以用于类似的产品上,任何本领域的技术人员在本发明的领域内,所作的变化或修饰皆涵盖在本发明的专利范围之中。
