一种与乳腺癌驱动基因突变相关的抗原肽组合及其应用
1.本技术为申请号202110592054.1、申请日2021年5月28日、发明名称“一种与乳腺癌驱动基因突变相关的抗原肽及其应用”的分案申请。
技术领域
2.本发明涉及一种与乳腺癌驱动基因突变相关的抗原肽组合及其应用,属于生物医药技术领域。
背景技术:
3.乳腺癌已成为当前社会的重大公共卫生问题。乳腺癌的病因尚未完全清楚,研究发现乳腺癌的发病存在一定的规律性,具有乳腺癌高危因素的女性容易患乳腺癌。所谓高危因素是指与乳腺癌发病有关的各种危险因素。
4.乳腺癌的治疗多采用手术、放疗、化疗、内分泌治疗、生物靶向治疗及中医药辅助治疗等多种手段。外科手术在乳腺癌的诊断、分期和综合治疗中发挥着重要作用。放疗是利用放射线破坏癌细胞的生长、繁殖,达到控制和消灭癌细胞的作用。手术、放疗均属于局部治疗。化学治疗是一种应用抗癌药物抑制癌细胞分裂,破坏癌细胞的治疗方法,简称化疗。内分泌治疗是采用药物或去除内分泌腺体的方法来调节机体内分泌功能,减少内分泌激素的分泌量,从而达到治疗乳腺癌的目的。但是放化疗虽然能提高远期生存率,但并发症多,疗效不满意。
5.随着人们对肿瘤驱动基因突变和个性化精准免疫应答反应本质的认识,提出了个性化定制的肿瘤驱动基因突变相关肽抗原,作为肿瘤特异性新抗原免疫细胞治疗的新概念,通过肿瘤独特的驱动基因突变相关抗原,诱导人体的天然t细胞免疫防御系统来选择性地破坏肿瘤基因突变细胞,从而有效地阻止多种癌症的发生,这一技术领域已经在2019年被美国评为十大科技创新技术研究领域。
6.然而由于技术需要多学科,高技术,多平台的协作研究,目前乳腺癌驱动基因突变相关的抗原肽,未能被系统性地发现并建立起较为完整的肽库,因此尚未能形成效果优越的治疗剂。
技术实现要素:
7.为了克服现有技术的不足,本发明的第一个目的在于提供一种与乳腺癌驱动基因突变相关的抗原肽组合,该与乳腺癌驱动基因突变相关的抗原肽组合具有与dc细胞上mhc i分子高度的亲和力,并能有效地刺激、诱导产生特异性细胞毒性t淋巴细胞(ctls),可用于与乳腺癌相关驱动基因突变的肿瘤细胞的免疫清除,具备良好治疗潜力。
8.本发明的第二个目的在于提供一种上述与乳腺癌驱动基因突变相关的抗原肽组合的应用。
9.实现本发明的第一个目的可以通过采取如下技术方案达到:一种与乳腺癌驱动基因突变相关的抗原肽组合,抗原肽组合的序列为seq id no.10和seq id no.17。
10.实现本发明的第二个目的可以通过采取如下技术方案达到:一种与乳腺癌驱动基因突变相关的抗原肽组合的应用,将如上所述的与乳腺癌驱动基因突变相关的抗原肽组合用于诱导产生特异性细胞毒性t细胞克隆。
11.或,一种与乳腺癌驱动基因突变相关的抗原肽组合的应用,将如上所述的与乳腺癌驱动基因突变相关的抗原肽组合用于制备可诱导产生特异性细胞毒性t细胞克隆的人体免疫活性调节剂。
12.或,一种与乳腺癌驱动基因突变相关的抗原肽组合的应用,将如上所述的与乳腺癌驱动基因突变相关的抗原肽组合用于制备预防和干预palb2和kmt2c基因的突变的细胞培养液。
13.或,一种与乳腺癌驱动基因突变相关的抗原肽组合的应用,将如上所述的与乳腺癌驱动基因突变相关的抗原肽组合用于制备乳腺癌风险干预治疗剂。
14.本发明从特定种类的癌症为出发点进行了全面的研究,针对性地研究乳腺癌的发生机制,实现清除palb2和kmt2c乳腺癌驱动基因突变的乳腺癌细胞,可以抑制肿瘤细胞的增长,预防乳腺癌的发生。而免疫学研究证实,cd8阳性t淋巴细胞ctl发挥细胞免疫的原理为:ctl细胞通过识别与mhc-i分子结合的抗原肽被激活,被激活的ctl可以杀死相应的靶细胞,发挥免疫监视作用。
15.相比现有技术,本发明的有益效果在于:
16.1、本发明与乳腺癌驱动基因突变相关的抗原肽组合(neoantigen),是指肿瘤细胞表达的可激活t细胞的抗原肽;通过高通量基因测序和数据分析,发现患者的肿瘤的个体化的众多体细胞突变,筛选出与驱动基因突变相关的抗原肽组合作为靶标,经体外化学合成,负载到抗原提成细胞(apc)上,从而起到激活t细胞识别多种新抗原肽,进而产生杀伤突变的肿瘤细胞的疗效;
17.2、本发明筛选得到的与乳腺癌驱动基因突变相关的抗原肽组合,具有与d c细胞上mhc i分子高度的亲和力并能有效地刺激、诱导产生特异性细胞毒性t淋巴细胞(ctls),抑制肿瘤细胞生长,说明其具备良好的多肽疫苗及dc疫苗的潜力,具有良好的临床转化及疾病预防前景。
具体实施方式
18.下面,结合具体实施方式,对本发明做进一步描述:
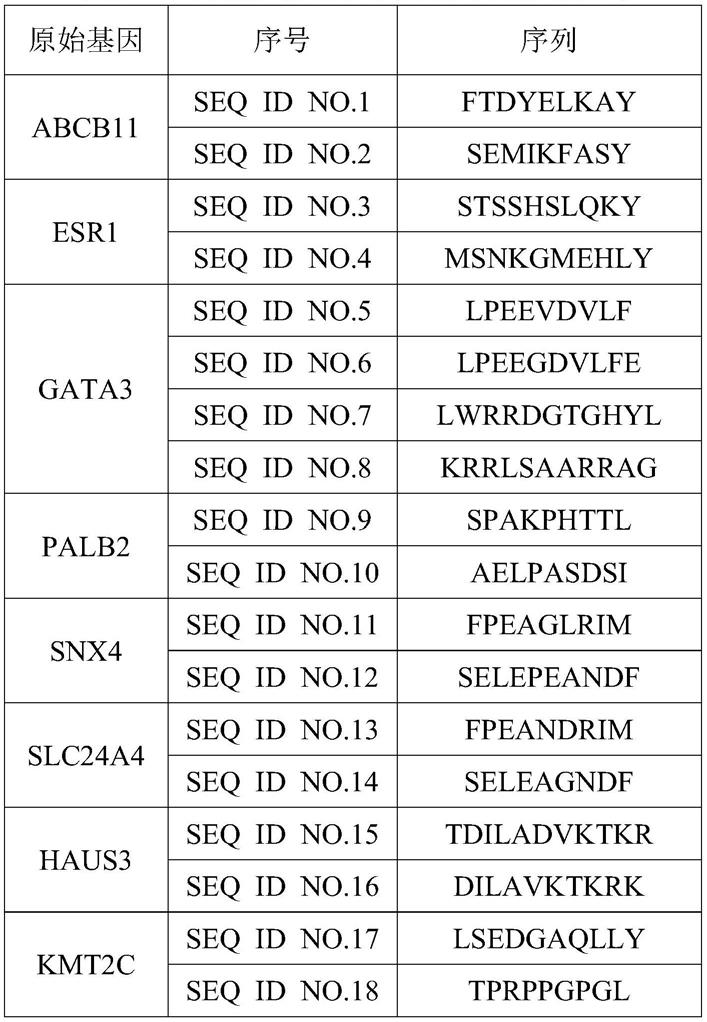
19.实施例中使用与乳腺癌驱动基因突变相关的抗原肽如表格1所示:
20.表格1与乳腺癌驱动基因突变相关的抗原肽序列
[0021][0022]
与乳腺癌驱动基因突变相关的抗原肽特异性ctl克隆建立的操作如下:
[0023]
同一健康捐献者的105个cd8
+
t细胞通过负载与乳腺癌驱动基因突变相关的抗原肽的104个mo-dcs间隔1周刺激2次后,再通过自体105个丝裂霉素c处理过的负载与乳腺癌驱动基因突变相关的抗原肽的pbmc刺激1次后,经标准细胞毒试验筛选获得。
[0024]
t2细胞加载5um与乳腺癌驱动基因突变相关的抗原肽作为靶细胞,ctl的与乳腺癌驱动基因突变相关的抗原肽特异性细胞毒性通过ldh释放试验得以证实。
[0025]
ldh乳酸脱氢酶细胞毒性检测:
[0026]
1)用含5vt%小牛血清的rpmi-1640培养液将靶细胞调整到5
×
10
4-2
×
105/ml;
[0027]
2)在96孔圆底细胞培养板中加入靶细胞,每孔加100μl。3个效应细胞自然释放对照孔不加靶细胞,只加100μl培养液;
[0028]
3)向各孔加100μl ctl效应细胞(cd8+t细胞),效应细胞与靶细胞的比例为10:1;
自然释放孔不加效应细胞只加100μl培养液,最大释放孔中加100μl 1vt%np40。每个实验置三个复孔;
[0029]
4)置37℃5vt%co2的二氧化碳培养箱中培养4-6h;
[0030]
5)离心培养板200
×
g 10min;每孔吸出150μl上清液,对应加入另一块96孔酶联检测板中;向第二块板每孔依次加20μl 0.4mol/l乳酸溶液、20μl 4mmol/l 2-p-碘苯酯-3-p-氯化硝基苯四唑,20μl反应液(含0.03vt%bsa,2.7u/ml硫辛酰胺脱氢酶,4.5mmol/l氢化型辅酶i(nad+),1.2vt%蔗糖的p bs),室温中放置20min;
[0031]
6)在酶联检测仪上测定各孔的光密度(od值),检测波长492nm,参考波长650nm。
[0032]
采用以上体外诱导建立与乳腺癌驱动基因突变相关的抗原肽特异性ctl克隆的方法,本发明还建立了mhc-i限制性ctl克隆,通过ifn-γ释放实验证实其多肽特异性免疫应答效应。
[0033]
ifn-γ释放实验:
[0034]
1)包被抗体,取44μl capture antibody和12ml coat buff以1:250倍稀释,将上述液体以每孔100μl包被96孔酶标板,4℃过夜;
[0035]
2)洗板3次,配置洗液,50ml加入蒸馏水配成1000mlwash buff,1:20倍稀释,用自动洗板机洗板3次;
[0036]
3)阻断每孔220μl assay dilution室温放置1h;
[0037]
4)洗板3次;
[0038]
5)配备标准品,等比稀释,建立浓度梯度分别为空白孔,4.7pg/ml,9.4pg/ml,18.8pg/ml,37.5pg/ml,75pg/ml,150pg/ml,300pg/ml。依次加入待测样品,副孔,浓度过高的需要稀释。室温放置2h;
[0039]
6)洗板5次;
[0040]
7)配置检测抗体(二抗)48μl detector antibody加入12ml assay dilution配为一液,加样时立时将48μl sav-hrp加入一液,每孔100μl室温放置1h;
[0041]
8)洗板7次;
[0042]
9)加入显色底物链霉素亲和素过氧化物酶,避光,30min;
[0043]
10)加入终止液,在酶标仪上用450nm为测量波长,620nm为参考波长进行比色制作标准曲线。
[0044]
结果如表格2所示,分别为seq id no.1-18的抗原肽ifn-γ释放实验数据,以pbs磷酸盐缓冲液和阴性对照肽(对照肽序列如seq id no.19所示为:aaaaaaaaa)作为对照,实验结果为吸光度值。上述实验数据表明,本发明建立的ctl表位是极其有效的,预测结果与实验结果符合性非常好。
[0045]
表格1抗原肽ifn-γ释放实验结果(吸光度值)
[0046]
序号抗原肽pbs对照阴性对照seq id no.14853236seq id no.24793237seq id no.34693038seq id no.44723139seq id no.54733440
seq id no.64753339seq id no.74783238seq id no.84853237seq id no.94833236seq id no.104693235seq id no.114683234seq id no.124673235seq id no.134653236seq id no.144713037seq id no.154723038seq id no.164793039seq id no.174753040seq id no.184763041
[0047]
以至少两种抗原肽进行组合:
[0048]
组合1:seq id no.3、seq id no.7、seq id no.13和seq id no.17;
[0049]
组合2:seq id no.10和seq id no.17;
[0050]
组合3:seq id no.4、seq id no.7、seq id no.10、seq id no.13、seq id no.15和seq id no.17;
[0051]
以上三个抗原肽组合进行ifn-γ释放实验,以pbs磷酸盐缓冲液和阴性对照肽(对照肽序列如seq id no.19所示为:aaaaaaaaa)作为对照,实验结果为吸光度值,结果如表格3所示。
[0052]
表格3抗原肽组合的ifn-γ释放实验结果(吸光度值)
[0053]
组合抗原肽pbs对照阴性对照组合1623
±
1828
±
239
±
3组合2635
±
3529
±
138
±
3组合3610
±
1432
±
139
±5[0054]
可见,通过将上述乳腺癌驱动基因突变相关的抗原肽中的至少两条经树突状细胞提呈与细胞毒性淋巴t细胞共培养,可诱导筛选得到抗原肽特异性细胞毒性t淋巴细胞。这种抗原特异性细胞毒性t淋巴细胞可用于与乳腺癌相关驱动基因突变的肿瘤细胞的免疫清除,预防相关疾病的发生,尤其是肿瘤疾病。
[0055]
将上述抗原肽的至少两条与树突状细胞(dendritic cell,dc)加载回输,可以作为dc疫苗用于疾病预防,刺激机体产生针对乳腺癌驱动基因突变相关的多肽特异性抗细胞毒性t细胞,进而实现乳腺癌驱动基因突变相关疾病的预防。
[0056]
本发明与乳腺癌驱动基因突变相关的抗原肽组合长度较短,化学合成难度小,可以直接合成得到高纯的产物,应用成本大大降低,同时效果明确,具有很好的应用潜力。
[0057]
对于本领域的技术人员来说,可根据以上描述的技术方案以及构思,做出其它各种相应的改变以及变形,而所有的这些改变以及变形都应该属于本发明权利要求的保护范围之内。
