1.本发明属于给水排水工程/环境工程领域,主要涉及一种同步去除水中微塑料和喹诺酮类抗生素的方法。
背景技术:
2.微塑料(mps)是一种新兴环境污染物,它被定义为小于5mm的塑料碎片,具有颗粒状、片状、丝状等不同形状。微塑料的来源复杂,有来自个人护理用品和工业生产过程所产生的初级微塑料,以及普通微塑料在环境中老化降解所产生的次级微塑料。微塑料对化学和生物降解具有较强的稳定性,被释放后会在环境中累积并持久存在,并且由于其微小的体积以及稳定的特性,这些废弃的聚合物颗粒会在水生或陆地生态系统中不断迁移、转化。此外,微塑料能吸附各种各样的有机污染物、重金属、病原菌、甚至抗性基因,因此,其可成为各种环境污染物的富集载体,从而对食物链顶端的人类构成潜在威胁。由于给水处理厂直接从淡水生态系统中获取原水,淡水环境中的微塑料将进入人类日常用水循环中。
3.在给水厂常规处理工艺之前,常常采用预氧化技术作为辅助方法,一般包括氯处理、臭氧氧化、高锰酸钾氧化等,其目的是提高对原水中有机物和微生物的去除率。目前大部分预氧化技术主要针对的是水体中的有机污染物,或是提升后续工艺中混凝沉淀的处理效果,尚未有针对性去除原水中微塑料的技术。如能开发合适的预氧化技术,在提高原水中有机物的去除率的同时还能去除微塑料,则能在给水厂前端有效拦截微塑料,降低其对饮用水安全的潜在风险。因此,开发一种能同步去除水中微塑料和有机污染物的预氧化技术具有重要意义。
技术实现要素:
4.针对现有技术的缺点和不足,本发明的目的在于提供一种同步去除水中微塑料和喹诺酮类抗生素的方法。本发明采用高铁酸盐预氧化的方法,经过特定的条件调控,使得高铁酸盐预氧化过程中产生新生态铁氧化物(fe
xox
),以其为媒介提高预氧化过程水中微塑料的去除率;高铁酸盐的强氧化性还可以降解去除水中的喹诺酮类抗生素,且微塑料颗粒表面生成的新生态铁氧化合物具有较大的比表面积,对水体中的喹诺酮类抗生素具有吸附作用,可以作为吸附剂协同提高喹诺酮类抗生素的去除率,达到同步去除水中微塑料和喹诺酮类抗生素的效果。
5.本发明目的通过以下技术方案实现:
6.一种同步去除水中微塑料和喹诺酮类抗生素的方法,包括以下步骤:
7.(1)向含有微塑料和喹诺酮类抗生素的水体中投加高铁酸盐后进行振荡反应;
8.(2)将步骤(1)振荡反应后的混合液静置,即可同步去除微塑料和喹诺酮类抗生素。
9.优选的,步骤(1)所述水体的ph为3~11。
10.更优选的,步骤(1)所述水体的ph=6。
11.优选的,步骤(1)所述微塑料为尺寸在1~500μm的聚苯乙烯(ps)、聚对苯二甲酸乙二醇酯(pet)或聚氯乙烯(pvc)中的一种或两种以上。
12.优选的,步骤(1)所述水体中微塑料的浓度为5~250mg/l,喹诺酮类抗生素的浓度为0.5~10mg/l。
13.优选的,步骤(1)所述喹诺酮类抗生素为环丙沙星(cpfx)。
14.优选的,步骤(1)所述高铁酸盐为k2feo4或na2feo4中的一种或两者的组合。
15.优选的,步骤(1)中高铁酸盐的投加量为5~40mg/l。
16.更优选的,步骤(1)中高铁酸盐的投加量为5mg/l。
17.优选的,步骤(1)所述振荡反应的转速为300~500rpm,时间为0.5~2h。
18.更优选的,步骤(1)所述振荡反应的时间为2h。
19.优选的,步骤(2)所述静置具体为静置30min以上,至微塑料自由沉降到稳定状态。
20.与现有技术相比,本发明具有以下优点:
21.(1)本发明采用高铁酸盐预氧化技术可以提升微塑料的下沉率,并且通过条件控制,获得最佳的反应条件,从而实现水中微塑料的快速沉降去除。
22.(2)本发明基于高铁酸盐预氧化技术,进行条件控制,提高体系中新生态铁氧化物的生成效率,从而提高其对体系中喹诺酮类抗生素的吸附效果,实现水中微塑料和喹诺酮类抗生素同步高效去除。
23.(3)本发明技术经济成本较低,高铁酸盐在水体中反应迅速,且无残留毒性,不会对水体造成二次污染或引起其他潜在的环境风险,能有效的提高原水处理,甚至是污水处理过程中,对微塑料和喹诺酮类抗生素的去除效率,适用范围广。
附图说明
24.图1为模拟实验1中未经处理的100μm pvc微塑料原样的sem图。
25.图2为模拟实验1中ph=3时100μm的pvc微塑料经k2feo4氧化后的sem图。
26.图3为模拟实验1中ph=6时100μm的pvc微塑料经k2feo4氧化后的sem图。
27.图4为模拟实验1中ph=8时100μm的pvc微塑料经k2feo4氧化后的sem图。
28.图5为模拟实验1中ph=11时100μm的pvc微塑料经k2feo4氧化后的sem图。
29.图6为模拟实验1中100μm的pvc微塑料在不同ph下经k2feo4氧化后的xps图(o1s)。
30.图7为模拟实验1中100μm的pvc微塑料在不同ph下经k2feo4氧化后的xps图(fe2p)。
31.图8为模拟实验1中6.5μm的微塑料在不同k2feo4浓度下的下沉率。
32.图9为模拟实验1中6.5μm的微塑料在不同ph下经k2feo4氧化后的下沉率。
33.图10为模拟实验2中cpfx的去除率。
34.图11为cpfx浓度标准曲线。
35.图12为实施例1中pet、pvc微塑料在不同ph条件下的下沉率。
36.图13为实施例1中cpfx在不同ph条件下的去除率。
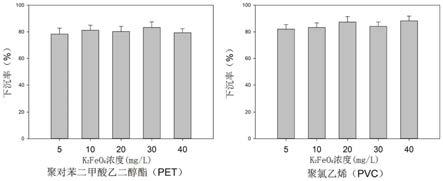
37.图14为实施例2中pet、pvc微塑料在不同k2feo4浓度下的下沉率。
38.图15为实施例2中cpfx在不同k2feo4浓度下的去除率。
39.图16为对比例1中k2feo4单独去除cpfx的效果。
具体实施方式
40.下面结合实施例对本发明作进一步详细的描述,但本发明的实施方式不限于此。模拟实验和实施例、对比例均在室温下进行,所使用的k2feo4纯度为99%(cas#:39469-86-8)。对于未特别注明的工艺参数,可参照常规技术进行。
41.本发明首先以模拟水体进行实验探究同步去除水中微塑料和喹诺酮类抗生素的最佳反应条件。
42.模拟实验和实施例中的过滤装置由10ml针筒和亲水ptfe针式滤器(0.45μm)组成,具体过滤步骤为:
43.(1)过滤前称量每组过滤装置的质量m1;
44.(2)反应装置静置30min后,使用5ml移液枪将漂浮于液体表面的微塑料颗粒转移至10ml针筒内,通过亲水ptfe针式滤器(0.45μm)将溶液与微塑料颗粒分离,并使用9.8%的硫酸溶液润洗过滤装置,去除会影响微塑料整体质量的fe2o3颗粒;
45.(3)使用超纯水(电阻率18.2mω,溶解性有机碳doc《5μg/l)冲洗三次过滤装置(目的是去除残留的k2feo4以及h2so4溶液),每次使用超纯水的量为10ml;再使用10ml无水乙醇(99%)润洗一次,缩短烘干时间;将留有微塑料颗粒的过滤装置放入50℃的烘箱中,烘干后称量其整体质量m2。
46.模拟实验和实施例中微塑料下沉率的计算方式为:过滤装置中所含有的微塑料的质量m
上浮
=m
2-m1,每组反应装置中的微塑料的下沉率为下沉质量与投入微塑料的总质量m
总
之比:
[0047][0048]
模拟实验和实施例、对比例中cpfx的浓度通过分光光度法测得,使用紫外分光光度计对取样的溶液在276nm波长条件下进行检测,并通过cpfx浓度标准曲线(图11),将测得的吸光度换算为溶液中cpfx的浓度。
[0049]
模拟实验中ph=3、6、8、11的溶液由42.5wt%的h3po4溶液、0.2mol/l的na2hpo4溶液、0.2mol/l的nah2po4溶液、0.2mol/l的naoh溶液与超纯水按不同比例混合配制而成。
[0050]
实施例和对比例中将从附近存在医药废水排放口的河涌中获取的水样作为待处理水体,使用真空抽滤装置(0.45μm)分离水体中的固体与溶液,从多个样本中分别测算固体中微塑料颗粒的种类、浓度以及溶液中cpfx的平均浓度。水样检测出pet与pvc微塑料颗粒的存在,浓度分别为11.32mg/l和14.43mg/l,水样中的原始cpfx浓度约为562μg/l。
[0051]
实施例和对比例中水体的ph用42.5wt%的h3po4溶液、0.2mol/l的na2hpo4溶液、0.2mol/l的nah2po4溶液、0.2mol/l的naoh溶液调节为3、6、8、11。
[0052]
模拟实验1:不同反应条件对微塑料沉降效果的影响
[0053]
本实验以6.5μm、100μm、500μm的ps、pet、pvc微塑料为实验对象,在ph为3,6,8,11的溶液中以5mg/l、10mg/l、20mg/l、30mg/l、40mg/l的k2feo4固体颗粒投加浓度探究高铁酸盐预氧化去除微塑料的最佳反应条件。
[0054]
实验步骤为:
[0055]
(1)在装有200ml溶液的烧杯中加入50mg的微塑料进行振荡形成混合液,同时设置一个装有200ml超纯水的烧杯作为对照组;
[0056]
(2)向步骤(1)的烧杯中投加k2feo4固体颗粒,以500rpm的转速继续振荡反应0.5h后,将反应装置静置0.5h,使微塑料颗粒自由沉降至稳定状态,过滤后计算得到微塑料的下沉率。
[0057]
本实验的结果如图1~9和表1~3所示:
[0058]
由图1、2、3、4、5可见,相比于微塑料原样,经过k2feo4预氧化处理的微塑料颗粒表面附着了大量的细微颗粒,这些颗粒为氧化过程中产生的新生态铁氧化物混合体。不同ph条件下,微塑料表面铁氧化物的附着程度有所不同。其中,ph=3时,微塑料表面附着的铁氧化物较少,随着溶液ph向中性及碱性方向移动,溶液中的k2feo4的反应机理发生变化,生成的铁氧化物增多,当ph=6时,微塑料表面覆盖的新生态铁氧化物最多。
[0059]
由图6、7可见,微塑料经k2feo4氧化后表面的fe2p和o1s谱强度均较高,表明其表面有铁氧化合物存在,可能为fe2o3,feooh等。
[0060]
由表1可见,经k2feo4氧化后pvc微塑料的下沉率均有所提升,其中最小粒径(6.5μm)的pvc颗粒,其下沉率从56.3%提升到96.4%,接近100%。
[0061]
由表2可见,pvc的原始密度为1.42g/cm3,大于水的密度,在不同ph条件经k2feo4预氧化处理之后,pvc微塑料的密度均有所增加,特别在ph=6条件下,其密度增加程度最显著。例如,6.5μm的pvc密度从1.42g/cm3增加到1.69g/cm3,而密度的增加程度和下沉率的提升程度成正比。
[0062]
由表3可见,经k2feo4氧化后的pvc微塑料的接触角显著降低,在ph=6时从94.1
°
降低至35.9
°
,说明pvc微塑料表面从疏水性往亲水性转变,这将有利于水的浸润,从而提高其下沉率。
[0063]
由图8可见,微塑料下沉率受到k2feo4浓度变化的影响较为微弱,当k2feo4投加浓度为5mg/l时,pet和pvc微塑料的下沉率均提升至80%以上,ps的下沉率达到60%以上,随后进入平台期,并没有随k2feo4浓度的增大而提高,这说明投加5mg/l的k2feo4投加浓度即可达到良好的沉降效果。
[0064]
由图9可见,与对照组相比微塑料下沉率在不同ph条件下均有明显提升,当ph=6时,下沉率明显高于其他ph条件,这与表2、表3中微塑料颗粒的微观表征结果相符,即在溶液ph=6的氧化条件下,微塑料表面的新生态铁氧化物较多,表面亲水性较强,对微塑料颗粒的密度改变较为明显。
[0065]
表1模拟实验1中的pvc经k2feo4氧化后的下沉率变化
[0066][0067]
表2模拟实验1中的pvc经k2feo4氧化后的密度变化(g/cm3)
[0068][0069]
表3模拟实验1中500μm的pvc经k2feo4氧化后的表面接触角变化
[0070][0071]
模拟实验2:k2feo4对微塑料和cpfx的同步去除
[0072]
本实验以6.5μm的pvc微塑料和cpfx为实验对象,探究k2feo4对微塑料颗粒和cpfx的同步去除效果。
[0073]
实验步骤为:
[0074]
(1)将50mg 6.5μm的pvc微塑料和2mg cpfx加入到200ml ph=3、6、8、11的溶液中进行振荡形成混合液;(同时设置一个装有200ml超纯水的烧杯作为对照组)
[0075]
(2)向步骤(1)的四个烧杯中分别投入1mg k2feo4固体颗粒以500rpm的转速继续振荡反应2h,并分别在0.5h、1h、1.5h、2h取样检测cpfx的去除率;关闭振荡器将反应装置静置0.5h,使微塑料颗粒自由沉降至稳定状态,过滤后计算得到微塑料的下沉率。
[0076]
本实验的结果如图10和表4所示:
[0077]
由图10可见,当ph=3,6,8时均能实现cpfx的有效去除,经过2h的反应后其去除率最高接近100%,这归因于k2feo4的氧化反应,以及所生成的新生态铁氧化物的吸附作用,两者共同作用对cpfx产生显著的去除效应。
[0078]
由表4可见,6.5μm的pvc微塑料的下沉率较对照组有显著提升。结合图10和表4可以看出,以本发明提出的反应条件进行k2feo4氧化,能够实现对水中微塑料和喹诺酮类抗生素的同步去除。
[0079]
表4模拟实验2中的pvc经k2feo4氧化后的下沉率变化
[0080][0081]
实施例1
[0082]
(1)向4个装有200ml ph=3、6、8、11的待处理水体的烧杯中分别投入1mg(即投加浓度为5mg/l)k2feo4固体颗粒以500rpm的转速振荡反应2h,并分别在0.5h、1h、1.5h、2h取样检测cpfx的去除率;
[0083]
(2)关闭振荡器将反应装置静置0.5h,使微塑料颗粒自由沉降至稳定状态,过滤后计算微塑料的下沉率。每组实验设置三个平行样,结果取平均值。
[0084]
本实施例的结果如图12、13所示:
[0085]
由图12可见,当ph=6时,微塑料下沉率明显高于其他ph条件,根据模拟实验中的实验结果,这是由于微塑料表面的新生态铁氧化物较多,表面亲水性较强,对颗粒的密度改变较为明显。
[0086]
由图13可见,在实际水体中,当ph=3,6,8时均能实现cpfx的有效去除,经过2h的反应后其去除率超过90%,这与模拟实验中的实验结果相符:k2feo4的氧化反应以及所生成的新生态铁氧化物共同对cpfx产生显著的去除效应。
[0087]
实施例2
[0088]
(1)向5个装有200ml ph=6待处理水体的烧杯中分别投加1mg、2mg、4mg、6mg、8mg(分别对应投加浓度5mg/l、10mg/l、20mg/l、30mg/l、40mg/l)k2feo4固体颗粒以500rpm的转速振荡反应2h,并分别在0.5h、1h、1.5h、2h取样检测cpfx的去除率;
[0089]
(2)关闭振荡器将反应装置静置0.5h,使微塑料颗粒自由沉降至稳定状态,过滤后
计算微塑料的下沉率。每组实验设置三个平行样,结果取平均值。
[0090]
本实施例的结果如图14、15所示:
[0091]
由图14可见,当k2feo4投加浓度为5mg/l时,pet和pvc微塑料在实际水体中的下沉率均提升至75%以上,且并未随k2feo4浓度的增大而提高,这说明5mg/l的k2feo4投加浓度即可达到良好的沉降效果。
[0092]
由图15可见,k2feo4投加浓度为5mg/l时,在反应2h后cpfx的去除率超过90%,说明5mg/l的k2feo4投加浓度即可达到良好的去除效果。
[0093]
对比例1
[0094]
本对比例将待处理水体经真空抽滤分离除得到的溶液(即去除了微塑料仅保留cpfx的滤液)作为实验对象。
[0095]
向200ml ph=6的滤液中投加1mg k2feo4(即投加浓度为5mg/l)固体颗粒以500rpm的转速振荡反应2h,并分别在0.5h、1h、1.5h、2h取样检测cpfx的去除率。
[0096]
本对比例的结果如图16所示:
[0097]
由图16可见,在ph=6、k2feo4投加浓度为5mg/l的条件下,经过2h的反应后,cpfx的去除率不到70%,远低于微塑料和cpfx的同步去除实验中的cpfx去除效率。因此,本发明提出的反应条件能够实现对实际水体中微塑料和喹诺酮类抗生素的同步去除,且k2feo4的氧化反应以及所生成的新生态铁氧化物对cpfx的去除具有协同作用。
[0098]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
