1.本发明涉及涂覆有西洛他唑的支架及其制造方法,更详细而言,涉及具有含有西洛他唑的两个以上层的支架及其制造方法。
背景技术:
2.近年来,心肌梗死、心绞痛、脑卒中、外周血管疾病等动脉硬化性疾病在增加。作为针对动脉硬化性疾病的可靠的治疗法,广泛使用例如心脏的冠状动脉的经皮冠状动脉成形术等以外科方式使血管的狭窄部或闭塞部扩大的经皮血管成形术(percutaneous transluminal angioplasty;以下简称为“pta”)。pta中,特别是对冠状动脉的狭窄部或闭塞部进行的治疗法被称为经皮冠状动脉成形术(percutaneous transluminal coronary angioplasty;以下简称为“ptca”)。
3.ptca为如下手术:将在前端带有球囊(ballon)的细管(球囊导管)或支架从胳膊或大腿部的动脉插入,从心脏冠状动脉的狭窄部通过后,使前端的球囊膨胀而使狭窄的血管扩展,由此使血流恢复。由此,病变部的血管内腔扩张,由此使从血管内腔通过的血流增加。该ptca除了用于动脉硬化性疾病以外还用于血液透析患者的在胳膊形成的分流血管的狭窄治疗等。
4.一般而言,进行了ptca的血管部位会受到内皮细胞的剥离或弹性板损伤等伤害,引起作为血管壁的治愈反应的血管内膜的增殖,因此,通过ptca成功地扩大狭窄病变部的病例中的约30%~约40%发生再狭窄。
5.人的再狭窄的成因认为主要是在ptca的1~3天后产生的单核细胞的粘附和/或浸润中观察到的炎症过程以及在约45天后增殖性达到最高峰的平滑肌细胞所引起的内膜肥厚形成过程。在发生了再狭窄的情况下,需要再次进行ptca,因此,当务之急是建立其预防法和治疗法。
6.因此,积极地进行如下尝试:通过使用在支架等的表面负载有抗癌剂、免疫抑制剂、抗炎剂或平滑肌细胞的增殖抑制剂的药剂溶出型的管腔内留置用医疗器械(支架),在管腔内的留置部位使药剂以数天程度局部性地释放,从而实现再狭窄率的降低化。
7.作为涂布于药剂溶出型支架的药剂,通常是可作为抗癌剂和免疫抑制剂发挥作用的莫司系的药剂。这些药剂利用其强的细胞毒性而具有强力地抑制作为再狭窄的主要原因的血管平滑肌细胞的增殖、所谓内膜肥厚的效果。但是,由于还强力地抑制血管内皮细胞的再生,存在可能诱发迟发性支架内血栓症这样的临床上的重要课题。
8.也尝试了使用莫司系以外的药剂、例如虽然预料难溶于水而难以制备、但无细胞毒性的西洛他唑。例如,专利文献1提出了通过涂覆在由金属或高分子材料构成的支架主体的表面而含有具有40000~600000的分子量的含有生物吸收性聚合物和西洛他唑的混合物的药剂溶出型支架(参考权利要求书和[0015]等)。此外,专利文献1公开了:该支架在支架留置后的炎症过程、内膜肥厚形成过程中发生再狭窄的时期使药物溶出,作用于血管内细胞,具有有效的内膜肥厚抑制作用,能够大幅改善以高概率发生的支架留置后的再狭窄(参
考[0028])。
[0009]
现有技术文献
[0010]
专利文献
[0011]
专利文献1:wo2016/067994
技术实现要素:
[0012]
发明所要解决的问题
[0013]
专利文献1中公开的支架被用于心脏冠状动脉等较粗的动脉等,要求作用于在ptca后的1~3天后产生的单核细胞的粘附、浸润中观察到的炎症过程。因此,专利文献1中记载的支架要求从设置起至数天间释放西洛他唑而发挥效果。
[0014]
另一方面,近年来,粗度更细的外周动脉的梗塞等所引起的外周动脉疾病(pad)受到关注。例如,有如下疾病:在脚部的血管发生动脉硬化,血管变细或者堵塞,在脚部不能流通足够的血液。由此,在步行时出现脚部发麻、痛、冷等症状。随着疾病发展,变得不能行走(间歇性跛行)、或者即使一动不动脚部也会疼痛。如果进一步恶化,有时还会在脚部产生溃疡或者坏死,严重时有时还必须对脚部进行手术。
15.pad即使仅显示出手脚的症状,动脉硬化也可能不局限于手脚而波及身体内的血管。如果放任pad,则也有可能引起心肌梗死、心绞痛和脑梗死等。对于pad,根据病状的发展和治疗目标而有药物疗法、物理疗法和手术等各种治疗法。如果能够实现外周动脉用的药物留置型支架,则能够提供以低侵袭治疗pad的新治疗方法。
[0016]
本发明人进行了各种研究,结果,认为需要与心脏冠状动脉用药物留置型支架(例如专利文献1)相比能够更长期间(例如6~12个月)地在病态血管动脉存在有效成分的支架。
[0017]
本发明的目的在于提供能够更长期间(例如6~12个月)地在病态血管存在有效成分的药物留置型支架。这样的药物留置型支架能够适合用于外周血管(例如外周动脉血管)的治疗,能够提供更低侵袭的治疗方法。
[0018]
用于解决问题的方法
[0019]
本发明人反复进行深入研究的结果发现,可以得到如下药物留置型支架:其具有在支架骨架上堆积两个以上层而成的堆积层,堆积层的各层含有结晶性的西洛他唑,上述两个以上层中的至少一层含有生物吸收性聚合物,在体外进行溶出率试验24小时后上述结晶性的西洛他唑溶出5质量%以下。进而发现,这样的药物留置型支架适合用于外周血管,从而完成了本发明。
[0020]
本说明书包括下述的方式。
[0021]
1.一种支架,其具有支架骨架和在支架骨架上堆积两个以上层而成的堆积层,堆积层的各层含有结晶性的西洛他唑(clz),上述两个以上层中的至少一层含有生物吸收性聚合物,其中,
[0022]
在体外使支架与37℃的含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起24小时后,上述结晶性的西洛他唑溶出5质量%以下。
[0023]
2.一种支架,其具有支架骨架和在支架骨架上堆积两个以上层而成的堆积层,堆积层的各层含有结晶性的西洛他唑(clz),上述两个以上层中的至少一层含有生物吸收性
聚合物,其中,
[0024]
在体外使支架在37℃下与含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起15天后,上述结晶性的西洛他唑溶出20质量%以下。
[0025]
3.如上述1或2所述的支架,其中,堆积层具有至少两层,靠近支架的第一层的西洛他唑含量比远离支架的第二层的西洛他唑含量大。
[0026]
4.如上述1~3中任一项所述的支架,其中,堆积层具有至少两层,靠近支架的第一层的西洛他唑含量比远离支架的第二层的西洛他唑含量大,两层均含有生物吸收性聚合物。
[0027]
5.如上述1~4中任一项所述的支架,其中,生物吸收性聚合物含有90质量%以上的聚乳酸。
[0028]
6.如上述1~5中任一项所述的支架,其中,生物吸收性聚合物以6:4~8:2的质量比率含有l丙交酯和dl丙交酯,并且具有1.8~4.5dl/g的粘度。
[0029]
7.如上述1~5中任一项所述的支架,其中,生物吸收性聚合物含有90质量%以上的l丙交酯,并且具有0.6~1.4dl/g的粘度。
[0030]
8.如上述1~7中任一项所述的支架,其用于外周血管。
[0031]
9.一种支架,其包括支架骨架、堆积在支架骨架上的第一层和堆积在第一层上的第二层,
[0032]
第一层和第二层各自含有西洛他唑和生物吸收性聚合物,
[0033]
上述生物吸收性聚合物以6:4~8:2的质量比率含有l丙交酯和dl丙交酯,并且具有1.8~4.5dl/g的粘度,
[0034]
第一层含有西洛他唑470
±
47μg和上述生物吸收性聚合物313
±
31μg,第二层含有西洛他唑30
±
3μg和上述生物吸收性聚合物270
±
27μg。
[0035]
发明效果
[0036]
本发明的实施方式的药物留置型支架能够使结晶性的西洛他唑在体外进行溶出率试验24小时后溶出5质量%以下。因此,本发明的实施方式的药物留置型支架能够在更长期间释放结晶性西洛他唑,能够更适合地用于外周血管。
附图说明
[0037]
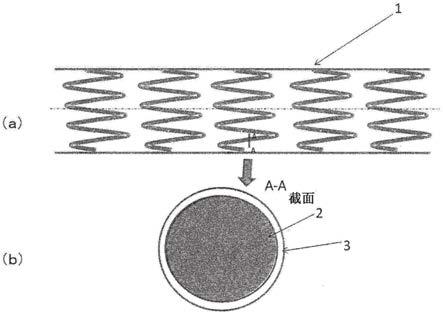
图1示意性地示出本发明的一个实施方式的支架的整个形状(a)和支架的a-a间的截面(b)。
[0038]
图2示意性地示出使用超声波喷雾器将涂覆剂涂覆在支架上的情形。
具体实施方式
[0039]
本发明的一个实施方式的支架具有支架骨架和在支架骨架上堆积两个以上层而成的堆积层,堆积层的各层含有结晶性的西洛他唑,上述两个以上层中的至少一层含有生物吸收性聚合物,在体外使支架与37℃的含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起24小时后,上述结晶性的西洛他唑溶出5质量%以下。
[0040]
本发明的另一个实施方式的支架具有支架骨架和在支架骨架上堆积两个以上层而成的堆积层,堆积层的各层含有结晶性的西洛他唑,上述两个以上层中的至少一层含有
生物吸收性聚合物,其中,在体外使支架在37℃下与含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起15天后,上述结晶性的西洛他唑溶出20质量%以下。
[0041]
本发明的又一实施方式的支架具有支架骨架、堆积在支架骨架上的第一层和堆积在第一层上的第二层,第一层和第二层各自含有西洛他唑和生物吸收性聚合物,上述生物吸收性聚合物以6:4~8:2的质量比率含有l丙交酯和dl丙交酯,并且具有1.8~4.5dl/g的粘度,第一层含有西洛他唑470
±
47μg和上述生物吸收性聚合物313
±
31μg,第二层含有西洛他唑30
±
3μg和上述生物吸收性聚合物270
±
27μg。
[0042]
本发明的实施方式的支架具有支架骨架和在该支架骨架上堆积两个以上层而成的堆积层。
[0043]
本发明的实施方式中,“支架骨架”是指形成支架的骨架,通常,使用例如金属或高分子材料而成形为网眼粗的圆筒状,只要可以得到作为本发明目标的支架,则没有特别限制。
[0044]
作为金属制支架骨架,可以例示例如镍、钴、铬、钛和不锈钢等适当的合金制支架骨架,优选为以钴铬合金作为主成分的金属制支架骨架。
[0045]
本发明的实施方式的支架具有在其支架骨架上堆积两个以上层而成的堆积层。该堆积层的各层含有结晶性的西洛他唑,上述两个以上层中的至少一层含有生物吸收性聚合物。
[0046]
本说明书中,“西洛他唑”的化学名为6-[4-(1-环己基-1h-四唑-5-基)丁氧基]-3,4-二氢喹诺酮。已知西洛他唑具有血小板凝集抑制作用、磷酸二酯酶(pde)的抑制作用、抗溃疡作用、降压作用和消炎作用,作为抗血栓剂、脑循环改善剂、消炎剂、抗溃疡剂、降压剂、抗哮喘剂、磷酸二酯酶抑制剂等有用,只要可以得到作为本发明目标的支架则没有特别限制。需要说明的是,西洛他唑也包括其药学上可接受的盐。
[0047]
另外,西洛他唑优选为晶体。与不具有晶体结构的(非晶形)西洛他唑相比,具有晶体结构的西洛他唑更能够将溶出率抑制得较低,因此优选。
[0048]
本发明的实施方式中,生物吸收性聚合物只要可以得到作为本发明目标的支架则没有特别限制。作为生物吸收性聚合物,可以列举例如包含丙交酯的聚乳酸等,其分子量(mw:重均分子量)可以为40000~700000。另外,其粘度可以为0.4~5.0dl/g,也可以为0.4~4.2dl/g。此外,生物吸收性聚合物含有dl丙交酯、l丙交酯等,可以含有乙交酯、己内酯等。更具体而言,可以例示分子量为10000~1000000的含有dl丙交酯的聚合物、以6:4~8:2的质量比率含有l丙交酯和dl丙交酯、分子量为300000~650000或粘度为1.8~4.5dl/g的聚合物、分子量为50000~150000或含有90质量%以上的l丙交酯、粘度为0.6~1.4dl/g的聚合物(包括l丙交酯100质量%的聚l乳酸)。作为生物吸收性聚合物,可以使用市售品,可以例示例如lr704s(商品名)、l206s(商品名)、lr706s(商品名)等。生物吸收性聚合物可以单独使用或者组合使用。
[0049]
生物吸收性聚合物优选含有90质量%以上的聚乳酸,更优选含有93质量%以上,进一步优选含有96质量%。在生物吸收性聚合物含有90质量%以上的聚乳酸的情况下,可以发挥能够进行缓释这样的有利效果。
[0050]
优选堆积层具有至少两层,靠近支架骨架的第一层的西洛他唑含量比远离支架骨架的第二层的西洛他唑含量大。更靠近支架骨架的层的西洛他唑的含量更大的情况下,可
以发挥能够长期进行缓释这样的有利效果。
[0051]
第一层的西洛他唑的含量优选为300~750μg,更优选为350~550μg,进一步优选为440~480μg。进而,第一层优选含有470
±
47μg的西洛他唑。
[0052]
第二层的西洛他唑的含量优选为0~100μg,更优选为10~80μg,进一步优选为20~60μg。进而,第二层优选含有30
±
3μg的西洛他唑。
[0053]
第一层的西洛他唑的含有率优选为40~100质量%,更优选为50~70质量%,进一步优选为55~65质量%。
[0054]
第二层的西洛他唑的含有率优选为0~50质量%,更优选为2~20质量%,进一步优选为5~10质量%。
[0055]
优选堆积层具有至少两层,靠近支架的第一层的西洛他唑含量比远离支架的第二层的西洛他唑含量大,两层均含有生物吸收性聚合物。
[0056]
第一层的生物吸收性聚合物的含量优选为0~500μg,更优选为250~350μg,进一步优选为300~320μg。进而,第一层优选含有313
±
31μg的生物吸收性聚合物。
[0057]
第二层的生物吸收性聚合物的含量优选为180~540μg,更优选为200~300μg,进一步优选为260~285μg。进而,第二层优选含有270
±
27μg的生物吸收性聚合物。
[0058]
第一层的生物吸收性聚合物的含有率优选为0~60质量%,更优选为25~50质量%,进一步优选为35~45质量%。
[0059]
第二层的生物吸收性聚合物的含有率优选为70质量%以上,更优选为80质量%以上,进一步优选为90质量%以上。
[0060]
对于本发明的实施方式的支架而言,在体外使支架与37℃的含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起24小时后,上述结晶性的西洛他唑溶出3质量%以下。
[0061]
对于本发明的实施方式的支架而言,在体外在37℃下使支架与含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起15天后,上述结晶性的西洛他唑优选溶出20质量%以下,在使支架接触起8天后,上述结晶性的西洛他唑优选溶出7质量%以下,在使支架接触起1天后,上述结晶性的西洛他唑优选溶出5质量%以下,更优选溶出3质量%以下。
[0062]
对于本发明的实施方式的支架而言,在体外在37℃下使支架与含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起15天后,上述结晶性的西洛他唑例如可以溶出1.0质量%以上,可以溶出0.1质量%以上,在使支架接触起8天后,上述结晶性的西洛他唑例如可以溶出0.5质量%以上,可以溶出0.05质量%以上,在使支架接触起1天后,上述结晶性的西洛他唑例如可以溶出0.1质量%以上,可以溶出0.01质量%以上。
[0063]
在体外使支架与37℃的含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起上述时间后,上述结晶性的西洛他唑溶出上述比例以下的情况下,西洛他唑可以释放超过3个月,因此,能够使西洛他唑在生物体内部存在极长期间。
[0064]
因此,本发明的实施方式的支架能够适合用于例如外周血管、优选外周动脉血管。
[0065]
此外,本发明的实施方式的支架也能够用于例如心脏的冠状动脉、下肢动脉等以往使用支架的较粗的动脉等。
[0066]
只要可以得到作为本发明目标的支架,则本发明的实施方式的支架的制造方法没
有特别限制。
[0067]
本发明的实施方式的支架可以使用例如下述制造方法来制造,所述制造方法包括:(i)准备支架骨架;(ii)准备含有西洛他唑的混合物;(iii)利用该混合物对支架骨架进行涂覆;重复进行(ii)和(iii)(但是,要调整西洛他唑的含量等)。
[0068]
含有西洛他唑的混合物可以在西洛他唑的基础上含有上述生物吸收性聚合物。混合物可以进一步含有添加剂等溶剂。由于西洛他唑为难溶性,因此需要生物吸收性聚合物防止涂层的剥落并且维持高强度。
[0069]
西洛他唑与生物吸收性聚合物、例如聚乳酸的混合质量比率优选为1:0.5~1:1.5。在该比率的范围内的情况下,能够得到更良好的内膜肥厚效果。另外,混合质量比率为1:1.1~1:1.5的情况下,能够进一步提高涂覆强度和缓释的效果。
[0070]
本发明的实施方式中,对于将西洛他唑与生物吸收性聚合物的混合物涂覆到支架骨架上的方法而言,只要可以得到作为本发明目标的支架则没有特别限制,可以使用以往所使用的例如简易喷雾法、浸渍法、电沉积法、超声波喷雾法等,从涂覆的观点考虑,优选使用超声波喷雾法。
[0071]
需要说明的是,上述的实施方式可以适当组合。
[0072]
以下,参考附图对本发明的实施方式进行详细说明。
[0073]
图1(a)示意性地示出本发明的一个方式的药剂溶出型支架1。药剂溶出型支架1具备具有长度方向轴线的圆筒状的形态,并具备管腔。药剂溶出型支架1中,关于圆筒状的形态,以具有粗网眼状的侧面、可以向侧方扩张的方式来形成。通常,网眼可以利用形成支架骨架的构件2(金属或高分子材料等的线)来形成。药剂溶出型支架1通常以未扩张形态插入到身体内,在血管内的治疗部位扩张并留置在该血管内。扩张可以利用球囊导管在血管内实现。图1(a)中示意性地记载了网眼。只要可以得到作为本发明目标的支架,则网眼的图案没有特别限制。
[0074]
图1(b)示意性地示出图1(a)中的形成支架骨架的线的截面(a-a截面)。
[0075]
本发明的一个方式的药剂溶出型支架1在支架骨架构件2上形成有堆积层3。支架骨架构件2可以使用任意的方法来制作。例如,可以利用激光、放电等离子加工、化学蚀刻或其他手段,由中空或形成的不锈钢管来制作。支架骨架构件2可以由镍、钴、铬、钛或不锈钢的适当的合金等形成。
[0076]
堆积层3由至少两个层形成。图1(b)中未示出两个以上层。
[0077]
图2示意性地示出在支架骨架构件2上涂布而形成堆积层3的超声波喷涂装置4。涂覆工序中,首先,优选利用等离子处理装置(未图示)在涂覆工序前对支架骨架构件2的表面进行等离子处理。等离子处理后,将支架骨架构件2安装到芯轴上,安装于超声波喷涂装置4中。超声波喷涂装置4中,将涂覆液利用注射泵通过配管6来送液,利用超声波喷雾喷嘴5进行雾化后喷射。喷雾中,在超声波喷嘴5下使支架骨架构件2旋转并且使其直线移动,由此在支架骨架构件2上堆积出堆积层3。然后,使支架骨架构件2一边旋转并直线移动一边在氮气气流下干燥,进一步在减压下在干燥器中干燥,由此,可以制作药剂溶出型支架1。根据堆积层3所含有的层的数量来变更涂覆液,对支架骨架构件进行多次涂覆,从而形成堆积层3。
[0078]
使用以与应形成的堆积层3对应的比例使西洛他唑和生物吸收性聚合物溶解于溶剂中而得到的混合物,准备涂覆液。堆积层3含有两个以上层,因此,需要准备两种以上涂覆
液。作为涂覆溶剂,为了能够在涂覆后容易除去,可以使用沸点低的挥发性溶剂。作为挥发性溶剂,可以例示例如甲醇、乙醇、三氟乙醇、六氟异丙醇、异戊醇、乙酸甲酯、乙酸乙酯、丙酮、甲乙酮、二氯甲烷、氯仿、二氯乙烷和含有它们中的至少两种的混合溶剂。
[0079]
实施例
[0080]
以下,通过实施例和比较例对本发明更具体且详细地进行说明,但这些实施例只不过是本发明的一个方式,本发明不受这些例子的任何限定。
[0081]
将本实施例中使用的各种聚合物示于下述表1中。
[0082]
[表1]
[0083][0084]
上述的聚合物的粘度是指极限粘度[η](dl/g),利用毛细管粘度计法进行测定。关于极限粘度,准备浓度c(g/dl)的试样溶液,由该试样溶液的流下时间(t)和溶剂的流下时间(t0)的测定值利用下式来计算。
[0085][0086]
作为装置,使用乌氏粘度计,作为溶剂,使用氯仿(25℃)。
[0087]
此外,使用马克-库恩-霍温克(mark-kuhn-houwink)公式(马克-霍温克-樱田公式),求出重均分子量(mw)。
[0088]
实施例1
[0089]
使用钴铬合金作为支架骨架构件2,准备将西洛他唑(clz)用二氯甲烷溶解的溶液。通过超声波喷涂将该溶液涂敷到作为基底材料的钴铬合金上,形成由440μg的西洛他唑形成的第一层。
[0090]
接着,准备将西洛他唑与聚合物(a)以1:9(质量比)混合并用二氯甲烷溶解的溶液。通过超声波喷涂将该溶液涂敷到第一层上,形成由540μg的聚合物(a)和60μg的西洛他唑形成的第二层,得到实施例1的支架。
[0091]
实施例2~3
[0092]
除了将聚合物(a)变为聚合物(b)或(c)以外,使用与实施例1中记载的方法同样的方法,制造实施例2~3的支架。
[0093]
比较例1~3
[0094]
除了将聚合物(a)变为聚合物(d)~(f)以外,使用与实施例1中记载的方法同样的方法,制造比较例1~3的支架。
[0095]
实施例4
[0096]
使用钴铬合金作为支架骨架构件2,准备将西洛他唑与聚合物(b)以3:2的比例混合并溶解于二氯甲烷中的溶液。通过超声波喷涂将该溶液涂敷到作为支架骨架构件的钴铬合金上,形成由313μg的聚合物(b)和470μg的西洛他唑形成的第一层。
[0097]
接着,准备将西洛他唑与聚合物(b)以1:9(质量比)的比例混合并溶解于二氯甲烷中的溶液。通过超声波喷涂将该溶液涂敷到第一层上,形成由270μg的聚合物(b)和30μg的西洛他唑形成的第二层,得到实施例4的支架。
[0098]
实施例5
[0099]
使用钴铬合金作为支架骨架构件2,准备将西洛他唑与聚合物(b)以3:2的比例混合并溶解于二氯甲烷中的溶液。通过超声波喷涂将该溶液涂敷到作为基底材料的钴铬合金上,形成由323μg的聚合物(b)和485μg的西洛他唑形成的第一层。
[0100]
接着,准备将西洛他唑与聚合物(b)以1:19(质量比)的比例混合并溶解于二氯甲烷中的溶液。通过超声波喷涂将该溶液涂敷到第一层上,形成由285μg的聚合物(b)和15μg的西洛他唑形成的第二层,得到实施例5的支架。
[0101]
实施例6
[0102]
使用钴铬合金作为支架骨架构件2,准备将西洛他唑与聚合物(b)以3:2的比例混合并溶解于二氯甲烷中的溶液。通过超声波喷涂将该溶液涂敷到作为基底材料的钴铬合金上,形成由313μg的聚合物(b)和470μg的西洛他唑形成的第一层。
[0103]
接着,准备将西洛他唑与聚合物(c)以1:9(质量比)的比例混合并溶解于二氯甲烷中的溶液。通过超声波喷涂将该溶液涂敷到第一层上,形成由270μg的聚合物(c)和30μg的西洛他唑形成的第二层,得到实施例6的支架。
[0104]
实施例7
[0105]
使用钴铬合金作为支架骨架构件2,准备将西洛他唑与聚合物(b)以3:2的比例混合并溶解于二氯甲烷中的溶液。通过超声波喷涂将该溶液涂敷到作为基底材料的钴铬合金上,形成由490μg的聚合物(b)和735μg的西洛他唑形成的第一层。
[0106]
接着,准备将西洛他唑与聚合物(b)以1:19(质量比)的比例混合并溶解于二氯甲烷中的溶液。通过超声波喷涂将该溶液涂敷到第一层上,形成由285μg的聚合物(b)和15μg的西洛他唑形成的第二层,得到实施例7的支架。
[0107]
实施例8
[0108]
除了形成由180μg的聚合物(b)和270μg的西洛他唑形成的第一层以外,使用与实施例4中记载的方法同样的方法,得到实施例8的支架。
[0109]
实施例9
[0110]
除了形成由247μg的聚合物(b)和370μg的西洛他唑形成的第一层以外,使用与实施例4中记载的方法同样的方法,得到实施例9的支架。
[0111]
西洛他唑的溶出试验(体外)
[0112]
1.西洛他唑的溶出试验方法
[0113]
使用溶出试验器400-ds(apparatus 7),试验液使用含有0.25质量%月桂基硫酸
钠的磷酸塩缓冲氯化钠溶液10ml,将溶出试验液的温度设定为37℃,以dip speed 10进行试验。
[0114]
在0.5小时、1小时、3小时、6小时、9小时、12小时、18小时、24小时后进行取样,在各个采集时间将试验液进行总量更换。
[0115]
2.西洛他唑的溶出率测定(hplc测定)
[0116]
对于各个试样溶液和标准溶液10μl,在以下的条件下进行hplc测定,由西洛他唑的峰面积值at和as计算出溶出率。
[0117]
溶出率的计算中,使用下式来进行计算。
[0118][0119]
支架1个中的西洛他唑的显示量(c)使用由涂覆质量算出的西洛他唑搭载量。
[0120]
测定条件
[0121]
检测器:紫外吸光光度计(测定波长:254nm)
[0122]
柱:在内径4.6mm
×
长度150mm的不锈钢管中填充有5μm的液相色谱用十八烷基甲硅烷基化硅胶的柱
[0123]
柱温:25℃附近的恒定温度
[0124]
流动相:水/乙腈/甲醇混液(10:7:3,v/v/v)
[0125]
流量:以使西洛他唑的保留时间为约9分钟的方式进行调整
[0126]
基于兔髂动脉埋入的动脉组织中的西洛他唑浓度和支架上的西洛他唑残存量(体内)
[0127]
向兔髂动脉中埋入实施例和比较例的各支架。埋入以下述方式进行。
[0128]
首先,将兔的颈部切开,露出右颈动脉,留置插管器。将球囊导管用导丝从插管器插入,在x射线透视下使其移动至髂动脉的处置部位的远端部。然后,将造影用导管沿着导丝插入,进行髂动脉的处置部位的血管造影。处置部位的血管造影结束后,在x射线透视下,将样本的球囊导管沿着球囊导管用导丝插入至处置部位。在确认样本的支架(标准直径扩张压9atm时支架直径2.75mm)位于髂动脉的处置部(预定血管直径2.5mm)后,使用
インデフレーター
使球囊在14atm(过扩张、预定支架直径3.0mm、20质量%过扩张)下保持1次20秒的扩张,确认支架扩张后,使球囊收缩,将
インデフレーター
取出,将球囊导管沿着球囊导管用导丝抽出。通过同样的方法对左右的髂动脉进行处置。
[0129]
接着,沿着球囊导管用导丝使造影用导管移动至处置部位的近前处,使用稀释造影剂进行血管造影。通过同样的方法对左右的髂动脉进行处置后,抽出造影用导管。最后,将导管鞘插入部位的血管结扎,将皮肤和肌层缝合。通过上述步骤,在兔的髂血管内留置支
架。
[0130]
从埋入起90天后,对各支架的埋入部位的动脉组织中的西洛他唑浓度和支架残存量进行分析。
[0131]
作为前处理,将各支架的埋入部位的动脉组织分离为支架和动脉组织。将通过液液萃取法从分离出的各试样中得到的有机层干固,作为试样。对于所得到的试样,通过使用电喷雾电离法的lc/ms/ms法对西洛他唑进行定量,计算出动脉组织中的西洛他唑浓度(1g的组织中的西洛他唑的μg数:μg/g组织)和西洛他唑残存量(支架上的西洛他唑的残存率(%))。
[0132]
基于猪髂动脉埋入的动脉组织中的西洛他唑浓度和支架上的西洛他唑残存量(体内)
[0133]
基于猪髂动脉埋入的动脉组织中的西洛他唑浓度和西洛他唑残存量的评价中,使用与对兔进行的方法同样的方法,对猪分析基于髂动脉埋入的动脉组织中的西洛他唑浓度(1g的组织中的西洛他唑的μg数:μg/g组织)和西洛他唑残存量(支架上的西洛他唑的残存率(%))。
[0134]
[表2]
[0135][0136]
[表3]
[0137][0138]
a:表示1g的组织中的西洛他唑的μg数。单位为μg/g组织。
[0139]
[表4]
[0140][0141]
a:表示1g的组织中的西洛他唑的μg数。单位为μg/g组织。
[0142]
实施例1~9的支架均具有支架骨架和在支架骨架上堆积两个以上层而成的堆积层,堆积层的各层含有结晶性的西洛他唑,上述两个以上层中的至少一层含有生物吸收性聚合物,在体外使支架与37℃的含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起24小时后,上述结晶性的西洛他唑溶出5质量%以下。
[0143]
另外,实施例1~9的支架均具有支架骨架和在支架骨架上堆积两个以上层而成的堆积层,堆积层的各层含有结晶性的西洛他唑,上述两个以上层中的至少一层含有生物吸收性聚合物,在体外使支架与37℃的含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起15天后,上述结晶性的西洛他唑溶出20质量%以下。
[0144]
因此,实施例1~9的支架能够超过3个月地缓释西洛他唑。
[0145]
需要说明的是,作为两个以上层,不限于两层,也可以应用三层以上,这是不言而喻的。
[0146]
与此相对,对于比较例1~3的支架而言,在体外使支架与37℃的含有0.25质量%月桂基硫酸钠的磷酸缓冲氯化钠溶液即溶出介质接触起24小时后,结晶性的西洛他唑均溶出超过5质量%。
[0147]
因此,比较例1~3的支架无法超过3个月地缓释西洛他唑。
[0148]
产业上的可利用性
[0149]
本发明的实施方式的药物留置型支架能够使结晶性的西洛他唑在体外进行溶出率试验24小时后溶出5质量%以下。或者,本发明的实施方式的药物留置型支架能够使结晶
性的西洛他唑在体外进行溶出率试验15天后溶出20质量%以下。因此,本发明的实施方式的药物留置型支架能够在更长期间释放结晶性西洛他唑,能够适合用于外周血管。
[0150]
[关联申请]
[0151]
需要说明的是,本技术以2019年7月9日在日本提交的申请号2019-127529为基础申请而要求基于巴黎公约第4条的优先权。该基础申请的内容通过参考并入本说明书中。
[0152]
符号说明
[0153]
1:支架
[0154]
2:支架骨架构件
[0155]
3:堆积层
[0156]
4:超声波喷涂装置
[0157]
5:超声波喷雾喷嘴
[0158]
6:配管
