1.本发明属于生物医药技术领域。更具体地,涉及一种中药组合物在防治炎症性贫血中的应用。
背景技术:
2.贫血的分类及诱因比较复杂,炎症性贫血(ai)也称慢性炎症性贫血(anemia of chronic disease,acd),是贫血中的一种,表现为血清铁和转铁蛋白饱和度降低,红细胞生成时可利用铁量减少,红细胞的生成速度减慢。慢性炎症性贫血主要是铁代谢紊乱和铁纳入红系前体细胞异常,炎症因子诱导产生铁调素增多是慢性炎症性贫血的关键。如机体炎性细胞因子il-1、il-6、tnf-a、bmp水平升高,炎症细胞因子通过不同的信号传导途径引起铁调素转录增加,血清水平升高。铁调素水平增高,使铁输出通道关闭,导致单核巨噬细胞再循环铁阻留和胃肠道铁吸收减少。
3.因此,炎症性贫血不是缺铁,而是铁利用和铁代谢的问题,这种情况下补充铁剂是不理想的,过多铁剂的摄入产生铁过载,导致毒性发生。
4.目前在临床,炎症性贫血主要治疗原则是治疗基础病及输血,然而就依赖基础病的治疗成效不佳,而且一般的炎症性贫血为轻度或中度的贫血,也不建议输血治疗,长期输血会导致铁负荷过多、肾移植时易对人类白细胞抗原hla致敏和其他输血不良反应。
5.申请人研发的一种由当归、黄芪、阿胶、益母草和陈皮组成的中药方(zl200610011863.4),对产后贫血具有明显的改善作用。但是该中药方对炎症性贫血等其他类型的贫血是否仍有作用以及效果如何,尚未有相关研究探索。
技术实现要素:
6.本发明旨在提供一种能够预防与治疗炎症性贫血的中药方,也拓展了该组方的应用范围。
7.本发明的目的是提供一种中药组合物在制备预防和/或治疗炎症性贫血中的药物中的应用。
8.本发明上述目的通过以下技术方案实现:
9.一种中药组合物在制备预防炎症性贫血的药物中的应用,以及在制备治疗炎症性贫血的药物中的应用,所述中药组合物包括当归、黄芪、阿胶、益母草和陈皮。
10.另外,优选地,所述中药组合物包括当归20-500份、黄芪20-500份、阿胶10-300份、益母草20-500份、陈皮1-100份。
11.更优选地,所述中药组合物包括当归80-120份、黄芪80-120份、阿胶24-36份、益母草120-180份、陈皮2.4-3.6份。
12.另外,上述中药组合物的制备方法包括步骤如下:
13.(1)将黄芪、益母草加3-10倍量水煎煮1-5次,每次1-3小时,合并煎液,滤过,滤液浓缩至相对密度为1.10-1.25(50-90℃)的清膏,备用;
14.(2)当归、陈皮粉碎成粗粉,用3-8倍量40-95%的乙醇作溶剂,浸渍8-90h后渗漉,收集渗漉液,渗漉液回收乙醇并浓缩至相对密度为1.10-1.25(50-90℃)的清膏,备用;
15.(3)将阿胶溶于上述黄芪、益母草清膏中,再加入当归、陈皮清膏,混合即可。
16.更优选地,步骤(1)是将黄芪、益母草第一次加4.8-6倍量水煎煮2小时,滤出煎液后,第二次加3.2-4.8倍量水煎煮1.5小时,滤出煎液,合并煎液,滤过,滤液浓缩至相对密度为1.10-1.15(60-70℃)的清膏,备用。
17.更优选地,步骤(2)是将当归、陈皮粉碎成粗粉,用4-5倍量60-80%的乙醇作溶剂,浸渍40-60h后渗漉,收集渗漉液,渗漉液减压浓缩至相对密度为1.10-1.15(60-70℃)的清膏,备用。
18.本发明具有以下有益效果:
19.本发明研究显示,由当归、黄芪、阿胶、益母草和陈皮制成的中药对炎症性贫血具有显著的预防与治疗效果,且无副作用,既拓宽了该组分的适应症范围,也为炎症性贫血的预防与治疗提供了一种新的中药组方选择。
具体实施方式
20.以下结合具体实施例来进一步说明本发明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
21.除非特别说明,以下实施例所用试剂和材料均为市购。
22.本实施例中所使用的药物为中药组合物制备成丸剂的剂型,即补血益母丸,但是并不局限于只是丸剂才具有实施例中所述效果。
23.实施例1脂多糖诱导小鼠炎症性贫血模型实验
24.一、材料和方法:
25.1、中药方:中药组合物包括当归100份、黄芪100份、阿胶30份、益母草150份、陈皮3份。制备方法如上文所述,制备成丸剂。
26.2、动物c57b6雄性小鼠,8周龄,适应性喂养一周后,按体重随机分为四组,分别为空白对照组(con),中药方组(aa),脂多糖组(lps),脂多糖采用pbs溶解,脂多糖和中药方组(lps+aa),每组5只。
27.各组小鼠给药,空白对照组给予pbs,中药方组按照3.12g/kg,口服给药,脂多糖组按照1mg/kg腹腔注射,脂多糖和中药方组同时给予3.12g/kg中药方和1mg/kg脂多糖,中药方口服,脂多糖采用腹腔注射。
28.给药6小时和24小时以后,摘眼球取血,常规解剖取脾脏。
29.3、制备血清:
30.摘眼球获得的血样室温放置1小时,4000转离心5分钟,取上清液,再次4000转离心5分钟,取上清液即为血清。
31.4、血清铁检测
32.使用pointe的iron/tibc reagent set试剂盒测量血清铁指标用:
33.准备分别标记有blank,standard和sample的96孔板,每孔中加入100μliron buffer,在blank中加入20μl去离子水,在standard中加入20μl的iron standard(500μg/dl),在sample中加入样品20μl,以blank为0,用酶标仪测定560nm每个孔的吸收读数(a1),
每个孔中加入2μl的iron color reagent,混合均匀,37度放置10分钟,以blank为0,用酶标仪测定560nm每个孔的吸收读数(a2);
34.血清铁(μg/dl)=(a2sample-a1sample)/(a2std-a1std)*concentration of st;
35.5、制备组织蛋白:
36.0.01克脾脏组织,加100μl ripa裂解液,振荡器震荡,60赫兹,3分钟,13200转离心15分钟,取上清。
37.二、实验结果:
38.实验结果表明:在生理情况下,中药方显著增加血清铁和载铁饱和度,在炎症性贫血情况下,中药方可以显著的抑制血清铁和载铁饱和度的下降。
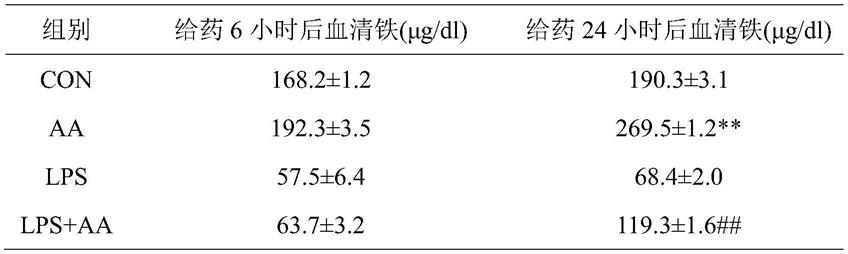
39.生理情况下,用药6小时后,中药方增加血清铁,增长较缓慢,而用药24小时以后,可以极显著的增加血清铁的含量,p《0.01(表1)。
40.炎症情况下,用药6小时后,中药方对脂多糖导致的血清铁的下降有上调作用,但没有显著性差异,而用药24小时后,中药方可以抑制脂多糖诱导的血清铁的下降,有显著性差异,p《0.05(表1)。
41.表1:给药后各实验组血清铁的含量
[0042][0043]
注:与con组比较,**p<0.01;与lps组比较,##p<0.01。
[0044]
综上可知,小鼠口服中药方可以显著的增加血清铁的含量以及改善脂多糖导致的炎症性贫血。
[0045]
同时,本发明检测了用药6小时和24小时血清总铁结合能力,实验结果表明,中药方无论在生理还是炎症性情况下,对于载铁饱和度,用药6小时在生理和炎症情况下中药方对载铁饱和度都没有影响;用药24小时后,生理情况下,中药方可以显著增加载铁饱和度p《0.05,炎症情况下,中药方可以抑制脂多糖导致的载铁饱和度的下降,具有极显著差异(p《0.001)(表2)。
[0046][0047]
注:与con组比较,**p<0.01;与lps组比较,##p<0.001。
[0048]
实施例2弗氏完全佐剂诱导大鼠炎症性贫血药理药效实验
[0049]
1、实验材料
[0050]
实验动物:雄性sd大鼠,150
±
2g,6-8周龄,市购。
[0051]
中药组方同实施例1。
[0052]
2、动物饲养及分组
[0053]
雄性sd大鼠适应性喂养一周后,称重后用苦味酸标记,每笼5只喂养,笼内垫料两天更换一次并用75%酒精擦拭消毒,动物房温度23
±
2℃,相对湿度为50
±
20%,自然采光。所有大鼠自由饮食和饮水,所有操作严格遵循《实验动物管理条例》。
[0054]
采用大鼠足趾皮下注射0.15ml结核分歧杆菌浓度为10mg/ml的弗氏完全佐剂的方法建立模型,对照组大鼠足趾皮下注射0.15ml生理盐水。
[0055]
给药方案及分组:大鼠随机分为7组:
[0056]
模型组(acd):每天灌胃1ml双蒸水,共28天;
[0057]
对照组(con):每天灌胃1ml双蒸水,共28天;
[0058]
rhepo治疗组(esa):实验结束前3天开始按2000u/kg体重剂量给大鼠腹腔注射rhepo(重组人红细胞生成素),每天一次,共三次;
[0059]
双氯芬酸钠治疗组(df):以10mg/kg体重剂量每天给大鼠灌胃双氯芬酸钠溶液,共28天;
[0060]
双氯芬酸钠和rhepo联合给药组(df/esa):以10mg/kg体重剂量每天给大鼠灌胃双氯芬酸钠溶液,共28天;并在实验结束前3天开始按2000u/kg体重剂量给大鼠腹腔注射rhepo,每天一次,共三次;
[0061]
中药治疗组(aa):以2.16g/kg体重剂量每天给大鼠口服中药组方,共28天。
[0062]
2、造模前后大鼠体重变化如表3
[0063]
表3各组大鼠体重造模前后变化
[0064][0065]
注:与对照组(con)比较,##p<0.01;与模型组(acd)相比,**p<0.01。
[0066]
结果显示,与对照组相比,造模后模型组大鼠体重显著降低。给药aa治疗组显著缓解了acd大鼠体重下降。
[0067]
3、中药组方对acd大鼠血清炎性因子的影响
[0068]
采用酶联免疫分析法检测各组大鼠血清促炎性因子tnf-α、il-6水平,结果如表4。
[0069]
表4中药组方对acd大鼠血清tnf-α、il-6水平的影响
[0070][0071]
注:与对照组(con)比较,##p<0.01;与模型组(acd)相比,**p<0.01,*p<0.05。
[0072]
结果显示,与对照组相比,acd模型组大鼠血清促炎性因子tnf-α、il-6水平均有明显提高。给药aa治疗组可以显著抑制acd大鼠血清促炎性因子tnf-α、il-6的分泌。
[0073]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
