1.本发明属于化合物技术领域,尤其涉及一种玫瑰石斛吲哚生物碱类化合物、制备方法及应用。
背景技术:
2.目前,玫瑰石斛为兰科石斛属植物玫瑰石斛(dendrobium crepidatum lindl.expaxt.)的新鲜或干燥茎。其花观赏价值极高,花姿优雅,玲珑可爱,花色鲜艳,气味芳香,被喻为“四大观赏洋花”之一。其茎滋阴益胃,生津除烦。用于口干烦渴,阴伤津亏,病后虚热,目暗不明,食欲不振。有关玫瑰石斛的研究较少,且主要集中于抗炎和抗肺损伤方面。目前,有关玫瑰石斛提取物的相关专利多集中在其组织培养方面,关于玫瑰石斛吲哚生物碱类化合物制备的相关技术方案尚未见报道。因此,亟需一种玫瑰石斛吲哚生物碱类化合物及其制备方法,以填补现有技术的空白。
3.通过上述分析,现有技术存在的问题及缺陷为:现有技术中关于玫瑰石斛吲哚生物碱类化合物制备的相关技术方案尚未见报道。
4.解决以上问题及缺陷的难度为:吲哚里西啶类生物碱是以吲哚里西啶结构为基本骨架的生物碱,多数生物碱还含有苯环结构,这也增加了其吸收光谱的强度,此类生物碱可形成二倍体结构,同时,多数吲哚里西啶类生物碱为对映异构体,含有手性中心,这也使得多种生物碱的吸光度比较小。
5.相比于石斛属中分离得到的其他成分的数量,石斛中的生物碱单体化合物的数量还是较少,这可能与生物碱的提取方法及其结构相关。生物碱中的共轭基团不多,在紫外下的吸收较弱,而且生物碱需要特定的显色剂碘化铋钾来显色,种种原因增加了生物碱分离的难度,前期研究者多是通过柱色谱分离的方式分离纯化生物碱,但是对于石斛属的多种石斛来说,其中的生物碱成分结构类似,极性相近,利用此种方法很难得到单一的生物碱成分。
6.解决以上问题及缺陷的意义为:生物碱是一类有具有多种优良活性的化合物,多有抗阿尔茨海默症、抗炎和抗肿瘤等多种功效,玫瑰石斛中分离到的生物碱多为吲哚里西啶类,以抗炎活性为主。迄今为止,石斛属中的吲哚里西啶类生物碱数量仍很少,因此,进一步甄选石斛材料进行生物碱成分的分离鉴定,以扩充石斛属的化合物库是非常有必要的,也有利于活性探索的进一步深入。
技术实现要素:
7.针对现有技术存在的问题,本发明提供了一种玫瑰石斛吲哚生物碱类化合物、制备方法及应用。
8.本发明是这样实现的,一种玫瑰石斛吲哚生物碱类化合物制备方法,所述玫瑰石斛吲哚生物碱类化合物制备方法包括以下步骤:
9.步骤一,将玫瑰石斛生物碱粗提物,经常压硅胶柱色谱分离、石油醚-丙酮梯度洗
脱以及tlc检测合并,共得到5个馏分fr.1-fr.5;
10.步骤二,将fr.2经硅胶柱层析分离,经30:1的石油醚-丙酮等度洗脱和tlc检测合并,共得到5个馏分fr.2.1-fr.2.5;
11.步骤三,将fr.2.1经凝胶柱色谱分离得到化合物1、化合物2和化合物3;其中,所述凝胶柱色谱的二氯甲烷:甲醇=1:1;
12.步骤四,将fr.2.2经凝胶柱色谱及半制备液相等度分离纯化,得到化合物4和化合物6;
13.步骤五,将fr.2.3经半制备液相等度分离纯化得到化合物8;
14.步骤六,将fr.2.4经半制备液相梯度分离纯化得到化合物9、化合物10、化合物11和化合物12;
15.步骤七,将fr.4经凝胶柱色谱,共得到6个馏分fr.4.1-fr.4.6,并将fr.4.2经凝胶柱色谱分离得到化合物5和化合物7。
16.进一步,步骤一中,所述石油醚-丙酮梯度洗脱参数包括:50:1,30:1,20:1,15:1,10:1,5:1,2:1,丙酮。
17.进一步,步骤四中,所述二氯甲烷:甲醇=4:3,所述半制备液相为65%的乙腈-水,2ml/min。
18.进一步,步骤五中,所述半制备液相为70%的甲醇-水,2ml/min,254nm。
19.进一步,步骤六中,所述半制备液相为60-100%甲醇-水,30min,2ml/min,254nm。
20.进一步,步骤七中,所述fr.4经过的凝胶柱色谱的二氯甲烷:甲醇=1:1;所述fr.4.2经过的凝胶柱色谱的二氯甲烷:甲醇=2:1。
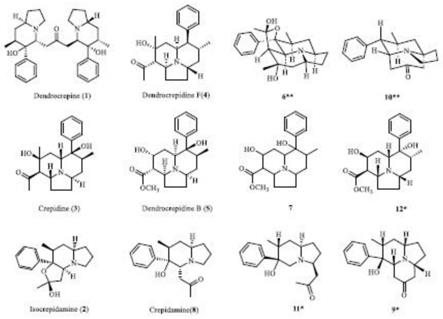
21.本发明的另一目的在于提供一种应用所述的玫瑰石斛吲哚生物碱类化合物制备方法制备得到的玫瑰石斛吲哚生物碱类化合物,所述玫瑰石斛吲哚生物碱类化合物的结构如下:
[0022][0023]
本发明的另一目的在于提供一种所述的玫瑰石斛吲哚生物碱类化合物在对lps诱导raw 264.7细胞释放no抑制中的应用。
[0024]
进一步,所述玫瑰石斛吲哚生物碱类化合物对lps诱导raw 264.7细胞释放no抑制的确定方法,包括:
[0025]
(1)mtt法测定化合物1、2、3对raw 264.7细胞的毒性作用
[0026]
用含10%胎牛血清的培养液dmem或者rmpi1640配成细胞悬浮液,取每孔200μl的raw 264.7细胞悬液5
×
104个/ml接种于96孔培养板,于5%co2,37℃恒温培养箱中培养24小时;吸出里面的培养基后加入200μl浓度为30μm的待测化合物溶液,空白对照组加入200μl dmem完全培养液,每孔终体积200μl;37℃培养24h后,吸弃孔内培养上清液,每孔加mtt溶液200μl;置于37℃、5%co2培养箱内继续培养4h后,除去上清液,加入等体积的dmso溶解甲臜,震荡均匀后于570nm处测定每孔的吸光值;根据光密度od值推测出活细胞的数目,记录结果,并计算出raw 264.7细胞的存活率。
[0027]
(2)化合物1-3对lps诱导的raw 264.7细胞产生no的测定
[0028]
通过硝酸盐还原酶法检测培养基中亚硝酸钠的量来评估raw 264.7细胞中no的释放,让raw 264.7细胞在96孔细胞培养板上生长,并在5%co2的环境中于37℃培养24h,实验组分别加入200μl浓度为30μl的化合物1、2、3,空白对照组则加入200μl的dmem完全培养液,阳性对照组添加200μl浓度为30μm的地塞米松溶液,阴性对照组则添加200μl浓度为5μg/ml的lps,继续培养2h,加入lps 5μg/ml,在相同条件下继续培养24h,收集培养上清液进行检测;根据no测定试剂盒,利用硝酸还原酶法的说明测定细胞中no的含量。
[0029]
(3)数据处理
[0030]
实验数据od值采用“平均数
±
标准差”来表示,数理统计及方差分析工作采用spss完成。
[0031]
进一步,步骤(2)中,所述96孔细胞培养板每孔2
×
104个细胞。
[0032]
结合上述的所有技术方案,本发明所具备的优点及积极效果为:本发明提供的玫瑰石斛吲哚生物碱类化合物制备方法简单易行,制备得到的玫瑰石斛吲哚生物碱类化合物对lps诱导raw 264.7细胞释放no具有抑制作用。
附图说明
[0033]
为了更清楚地说明本发明实施例的技术方案,下面将对本发明实施例中所需要使用的附图做简单的介绍,显而易见地,下面所描述的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下还可以根据这些附图获得其他的附图。
[0034]
图1是本发明实施例提供的玫瑰石斛吲哚生物碱类化合物制备方法流程图。
[0035]
图2是本发明实施例提供的玫瑰石斛吲哚生物碱类化合物制备方法原理图。
[0036]
图3是本发明实施例提供的玫瑰石斛吲哚生物碱类化合物结构示意图。
具体实施方式
[0037]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0038]
针对现有技术存在的问题,本发明提供了一种玫瑰石斛吲哚生物碱类化合物、制
2'),7.30(1h,m,h-3'),7.36(1h,m,h-4'),7.30(1h,m,h-5'),7.26(1h,m,h-6');13c-nmr(150mhzv,dmso-d6):52.3(c-1),41.6(c-2),65.4(c-3),32.7(c-4),33.4(c-5),76.1(c-6),40.5(c-7),33.4(c-8),61.6(c-9),28.1(c-10),30.2(c-11),170.5(c-12),49.5(c-13),20.1(c-14),142.2(c-1'),127.3(c-2'),126.6(c-3'),126.0(c-4'),126.6(c-5'),127.3(c-6')。以上数据与文献报道的dendrocrepidine b基本一致。
[0063]
化合物6(dc-3)
[0064]
白色粉末,[α]d25+4.44(c0.1,meoh);uv(meoh)max(logε)205(3.70);ir(neat)max 3433,2965,1209,1032,935,755cm-1;for 1h nmr and 13c nmr data见表2-2;positive hr-esi-ms:m/z 344.2230[m+h]+(calcd 344.2226for c21h30no3).
[0065]
化合物7(dc-4)
[0066]
橙黄色油状物,1h-nmr(600mhz,dmso-d6):2.99(1h,dt,j=1.8,6.0,10.8hz,h-1),2.47(1h,dd,j=3.0,11.4hz,h-2),4.31(1h,m,h-3),1.97(1h,m,h-4a),1.85(1h,m,h-4b),3.69(1h,m,h-5),1.28(2h,dd,j=7.2,13.2hz,h-7),1.81(1h,m,h-8a),1.24(1h,m,h-8b),1.85(1h,m,h-9),1.43(1h,m,h-10a),2.07(1h,m,h-10b),1.67(1h,m,h-11a),1.82(1h,m,h-11b),3.65(3h,s,h-13);0.58(3h,d,j=7.2hz,h-14),7.24(1h,m,h-2'),8.01(1h,m,h-3'),7.17(1h,m,h-4'),8.01(1h,m,h-5'),7.24(1h,m,h-6')。以上数据与文献以上数据与文献[12]报道的dendrocrepidine b基本一致。
[0067]
化合物8(dc-5)
[0068]
白色粉末,1h-nmr(600mhz,dmso-d6):2.70(1h,m,h-1),1.90(1h,m,h-3),1.68(1h,ddd,j=2.4,4.2,12.6hz,h-4a),1.32(1h,m,h-4b),2.60(1h,m,h-5),1.25(1h,m,h-6a),1.77(1h,m,h-6b),1.35(1h,m,h-7a),1.85(1h,m,h-7b),2.20(2h,m,h-8),2.80(2h,dd,j=4.2,16.8hz,h-9a),2.36(1h,dd,j=8.4,16.8hz,h-9b),2.05(3h,s,h-11),0.52(3h,d,j=6.6hz,h-12),7.32(1h,m,h-2'),7.47(1h,m,h-3'),7.21(1h,m,h-4'),7.47(1h,m,h-5'),7.32(1h,m,h-6');13c-nmr(150mhzv,dmso-d6):62.1(c-1),63.2(c-2),37.8(c-3),28.2(c-4),72.5(c-5),34.8(c-6),28.1(c-7),58.2(c-8),46.9(c-9),207.3(c-10),29.9(c-11),14.4(c-12),144.9(c-1'),127.1(c-2'),124.4(c-3'),125.6(c-4'),124.4(c-5'),127.1(c-6')。以上数据与文献报道的crepidamine基本一致。
[0069]
化合物9(dc-6)
[0070]
白色针状物,[α]d25-4.0(c0.1,meoh);uv(meoh)max(logε)209(3.81);ir(neat)max 3482,2964,2872,1708,999,776,709cm-1;for 1h nmr and 13c nmr data见表2-3;positive hr-esi-ms:m/z 286.1809[m+h]+(calcd 286.1807for c18h24no2).
[0071]
化合物10(dc-7)
[0072]
黄色油状物,[α]d25-26.0(c0.1,meoh);uv(meoh)max(logε)205(4.03);ir(neat)max 2924,2874,1708,1056,1031,704cm-1;for 1h nmr and 13c nmr data见表2-2;positive hr-esi-ms:m/z 270.1857[m+h]+(calcd 270.1858for c18h24no).
[0073]
化合物11(dc-8)
[0074]
白色针状物,[α]d25-3.0(c0.1,meoh);uv(meoh)max(logε)206(3.68);ir(neat)max 2930,1714,1036,766,704cm-1;for 1h nmr and 13c nmr data见表2-3;positive hr-esi-ms:m/z 288.1968[m+h]+(calcd 288.1964 for c18h26no2).
[0075]
化合物12(dc-9)
[0076]
白色粉末,[α]d25+66.0(c0.1,meoh);uv(meoh)max(logε)205(2.15);ir(neat)max 3457,1722,1450,1316,1194,1060,1021,933cm-1;for 1h nmr and 13c nmr data见表2-3。
[0077]
化合物12的单晶数据已经上传至剑桥体库(cambridge crystallographic data centre)[deposition number:ccdc 1908235]。
[0078]
实施例2:化合物对lps诱导raw 264.7细胞释放no的抑制作用
[0079]
(1)材料
[0080]
dmem培养液(美国gibco公司)、胎牛血清(美国gibco公司)、rpmi-1640培养液(美国gibco公司)、磷酸盐缓冲液(上海beyotime公司)、双抗(美国hyclone公司)、dmso(美国sigma公司)、mtt(美国sigma公司),本发明化合物及地塞米松均用dmso配制;
[0081]
(2)mtt法测定化合物1、2、3对raw 264.7细胞的毒性作用
[0082]
用含10%胎牛血清的培养液(dmem或者rmpi1640)配成细胞悬浮液,取每孔200μl的raw 264.7细胞悬液(5
×
104个/ml)接种于96孔培养板,于5%co2,37℃恒温培养箱中培养24小时;吸出里面的培养基后加入200μl浓度为30μm的待测化合物溶液,空白对照组加入200μl dmem完全培养液,每孔终体积200μl;37℃培养24h后,吸弃孔内培养上清液,每孔加mtt溶液200μl;置于37℃、5%co2培养箱内继续培养4h后,除去上清液,加入等体积的dmso溶解甲臜,震荡均匀后于570nm处测定每孔的吸光值;根据光密度od值推测出活细胞的数目,记录结果,并计算出raw 264.7细胞的存活率,结果见表1。
[0083]
(3)化合物1-3对lps诱导的raw 264.7细胞产生no的测定
[0084]
通过硝酸盐还原酶法检测培养基中亚硝酸钠的量来评估raw 264.7细胞中no的释放,让raw 264.7细胞在96孔细胞培养板(每孔2
×
104个细胞)上生长,并在5%co2的环境中于37℃培养24h,实验组分别加入200μl浓度为30μl的化合物1、2、3,空白对照组则加入200μl的dmem完全培养液,阳性对照组添加200μl浓度为30μm的地塞米松溶液,阴性对照组则添加200μl浓度为5μg/ml的lps,继续培养2h,加入lps(5μg/ml),在相同条件下继续培养24h,收集培养上清液进行检测;根据一氧化氮(no)测定试剂盒(硝酸还原酶法)的说明测定细胞中no的含量。
[0085]
(4)数据处理
[0086]
实验数据od值采用“平均数
±
标准差”来表示,数理统计及方差分析工作采用spss完成。
[0087]
(5)结果与讨论
[0088]
化合物1-3在30μm下对raw 264.7细胞的存活率影响见表1,化合物1-3在30μm下对lps诱导raw 264.7细胞产生no的影响见表2。
[0089]
表1化合物1-3在30μm下对raw 264.7细胞的存活率影响
[0090]
化合物存活率(%)地塞米松89.93
±
0.79化合物188.65
±
6.64化合物288.11
±
4.68化合物389.84
±
4.67
[0091]
该结果证明化合物1、2、3在浓度为30μm时对raw 264.7细胞的存活率影响与地塞米松基本相当;
[0092]
表2化合物1-3在30μm下对lps诱导raw 264.7细胞产生no的影响
[0093]
组别no的含量(pg/ml)空白对照组2.03
±
0.08阴性对照组15.76
±
0.17地塞米松9.78
±
0.16化合物19.85
±
0.17化合物210.34
±
0.03化合物39.64
±
0.29
[0094]
化合物1、3在30μm浓度下对lps诱导raw 264.7细胞产生no具有显著的抑制活性,其中化合物3的活性显著优于地塞米松;化合物1、3能够明显降低lps诱导raw 264.7细胞上清液中的亚硝酸根浓度。如表2所示,与空白组相比,阴性对照组的细胞上清液中含有大量亚硝酸根,表明lps能够明显引起炎症反应。与lps组相比,表明给药组和阳性对照组的亚硝酸根浓度明显降低,no的释放得到抑制。化合物1、3几乎能完全抑制no的释放,与地塞米松作用相当;化合物2与lps组相比对no的释放有显著抑制作用,但其活性低于地塞米松。
[0095]
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,都应涵盖在本发明的保护范围之内。
