1.本发明涉及光电材料领域,具体而言,本发明涉及一种有机硼化合物及其在有机电致发光器件中的应用。
背景技术:
2.有机电致发光器件(oled)包含阴极、阳极及位于两极之间的有机层,有机层包括空穴传输层、电子传输层、发光层等多层结构。在外加电场驱动下,空穴和电子首先分别由阳极和阴极注入,然后在空穴传输层和电子传输层中相向运动,继而在发光层中复合成激子辐射跃迁发出各色光。
3.为了将oled应用于全色彩显示,实现具有高效率的红绿蓝三色器件是首要问题。目前,对于绿光和红光oled,基于磷光和热活化延迟荧光(tadf)机理的发光材料均已实现100%的内量子效率,且已经实现规模产业化,被广泛应用于商业化的全色显示设备中。然而高质量显示的深蓝光oled材料始终未能实现重大的突破,蓝光材料带隙宽,其电致发光过程中的载流子传递和能量转移过程困难且不稳定,而且高电流密度下激子间的相互淬灭失活现象十分严重,因此绝大多数深蓝光器件会出现非常严重的器件效率滚降和较低的亮度,而且使用寿命也非常短。
4.近年来,含有机硼和氮共嵌的新型π-共扼有机单元材料由于具有良好的光物理和电化学性能,成为了蓝光oled材料体系的研究热点,咪唑同时具有酸性和碱性,是一种双极性化合物,将其运用于蓝光oled材料中,对于调节载流子的平衡性具有重要意义。
技术实现要素:
5.本发明的目的在于提供一种有机硼化合物及其在有机电致发光器件中的应用,提高目前深蓝光发光材料载流子传输平衡性,从而使得深蓝光oled器件在发光效率、稳定性、光色、寿命等方面具有优良的综合性能。
6.本发明第一个方面提供了一种有机硼化合物,其化合物结构通式如式(1)所示:
[0007][0008]
其中,相同或相异,分别独立地表示为空或单键或-x
0-,x0选自o、s、n(r2)和c(r3)(r4)中的任意一种;
[0009]
ar、ar1和ar2彼此相同或不同,各自独立地选自苯环、碳原子数不超过18的稠合芳环、碳原子数不超过18的稠合芳杂环、r1取代的苯环、r1取代的碳原子数不超过18的稠合芳
环和r1取代的碳原子数不超过18的稠合芳杂环中的任意一种;
[0010]
r0选自氢、氟基、硝基、氰基、c
1-12
的烷基、c
6-30
的芳基、c
3-30
的杂芳基和c
6-30
的芳胺基中的任意一种;
[0011]
r1选自氢、氟基、硝基、氰基、c
1-12
的烷基、c
1-12
的烷氧基、c
3-12
的环烷基、c
2-20
的杂环烷基、c
6-30
的芳基、c
3-30
的杂芳基和c
6-30
的芳胺基中的任意一种;
[0012]r2-r4彼此相同或不同,各自独立地选自c
1-12
的烷基和c
6-30
的芳基中的任意一种。
[0013]
进一步的,ar、ar1和ar2彼此相同或不同,各自独立地选自以下任意一种:未取代的或被r1取代的苯、未取代的或被r1取代的萘、未取代的或被r1取代的二苯并呋喃、未取代的或被r1取代的二苯并噻吩、未取代的或被r1取代的9,9-二甲基芴、未取代的或被r1取代的咔唑,其中,使用的符号和标记具有权利要求1中给出的含义。即,r1的定义与上述化学式1中的r1相同。
[0014]
进一步的,当ar、ar1和ar2各自独立地为未取代或被r1取代的苯时,所述有机硼化合物为式1-1所示的化合物:
[0015][0016]
当ar、ar1各自独立地为未取代或被r1取代的苯,且ar2为未取代或被r1取代的萘、未取代的或被r1取代的二苯并呋喃、未取代的或被r1取代的二苯并噻吩、未取代的或被r1取代的9,9-二甲基芴、未取代的或被r1取代的咔唑中的任意一种时,所述有机硼化合物为式1-2所示的化合物:
[0017][0018]
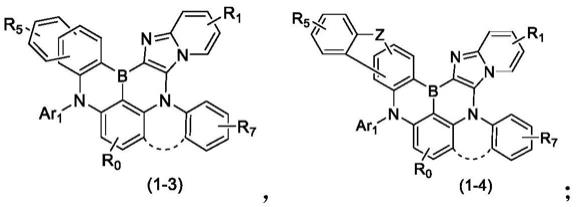
当ar为未取代的或被r1取代的萘、未取代的或被r1取代的二苯并呋喃、未取代的或被r1取代的二苯并噻吩、未取代的或被r1取代的9,9-二甲基芴、未取代的或被r1取代的咔唑中的任意一种,且ar2为未取代或被r1取代的苯时,所述有机硼化合物为式1-3或式1-4所示的化合物:
[0019][0020]
当ar、ar2各自独立地为未取代的或被r1取代的萘、未取代的或被r1取代的二苯并呋喃、未取代的或被r1取代的二苯并噻吩、未取代的或被r1取代的9,9-二甲基芴、未取代的或被r1取代的咔唑中的任意一种时,所述有机硼化合物为式1-5或式1-6所示的化合物:
[0021][0022]
其中,ar1、ar2的定义与权利要求2中的ar1、ar2的定义相同,
[0023]
的定义与上述式1中的相同,
[0024]
r0的定义与上述式1中的r0相同,
[0025]
r1的定义与上述式1中的r1相同,
[0026]
r5、r6、r7的定义与上述式1中的r1相同,
[0027]
z选自o、s、c(ch3)2、n(ph)中的任意一种。
[0028]
进一步的,r2为未取代的或由氟基、硝基、氰基、甲基、叔丁基取代的苯基中的任意一种。
[0029]
进一步的,r3与r4彼此相同,均为甲基。
[0030]
进一步的,r1选自:氢,氟基,硝基,氰基,甲基,叔丁基,未取代的或由氟基、硝基、氰基、甲基、叔丁基、苯基取代的苯基中的任意一种。
[0031]
进一步的,r0独立地为氢,氟基,硝基,氰基,甲基,叔丁基,未取代的或由氟基、硝基、氰基、甲基、叔丁基取代的苯基、联苯基、式a1所示基团、式a2所示基团和式a3所示基团中的任意一种:
[0032][0033]
其中,x1选自o、s、n(r8)、c(r9)(r
10
),r
8-r
10
彼此相同或不同,各自独立地选自甲基,未取代的或由氟基、硝基、氰基、甲基、叔丁基取代的苯基中的任意一种。
[0034]
进一步的,式1所示有机硼化合物选自以下结构式中的任意一种:
[0035]
[0036]
[0037]
[0038][0039]
本发明第二个方面提供了一种有机电致发光器件,主要包括阴极、阳极以及位于所述阴极和所述阳极之间的有机层,所述有机层包含上述任一所述的有机硼化合物。
[0040]
进一步的,两电极之间的有机层包括发光层,发光层包含上述任一所述的有机硼化合物。
[0041]
本发明所提供的有机硼化合物以具有较强缺电子性质的咪唑并吡啶与芳胺、咔唑、吖啶等供电子性质的基团氮键接构成供受体型主体骨架,化合物整体上的载流子迁移率更加平衡,因此,可以获得较高的荧光量子产率,并利用硼对主体中心进行修饰形成刚性大共轭结构,因此化合物homo得以降低从而获得较宽带隙,可以实现稳定的深蓝光发射,同时也可获得较好的热力学稳定性,进而应用至有机电致发光器件,在器件的启动电压、发光效率及寿命等方面具有显著优势。
具体实施方式
[0042]
应当理解的是,此处所描述的具体实施方式仅用于说明和解释本发明,并不用于
限制本发明。
[0043]
合成实施例1:合成化合物(7)
[0044]
s1:在反应器中,投入3-溴咪唑并[1,2-a]吡啶(35mmol,6.90g)、2,3-二氯-5-氟-均三甲基苯胺(30mmol,8.95g)、叔丁醇钠(60mmol,5.76g)、三二亚苄基丙酮二钯(0.15mmol,0.14g)、三叔丁基膦四氟硼酸盐(0.15mmol,0.04g)、甲苯100ml后,充分搅拌混合后,在氮气保护下,加热回流反应,液相监测反应完成,冷却至室温,投入二苯胺(30mmol,5.08g),充分搅拌混合,在氮气保护下,继续加热回流反应,液相监测反应完成,冷却至室温,用水和二氯甲烷的混合物对反应液进行萃取,有机相硫酸镁干燥后浓缩,用1:10的二氯甲烷与石油醚混合溶剂在硅胶柱中纯化分离,即可得到以下化学式(7a)所表示的化合物10.18g,收率62%;
[0045][0046]
s2:在反应器中,投入上述(7a)所表示的化合物(15mmol,8.21g),10氢-吩噁嗪(20mmol,3.66g),碳酸铯(22.5mmol,7.33g)、n,n-二甲基甲酰胺100ml后,充分搅拌混合后,在氮气保护下,加热回流反应,液相监测反应完成,冷却至室温,加入50ml-100ml水,过滤,滤液用二氯甲烷萃取2遍后浓缩,与滤饼一起用乙醇打浆2遍,即可得到以下化学式(7b)所表示的化合物8.52g,收率80%;
[0047][0048]
s3:在反应器中,将上述(7b)所表示的化合物(10mmol,7.10g)溶解于50ml的叔丁基苯溶液中,反应液降温至-40℃,在氮气保护下,缓慢滴加32.5ml 2.5m正己烷叔丁基锂溶液,保温搅拌0.5-2h,投入三溴化硼(15mmol,3.76g),将反应液升至室温搅拌0.5-2h,将反应液降温至0℃,加入n,n-二异丙基乙胺(10mmol,1.29g),加热至120℃回流反应,液相监测反应完成,冷却至室温,加醋酸猝灭反应,用水和二氯甲烷的混合物对反应液进行萃取,有机相硫酸镁干燥后浓缩,用1:10的二氯甲烷与石油醚混合溶剂在硅胶柱中纯化分离,即可得到以下化学式(7)表示的化合物2.39g,收率35%;
[0049][0050]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为683.6275;核磁δ(ppm)=9.02(1h),8.79(1h),8.45(1h),7.78(2h),7.70(1h),7.62(1h),7.47(1h),7.35(2h),7.22(1h),6.89-6.95(4h)6.77(2h),6.70(1h),6.59(2h),6.26(1h),6.02(2h),5.22(2h),2.20(9h)。
[0051]
合成实施例2:合成化合物(13)
[0052]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为2,3-二氯-n-二苯胺(30mmol,7.14g),二苯胺替换为3,6-二苯基-9氢-咔唑(30mmol,9.58g),其它合成过程同实施例1,即可得到以下化学式(13a)所表示的化合物11.09g,收率58%;
[0053][0054]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(13a)所表示的化合物6.37g,其它合成过程同实施例1,即可得到以下化学式(13)表示的化合物1.89g,收率31%;
[0055][0056]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为610.5309;核磁δ(ppm)=9.05(1h),8.90(1h),8.76(1h),8.45(1h),8.22(1h),8.06(1h),7.95(1h),7.81-7.87(4h),7.72(2h),7.62(3h),7.48(2h),7.32(2h),7.20(2h),7.05(1h),6.73(1h),6.25(1h),6.14(2h)。
[0057]
合成实施例3:合成化合物(26)
[0058]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为n-(2,3-二氯苯基)-[1,1'-联苯]-4-胺(30mmol,9.43g),二苯胺替换为5-(p-甲苯基)-5,10-二氢吩嗪(30mmol,8.17g),其它合成过程同实施例1,即可得到以下化学式(26a)所表示的化合物12.79g,收率
64%;
[0059][0060]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(26a)所表示的化合物6.66g,其它合成过程同实施例1,即可得到以下化学式(26)表示的化合物2.11g,收率33%;
[0061][0062]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为639.5615;核磁δ(ppm)=9.03(1h),8.42(1h),8.11(1h),7.78(2h),7.71(1h),7.63(1h),7.55(2h),7.48(2h),7.40(1h),7.32(2h),7.27(1h),7.21(2h),7.16(1h),6.97-7.03(5h),6.89(1h),6.26(1h),6.14(2h),2.26(3h)。
[0063]
合成实施例4:合成化合物(28)
[0064]
s1:将实施例1中s1中的二苯胺替换为10氢-吩噻嗪(30mmol,5.98g),其它合成过程同实施例1,即可得到以下化学式(28a)所表示的化合物10.39g,收率60%;
[0065][0066]
s2:将实施例1中s2中的(7a)替换为本实施例上述(28a)所表示的化合物8.66g,10氢-吩噁嗪替换为9氢-咔唑(20mmol,3.34g),其它合成过程同实施例1,即可得到以下化学式(28b)所表示的化合物9.02g,收率83%;
[0067][0068]
s3:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(28b)所表示的化合物7.24g,其它合成过程同实施例1,即可得到以下化学式(28)表示的化合物2.52g,收
率36%;
[0069][0070]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为697.6698;核磁δ(ppm)=9.10(1h),8.47(1h),8.18(2h),7.95(1h),7.83(1h),7.75(2h),7.64(1h),7.50(2h),7.21(3h),7.12(1h),7.00(1h),6.87-6.94(4h),6.80(2h),6.31(1h),2.20(9h)。
[0071]
合成实施例5:合成化合物(33)
[0072]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为2-氯-9氢-咔唑(30mmol,6.05g),二苯胺替换为4,4'-二氰基二苯胺(30mmol,6.58g),其它合成过程同实施例1,即可得到以下化学式(33a)所表示的化合物8.56g,收率57%;
[0073][0074]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(33a)所表示的化合物5.01g,其它合成过程同实施例1,即可得到以下化学式(33)表示的化合物1.73g,收率34%;
[0075][0076]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为508.3561。
[0077]
合成实施例6:合成化合物(39)
[0078]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为2-氯-10氢-吩噻嗪(30mmol,7.01g),二苯胺替换为二(4-(叔丁基)苯基)胺(30mmol,8.44g),其它合成过程同实施例1,即可得到以下化学式(39a)所表示的化合物10.53g,收率59%;
[0079]
[0080]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(39a)所表示的化合物5.95g,其它合成过程同实施例1,即可得到以下化学式(39)表示的化合物1.87g,收率31%;
[0081][0082]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为602.6023。
[0083]
合成实施例7:合成化合物(46)
[0084]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为2-氯-9氢-咔唑(30mmol,6.05g)、3-溴咪唑并[1,2-a]吡啶替换为3-溴-7-苯基咪唑并[1,2-a]吡啶(35mmol,9.56g),二苯胺替换为9氢-咔唑(30mmol,5.02g),其它合成过程同实施例1,即可得到以下化学式(46a)所表示的化合物9.60g,收率61%;
[0085][0086]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(46a)所表示的化合物5.25g,其它合成过程同实施例1,即可得到以下化学式(46)表示的化合物1.86g,收率35%;
[0087][0088]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为532.4167。
[0089]
合成实施例8:合成化合物(49)
[0090]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为2-氯-9氢-咔唑(30mmol,6.05g),二苯胺替换为9,9-二甲基-9,10-二氢吖啶(30mmol,6.28g),其它合成过程同实施例1,即可得到以下化学式(49a)所表示的化合物9.57g,收率65%;
[0091][0092]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(49a)所表示的化合物4.91g,其它合成过程同实施例1,即可得到以下化学式(49)表示的化合物1.84g,收率37%;
[0093][0094]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为498.3928。
[0095]
合成实施例9:合成化合物(52)
[0096]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为2-氯-10氢-吩噁嗪(30mmol,6.53g),二苯胺替换为10氢-吩噁嗪(30mmol,5.50g),其它合成过程同实施例1,即可得到以下化学式(52a)所表示的化合物9.08g,收率63%;
[0097][0098]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(52a)所表示的化合物4.81g,其它合成过程同实施例1,即可得到以下化学式(52)表示的化合物1.66g,收率34%;
[0099][0100]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为488.3175。
[0101]
合成实施例10:合成化合物(58)
[0102]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为2-氯-5-苯基-5,10-二氢吩嗪(30mmol,8.78g),二苯胺替换为3,6-二氟-9氢-咔唑(30mmol,6.10g),其它合成过程同实施例1,即可得到以下化学式(58a)所表示的化合物10.36g,收率60%;
[0103][0104]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(58a)所表示的化合物5.76g,其它合成过程同实施例1,即可得到以下化学式(58)表示的化合物1.87g,收率32%;
[0105][0106]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为583.4043。
[0107]
合成实施例11:合成化合物(65)
[0108]
s1:将实施例1中s1中的的2,3-氯-5-氟-均三甲基苯胺替换为(2,3-二氯-5-氟苯基)萘-2-胺(30mmol,9.18g),二苯胺替换为9氢-咔唑(30mmol,5.02g),其它合成过程同实施例1,即可得到以下化学式(65a)所表示的化合物9.13g,收率55%;
[0109][0110]
s2:将实施例1中s2中的(7a)替换为本实施例上述(65a)所表示的化合物8.30g,10氢-吩噁嗪替换为二苯胺(20mmol,3.38g),其它合成过程同实施例1,即可得到以下化学式(65b)所表示的化合物g,收率81%;
[0111][0112]
s3:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(65b)所表示的化合物7.02g,其它合成过程同实施例1,即可得到以下化学式(65)表示的化合物2.50g,收率37%;
[0113][0114]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为675.6066;核磁δ(ppm)=9.04(1h),8.67(1h),8.47(1h),8.18(1h),7.98(2h),7.87(1h),7.70(1h),7.60(1h),7.47-7.54(6h),7.41(1h),7.38(1h),7.33(1h),7.20(1h),7.11(5h),7.01(1h),6.94(2h),6.25(1h),5.22(2h)。
[0115]
合成实施例12:合成化合物(70)
[0116]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为n-(2,3-二氯-5-硝基苯基)-9,9-二甲基-9氢-芴-2-胺(30mmol,11.98g),二苯胺替换为10氢-吩噻嗪(30mmol,5.98g),其它合成过程同实施例1,即可得到以下化学式(70a)所表示的化合物11.80g,收率58%;
[0117][0118]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(70a)所表示的化合物6.78g,其它合成过程同实施例1,即可得到以下化学式(70)表示的化合物2.28g,收率35%;
[0119][0120]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为651.5478;核磁δ(ppm)=9.02(1h),8.43(1h),8.19(1h),8.04(2h),7.98(1h),7.87(2h),7.75(1h),7.63(1h),7.51(1h),7.44(1h),7.38(1h),7.12-7.21(3h),7.02(2h),6.91(1h),6.25(1h),1.79(6h)。
[0121]
合成实施例13:合成化合物(73)
[0122]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为n-(2,3-二氯苯基)-2,
4,6-三甲基胺(30mmol,8.41g),二苯胺替换为n-(4-(叔丁基)苯基)二苯并呋喃-2-胺(30mmol,9.46g),其它合成过程同实施例1,即可得到以下化学式(73a)所表示的化合物10.74g,收率53%;
[0123][0124]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(73a)所表示的化合物6.75g,其它合成过程同实施例1,即可得到以下化学式(73)表示的化合物2.47g,收率38%;
[0125][0126]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为648.6126;核磁δ(ppm)=9.06(1h),8.45(1h),8.33(1h),8.05(1h),7.74(1h),7.61(1h),7.63(1h),7.43-7.51(3h),7.36(1h),7.25(1h),7.13(2h),6.95(2h),6.23(1h),6.14(2h),2.20(9h),1.35(9h)。
[0127]
合成实施例14:合成化合物(80)
[0128]
s1:将实施例1中s1中的2,3-氯-5-氟-均三甲基苯胺替换为2-氯-10氢-吩噁嗪(30mmol,6.53g),二苯胺替换为氮-(2,5-二甲基-[1,1'-联苯基]-4-基)萘-2-胺(30mmol,9.70g),其它合成过程同实施例1,即可得到以下化学式(80a)所表示的化合物10.61g,收率57%;
[0129][0130]
s2:将实施例1中s3中的(7b)所表示的化合物替换为本实施例上述(80a)所表示的化合物6.21g,其它合成过程同实施例1,即可得到以下化学式(80)表示的化合物2.08g,收率33%;
[0131][0132]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为628.5389;核磁δ(ppm)=9.02(1h),8.48(1h),7.84(1h),7.79(1h),7.70(1h),7.64(1h),7.54(2h),7.38-7.47(4h),7.30(2h),7.21(3h),7.15(1h),7.06(1h),6.98(1h),6.85(1h),6.77(1h),6.26(1h),2.47(3h),2.19(3h)。
[0133]
合成实施例15:合成化合物(81)
[0134]
将实施例1中的2,3-二氯-5-(10氢-吩噁嗪-10-基)-n-二苯胺替换为n-(2,3-二氯苯基)萘-2-胺(30mmol,8.65g),二苯胺替换为2,2-二萘胺(30mmol,8.08g),其它合成过程同实施例1,即可得到以下化学式(81a)所表示的化合物11.28g,收率59%;
[0135][0136]
将实施例1中(7a)所表示的化合物替换为本实施例上述(81a)所表示的化合物6.37g,其它合成过程同实施例1,即可得到以下化学式(81)表示的化合物2.32g,收率38%;
[0137][0138]
对所得化合物进行检测分析,结果如下:质谱仪maldi-tof-ms(m/z)为610.5306;核磁δ(ppm)=9.03(1h),8.44(1h),7.75-7.87(6h),7.61(1h),7.54(2h),7.49(3h),7.43(3h),7.38(2h),7.31(1h),7.26(1h),7.06(1h),7.01(2h),6.25(1h),6.14(2h)。
[0139]
器件实施例1
[0140]
将带有50nm ito透明薄膜的玻璃基板依次用丙酮、异丙醇和去离子水各超声清洗10min,105℃下真空干燥2h,然后进行uv臭氧洗涤15min,即将ito玻璃基板传送至真空蒸镀机。
[0141]
在形成有ito薄膜一侧的面上,真空蒸镀4,4',4
”‑
三[2-萘基(苯基)氨基]三苯胺(2t-nata),以形成80nm厚的空穴注入层;
[0142]
下一步,在上述空穴注入层上,真空蒸镀n,n'-二苯基-n,n'-(1-萘基)-1,1'-联苯-4,4'-二胺(npb),以形成30nm厚的空穴传输层;
[0143]
下一步,在上述空穴传输层上,真空蒸镀上述合成实施例1中所制备的化合物7,以
形成30nm厚度的发光层;
[0144]
下一步,在上述发光层上,真空蒸镀双(2-甲基-8-羟基喹啉-n1,o8)-(1,1'-联苯-4-羟基)铝(balq),以形成10nm厚度的空穴阻挡层;
[0145]
下一步,在上述空穴阻挡层上,真空蒸镀8-羟基喹啉铝(alq3),以形成20nm厚度的电子传输层;
[0146]
最后,在上述电子传输层上,真空蒸镀铝(al),以形成100nm的阴极。
[0147]
器件实施例2至器件实施例15
[0148]
按照与器件实施例1相同的方法制备有机电致发光器件,不同的是分别使用上述合成实施例2至合成实施例15中所合成的化合物替换上述合成实施例1中所制备的化合物7。
[0149]
对上述各器件实施例所制备的有机电致发光器件进行性能测试,结果如表1所示:
[0150]
表1
[0151]
[0152][0153]
从上表1的数据可看出,本发明提供的以咪唑并吡啶与芳胺、咔唑、吖啶等基团环氮键接构成主体,并利用硼对主体中心进行修饰所构成的化合物,具有刚性大共轭结构,双极性咪唑并吡啶基团可以对化合物供电性与受电性进行调节,同时使得化合物homo降低,因此化合物材料可以实现稳定、高效的深蓝光发射,使用本发明化合物作为发光层材料所制备的有机电致发光器件,制备简单高效,在驱动电压、电流效率、光色及寿命方面获得了显著进步。
[0154]
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
