1.本发明属于荧光分析检测技术领域,具体涉及一种荧光探针,更具体地说,本发明涉及一种硫脲基修饰的芘衍生物荧光探针及其制备方法和应用。
背景技术:
2.近年来,随着工业和生物医药领域的快速发展,阴、阳离子作为构成自然界和现代工农业发展不可缺少的资源,极大的促进了人类社会的发展,但是过量的阴、阳离子会造成环境污染,动植物患病或者死亡,另一方面会通过食物链聚集在人体中,损害人类身心健康。因此开发出便捷快速的方法来检测阴、阳离子具有非常重要的价值。
3.传统检测以上这些物质的方法有分子印迹法、纳米颗粒法、高效液相色谱法、质谱法、电化学方法等,但这些方法都要借助复杂昂贵的仪器,成本较高,并且样品的前处理过程繁琐且要求高,存在不易实时监测等缺陷。相比之下,人们更倾向于利用成本较低、操作简便、灵敏度高的化学传感器来达到相同的检测目的。其中,荧光探针可将分子识别转变为可探测的荧光信号,具有选择性好、灵敏度高、易操作等优点,成为检测上述目标物质的热门工具。
4.芘作为一种常见的,结构易修饰的荧光团,具有高消光系数、寿命长、高能量激发单纯态等特点。它们的衍生物具有超分子结构组装性能以及易形成激基缔合物的特点,可以作为聚集现象所普及的典型荧光探针,并且具有独特的高疏水性、高灵敏度、高荧光量子产率、对微环境的变化极其敏感等特点。因此,选择将芘或芘的衍生物作为荧光团,设计并开发出可快速、高效、灵敏地检测出金属离子或有毒的阴离子等的荧光分子探针,并成功应用于实际检测中,这对我们进一步监测环境,维持环境的可持续发展具有重要意义。
5.基于上述理由,特提出本技术。
技术实现要素:
6.针对上述现有技术存在的问题或缺陷,本发明的目的在于提供一种硫脲基修饰的芘衍生物荧光探针及其制备方法和应用。本发明利用紫外可见光谱和荧光光谱等分别对目标化合物进行研究,证实本发明提供的硫脲基修饰的芘衍生物荧光探针属于“off-on”型荧光探针,可特异性识别金属离子ag
+
或有毒的阴离子so
42-、cn-,且检出限低。
7.为了实现本发明的上述第一个目的,本发明采用的技术方案如下:
8.一种硫脲基修饰的芘衍生物荧光探针,结构式如下式一所示,其中:r为甲基或苯基
[0009][0010]
具体地,当所述r为时,目标化合物为2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺,结构式如下式二所示:
[0011][0012]
具体地,当所述r为时,目标化合物为2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺,结构式如下式三所示:
[0013][0014]
本发明的第二个目的在于提供上述所述硫脲基修饰的芘衍生物荧光探针的制备方法,所述方法步骤如下:
[0015]
将2-肼基-n-(芘-1-基)乙酰胺溶解在乙腈中,将所得混合溶液缓慢升温至60~70℃,然后在回流状态下向所述混合溶液中缓慢滴加异硫氰酸酯类化合物,滴加结束后,将反应体系继续在60~70℃回流条件下恒温反应5~7h;反应结束后,冷却,静置,抽滤,纯化,得到目标化合物。
[0016]
具体地,上述所述硫脲基修饰的芘衍生物荧光探针,其合成路线如下式四所示:
[0017]
其中r为甲基或苯基;
[0018]
进一步地,上述技术方案,所述2-肼基-n-(芘-1-基)乙酰胺与异硫氰酸酯类化合物的摩尔比为1:10~20,较优选为1:15。
[0019]
进一步地,上述技术方案,所述异硫氰酸酯类化合物为异硫氰酸甲酯或异硫氰酸苯酯。
[0020]
进一步地,上述技术方案,所述乙腈的用量可不做具体限定,只要能实现2-肼基-n-(芘-1-基)乙酰胺的完全溶解即可,例如所述2-肼基-n-(芘-1-基)乙酰胺与乙腈的用量可以为0.01摩尔份:(20~100)体积份,较优选为0.01摩尔份:(30~50)体积份,其中:所述摩尔份与体积份之间是以mol:ml作为基准的。
[0021]
进一步地,上述技术方案,所述恒温反应时间优选为6h。
[0022]
具体地,上述所述2-肼基-n-(芘-1-基)乙酰胺,结构式如下式五所示:
[0023][0024]
进一步地,上述技术方案,所述2-肼基-n-(芘-1-基)乙酰胺采用下述方法制得,步骤如下:
[0025]
(a)将1-氨基芘溶解在适量二氯甲烷中,并加入少量三乙胺作缚酸剂,得到混合液;然后在冰水浴条件下按配比向所得混合液中缓慢滴加氯乙酰氯,滴加完毕后,将反应体系在常温条件下反应10~14h;反应结束后,静置,抽滤,将所得滤渣重结晶,得到白色固体,即中间体2-氯-n-(芘-1-基)乙酰胺;
[0026]
(b)将步骤(a)获得的中间体2-氯-n-(芘-1-基)乙酰胺溶解在适量的1,4-二氧六环中,缓慢升温至25~35℃,在回流状态下将由水合肼和无水乙醇组成的混合溶液缓慢滴加到体系中,滴加结束后,将反应体系继续在回流、25~35℃条件下恒温反应4~8h;反应结束后,萃取有机相,干燥,将所得粗品纯化,得到所述的2-肼基-n-(芘-1-基)乙酰胺。
[0027]
具体地,上述步骤(a)中所述中间体2-氯-n-(芘-1-基)乙酰胺的合成路线如下式六所示:
[0028][0029]
具体地,上述步骤(b)中所述2-肼基-n-(芘-1-基)乙酰胺的合成路线如下式七所示:
[0030][0031]
进一步地,上述技术方案,步骤(a)中,所述1-氨基芘与氯乙酰氯的摩尔比为1:
(1.1~2),较优选为1:(1.4~1.6)。
[0032]
进一步地,上述技术方案,步骤(a)中,所述二氯甲烷的用量可不做具体限定,只要能实现1-氨基芘的完全溶解即可,例如所述1-氨基芘与二氯甲烷的用量可以为(0.1~0.3)摩尔份:100体积份,其中:所述摩尔份与体积份之间是以mol:ml作为基准的。
[0033]
进一步地,上述技术方案,步骤(a)中,所述三乙胺与1-氨基芘的质量比为(0.5~1):1。
[0034]
进一步地,上述技术方案,步骤(a)中,所述常温反应时间优选为12h。
[0035]
具体地,上述技术方案,步骤(a)中,所述常温是指四季中自然室温条件,不进行额外的加热或冷却处理,一般常温控制在10~30℃,最好是15~25℃。
[0036]
进一步地,上述技术方案,步骤(b)中,所述2-氯-n-(芘-1-基)乙酰胺与水合肼的用量比为(1~2)mmol:(5~15)ml。
[0037]
进一步地,上述技术方案,步骤(b)中,所述1,4-二氧六环的用量可不做具体限定,只要能实现2-氯-n-(芘-1-基)乙酰胺的完全溶解即可,例如所述2-氯-n-(芘-1-基)乙酰胺与1,4-二氧六环的用量可以为(1~2)摩尔份:(10~50)体积份,其中:所述摩尔份与体积份之间是以mmol:ml作为基准的。
[0038]
进一步地,上述技术方案,步骤(b)中,所述恒温反应时间为6h。
[0039]
进一步地,上述技术方案,步骤(b)中,所述水合肼和无水乙醇的体积比优选为1:1。
[0040]
本发明的第三个目的在于提供上述所述硫脲基修饰的芘衍生物荧光探针的应用。
[0041]
一方面,本发明提供了所述2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺在特异性识别污水或废水等中的有毒阴离子的应用。
[0042]
进一步地,上述技术方案,所述有毒阴离子为so
42-和/或cn-。
[0043]
另一方面,本发明还提供了所述2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺在特异性识别污水或废水等中阳离子的应用。
[0044]
进一步地,上述技术方案,所述阳离子为ag
+
。
[0045]
与现有技术相比,本发明具有如下有益效果:
[0046]
(1)本发明选用芘衍生物做荧光团,先将芘衍生物修饰成带活泼氨基结构的中间体,再引入硫脲基作为识别基团,合成了两种有机小分子荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺和2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺,并利用紫外可见光谱和荧光光谱等分别对所述有机小分子荧光探针进行研究,证实本发明提供的硫脲基修饰的芘衍生物荧光探针均属于“off-on”型探针,可特异性识别金属离子ag
+
或有毒的阴离子so
42-、cn-,且检出限低。
[0047]
(2)本发明制备的“off-on”型探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺识别so
42-和cn-,响应出蓝色荧光,检出限分别为4.84nm和10.01nm;且本发明制备的“on-off”型探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺特异性识别ag
+
,响应时蓝色荧光消失,检出限为0.55μm。此外,本发明采用的检测方法简单易操作,在监测污染水质中的阴、阳离子等方面具有潜在的应用价值。
附图说明
[0048]
图1中(a)、(b)依次为不同阴离子对实施例1制备的化合物2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的荧光和紫外光谱的影响对比图;
[0049]
图2中(a)、(b)依次为实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺+so
42-、实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺+cn-在各种竞争阴离子存在时的荧光强度对比图;
[0050]
图3为加入不同体积so
42-后实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的荧光滴定光谱对比图;
[0051]
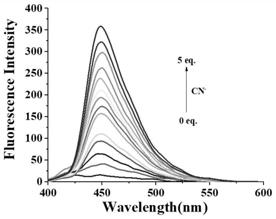
图4为加入不同体积cn-后实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的荧光滴定光谱对比图;
[0052]
图5为实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺和so
42-的job曲线图;
[0053]
图6中(a)、(b)依次为实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺和cn-的可逆性测试结果图、实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺和cn-的job曲线图;
[0054]
图7中(a)、(b)依次为不同阳离子对实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的荧光和紫外光谱的影响对比图;
[0055]
图8为实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺+ag
+
在各种竞争阳离子存在时的荧光强度对比图;
[0056]
图9为加入不同体积ag
+
后实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的荧光滴定光谱图;
[0057]
图10为实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺和ag
+
的job曲线图。
具体实施方式
[0058]
下面通过实施案例对本发明作进一步详细说明。本实施案例在以本发明技术为前提下进行实施,现给出详细的实施方式和具体的操作过程来说明本发明具有创造性,但本发明的保护范围不限于以下的实施案例。
[0059]
为了更好地理解本发明而不是限制本发明的范围,在本技术中所用的表示用量、百分比的所有数字、以及其他数值,在所有情况下都应理解为以词语“大约”所修饰。因此,除非特别说明,否则在说明书和所附权利要求书中所列出的数字参数都是近似值,其可能会根据试图获得的理想性质的不同而加以改变。各个数字参数至少应被看作是根据所报告的有效数字和通过常规的四舍五入方法而获得的。
[0060]
本发明合成的化合物的结构表征方法如下:
[0061]
(1)数字熔点测定仪
[0062]
采用上海仪电物理光学仪器有限公司wrs-3型数字熔点仪,测定化合物溶程。熔点测定范围:23~320℃,温度数显最小示值为0.1℃。
[0063]
(2)红外光谱(ir)
[0064]
采用日本shimadzu(岛津)公司,irtracer-100型傅立叶变换红外光谱仪测定化合
物的红外光谱,溴化钾压片,波谱范围400~4000cm-1
。
[0065]
(3)核磁共振谱(nmr)
[0066]
采用德国bruker(布鲁克)公司,av-400型核磁共振波谱仪测定化合物的核磁共振谱,溶剂为氘代氯仿(cdcl3),内标tms(四甲基硅烷),频率分别为400mhz(1h nmr)和100mhz(
13
c nmr)。
[0067]
(4)高分辨质谱(hrms)
[0068]
采用德国bruker(布鲁克)公司,microtof-q ii 10410型高分辨质谱仪测定化合物的质谱。
[0069]
下述各实施例中涉及的检出限和结合常数的计算方法如下:
[0070]
(1)检出限的计算
[0071]
检出限(lod)的计算公式如下:
[0072]
lod=3s/ka[0073]
其中s是测定10次同一探针样品的最大荧光强度或吸光度的标准偏差;ka是紫外可见或荧光浓度滴定实验中线性方程的斜率。
[0074]
(2)结合常数的计算
[0075]
荧光增强型的结合常数(k)根据benesi-hildebrand计算:
[0076]
计算公式如下:
[0077]
1/(a-a0)=1/{k(a
max-a0)[q]}+1/(a
max-a0)
[0078]
其中,a0是探针本身对应的吸光度,a是探针与目标检测物结合后对应的吸光度,a
max
是探针与目标检测物结合后对应的最大的吸光度,[q]是目标检测物的浓度,a是常数,k是结合常数。
[0079]
荧光淬灭型的结合常数(k)根据stern-volmer计算:
[0080]
计算公式如下:
[0081]
i0/(i
0-i)=1/a+1/(ka[q])
[0082]
其中,i0是探针本身对应的荧光强度,i是探针与目标检测物结合后对应的荧光强度,[q]是目标检测物的浓度,a是常数,k是结合常数。
[0083]
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。例如,本发明下述实施例中涉及的1-氨基芘可通过商购渠道获得,其cas号:1606-67-3。
[0084]
实施例1
[0085]
本实施例的硫脲基修饰的芘衍生物荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺,采用下述方法制得,步骤如下:
[0086]
(1)2-氯-n-(芘-1-基)乙酰胺的合成:
[0087]
将1-氨基芘(5.0g,0.23mol)溶解在100ml二氯甲烷中,并加入三乙胺(5ml)作缚酸剂,得到混合液;在冰水浴0℃下用恒压滴液漏斗缓慢向所述混合液中滴加氯乙酰氯(3.5g,0.35mol),滴加完毕后常温反应12h;反应结束后静置,得到白色固体沉淀,对其抽滤,取滤渣得粗品;再利用无水乙醇为溶剂对所得粗品进行重结晶,得到白色固体,即所述2-氯-n-(芘-1-基)乙酰胺,其产率为85%;
[0088]
(2)2-肼基-n-(芘-1-基)乙酰胺的合成:
[0089]
将步骤(1)所得化合物2-氯-n-(芘-1-基)乙酰胺(0.5g,1.7mmol)溶解在30ml的1,
4-二氧六环中,缓慢升温至30℃,在回流状态下用恒压滴液漏斗将10ml水合肼和10ml乙醇的混合溶液缓慢滴加到体系中,反应6h;反应结束后加入蒸馏水至体系,再加入乙酸乙酯、饱和食盐水萃取上层有机相,反复3次;经无水硫酸镁干燥后、旋转蒸发掉溶剂得淡黄色固体粗品;利用二氯甲烷/甲醇硅胶柱,采用梯度淋洗的方式纯化,得到淡黄色固体,即纯品2-肼基-n-(芘-1-基)乙酰胺,其产率为58%;
[0090]
(3)2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的合成:
[0091]
将步骤(2)获得的2-肼基-n-(芘-1-基)乙酰胺(2.9g,0.01mol)溶解在30ml乙腈中,缓慢升温至65℃,在回流状态下用恒压滴液漏斗缓慢滴加异硫氰酸甲酯(0.15mol),充分反应6h;反应结束后冷却静置,析出白色固体,对其抽滤,取滤渣得粗品;用乙醇/石油醚为溶剂重结晶纯化粗产物,得到白色粉末状目标化合物,其产率为57%,熔点为224.4-224.7。
[0092]
结构表征测试结果如下:
[0093]
本实施例制备的目标化合物的红外光谱峰值数据如下:
[0094]
3265-3172(c-n),3037-2926(c-h),1693(c=o)。
[0095]
本实施例制备的目标化合物的核磁共振氢谱数据如下:
[0096]
10.73(s,1h),8.48
–
7.94(m,9h),4.56(s,2h),3.07(qd,j=7.3,4.8hz,2h),1.18(t,j=7.3hz,3h).
[0097]
本实施例制备的目标化合物的核磁共振碳谱数据如下:
[0098]
166.29,131.42,131.27,130.91,129.12,127.82,127.69,127.35,126.98,125.89,125.59,125.49,124.80,124.59,124.28,123.82,122.60,45.98,43.91,8.99.
[0099]
由本实施例制备的目标化合物的高分辨质谱图可知,其分子量/分子离子峰/理论分子量依次为362.1201/385.1095(+na)/385.1099(+na)。
[0100]
综合上述数据可知,本实施例制备的目标化合物为2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺。
[0101]
实施例2
[0102]
本实施例的硫脲基修饰的芘衍生物荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺,采用下述方法制得,步骤如下:
[0103]
将实施例1步骤(2)获得的2-肼基-n-(芘-1-基)乙酰胺(2.9g,0.01mol)溶解在30ml乙腈中,缓慢升温至65℃,在回流状态下用恒压滴液漏斗缓慢滴加异硫氰酸苯酯(0.15mol),充分反应6h;反应结束后冷却静置,析出白色固体,对其抽滤,取滤渣得粗品,用乙醇/石油醚为溶剂重结晶纯化粗产物,得到白色粉末状目标化合物,其产率为55%,熔点为231.8-232.2。
[0104]
结构表征测试结果如下:
[0105]
本实施例制备的目标化合物的红外光谱峰值数据如下:
[0106]
3265-3172(c-n),3037-2926(c-h),1693(c=o)。
[0107]
本实施例制备的目标化合物的核磁共振氢谱数据如下:
[0108]
10.53(s,1h),8.44
–
8.04(m,9h),7.65(dt,j=8.7,1.8hz,2h),7.40
–
7.28(m,2h),7.23
–
7.08(m,1h),3.35(s,1h).
[0109]
本实施例制备的目标化合物的核磁共振碳谱数据如下:
[0110]
180.90,168.37,140.28,131.87,131.31,130.97,128.81,128.55,127.72,127.62,127.14,126.93,125.75,125.46,124.89,124.85,124.63,124.38,124.33,123.71,122.92,57.26.
[0111]
由本实施例制备的目标化合物的高分辨质谱图可知,其分子量/分子离子峰/理论分子量依次为424.1358/425.1433(+h)/425.1436(+h)。
[0112]
综合上述数据可知,本实施例制备的目标化合物为2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺。
[0113]
性能测试:
[0114]
(一)实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对不同阴离子的选择性测试:
[0115]
用超纯水分别配置50ml浓度为10-2
mol/l的阴离子标准液(f-、cl-、i-、clo
4-、no
3-、hso
4-、ch3coo-、cn-、scn-、no
2-、so
42-、h2po
4-)以及浓度为1
×
10
-5
mol/l的实施例1所得荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的二甲基亚砜纯溶液作为标准液备用。
[0116]
将上述荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的标准液与不同阴离子标准液按照体积比为1:5的比例配置成多个10ml的待测样品,用荧光分光光度计对其进行荧光光谱测量,用紫外可见分光光度计对其进行紫外光谱测量,以此确定探针可识别的目标物。如图1所示,加入硫酸根离子和氰根离子后,会使荧光开启,且明显增强但增强效果不同,而在相同条件下其他离子的体系荧光可忽略不计。
[0117]
(二)实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺特异性识别硫酸根离子和氰根离子的干扰性检测:
[0118]
用超纯水分别配置50ml浓度为10-2
mol/l的硫酸根离子和氰根离子标准液备用,配置浓度为1
×
10
-5
mol/l的实施例1所得荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的二甲基亚砜纯溶液作为标准液备用。将浓度为1
×
10
-5
mol/l的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的二甲基亚砜纯溶液和浓度为10-2
mol/l的硫酸根离子和氰根离子标准液按照体积比为1:5的比例配置成多个相同的待测样品,然后再分别引入其它相同量的阴离子标准液(f-、cl-、i-、clo
4-、no
3-、hso
4-、ch3coo-、cn-、scn-、no
2-、so
42-、h2po
4-),检测在不同阴离子存在下探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺识别硫酸根离子和氰根离子的抗干扰能力。在图2中,在已经存在探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺和被检测离子体系中分别引入不同的其它阴离子测试光谱,结果显示探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对硫酸根离子和氰根离子的识别能力不受其他阴离子的影响。
[0119]
(三)实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对不同硫酸根离子和氰根离子的滴定检测
[0120]
配置50ml浓度为10-2
mol/l的硫酸根离子和氰根离子的超纯水纯溶液和浓度为1
×
10
-5
mol/l的实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的二甲基亚砜纯溶液作为标准液备用。将不同体积(0-5当量)的硫酸根离子和氰根离子标准液加入至探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的标准液中,配置为不同浓度比例的待测溶液;对上述溶液分别进行荧光光谱和紫外光谱测量,以此确定探
针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对不同浓度的硫酸根离子和氰根离子的识别能力。
[0121]
如图3所示,横坐标是波长(nm),纵坐标是荧光强度,so
42-的占比从0升至5eq.,探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的荧光逐渐增强,并且在5当量时达到最高。荧光强度与so
42-浓度之间存在良好的线性关系(r2=0.99)。经计算,结合常数(k)为2.4
×
106m-1
,检出限低至4.84nm,实现了对so
42-的定量检测。
[0122]
在图4中,横坐标是波长(nm),纵坐标是荧光强度,cn-的占比从0升至5eq.,探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的荧光逐渐增强,并且在5当量时达到最高。荧光强度与cn-浓度之间存在良好的线性关系(r2=0.99)。经计算,结合常数(k)为1.35
×
106m-1
,检出限低至10.01nm,实现了对cn-的定量检测。
[0123]
(四)实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺与硫酸根离子和氰根离子的络合比测试:
[0124]
配置50ml浓度为10-2
mol/l的硫酸根离子和氰根离子的超纯水纯溶液和浓度为1
×
10
-5
mol/l的实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的二甲基亚砜纯溶液作为标准液备用。将探针标准液与硫酸根离子和氰根离子标准液按照体积比1:0至1:10的配比分别配置不同比例的溶液;对上述溶液分别对其进行荧光光谱和紫外光谱测量,以此确定探针对硫酸根离子和氰根离子的配位比例。在图5中结果显示,当so
42-的占比为0.5时出现转折点。由此说明,在反应的最初阶段,探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺与so
42-的结合比为1:1。在图6(b)中结果显示,当cn-的占比为0.5时出现转折点。由此说明,在反应的最初阶段,探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺与so
42-的结合比为1:1。
[0125]
(五)实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对氰根离子的可逆性检测:
[0126]
配置50ml浓度为10-2
mol/l的硫酸根离子和氰根离子的超纯水纯溶液和浓度为1
×
10
-5
mol/l的实施例1制备的荧光探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的二甲基亚砜纯溶液作为标准液备用。在探针-cn-梯子体系中加入适量的h
+
,对其进行荧光光谱和紫外光谱测量;同一体系中再次引入等量的氰根离子,再次进行荧光光谱和紫外光谱测量;反复多次,以此确定探针对氰根离子的可逆性识别能力。
[0127]
图6(a)为加入h
+
后,探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对cn-的响应变化,加入cn-荧光开启;再加入等量的h
+
后,荧光关闭;再加入等量的cn-后,荧光再次开启;反复几次,荧光图谱如图6(a)所示。这是由于cn-与h
+
的结合能力大于与探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的配位能力,表明探针2-(2-(甲基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺可以作为用于检测cn-的化学可逆探针。
[0128]
(六)实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对不同金属离子的选择性
[0129]
用超纯水配置50ml浓度为10-2
mol/l的金属离子标准液(na
+
、k
+
、ca
2+
、zn
2+
、mg
2+
、fe
3+
、al
3+
、ni
2+
、sn
2+
、pb
2+
、hg
2+
、cr
2+
、ag
+
、co
2+
、mn
2+
、cu
2+
、ba
2+
、fe
2+
、cu
+
)以及浓度为1
×
10
-5
mol/l的实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的n,n-二甲基甲酰胺纯溶液作为标准液备用。
[0130]
将探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的标准液与不同金属离子标准液按照体积比为1:5的比例配置成多个10ml的待测样品,用荧光分光光度计对其进行荧光光谱测量,用紫外可见分光光度计对其进行紫外光谱测量,以此确定探针可识别的目标物。如图7(a)所示,加入银离子后,会使荧光大幅度降低,而在相同条件下其他离子的体系荧光可忽略不计。如图7(b)所示,当在体系中加入各种各样的金属离子时,体系的吸收光谱均无明显变化。
[0131]
(七)实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺特异性识别银离子的干扰性检测:
[0132]
用超纯水配置50ml浓度为10-2
mol/l的金属离子标准液(na
+
、k
+
、ca
2+
、zn
2+
、mg
2+
、fe
3+
、al
3+
、ni
2+
、sn
2+
、pb
2+
、hg
2+
、cr
2+
、ag
+
、co
2+
、mn
2+
、cu
2+
、ba
2+
、fe
2+
、cu
+
)以及浓度为1
×
10
-5
mol/l的实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的n,n-二甲基甲酰胺纯溶液作为标准液备用。将荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的n,n-二甲基甲酰胺纯溶液和银离子标准液按照体积比为1:5的比例配置成多个相同的待测样品(10ml),然后再分别引入其它相同量的金属离子标准液,检测在不同金属离子存在下探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺识别银离子的抗干扰能力。从图8中可以看出探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对银离子的识别能力不受其他金属离子的影响,具有良好的抗干扰能力。
[0133]
(八)实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对不同银离子的滴定检测
[0134]
用超纯水配置50ml浓度为10-2
mol/l的银离子标准液备用,配置浓度为1
×
10
-5
mol/l的实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的n,n-二甲基甲酰胺纯溶液作为标准液备用。将不同体积(0-5当量)的银离子标准液加入至探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的标准液中,配置为不同浓度比例的待测溶液;对上述溶液分别进行荧光光谱和紫外光谱测量,以此确定探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺对不同浓度的银离子的识别能力。
[0135]
在图9中,横坐标是波长(nm),纵坐标是荧光强度,ag
+
的占比从0升至5当量,探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的荧光逐渐减弱,并且在5当量时降到最低。荧光强度与ag
+
浓度之间存在良好的线性关系(r2=0.99)。经计算,结合常数(k)为1.6
×
106m-1
,检出限低至0.55μm,实现了对ag
+
的定量检测。
[0136]
(九)实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺与银离子的络合比测试:
[0137]
用超纯水配置50ml浓度为10-2
mol/l的银离子标准液备用,配置浓度为1
×
10
-5
mol/l的实施例2制备的荧光探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺的n,n-二甲基甲酰胺纯溶液作为标准液备用。将探针标准液与银离子标准液按照体积比为1:0至1:10的配比分别配置不同比例的溶液;对上述溶液分别对其进行荧光光谱和紫外光谱测量,以此确定探针对银离子的配位比例。在图10中结果显示,当ag
+
的占比约为0.66时出现转折点。由此说明,在反应的最初阶段,探针2-(2-(苯基氨基甲硫酰基)肼基)-n-(芘-1-基)乙酰胺与ag
+
的结合比为2:1。
