:
1.本发明属于汞离子细胞内成像纳米探针的制备与应用领域,具体涉及一种荧光标记适配体金属有机框架探针的制备方法及其在汞离子细胞内成像的应用。
背景技术:
2.随着国民经济增长,环境污染在全世界越来越严重,此现状引起了相关部门的高度重视。其中,重金属污染对居民健康以及公共安全的危害日益显现。汞是一种具有蓄积性和多亲和性的重金属元素,其在体内的过量蓄积可导致人体免疫系统、血液系统、神经系统以及生殖系统的严重损害,甚至具有致癌性。我国现已将汞污染纳入国家环境保护重点防控内容之一。因此,研究发展重金属汞污染物的体外以及细胞内的检测方法,对于汞离子污染的防控具有重要的意义。
3.目前汞污染物的检测方法主要有原子吸收分光光度法、原子荧光光谱法、电感耦合等离子体发射光谱法等。这些方法大多需要配备昂贵的设备和耗材,且所检测样品需要经过复杂的前处理来消除其他的干扰物。除此之外,它们还需要技术人员在专门的实验室进行监测分析。因此,开发快速、简便且灵敏度高的汞污染物检测方法是非常必要的。
4.适配体是短的单链寡核苷酸(dna或rna),它们可以通过与特异的目标结合,形成三级结构。适配体具有许多优点,例如制造成本低、无批次间的变异、拥有更高的可重复性、更好的热稳定性等。如:富t链在汞离子存在的情况下,可以与汞离子形成t-hg
2+-t错配结构,实现对汞离子的识别。利用这个特异性反应原理作为荧光探针构建的理论基础,就可设计出一种具有高特异性的荧光探针用于汞离子的识别。但由于适配体本身属于寡核苷酸链,容易降解,且其自身所带的负电荷限制了它进入细胞内发挥作用。
5.金属有机框架作为近年来新兴的一种纳米材料,由于其易于合成、高比表面积、低细胞毒性等特点受到了广泛的关注。它不仅可以保护dna链不受降解,还可以作为载体运输适配体进入细胞内。我们通过dna的磷酸骨架与zr-mofs上的锆不饱和位点相结合,使处于猝灭状态的t20/a10附载在zr-mofs上,合成了汞离子细胞内成像探针。
6.基于上述的思考,本项目建立了一种新型细胞内汞离子成像的荧光探针,为汞污染检测技术的研发提供实验依据,为细胞内汞离子污染的监测提供新思路和新技术平台。我们在t20的3’端修饰amca荧光基团,并设计与其配对且在5’端修饰dabcyl猝灭基团的a10,体外构建t20/a10杂交双链,使amca荧光基团处于猝灭状态。而由于t-hg
2+-t之间的作用力大于a-t之间的作用力,富t链更倾向于与汞离子形成t-hg
2+-t错配结构。因此,在有汞离子存在的情况下,可以实现荧光探针的荧光信号从无到有,并与汞离子的浓度呈线性相关,用于检测待测物中汞离子浓度的变化趋势。在信号探针的制备上,将金属有机框架zr-mofs与t20/a10进行孵育结合。荧光信号探针可以通过胞吞等作用进入细胞内部。在细胞内磷酸根离子的竞争结合下,t20/a10从zr-mofs表面游离出来。t20与汞离子形成“t-hg
2+-t”错配结构,导致荧光基团amca远离猝灭基团dabcyl,使荧光信号恢复。最终实现对细胞内汞离子的成像。
技术实现要素:
7.1.本发明的目的是用于重金属汞离子污染的细胞内成像的荧光探针的制备方法与应用,为汞污染检测技术的研发提供实验依据,为细胞内汞污染的监测提供新思路和新技术平台。其特征包括以下步骤:
8.(1)zr-mofs和t20/a10双链的制备;
9.(2)建立细胞内成像荧光探针,测定重金属汞离子,绘制标准曲线;
10.(3)细胞内汞离子的荧光成像。
11.2.本发明所述zr-mofs-t20/a10荧光探针的制备过程具体包括以下步骤,其特征包括以下步骤:
12.(1)zr-mofs纳米材料的制备:
13.将48mg对苯二甲酸和67.2mg四氯化锆各分散在12ml的dmf溶液中,得到澄清溶液。将两者混合后再加入16ml dmf溶液,然后边搅拌边加入2ml醋酸。在90℃油浴中加热12小时后得到zr-mofs溶液,取出冷却至室温。以10000rpm/min离心5min,使用无水乙醇离心清洗3次后,真空干燥过夜,得到白色固体状zr-mofs纳米材料。
14.(2)t20/a10 dna的制备:
15.将t20 dna与a10 dna分别分散在tris-hcl中,然后以摩尔浓度比1:1.5的比例混合。将混合物放在95℃的水浴锅中加热10min后,置于室温放置1小时,使t20/a10双链充分杂交。
16.(3)zr-mofs-t20/a10荧光探针的制备:
17.将1mg的zr-mofs加入10ml的超纯水中,超声5分钟,得到100ug/ml的zr-mofs溶液。然后将其与100nm双链dna共孵育1小时,得到zr-mofs-t20/a10荧光探针。用tris-hcl溶液离心清洗三次后,重悬于1ml tris-hcl溶液中,储存在4℃备用。
18.3.根据权利要求1所述的建立荧光生物探针,进行细胞内重金属汞离子成像,得到共聚焦荧光成像图,其特征在于包括以下步骤:
19.(1)将细胞爬片置于24孔板孔内,然后将消化后的hela以每孔约5万个细胞的细胞浓度,将细胞悬液加到24孔板中,置于37℃的co2培养箱中,孵育12小时。
20.(2)制备不同浓度的hg
2+
溶液,并将其加入到24孔板中,置于37℃的co2培养箱中,孵育12小时。
21.(3)将含有不同浓度hg
2+
的培养基弃去,使用pbs清洗1-2次。
22.(4)将提前制备好的荧光探针离心清洗3次,用1ml dmem培养基重悬,加到24孔板中,置于37℃的co2培养箱中,孵育3小时。
23.(5)取出24孔板并弃去培养基,使用pbs清洗1-2次,加入300μl多聚甲醛固定15分钟后,用pbs清洗三次,每次在摇床上震荡5分钟。
24.(6)在载玻片上滴加绿豆大小甘油,将清洗后的爬片从孔中取出,细胞面朝下覆于甘油上,然后在爬片四个角处涂抹透明指甲油固定。
25.(7)将固定爬片的载玻片置于共聚焦显微镜的载物台上,调整焦距至可以看清细胞。
26.(8)调整共聚焦显微镜发射波长至350nm处,收集400nm-550nm(蓝光区域)的荧光信号。
27.(9)根据所得的共聚焦显微镜荧光信号结果与重金属汞离子浓度之间的关系,制作共聚焦显微镜图,并绘制工作曲线。
28.与现有技术相比,本发明是一种定量检测重金属汞离子的细胞内成像荧光探针的制备方法与应用,其突出的特点是:
29.(1)将基于zr-mofs的纳米复合材料引入到细胞成像荧光探针的制备中,它的高比表面积大大提高了dna双链的固载量,同时它作为载体,成为探针进入细胞内不可缺少的一部分;
30.(2)通过利用t20适配体的特异识别功能,不仅作为汞离子细胞成像荧光探针构建的基础,并且确保了重金属汞离子检测的特异性;
31.(3)本方法制备的细胞成像荧光探针可为重金属汞离子提供新的定性定量检测思路,旨在为汞污染检测技术的研发提供实验依据,为细胞中汞污染的监测提供新思路和新技术平台。
32.(4)使用完全相同的纳米材料和修饰方法,只需通过改变适配体的类型即可实现多种金属离子检测的特异性,高灵敏检测,另外,此方法简便,快速,便于实现商品化,推进重金属污染物检测的发展。
附图说明:
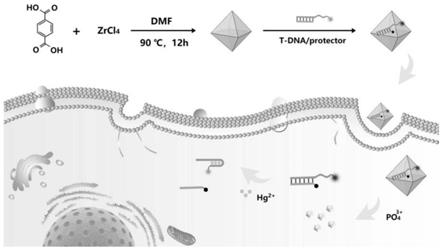
33.图1为本发明荧光探针的作用示意图。
34.图2为本发明荧光探针的扫描电镜图和电位图。
35.图3为本发明荧光探针在检测重金属汞离子时得到的荧光信号与汞离子浓度的线性关系,以及传感器的特异性。
36.图4为本发明荧光探针对不同浓度的汞离子的细胞内成像共聚焦图。
具体实施方式:
37.下面结合具体实施例对本发明进行进一步阐述,应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。
38.实施例1
39.步骤1.将48mg对苯二甲酸和67.2mg四氯化锆各分散在12ml的dmf溶液中,得到澄清溶液。将两者混合后再加入16ml dmf溶液,然后边搅拌边加入2ml醋酸。在90℃油浴中加热12小时后得到zr-mofs溶液,取出冷却至室温。以10000rpm/min离心5min,使用无水乙醇离心清洗3次后,真空干燥过夜,得到白色固体状zr-mofs纳米材料;
40.步骤2.将t20 dna与a10 dna分别分散在tris-hcl中,然后以摩尔浓度比1:1.5的比例混合。将混合物放在95℃的水浴锅中加热10min后,置于室温放置1小时,使t20/a10双链充分杂交;
41.步骤3.将100μg/ml zr-mofs与100nm双链dna混合,常温孵育1小时,得到混合物;
42.步骤4.将得到的混合物用tris-hcl溶液离心清洗3次后,重悬于1ml tris-hcl溶液中,储存在4℃备用;
43.步骤5.将细胞以5万个/孔的浓度接种于含有爬片的24孔板中,在37℃、5%co2、饱和湿度的细胞培养箱中培养12h;
44.步骤6.将不同浓度的hg
2+
加入到步骤5的24孔板中,在37℃、5%co2、饱和湿度的细胞培养箱中培养12h;
45.步骤7.将步骤4的探针离心后用dmem培养基超声重悬,加入到步骤6的24孔板中,在37℃、5%co2、饱和湿度的细胞培养箱中培养2h;
46.步骤8.弃去步骤7的24孔板中的培养基,用磷酸盐缓冲液冲洗三次;
47.步骤9.在步骤8的24孔板中加入300μl/孔多聚甲醛,孵育15min,以固定细胞形态;
48.步骤10.弃去步骤9的24孔板中的多聚甲醛,并使用磷酸盐缓冲液冲洗三次;
49.步骤11.滴加绿豆大小的甘油于载玻片上,将爬片的细胞面覆盖于甘油上,然后在爬片四周刷上封片油;
50.步骤12.将步骤11中制备好的样本用激光共聚焦显微镜进行拍摄成像,用350nm激发光照射,收取400nm-500nm范围内的荧光信号;
51.以上所述仅是本发明的优选实施方式,应当指出的是,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提条件下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
