用于预测对vx-001的应答的标志物的组合
技术领域
1.本发明涉及抗癌免疫疗法领域,更具体地涉及抗肿瘤疫苗接种领域。
背景技术:
2.癌症患者的总体状态通过常规血液检查进行评估,这些检查包括ldh谷氨酰胺(乳酸脱氢酶)、ggt(γ谷氨酰胺转移酶)、alp(碱性磷酸酶)、肝功能和炎症的标志物的水平,和/或能够确定中性粒细胞和淋巴细胞的绝对数量及其之间的比例的血细胞计数以及血小板计数。
3.已知这些常数是癌症患者的预后标志物,总体状态恶化的患者的生活预后较差。研究还表明,这可能会影响对某些治疗的应答,特别是免疫检查点抑制剂,免疫检查点抑制剂是近年来开发的物质,彻底改变了某些癌症的管理(ferrucci等人,annals oncol.[肿瘤学年鉴]2016)。
[0004]
提供抗癌免疫疗法以刺激细胞毒性t淋巴细胞(ctl)识别源自肿瘤抗原的肽,这些抗原由i类人白细胞抗原(hla-i)呈递在肿瘤细胞表面。根据它们对hla分子的亲和力,ctl靶向的肽可能是优势的或隐蔽的。
[0005]
肿瘤相关抗原(taa)经常由肿瘤细胞和正常组织两者表达,这与新抗原相反,新抗原是肿瘤特异性的,而且通常是患者特异性的。与新抗原相反,taa的优点是由许多肿瘤表达,但缺点是受耐受机制的影响,该耐受机制阻止自身免疫,即个体免疫系统识别自身抗原。
[0006]
端粒酶逆转录酶(tert)是一种参与肿瘤细胞永生化的酶,是许多肿瘤(85%的肿瘤)表达的taa型抗原。为了解决免疫系统对taa的耐受性问题,同时靶向肿瘤广泛表达的抗原,发明人提供了靶向隐蔽的tert肽的疫苗(vx-001),也就是说,tert肽对hla-a*0201分子(这是最常在人中表达的cmh-i分子)具有低亲和力并形成不稳定的肽/hla-i复合物(tourdot s.等人,2000,menez-jamet j.等人,2016)。鉴于对hla-i的亲和力与免疫原性之间的强相关性,这种隐蔽肽自然不具有免疫原性。为了用作针对癌症的疫苗,这种隐蔽肽已被优化以增强其免疫原性。
[0007]
因此,vx-001是抗肿瘤治疗性疫苗,由两种具有九个氨基酸的肽构成:由肿瘤细胞表达的天然隐蔽肽tert572(rlffyrksv,seq id no.1)及其优化变体tert572y(ylffyrksv,seq id no.2)。这两种肽分开施用,每种都与佐剂montanide(高度纯化的矿物油(drakeol 6vr)和表面活性剂(甘露醇单油酸酯)的混合物)一起。tert572y是免疫原性的优化的肽,用于前两次疫苗接种,以触发强烈的免疫应答。天然肽tert572在随后的疫苗接种步骤中施用,以便从tert572y刺激的所有t淋巴细胞中选择对天然tert572具有最高特异性的那些,天然tert572存在于与hla-a*0201相关的肿瘤细胞的表面。
[0008]
最近在一项随机iib期临床试验(vx-001-201)中,vx-001已在转移性或复发性i-iii期nsclc(非小细胞肺癌)患者中进行了测试。该试验中的疫苗方案包括以3周间隔的6次疫苗接种(2次疫苗接种tert572y,然后4次疫苗接种tert572),然后每12周加强(使用
tert572)直到疾病进展(georgoulias等人,clin lung cancer[临床肺癌].2013)。
[0009]
患者具有表达的hla-a*0201并患有表达tert的肿瘤。该研究的主要目标是跟踪总生存。这项研究的结果总体上没有统计学意义。然而,vx-001在某些患者中显示出显著的有效性。发明人因此研究了某些血液常数是否可能与对疫苗的临床应答或缺乏应答有关。该研究对患者进行了分层,其中鉴定了vx-001疫苗接种被证明具有统计学益处的患者的类别。
技术实现要素:
[0010]
发明人已表明抗肿瘤疫苗vx-001为具有正常ggt水平和/或正常ldh水平的患者提供了统计学上显著的益处,具有正常ggt和ldh水平的患者对治疗应答特别好。更精细的分层显示,患有非鳞状肿瘤的男性患者对治疗应答特别好。
[0011]
本发明因此涉及vx-001在具有正常γ谷氨酰胺转移酶(ggt)水平和/或正常乳酸脱氢酶(ldh)水平的hla-a*0201患者中,优选在患有非鳞状肿瘤的男性患者中治疗表达端粒酶逆转录酶(tert)的肿瘤的方法中的用途。
[0012]
本发明还涉及一种用于在体外确定患有表达tert的肿瘤的hla-a*0201患者是否可能对用vx-001进行抗癌疫苗接种产生有利应答的方法,该方法包括测量患者的ggt和ldh水平,如果这些水平中的至少一个是正常的,则患者对vx-001可能有利应答。
附图说明
[0013]
图1:具有正常ldh血清水平的患者的os和ttf。粗灰色曲线:接受过vx-001的患者;细黑色曲线:接受过安慰剂的患者。
[0014]
图2:具有正常ggt血清水平的患者的os和ttf。粗灰色曲线:接受过vx-001的患者;细黑色曲线:接受过安慰剂的患者。
[0015]
图3:具有正常alp血清水平的患者的临床应答。粗灰色曲线:接受过vx-001的患者;细黑色曲线:接受过安慰剂的患者。
[0016]
图4:对vx-001的临床应答和中性粒细胞的绝对数量。粗灰色曲线:接受过vx-001的患者;细黑色曲线:接受过安慰剂的患者。
[0017]
图5:对vx-001的临床应答以及中性粒细胞和淋巴细胞之间的比例。粗灰色曲线:接受过vx-001的患者;细黑色曲线:接受过安慰剂的患者。
[0018]
图6:对vx-001的临床应答和血小板数量。粗灰色曲线:接受过vx-001的患者;细黑色曲线:接受过安慰剂的患者。
[0019]
图7:具有正常ldh和ggt血清水平的患者的os和ttf。粗灰色曲线:接受过vx-001的患者;细黑色曲线:接受过安慰剂的患者。
[0020]
图8:具有正常ldh和ggt血清水平的患者亚组的生存的分析。nsq:非鳞状肿瘤。sq:鳞状肿瘤。or:对化疗的客观缓解。sd:疾病稳定。ecog:“美国东部肿瘤协作组(eastern cooperative oncology group)”功能指数。
[0021]
图9:具有正常ldh和ggt血清水平的患者的ttf(至治疗失败的时间)的分析。nsq:非鳞状肿瘤。sq:鳞状肿瘤。or:对化疗的客观缓解。sd:疾病稳定。ecog:“美国东部肿瘤协作组(eastern cooperative oncology group)”功能指数。
[0022]
图10:体现所研究的标志物组合的影响的患者生存。粗灰色曲线:接受过vx-001的患者;细黑色曲线:接受过安慰剂的患者。
[0023]
图11:体现由til(肿瘤浸润淋巴细胞)浸润和pd-l1表达定义的肿瘤免疫原性的影响的患者生存。灰色曲线:接受过vx-001的患者;黑色曲线:接受过安慰剂的患者。
[0024]
图12:体现由til(肿瘤浸润淋巴细胞)浸润和pd-l1表达定义的肿瘤免疫原性的影响的患者ttf。灰色曲线:接受过vx-001的患者;黑色曲线:接受过安慰剂的患者。
[0025]
图13:体现所研究的标志物的影响的其肿瘤为非免疫原性或免疫原性的患者的生存。ldh/ggt unl=ldh/ggt小于正常上限
[0026]
图14:体现所研究的标志物的影响的其肿瘤为非免疫原性或免疫原性的患者的ttf。ldh/ggt unl=ldh/ggt小于正常上限
具体实施方式
[0027]
本发明基于患者类别的鉴定,对于这些患者而言,vx-001-201研究结果表明vx-001疫苗接种显著有益。
[0028]
对于每个患者类别(如下所述),本发明涉及vx-001治疗表达tert的肿瘤的用途。
[0029]
对于这些患者类别中的每一个,本发明还涉及seq id no.2的tert572y肽诱导针对序列seq id no.1的隐蔽表位tert572的ctl应答的用途。
[0030]
对于这些患者类别中的每一个,本发明还涉及序列seq id no.1的肽tert572维持由预先施用给患者的seq id no.2的肽tert572y诱导的ctl应答的用途。
[0031]
如以下实验部分所示,第一类别的患者由患有表达tert的肿瘤并具有正常乳酸脱氢酶(ldh)水平的hla-a*0201患者组成。
[0032]
另一类别的可能对vx-001疫苗接种有利应答的患者由患有表达tert的肿瘤并具有正常γ谷氨酰胺转移酶(ggt)水平的hla-a*0201患者组成。
[0033]
患有表达tert的肿瘤并同时具有正常ggt水平和正常ldh水平的hla-a*0201患者构成了一类特别可能对vx-001疫苗接种产生有利应答的患者。
[0034]“正常ggt水平”和“正常ldh水平”是指低于由每个实验室根据该实验室使用的技术实施和试剂定义的正常上限(unl)的水平。鉴定水平是否正常对于本领域技术人员来说并不困难。
[0035]
本发明因此涉及vx-001在具有正常ggt水平和/或正常ldh水平的hla-a*0201患者中治疗表达tert的肿瘤的用途。
[0036]“治疗”在此是指至少减缓肿瘤的进展和/或延长患者的生存。
[0037]
根据本发明的具体实施方式,在接受至少一个化疗之后,将vx-001施用于具有正常ggt水平和/或正常ldh水平的患者。因此,vx-001是针对一线化疗进一步施用。
[0038]
根据本发明的另一个具体实施方式,将vx-001施用于患有非小细胞肺癌(nsclc)例如转移性或复发性nsclc的患者,所述患者具有正常ggt水平和/或正常ldh水平。
[0039]
发明人还表明,在具有正常ggt水平和/或正常ldh水平的患者中,男性对vx-001疫苗接种的应答在统计学上好于女性。
[0040]
根据本发明的另一个具体实施方式,因此将vx-001施用于具有正常ggt水平和/或正常ldh水平的男性患者。
[0041]
同样,vx-001-201研究的结果表明,vx-001在治疗非鳞状肿瘤方面比鳞状肿瘤在统计学上更有效。
[0042]
根据本发明的另一个具体实施方式,因此将vx-001施用于患有非鳞状肿瘤的具有正常ggt水平和/或正常ldh水平的患者。
[0043]
根据本发明的另一个具体实施方式,将vx-001施用于具有正常ggt水平和/或正常ldh水平的小于65岁的患者。
[0044]
根据本发明的另一个具体实施方式,将vx-001施用于具有正常ggt水平和/或正常ldh水平并且其癌症在化疗后不再进展的患者,例如在一线化疗后不再进展的患者。
[0045]
根据本发明的另一个具体实施方式,将vx-001施用于具有正常ggt水平和/或正常ldh水平且ecog得分为0的患者。
[0046]
vx-001-201研究的结果还表明,正常ldh和ggt血清水平与具有非免疫原性肿瘤的患者的更长生存和更长ttf相关。“非免疫原性肿瘤”在此是指以下肿瘤,该肿瘤不表达pd-l1分子(也就是说,如果至少1%的肿瘤细胞表达pd-l1:肿瘤比例得分《1%)和/或该肿瘤没有被淋巴细胞浸润(也就是说,当肿瘤浸润淋巴细胞或til完全不存在或数量很少时)。
[0047]
根据本发明的另一个具体实施方式,因此将vx-001施用于具有正常ggt水平和/或正常ldh水平并且其肿瘤不表达pd-l1分子和/或不被淋巴细胞浸润的患者。
[0048]
本发明还涉及一种用于在体外确定患有表达tert的肿瘤的hla-a*0201患者是否可能对用vx-001的抗癌治疗性疫苗接种产生有利应答的方法,该方法包括从来自所述患者的生物样品测量所述患者的ggt水平和ldh水平的步骤;根据这种方法,如果这些水平中的至少一个水平正常,则认为患者可能对抗癌疫苗接种产生有利应答,如果患者的ggt和ldh水平都正常,则情况更是如此。
[0049]
根据本发明的方法,认为如果肿瘤是非免疫原性的,也就是说如果它不表达pd-l1分子和/或没有被淋巴细胞浸润,则患者对用vx-001的抗癌疫苗接种产生有利应答的概率甚至更高。
[0050]
根据本发明的方法,如果患者进一步表现出以下一种或多种特征,则认为患者对用vx-001的抗癌治疗性疫苗接种产生有利应答的概率仍然较高:
[0051]
(i)他是男性
[0052]
(ii)他患有非鳞状肿瘤
[0053]
(iii)他小于65岁
[0054]
(iv)他的肿瘤在一线化疗后不再进展
[0055]
(v)他的ecog=0。
[0056]
当然,本发明的不同实施方式并不相互排斥,具有上述几种标准的患者类别都更有可能成为对用vx-001的疫苗接种的良好应答者。
[0057]
下面在实验部分中对本发明作进一步说明,但并不限定本发明的范围。
[0058]
实例
[0059]
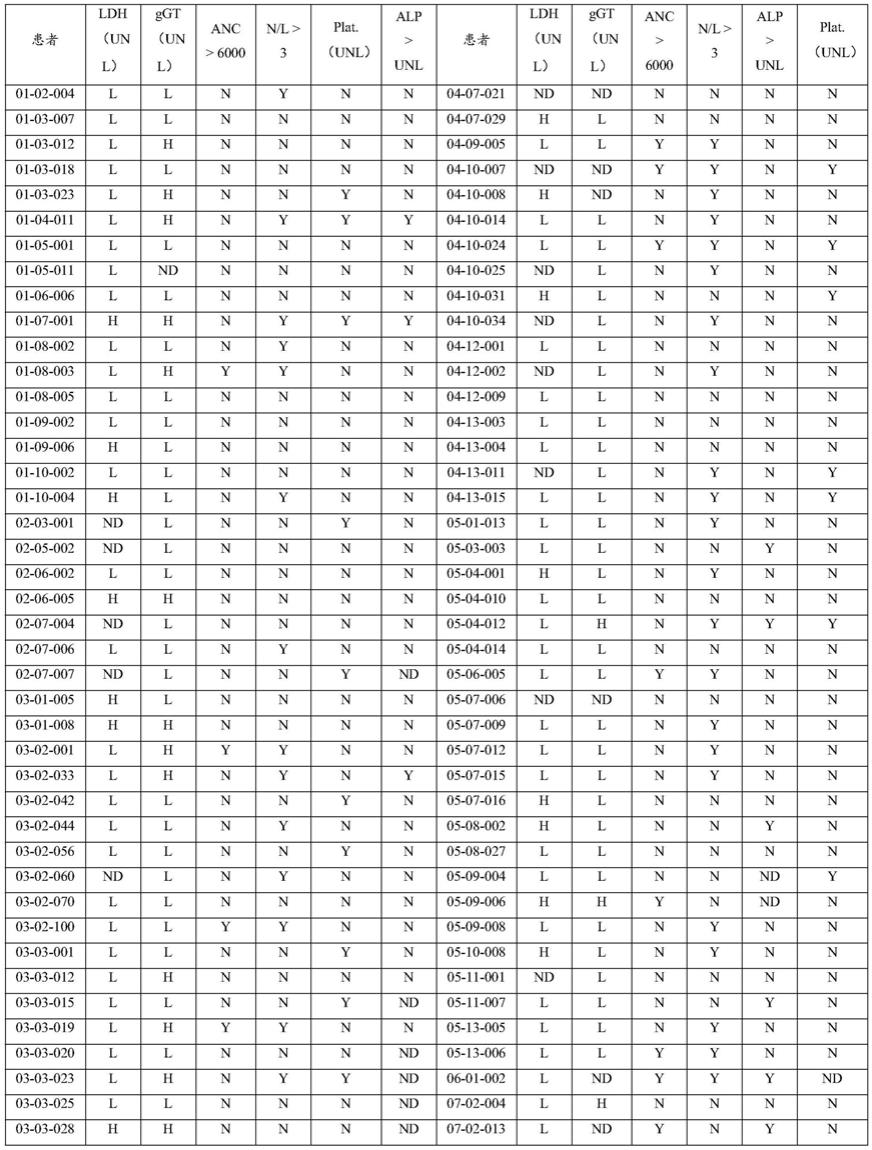
血液测试是在化疗后在临床试验招募患者的过程中进行的。由于每个实验室都应用自己的测试和自己的正常极限(unl或“正常上限”),数据是从患者的医疗档案中收集的,并根据相对于由实验室应用的正常极限获得的结果进行分类(表1)。研究的信息是ldh、ggt、alp的水平、中性粒细胞的绝对数量、血小板的绝对数量以及中性粒细胞和淋巴细胞之
间的比例。
[0060]
通过比较接受研究产品的患者和接受安慰剂的患者之间的两个标准,评估了在该临床试验中研究产品(vx-001)的有效性。
[0061]-患者的“总生存”(表示为os)
[0062]-称为“至治疗失败的时间”的时期,表示为ttf,在该时期期间疾病不再进展且患者除接受研究产品(或安慰剂)外未接受任何治疗。
[0063]
[0064][0065][0066]
表1:乳酸脱氢酶(ldh)、γ谷氨酰胺转移酶(ggt)、碱性磷酸酶(alp)的血清水平,中性粒细胞的绝对数量(anc)、中性粒细胞/淋巴细胞比例(n/l)和血小板(plat)的测量。
vx001-201研究中包括的患者分为几个亚组:l为如下患者,该患者具有正常水平的所考虑的标志物,符合进行测定的实验室标准,h为如下患者,该患者具有比各实验室制定的正常限值更高的水平;n=否;y=是;nd=未确定。
[0067]
1.对vx-001的临床应答和ldh水平
[0068]
在vx-001-201研究中包括的190名患者中,127名患者的ldh血清水平正常。在该群体中,vx-001疫苗接种使os和ttf相对于安慰剂组中的患者显著增加(图1)。
[0069]
2.对vx-001的临床应答和ggt水平
[0070]
在vx-001-201研究中包括的190名患者中,139名患者的ggt血清水平正常。在该群体中,vx-001疫苗接种使os相对于安慰剂组中的患者的os增加,但不显著(p=0.10)。相比之下,ttf显著增加(图2)。
[0071]
3.对vx-001的临床应答和碱性磷酸酶(alp)
[0072]
在vx-001-201研究中包括的190名患者中,160名患者的alp血清水平正常。在该群体中,与安慰剂组中的患者相比,vx-001疫苗接种不会导致os增加(p=0.74,图3)。患者的alp水平不影响患者对vx-001的应答能力。关于ttf的结果是相同的。
[0073]
4.对vx-001的临床应答和血细胞计数
[0074]
血细胞计数通常用于评估患者的炎症状态。因此,除了中性粒细胞的绝对数量外,还有中性粒细胞数量与淋巴细胞数量之间的比例以及血小板数量是患者总体健康状况的特征。
[0075]
a.对vx-001的临床应答和中性粒细胞的绝对数量
[0076]
中性粒细胞的绝对数量是常用的炎症标志物。特别是显示大量中性粒细胞与对免疫检查点抑制剂(ici)治疗的弱应答有关(ferrucci等人,annals oncol[肿瘤学年鉴]2016)。
[0077]
在用vx-001治疗的情况下,没有观察到中性粒细胞的数量有任何影响。在中性粒细胞水平高或正常的患者中,安慰剂组患者与接受治疗的患者之间未观察到生存差异(图4)。
[0078]
b.对vx-001的临床应答以及中性粒细胞和淋巴细胞之间的比例
[0079]
中性粒细胞数与淋巴细胞数之间的比例也观察到相同类型的结果。在中性粒细胞和淋巴细胞之间的比例小于3(该比例通常用作文献中的限值(mezquita等人,2018;ferrucci等人,2016))的患者中或高于3的那些患者中,安慰剂组的患者与接受治疗的患者之间没有观察到生存差异(图5)。
[0080]
c.对vx-001的临床应答和血小板
[0081]
最后,血小板的数量没有影响。在血小板水平高或正常的患者中(unl:“正常上限”),安慰剂组患者与接受治疗的患者之间未观察到生存差异(图6)。
[0082]
5.组合的因素
[0083]
a.ggt和ldh
[0084]
接下来评估当组合这些因素(特别是那些对患者的生存和ttf有影响的因素)时vx-001的临床有效性。
[0085]
在ldh和ggt水平均正常的97名患者中,vx-001治疗非常显著地提高了生存和ttf:分别为p=0.003和p=0.0019(图7)。
[0086]
对血清ldh和ggt水平正常的患者群体亚组进行更详细的生存分析表明,vx-001在以下患者中具有非常显著的影响:患有非鳞状癌的患者(或nsq,p=0.0038),男性(p=0.0024),吸烟者(p=0.0099),小于65岁的患者(p=0.0019),进入研究的对化疗有客观缓解(or,p=0.036)或具有疾病稳定(sd,p=0.034)、具有ecog为0(0.041)或ecog为1(p=0.039)的患者。相比之下,出人意料的是,vx-001并没有显著增加具有鳞状组织类型的癌症患者(sq,p=0.39)、女性(p=0.27)和65岁以上患者(p=0.08)的生存(图8)。
[0087]
同样,对血清ldh和ggt水平正常的患者群体亚组的ttf分析证实vx-001在以下患者中具有非常强的影响:患有非鳞状癌的患者(nsq,p=0.0009),男性(p=0.0064),吸烟者(p=0.001),65岁以下患者(p=0.0017),进入研究的对化疗有客观缓解(or,p=0.021)、具有ecog为0(0.021)的患者,而且在65岁以上的患者中也是如此(p=0.0017)。
[0088]
相比之下,vx-001并没有显著增加具有鳞状组织结构的癌症患者(sq,p=0.49)、女性(p=0.25)、和进入研究的化疗后具有疾病稳定(sd,p=0.074)或ecog为1(p=0.14)的患者的ttf(图9)。
[0089]
ldh和ggt水平的组合是唯一具有协同效应的因素组合,其他组合给出的结果至多与单独使用ldh水平的分析相同(图10)。
[0090]
6.体现肿瘤免疫原性的影响的ldh和ggt标志物的影响
[0091]
肿瘤的免疫原性取决于几个因素,其中最重要的是肿瘤内til(肿瘤浸润淋巴细胞)的存在以及肿瘤细胞对pd-l1分子的表达。我们分析了体现这两个参数的影响的vx-001对136名我们可获得活检切片的患者的影响。使用22c3 pharmdx试剂盒检测pd-l1。
[0092]
根据安捷伦(agilent)试剂盒的建议分析pd-l1的表达,该试剂盒能够定量表达pd-l1的肿瘤细胞(tps:肿瘤比例得分)。这些组被分为三组i)pd-l1阴性(《1%的细胞被标记;tps《1%),ii)pd-l1阳性(1%-49%的细胞被标记;tps 1%-49%)和iii)过表达pd-l1(》50%的细胞阳性;tps》50%)。根据til的肿瘤浸润(瘤内部位is,和基质部位ss)被定性为i)不存在(得分0),ii)非常稀少(得分1),iii)低(得分2),iv)一般(得分3)和v)高(得分4)。
[0093]
如果少于1%的肿瘤细胞表达pd-l1(tps;肿瘤比例得分;《1%)则肿瘤被归类为pd-l1阴性,如果肿瘤核心和肿瘤基质中的til完全不存在(得分0)或非常稀少(得分1)则肿瘤被归类为til阴性。各个结果呈现在表2中。
[0094]
[0095]
[0096][0097]
表2:可获得这些数据的患者的til和tps得分
[0098]
图11中显示的结果表明,vx-001延长了til阴性肿瘤患者(8.7个月相比于20.7个月,p=0.0089)和pd-l1阴性肿瘤患者(9.9个月相比于15.5个月;p=0.13)的生存,但没有延长til阳性肿瘤患者(16.3个月相比于14.3个月;p=0.197)和pd-l1阳性肿瘤患者(24.9个月与7.9个月;p=0.29)的生存。vx-001在til-且pd-l1-肿瘤患者中的临床有效性甚至更高(6.6个月相比于20.7个月,p=0.0049)。对ttf的分析获得了类似的结果。vx-001延长了til-肿瘤患者(2.7个月相比于3.6个月;p=0.041)、pd-l1-肿瘤患者(2.3个月相比于3.5个月;p=0.079)和til-/pd-l1-肿瘤患者(2.2个月相比于3.6个月;p=0.011)的ttf(图12)。
[0099]
根据由til的存在和pd-l1的表达定义的肿瘤的免疫原性分析ldh和ggt因素的影响表明,在患有非免疫原性肿瘤(til-、pd-l1-、til-/pd-l1-)的患者中,血清ldh和血清ggt
的正常水平与更长的生存(图13)和更长的ttf(图14)相关,但在患有免疫原性肿瘤(til+、pd-l1+、til+和/或pd-l1+)的患者中并非如此。
[0100]
参考文献
[0101]
ferrucci pf,ascierto pa,et al.,baseline neutrophils and derived neutrophil-to-lymphocyte ratio:prognostic relevance in metastatic melanoma patients receiving ipilimumab.ann oncol.2016apr;27(4):732-8.
[0102]
georgoulias v,et al.,a multicenter randomizedphase iib efficacy study of vx-001,a peptide-based cancer vaccine as maintenance treatment in advanced non-small-cell lung cancer:treatment rationale and protocol dynamics.clin lung cancer.2013jul;14(4):461-5.
[0103]
menez-jamet j,et al.,optimized tumor cryptic peptides:the basis for universal neo-antigen-like tumor vaccines.ann transl med.2016jul;4(14):266.
[0104]
mezquita,l.et al.,association of the lung immune prognostic index with immune checkpoint inhibitor outcomes in patients with advanced non-small cell lung cancer.jama oncol.2018mar 1;4(3):351-357.tourdot s,et al.,a general strategy to enhance immunogenicity of low-affinity hla-a2.1-associated peptides:implication in the identification ofcryptic tumor epitopes.eur j immunol.2000dec;30(12):3411-21.
