1.本发明属于纳米粒子制备技术领域,具体而言,涉及一种利用黑米花色苷抑制尿酸生成的纳米复合粒子及其制备与应用。
背景技术:
2.尿酸(uric acid,ua)是人类嘌呤代谢的终产物,主要由次黄嘌呤、黄嘌呤等在黄嘌呤氧化酶(xanthine oxidase,xo)的催化作用下生成,由于人类与其他动物不同,体内无尿酸氧化酶,不能将尿酸进一步分解成尿囊素,这使得人类发生尿酸代谢异常现象的可能性远高于其他生物。当体内尿酸水平过高,嘌呤代谢处于紊乱状态时,便会引发高尿酸血症。高尿酸血症已成为继“高血压、高血脂、高血糖”之后的“第四高”。目前常用别嘌呤醇、非布索坦等药物治疗尿酸,然而因较强的毒副作用常导致患者出现多种不良反应,因此导致传统药物的治疗方法受到限制。近些年,天然产物的开发利用逐渐成为研究热点。
3.黑米(nigrum rice)是由禾本科植物稻谷经长期培育形成的一类药食兼用的大米。其种植历史悠久,是我国古老而名贵的水稻品种。现代医学也证实黑米具有滋阴补肾、健脾暖肝、明目活血等功效。并且经研究证明,黑米所表现出来的保健功效是来自黑米皮中丰富的花色苷,而不是自身所含有的膳食纤维、维生素和矿物质等营养素。花色苷是在自然界广泛存在的一类黄酮化合物,在大部分植物的根、茎、叶、花、果实和种皮中都有不同比例的存在。随着黑米成熟度的增加,其种皮中的花色苷含量逐渐增加,使黑米的颜色发生由红、紫红、紫黑直至黑的变化。在我国,黑米资源丰富,但是目前对其的开发应用方面还较浅,种植者经简单加工便出售,经济效益较低。而黑米中花色苷存在于黑米种皮部位的天然色素,赋予黑米特有颜色,是一种以3,5,7-三羟基-2-苯基苯并吡喃为基本结构的黄酮类化合物,主要成分包括矢车菊素-3-葡萄糖苷、芍药素-3-葡萄糖苷等,具有抗氧化、降血糖血脂、抗炎、调节肠道菌群等多种生理活性。然而,黑米花色苷易受ph、温度、光照等外界环境影响,容易降解,其作为医药或食品成分的应用受到限制,且体内受胃肠消化作用的稳定性下降,实际应用时体内外生物利用度不高。
4.近年来,纳米技术已被广泛应用于提高小分子活性物质的稳定性。人们发现,纳米材料具有独特的理化性质,如尺寸效应和表面效应使其与生物表面相互作用时表现出超越传统分子之间相互作用所产生的生物学效应,因此纳米材料有望成为功能性食品和生物医学领域变革的基础性物质。cn112494435a供一种基于海洋多糖载体的花色苷纳米粒子,以海洋多糖、食源性荧光纳米粒子、透明质酸钠作为复合载体与花色苷结合,制备方法为:s1、将海藻酸钠溶解在磷酸盐缓冲盐水中,依次加入的edc和hobt及食源性荧光纳米粒子,得到荧光-海藻酸复合物;s2、将所述荧光海藻酸复合物加入到dmf和dcm混合物中,再加入dic和dmap;s3、加入花色苷和所述透明质酸后除去溶剂;s4、除去未反应的小分子,并冷冻干燥。该花色苷纳米粒子的制备过程中添加了edc、dmf、dmap等有机溶剂,后续除去溶剂时易产生残留,不适合用于食品配方中,且载体材料的种类较多,制备过程复杂,生产成本极高。
5.目前,构建纳米粒子大多使用化学修饰法,通过引入有机溶剂对分子结构进行修饰,但该方法较为复杂,且对花色苷的性能影响及合成产物的安全性有待考量。因此,研究并开发一种操作简单、安全高效的新型纳米复合材料构建方法具有重要意义。
技术实现要素:
6.鉴于现有技术的不足,本发明的目的在于提供一种安全性高,生产成本低,且可抑制尿酸生成的纳米复合粒子及其制备方法和应用。
7.为了实现上述技术目的,本发明人通过大量试验研究并不懈探索,最终仅以透明质酸钠作为包埋材料,通过简单的交联法,不使用任何有机溶剂,制备出了各项基本指标均符合理想要求的黑米花色苷纳米粒子,不仅有效改善了黑米花色苷的生物利用度,而且增强了黑米花色苷对尿酸生成的抑制作用。
8.具体地,本发明的目的是这样实现的:一种利用黑米花色苷抑制尿酸生成的纳米复合粒子,所述纳米复合粒子由透明质酸钠和黑米花色苷组成,且所述黑米花色苷包埋于透明质酸钠中。
9.进一步优选地,如上所述利用黑米花色苷抑制尿酸生成的纳米复合粒子,其中黑米花色苷与透明质酸钠的质量比为1:(8~10)。在本发明的试验例中,当黑米花色苷与透明质酸钠的质量比为1:9时,纳米复合粒子的稳定性最高。
10.进一步优选地,如上所述利用黑米花色苷抑制尿酸生成的纳米复合粒子,其在扫描电镜和透射电镜下观察到的结果是:黑米花色苷经透明质酸钠包埋后,呈现明显的双层结构,结构清晰,没有明显的团聚现象,类似于其他生物聚合物基纳米物质;并且纳米复合粒子分散均匀,整体形态呈单个的球形。
11.进一步优选地,如上所述利用黑米花色苷抑制尿酸生成的纳米复合粒子,其中的透明质酸钠的分子量为100~150万da。需要说明的是,透明质酸是一种天然的酸性粘多糖,由重复的d-葡萄糖醛酸和n-乙酰氨基葡萄糖苷胺通过β-1,3-糖苷键构成的双糖结构组成,广泛存在于动物组织,是肌肤水嫩的重要基础物质,具有良好的保湿性,还可改善皮肤代谢,使皮肤光滑、去皱、增加弹性、延缓衰老,同时又是良好的透皮吸收促进剂,目前主要用于化妆品技术领域。
12.另外,本发明还提供了一种上述利用黑米花色苷抑制尿酸生成的纳米复合粒子的制备方法,该方法包括如下步骤:
13.(1)称取透明质酸钠溶于去离子水中,配制透明质酸钠水溶液;
14.(2)在搅拌下将黑米花色苷溶液缓慢滴加至步骤(1)配制的透明质酸钠水溶液中,调节体系ph至3.3~4.3,搅拌反应2~4h后静置,得到透明质酸钠-黑米花色苷纳米复合粒子混悬液;
15.(3)将透明质酸钠-黑米花色苷纳米复合粒子混悬液冷冻干燥后,得到透明质酸纳包埋黑米花色苷的纳米复合粒子。
16.进一步优选地,如上所述利用黑米花色苷抑制尿酸生成的纳米复合粒子的制备方法,其步骤(2)中在搅拌之前间歇超声4-6min,超声频率58-60khz,间歇参数为工作10s,间歇5s。
17.此外,本发明的试验结果显示,单独黑米花色苷与透明质酸钠(0.9mg/ml)的体外
抑制率分别为10.17%和26.58%,但当使用纳米复合粒子作为抑制剂,进行体外抑制黄嘌呤氧化酶活性时,纳米复合粒子对黄嘌呤氧化酶的体外抑制率达48.57%,因此可以看出,黑米花色苷与透明质酸钠构成的纳米复合粒子可以有效抑制黄嘌呤氧化酶的活性,并且纳米复合粒子相对于单独黑米花色苷和透明质酸钠具有增强抑制黄嘌呤氧化酶活性的协同作用。因此,本发明还提供了上述的纳米复合粒子在制备抑制黄嘌呤氧化酶活性的食品、药品或保健品中的应用,以及上述的纳米复合粒子在制备抑制尿酸生成的食品、药品或保健品中的应用。
18.与现有技术相比,本发明提供的黑米花色苷纳米粒子具有如下优点和显著进步:
19.(1)本发明首次用透明质酸钠包埋黑米花色苷制备纳米复合粒子,并系统研究、比较透明质酸钠联合黑米花色苷的复合物与黑米花色苷对影响尿酸生成的关键酶的抑制效果,发现黑米花色苷与透明质酸钠构成的纳米复合粒子可以有效抑制黄嘌呤氧化酶的活性,且纳米复合粒子相对于单独黑米花色苷和透明质酸钠具有增强抑制黄嘌呤氧化酶活性的协同作用,为医药和功能食品领域中防治高尿酸方面提供了一种新的途径。
20.(2)本发明的黑米花色苷纳米粒子工艺简单,不使用任何有机溶剂,制备得到的黑米花色苷纳米粒子结构清晰,没有明显的团聚现象,类似于其他生物聚合物基纳米物质,并且纳米复合粒子分散均匀,粒径小,整体形态呈单个的球形,稳定性高。
21.(3)本发明制备的黑米花色苷纳米复合粒子在前12h释放速度较快,之后趋于平缓,60h之后体外释放总量达到60%。因此相较于单纯的黑米花色苷,纳米复合粒子在模拟生理环境条件下具有显著的体外缓释特性。缓释可以降低活性化合物的降解,从而增加更多活性化合物在胃肠中的吸收和生物利用率,说明黑米花色苷被透明质酸钠包埋后,可有效保护黑米花色苷,从而提高体内的生物利用度。
附图说明
22.图1:haa纳米复合粒子扫描电镜图像(a)和haa纳米复合粒子透射电镜图像(b、c)。
23.图2:ha、atc和haa纳米复合粒子的xrd图。
24.图3:透明质酸钠、黑米花色苷和纳米复合粒子的傅里叶红外光谱图。
25.图4:黑米花色苷和纳米复合粒子的体外缓释图。
26.图5:不同温度下黑米花色苷的稳定性曲线图(a:4℃,b:25℃,c:40℃),其中en和un分别代表纳米复合粒子(包埋形式)和花色苷(未包埋形式)。
27.图6:不同浓度抗坏血酸下黑米花色苷的稳定性曲线图。
28.图7:黑米花色苷在光照下的稳定性曲线图,其中en和un分别代表纳米复合粒子(包埋形式)和花色苷(未包埋形式)。
29.图8:黑米花色苷和纳米复合粒子光照10天的照片。
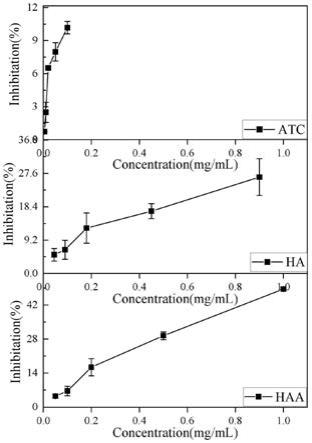
30.图9:haa纳米复合粒子、透明质酸钠、黑米花色苷对黄嘌呤氧化酶的抑制作用。
具体实施方式
31.下面通过具体实施方式对本发明作进一步详细说明,实施例中未注明具体技术操作步骤或条件者,均按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
32.实施例1:haa纳米复合粒子的构建
33.1.方法
34.1.1制备方法
35.准确称取一定质量透明质酸钠粉末溶于去离子水中,配制透明质酸钠水溶液,磁力搅拌使溶液澄清透明,在搅拌下用注射器将花色苷溶液缓慢滴加至透明质酸钠水溶液中,调节体系ph,超声5min(超声功率200w,频率59khz,工作10s,间歇5s),搅拌反应一段时间后静置,即得透明质酸钠-黑米花色苷纳米复合粒子混悬液,将其冷冻干燥后即获得负载花色苷的透明质酸钠纳米复合粒子(hyaluronic acid-black rice anthocyanin nanocomplex,haa)。
36.1.2工艺优化
37.为了研究纳米复合粒子制备条件对其基本性能的影响,以纳米复合粒子的平均粒径、zeta电位为指标,进行单因素实验。
38.1.2.1单因素考察
39.质量比对纳米复合粒子的影响:固定反应体系ph和搅拌时间,考察透明质酸钠和黑米花色苷质量比为8:1,9:1,10:1,11:1,12:1时对平均粒径和电位的影响。
40.反应体系ph对纳米复合粒子的影响:固定质量比和搅拌时间,考察体系ph为2.8,3.3,3.8,4.3,4.8时对平均粒径和电位的影响。
41.搅拌时间对纳米复合粒子的影响:固定质量比和反应体系ph,考察搅拌时间1h,2h,3h,4h,5h时对平均粒径和电位的影响。
42.1.2.2正交实验确定各单因素条件对haa平均粒径和电位的影响
43.影响haa平均粒径和电位的各单因素之间是相互联系的,为更好了解质量比、反应体系ph和搅拌时间对haa的影响。在上述单因素实验的基础上,设计三因素三水平正交实验表l9(34)。如表1和表2所示。
44.表1正交实验因素水平表
[0045][0046][0047]
表2正交实验因素设计表
[0048][0049]
按照上述正交优化方案制备3组haa纳米复合粒子,以平均粒径和电位为评价指标考察正交优化条件。
[0050]
2.结果分析
[0051]
2.1负载花色苷的透明质酸钠纳米复合粒子的制备
[0052]
2.1.1单因素实验结果分析
[0053]
本实验基于氢键和静电作用制备负载花色苷的透明质酸钠纳米复合粒子。首先以haa平均粒径和电位为评价指标,通过单因素考察影响haa性质的因素。
[0054]
(1)ha:atc质量比对haa的影响
[0055]
表3ha:atc质量比对haa的影响
[0056][0057][0058]
注:同列上标不同字母表示显著差异(p<0.05),值表示为平均值
±
sd(n=3)。
[0059]
由表3可以发现,在ha:atc=8:1,9:1,10:1时,haa的平均粒径均在200nm以内,粒径较小,且电位值绝对值较大,表明稳定性良好。因此该范围可作为haa制备的考察因素进一步分析。
[0060]
(2)反应体系的ph对haa的影响
[0061]
表4ph值对haa的影响
[0062][0063]
注:同列上标不同字母表示显著差异(p<0.05),值表示为平均值
±
sd(n=3)。
[0064]
综合表4可以看到,体系ph为3.3,3.8,4.3时,haa的平均粒径较小,电位值较小,符合理想状态,故选用该ph范围作为进一步分析。
[0065]
(3)搅拌反应时间对haa的影响
[0066]
表5反应搅拌时间对haa的影响
[0067][0068]
注:同列上标不同字母表示显著差异(p<0.05),值表示为平均值
±
sd(n=3)。
[0069]
由表5可以发现,在整个反应体系搅拌2h,3h,4h范围内,haa平均粒径逐渐变小,继续增大搅拌时间,粒径有变大趋势。另外综合pdi值和电位考虑,将搅拌时间2h,3h,4h作为进一步考察水平分析。
[0070]
2.1.2正交优化实验分析
[0071]
通过正交实验对haa制备参数进一步优化。在不同实验组合条件下,以haa平均粒径和电位值为评价指标的实验结果如表6和表7所示。
[0072]
表6正交设计平均粒径实验优化结果
[0073][0074]
由表6分析可知,以haa平均粒径为指标,各因素的影响顺序为r3》r2》r1,其中各因素对应的水平下分析结果为a:a2》a1》a3,b:b3》b1》b2,c:c2》c3》c1。故正交优化下的最佳工艺条件为:a2b3c2,即优化处方:质量比9:1,ph4.3,搅拌时间3h。
[0075]
表7正交设计电位实验优化结果
[0076]
[0077][0078]
由表7分析可知,以haa电位为考察指标,各因素的影响顺序为r3》r2》r1,其中各因素对应的水平下分析结果为a:a2》a1》a3,b:b3》b1》b2,c:c2》c3》c1。故正交优化下的最佳工艺条件为:a2b3c2,即优化处方:质量比9:1,ph4.3,搅拌时间3h。
[0079]
综上所述,从平均粒径和电位两方面探究haa最佳制备工艺时,所得到的工艺优化结果相同。
[0080]
相同条件下,运用上述所得到的最佳工艺条件平行制备的haa纳米复合粒子,分析结果如表8所示。
[0081]
表8正交优化条件的验证
[0082][0083]
可以看到,按正交优化条件下制备的3组平行样品,测定其粒径均为300nm左右,电位值小于-30,pdi值在可接受范围内,该条件下制备的复合粒子分布均匀且较为稳定,说明制备工艺符合目标要求。
[0084]
实施例2:haa纳米复合粒子的表征
[0085]
1.方法
[0086]
以实施例1中运用最佳工艺条件制备的haa纳米复合粒子9:1-ph4.3-3h作为样品,进行以下指标的测定分析:
[0087]
(1)包封率的测定(ee)
[0088]
取一定量纳米复合粒子于8000rpm下离心30min,采用ph示差法测定上清液中游离花色苷含量。花色苷包封率按照以下公式计算:
[0089][0090]
其中,ee是花色苷包封率(%);atc0是纳米复合粒子中初始花色苷含量;atc是上清液中游离花色苷含量。
[0091]
(2)形态学分析
[0092]
使用扫描电子显微镜(sem)(su8010,hitachi ltd.,japan)和透射电子显微镜(tem)(h-7650,japan)确定样品的表面形态。
[0093]
(3)结构分析
[0094]
使用x射线衍射仪(xrd)(d8 advance,brucker,karlsruhe,germany)扫描得到纳米复合粒子的xrd图谱。
[0095]
(4)光谱分析
[0096]
使用傅里叶变换红外光谱仪(ft-ir)(is50,usa)扫描得到透明质酸钠、黑米花色苷和纳米复合粒子的红外光谱图。
[0097]
(5)特性分析
[0098]
体外缓释:一定量纳米复合粒子冻干粉末悬浮于pbs缓冲液(0.1mol/l,ph7.4)中充分溶解,转入8-14kda透析袋中,密封后投入装有50mlpbs缓冲液的小瓶中,于37℃、100rpm恒温避光振荡,定时取出透析袋外透析液,并立即补加同温同量的新鲜缓冲液。计算累计释药百分率,并以累计释药百分率对时间作图,绘制纳米复合粒子体外缓释曲线。
[0099]
2.表征结果
[0100]
(1)包埋率
[0101]
根据ph示差法测定三组haa纳米复合粒子的包埋率,结果如表9所示。
[0102]
表9haa纳米复合粒子包埋率
[0103][0104]
(2)形态学分析
[0105]
纳米复合粒子的扫描电镜和透射电镜如图1所示。图1(a)显示,合成的纳米复合粒子结构清晰,没有明显的团聚现象,类似于其他生物聚合物基纳米物质。图1(b)可以看出,纳米复合粒子分散均匀,整体形态呈单个的球形,图1(c)是单个纳米复合粒子的透射电镜图,可发现黑米花色苷经透明质酸钠包埋后,呈现明显的双层结构,可直观反映黑米花色苷已成功载入透明质酸钠中。
[0106]
(3)结构分析
[0107]
图2是透明质酸钠、黑米花色苷和纳米复合粒子的x射线衍射图谱。atc的xrd图出
现多处明显较窄的衍射峰(如2θ=31.71
°
,45.55
°
等),这表明黑米花色苷具有高度结晶的特征。而ha在2θ=11.31
°
,19.73
°
处出现两个相对较宽的衍射峰,表明其半结晶的特征。与atc和ha相比,haa纳米复合物的峰更弱,显示非晶态聚合物的特征。该结果表明,atc被加入到ha中后,atc分子的晶体结构被覆盖,衍射峰强度显著降低,这可能与atc和ha之间新形成的分子间氢键有关,被成功结合到ha分子上。
[0108]
(4)光谱分析
[0109]
对透明质酸钠-黑米花色苷纳米复合粒子组成成分间的键合情况进行了傅里叶红外光谱测试,结果如图3所示。在黑米花色苷的图谱中,1245cm-1
是由苯并吡喃芳香环引起的伸缩振动峰,这是典型的类黄酮结构峰,1641cm-1
、1444cm-1
处的峰分别对应芳香环骨架中c=c和c=o的伸缩振动。透明质酸钠谱图中的1633cm-1
处是coo-的特征峰。在纳米复合粒子图谱中,c=o的伸缩振动(1648cm-1
)显示出蓝移吸收峰,这可能是因为透明质酸钠和黑米花色苷之间存在新的化学键,另外1303cm-1
处的伸缩振动变强,则归因于引入了黑米花色苷,透明质酸在1046cm-1
处强而宽的糖基吸收峰在纳米复合粒子处吸收变弱,说明两者之间存在氢键,这些均从侧面证实了透明质酸钠和黑米花色苷的成功结合。
[0110]
(5)特性分析
[0111]
体外释放情况对纳米复合粒子能否在体内外较好发挥活性作用至关重要。图4显示,黑米花色苷在前12h内较快速释放,4h时已达到60%,有突释行为。而纳米复合粒子在前12h释放速度较快,之后趋于平缓,60h之后体外释放总量达到60%。因此相较于黑米花色苷,纳米复合粒子在模拟生理环境条件下具有显著的体外缓释特性。缓释可以降低活性化合物的降解,从而增加更多活性化合物在胃肠中的吸收和生物利用率。说明黑米花色苷被透明质酸钠包埋后,可有效保护黑米花色苷,提高活性利用。
[0112]
实施例3:haa纳米复合粒子的稳定性测定试验
[0113]
1.方法
[0114]
以实施例1中运用最佳工艺条件制备的haa纳米复合粒子9:1-ph4.3-3h(第一组)作为样品,进行以下指标的测定分析:
[0115]
在4℃、25℃、40℃三种常规储存温度下放置,定时检测花色苷残留率;在0.1、0.25、0.5、1.0mg/ml抗坏血酸浓(aa)度条件下25℃避光储存6天,检测花色苷残留率;在25℃暴露于光照下储存,检测花色苷残留率。花色苷残留率按照以下公式计算:
[0116][0117]
其中,r代表花色苷残留率(%);c
t
代表t时刻取样花色苷含量(mg/l);c0代表初始花色苷含量(mg/l)
[0118]
2.稳定性分析结果
[0119]
图5显示,haa纳米复合粒子4℃储藏18天、25℃储藏6天、40℃储藏3天后的花色苷残留率分别为87.18%、73.68%、71.71%,而黑米花色苷在4℃、25℃、40℃储藏同样时间后的残留率为75.09%、44.68%、33.37%,可知haa纳米复合粒子的热稳定性优于游离花色苷。
[0120]
图6显示,不同aa浓度(0.1mgml、0.25mg/ml、0.5mg/ml、1.0mg/ml)下花色苷残留率随储存天数的延长逐渐降低,6天后残留率分别为60.39%、51.08%、32.24%、24.49%,然
而在所有aa浓度下,haa纳米复合粒子中花色苷残留率分别提高了32.27%、31.5%、48.42%、54.84%。aa是果汁饮料中常见的添加剂,一定量aa对花色苷有降解作用,而纳米复合粒子的包埋提供了物理屏障,阻止了花色苷与aa的直接接触,从而提高了稳定性。
[0121]
图7显示,光照10天后,游离花色苷残留率为23.28%,而haa纳米复合粒子中花色苷残留率同比增加了43.63%,复合粒子保护作用明显。另外,图8显示,随着光照时间的延长,花色苷颜色由微粉色变为浅黄色,最终转为暗黄色,而haa纳米复合粒子的颜色变化较不明显,说明haa在光照下可有效保护黑米花色苷降解。
[0122]
实施例4:haa纳米复合粒子对黄嘌呤氧化酶的体外抑制活性研究
[0123]
整个体外抑制酶活过程均在紫外-可见分光光度计的时间/动力学软件下进行,且保持反应体系是ph7.5的0.05mol/l磷酸盐缓冲液(phosphate buffered saline,pbs)体系。取2ml 0.05mol/lph7.5的磷酸盐缓冲液、1ml 0.012u/ml的xo溶液、1ml样品加入试管中混合均匀,25℃恒温水浴孵化30min,加入1ml 0.2mg/ml黄嘌呤启动反应。利用紫外-可见分光光度计的时间/动力学软件每隔10s检测反应体系中尿酸在290nm处的吸光度,测定不同浓度haa纳米复合粒子存在下反应体系中xo催化生成尿酸的活力,每个样品平行检测3次。
[0124]
在有抑制剂存在下,酶反应活性用b表示,无抑制剂存在下,酶反应活性用a表示。则haa纳米复合粒子对xo的相对抑制率为:i(%)=(1-b/a)
×
100%=[1-(od
a-odb)/(od
c-odd)]
×
100%
[0125]
式中:oda表示反应体系中加入样品、xo、pbs、黄嘌呤底物后的吸光度;odb表示反应体系中加入样品、pbs、黄嘌呤底物后的吸光度;odc表示反应体系中加入xo、pbs、黄嘌呤底物后的吸光度;odd表示反应体系中加入pbs、黄嘌呤底物后的吸光度。具体方案见表10。
[0126]
表10体外抑制模型测定方案
[0127][0128]
haa纳米复合粒子、透明质酸钠、黑米花色苷对黄嘌呤氧化酶的体外抑制作用如图9所示。根据先前haa纳米复合粒子的工艺条件可知透明质酸钠与黑米花色苷的质量比为9:1,按透明质酸钠与黑米花色苷分别占haa纳米复合粒子的比例折合得到的浓度分别检测对黄嘌呤氧化酶活性的体外抑制作用。图9显示,单独黑米花色苷(0.1mg/ml)与透明质酸钠(0.9mg/ml)的体外抑制率分别为10.17%和26.58%,这表明黑米花色苷与透明质酸钠均对xo有抑制效果。但当使用haa纳米复合粒子作为抑制剂,进行体外抑制xo活性时,haa纳米复合粒子(1mg/ml)对xo的体外抑制率达48.57%,并且随着haa纳米复合粒子浓度增加,体外抑制效果越好,因此,haa纳米复合粒子可以有效抑制黄嘌呤氧化酶的活性,并且haa纳米复合粒子相对于单独黑米花色苷具有增强的体外抑制xo活性。
