30:47e-47,2002),是最常用的技术。为了扩增端粒重复序列及降低引物二聚体扩增的可能性,cawthon建议使用与端粒重复序列中富含g/c的片段结合的引物,在其他碱基与端粒处有一个错配,而它们之间有两个错配。该方法的本质是通过确定端粒重复序列的拷贝数(t)与每个基因组已知固定拷贝数的参考基因的拷贝数(s)的比率(t/s值)来估计相对平均端粒长度。作为参考基因,cawthon建议使用36b4(编码核糖体蛋白侧茎亚基p0,rplp0)。qpcr同样需要高质量的dna,但需要的dna量很少。这种方法对dna的需求量小,可用于高通量检测,适用于临床诊断和流行病学等大规模样本研究。例如,专利cn201910312065.2提供了一种检测绝对端粒长度的pcr方法,通过对端粒和36b4基因进行定量检测,用于计算待测样本dna的平均绝对端粒长度。专利cn202011223112.5提供了另外一种端粒相对长度检测试剂盒,包括端粒基因和内参基因的检测引物探针组合物,其内参基因为yh-1。但上述方法检测的准确性和重复性均较差。
5.因此,亟需提供一种端粒长度检测的灵敏度、准确性及重复性均较好的试剂盒及检测方法。
技术实现要素:
6.为了解决现有技术中的上述问题,本技术提供了一种端粒长度检测的引物组合物及其试剂盒。本技术所述的试剂盒包括检测端粒重复序列(tel)、干扰素编码基因(interferon beta 1,ifnb1)、真核翻译延伸因子(eukaryotic translation elongation factor 1gamma,eef1g)、过氧化物氧化还原酶(peroxiredoxin1,prdx1)、核糖体蛋白(ribosomal protein sa,rpsa)和/或细胞骨架蛋白(vimentin,vim)的引物组合物,本技术所述的引物组合物或试剂盒的检测稳定性、重复性、灵敏度较好,可用于高通量处理待检测样本,为端粒长度的检测、癌症或分子流行病学的研究提供了新的思路。
7.为了实现上述发明目的,本发明提供如下技术方案:
8.一方面,本发明提供了干扰素编码基因ifnb1、真核翻译延伸因子eef1g、过氧化物氧化还原酶prdx1、核糖体蛋白rpsa和/或细胞骨架蛋白vim在制备端粒长度检测产品中的应用。
9.另一方面,本发明提供了一种检测端粒长度的引物组合物,所述的引物组合物用于检测端粒重复序列tel、干扰素编码基因ifnb1、真核翻译延伸因子eef1g、过氧化物氧化还原酶prdx1、核糖体蛋白rpsa和/或细胞骨架蛋白vim。
10.具体地,
11.(1)所述的端粒重复序列tel的引物组合物为:
12.f(seq id no:1):5'-cggtttgtttgggtttgggtttgggtttgggtttgggtt-3';
13.r(seq id no:2):5'-ggcttgccttacccttacccttacccttacccttaccct-3';
14.(2)所述的干扰素编码基因ifnb1引物组合物为:
15.f(seq id no:3):5'-atgaccaacaagtgtctcctcc-3';
16.r(seq id no:4):5'-ggaatccaagcaagttgtagctc-3';
17.(3)所述的真核翻译延伸因子eef1g引物组合物为:
18.f(seq id no:5):5'-aaccgcacccctgaatttctc-3';
19.r(seq id no:6):5'-ggcgttgctctcaaacacac-3';
20.(4)所述的过氧化物氧化还原酶prdx1引物组合物为:
21.f(seq id no:7):5'-tcaagcctgatgtccaaaagag-3';
22.r(seq id no:8):5'-accgcagcctggcactaa-3';
23.(5)所述的核糖体蛋白rpsa引物组合物为:
24.f(seq id no:9):5'-gtggcaccaatcttgacttcc-3';
25.r(seq id no:10):5'-gcagggttttcaatggcaacaa-3';
26.(6)所述的细胞骨架蛋白vim引物组合物为:
27.f(seq id no:11):5'-gcgaggagagcaggatttctc-3';
28.r(seq id no:12):5'-agtgggtatcaaccagagggag-3'。
29.另一方面,本发明提供了上述引物组合物在制备检测端粒长度产品中的应用。
30.具体地,所述的产品包括但不限于独立试剂、芯片或试剂盒。
31.又一方面,本发明提供了一种检测端粒长度的产品,所述的产品包括上述引物组合物。
32.具体地,所述的产品包括但不限于独立试剂、芯片或试剂盒。
33.具体地,所述的产品还包括pcr酶、缓冲液、dntp、模板及去离子水等。
34.又一方面,本发明提供了上述引物组合物或产品在检测端粒长度中的应用。
35.又一方面,本发明提供了一种检测端粒长度的方法,所述的方法为非疾病诊断和治疗方法,所述的方法包括利用上述引物组合物或产品对待测样本中端粒长度进行检测。
36.具体地,所述的方法包括以下步骤:
37.(1)提取检测样本的rna;
38.(2)利用引物组合物扩增步骤(1)提取的样本dna;
39.(3)对扩增结果进行分析。
40.具体地,步骤(2)中所述的扩增反应体系为:10μl反应体系如下:2
×
chamq sybr qpcr master mix,5μl;50
×
rox reference dye,0.2μl;基因组dna,20-40ng;端粒重复序列扩增引物10μm,0.2μl;内参基因引物10μm,0.2μl。
41.具体地,步骤(2)中所述的扩增反应条件为:预变性:95℃30s;循环反应:94℃10s,60℃30s,40个循环;熔解曲线:95℃15s,60℃60s,95℃15s。
42.又一方面,本发明提供了上述引物组合物或产品在制备癌症遗传评估、生物学年龄评价和/或分子流行病学评估产品中的应用。
43.与现有技术相比,本发明具有如下有益效果:
44.(1)本发明首次发现了干扰素编码基因ifnb1、真核翻译延伸因子eef1g、过氧化物氧化还原酶prdx1、核糖体蛋白rpsa和/或细胞骨架蛋白vim在端粒长度检测中的应用。
45.(2)采用本发明提供的引物组合物检测端粒长度,具有较好的灵敏度和准确度、重复性,扩增效率高,且操作简便,快速省时,可用于高通量筛选和时间监测,对于癌症的遗传、生物学年龄评价和分子流行病学研究具有重要的实践意义。
附图说明
46.图1为扩增曲线检测结果图。
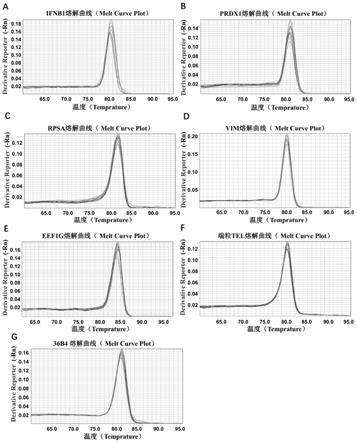
47.图2为熔解曲线检测结果图。
具体实施方式
48.下面结合具体实施例,对本发明作进一步详细的阐述,下述实施例不用于限制本发明,仅用于说明本发明。以下实施例中所使用的实验方法如无特殊说明,实施例中未注明具体条件的实验方法,通常按照常规条件,下述实施例中所使用的材料、试剂等,如无特殊说明,均可从商业途径得到。
49.实施例中未注明具体技术或条件者,均按照本领域内的文献所描述的技术或条件(如参考j.萨姆布鲁克等著,黄培堂等译的《分子克隆实验指南》,第三版,科学出版社)或者按照产品说明书进行。
50.实施例1.一种检测端粒长度的引物组合物
51.内参基因的选择:选取干扰素编码基因ifnb1、真核翻译延伸因子eef1g、过氧化物氧化还原酶prdx1、核糖体蛋白rpsa和/或细胞骨架蛋白vim作为内参基因。
52.所述的引物组合物用于检测端粒重复序列tel、干扰素编码基因ifnb1、真核翻译延伸因子eef1g、过氧化物氧化还原酶prdx1、核糖体蛋白rpsa和/或细胞骨架蛋白vim。
53.(1)所述的端粒重复序列tel的引物组合物为:
54.f(seq id no:1):5'-cggtttgtttgggtttgggtttgggtttgggtttgggtt-3';
55.r(seq id no:2):5'-ggcttgccttacccttacccttacccttacccttaccct-3';
56.(2)所述的干扰素编码基因ifnb1引物组合物为:
57.f(seq id no:3):5'-atgaccaacaagtgtctcctcc-3';
58.r(seq id no:4):5'-ggaatccaagcaagttgtagctc-3';
59.(3)所述的真核翻译延伸因子eef1g引物组合物为:
60.f(seq id no:5):5'-aaccgcacccctgaatttctc-3';
61.r(seq id no:6):5'-ggcgttgctctcaaacacac-3';
62.(4)所述的过氧化物氧化还原酶prdx1引物组合物为:
63.f(seq id no:7):5'-tcaagcctgatgtccaaaagag-3';
64.r(seq id no:8):5'-accgcagcctggcactaa-3';
65.(5)所述的核糖体蛋白rpsa引物组合物为:
66.f(seq id no:9):5'-gtggcaccaatcttgacttcc-3';
67.r(seq id no:10):5'-gcagggttttcaatggcaacaa-3';
68.(6)所述的细胞骨架蛋白vim引物组合物为:
69.f(seq id no:11):5'-gcgaggagagcaggatttctc-3';
70.r(seq id no:12):5'-agtgggtatcaaccagagggag-3'。
71.另外,用于扩增36b4(rplp0)的引物组合物为:
72.f(seq id no:13):5'-cagcaagtgggaaggtgtaatcc-3'(注明:此引物序列来源于cawthon);
73.r(seq id no:14):5'-cccattctatcatcaacgggtacaa-3'(注明:此引物序列来源于cawthon)。
74.实施例2.一种检测端粒长度的试剂盒
75.(1)包括实施例1所述的引物组合物。
76.(2)还包括pcr酶、缓冲液、dntp、模板及去离子水等。
77.其中,10μl反应体系如下:2
×
chamq sybr qpcr master mix,5μl;50
×
rox reference dye,0.2μl;基因组dna,20-40ng;端粒重复序列扩增引物10μm,0.2μl;内参基因引物10μm,0.2μl。
78.实施例3.一种检测端粒长度的方法
79.1.提取唾液/咽拭子/血液基因组dna
80.以唾液样本为例,使用口腔拭子基因组dna提取试剂盒(天根生化科技有限公司,dp322)提取基因组dna,操作严格参照说明书进行。
81.1.1.处理材料:按照要求取出唾液样本200-400μl,加入等体积的缓冲液gha,颠倒混匀。然后从中取出300-350μl的样品,加入10μl proteinase k溶液,涡旋10s混匀,65℃放置30min,每隔10min涡旋混匀。
82.1.2.加入500μl缓冲液gbs,充分颠倒混匀,室温放置5min。
83.1.3.将上一步所得溶液加入一个吸附柱cb2中,12000rpm离心30s,倒掉收集管中的废液,将吸附柱cb2放回收集管中。
84.1.4.向吸附柱cb2中加入500μl去蛋白液rd,12000rpm离心30s,倒掉收集管中的废液,将吸附柱cb2放回收集管中,并重复操作一次。
85.1.5.向吸附柱cb2中加入600μl漂洗液pwe,12000rpm离心30s,倒掉收集管中的废液,将吸附柱cb2放回收集管,并重复操作一次。
86.1.6.12000rpm离心2min,倒掉废液。将吸附柱cb2室温放置数分钟,以彻底晾干残余的漂洗液。
87.1.7.将吸附柱cb2转入一个干净的离心管中,向吸附膜中间位置悬空滴加50μl洗脱缓冲液tb,室温放置2-5min,12000rpm离心2min;为提高回收效率可将洗脱液再重复洗脱一次。
88.1.8.将溶液收集到离心管中,并于适当条件保存。
89.2.检测样本dna的质量
90.使用nanodrop仪器检测dna浓度和质量,要求:浓度≥100ng/μl;260/280范围是1.8-2.0,a260/a230≥1.8。
91.3.荧光定量qpcr检测基因组dna端粒长度
92.3.1.处理gdna:缓冲液te(ph8.0)稀释基因组dna样品为30-40ng/μl,95℃5min,冰浴5min,1000g短暂离心,保存在4℃。
93.3.2.对样品分别进行端粒重复序列tel、干扰素编码基因ifnb1、真核翻译延伸因子eef1g、过氧化物氧化还原酶prdx1、核糖体蛋白rpsa和细胞骨架蛋白vim的pcr扩增,检测其ct值,每个检测样品dna做3个平行孔均设三个平行孔,并设置三个阴性对照。
94.3.3.pcr扩增反应体系如下表1所示。
95.表1.qpcr反应体系
96.试剂使用量(μl)gdna,20-40ng/μl12
×
chamq sybr qpcr master mix荧光定量(vazyme)550
×
roxreferencedye 10.2primers(f+r),10μm0.4
ddh2o3.4total10
97.3.4.pcr扩增反应程序为:采用biosystemsquantstudio 6flex 96block实时荧光定量pcr检测系统(abi),pcr条件:第一阶段预变性:95℃,30s;第二阶段循环反应:95℃,10s;60℃,30s(荧光采集);40个循环;第三阶段熔解曲线:95℃,15s;60℃,1min;95℃,10s。使用quantstudiotmreal-time pcr software采集分析数据。
98.4.计算相对端粒长度
99.4.1.计算端粒(tel)及内参基因的ct值(取3组平行重复的均值);
100.4.2.计算每个样品的δct=ct
(tel)-ct
(reference)
,reference表示内参基因(即ifnb1、eef1g、prdx1、rpsa和/或vim);
101.4.3.计算每个样品的相对端粒长度t/s=2-[δct(sample)-δct(hela)]
,sample表示每个待测样品,hela表示hela细胞来源的参考基因组。
[0102]
实验例1.灵敏度检测
[0103]
按照实施例3的检测方法提取hela细胞来源的参考基因组dna并检测各基因及引物组合物的灵敏度。将hela细胞基因组dna做系列稀释(60ng、30ng、15ng、7.5ng和3.75ng五个梯度),每个样品设三个平行,按照实施例3的检测方法,分别得到tel、ifnb1、eef1g、prdx1、rpsa、vim和36b4(rplp0)的检测结果、扩增曲线及熔解曲线。检测结果如下表2所示,扩增曲线如图1所示,熔解曲线如图2所示。
[0104]
表2.灵敏度检测结果
[0105]
ct值(mean)telifnb1eef1gprdx1rpsavim36b460ng16.77724.62224.16822.39920.18423.55920.39330ng17.62326.06625.97223.58822.28824.75521.07715ng18.91327.94927.89025.29924.70326.38922.1267.5ng19.41729.71730.30526.93927.93027.78123.3643.75ng20.35231.96832.47529.03229.01728.38224.240
[0106]
由表2、图1及图2可知,本技术所述的引物组合物具有较好的检测灵敏度。
[0107]
且由图2可知,本技术所述的基因及引物组合物的熔解曲线呈细尖峰且只有单峰,表明引物的扩增产物单一,扩增结果良好。但36b4基因及其引物组合物的通解曲线在模板浓度较低时出现突起峰,表明其扩增产物为非单一性的产物,扩增结果较差。
[0108]
实验例2.重复性检测
[0109]
按照实施例3的检测方法提取20-30岁健康志愿者唾液样本基因组dna,稀释至30ng/μl,检测其相对端粒长度,重复检测三次,检测结果如下表3所示。该实验已获得志愿者许可。
[0110]
表3.重复性检测结果
[0111]
t/sifnb1eef1gprdx1rpsavim36b4第一次1.1203111.0460721.10165500.99890260.94852550.8159030第二次0.9926090.9559560.90772511.00109851.05426780.7947316第三次1.1869970.9970861.11524100.87377690.94416730.9873563最大相对偏差13.69%16.87%21.07%24.02%17.90%30.89%
变异系数(cv)7.33%3.68%9.10%6.21%5.18%9.96%
[0112]
由表2可知,本技术所述的引物组合物具有较好的检测重复性。
[0113]
实验例3.准确性检测
[0114]
选取20-30岁健康志愿者人群共22人,按照实施例3的检测方法分别提取该健康志愿者人群的唾液样本基因组dna,稀释至30ng/μl,检测其相对端粒长度,并与《automated assay of telomere length measurementand informatics for100,000subjects in the geneticepidemiology research on adult health and aging(gera)cohort》的检测结果进行对比。检测结果如下表4所示。
[0115]
表4.准确性检测结果
[0116]
samplet/s(eef1g)t/s(ifnb1)t/s(prdx1)t/s(rpsa)t/s(vim)std11.14701.30811.18600.90641.08940.131720.90821.37121.19160.84740.89230.204431.15231.34491.41061.03051.22110.135441.24271.31241.33291.08171.35370.098851.01881.36461.10901.01420.98230.139961.10241.41741.29390.96691.08820.160670.95001.23911.32050.98051.13580.143481.01771.33251.08491.01480.93270.136891.34251.51251.57111.25311.50670.1194101.05471.36691.16040.87431.05260.1613110.95600.89260.90771.00111.05430.0597121.82941.97231.76061.42111.36440.2368131.04611.12031.10170.99890.94850.0637141.55072.21371.77171.49711.68230.2544151.40012.02111.97881.92681.73530.2281161.24221.73831.38261.11381.04600.2455170.99711.28701.21520.87380.94420.1598181.38741.54371.31971.20311.13750.1425191.32361.96001.57701.33231.33200.2469201.65952.70912.06041.96301.88000.1510211.34931.69041.31461.25981.15810.1800221.11691.30101.08630.98631.21340.1080
[0117]
参照《automated assay of telomere length measurementand informatics for100,000subjects in the geneticepidemiology research on adult health and aging(gera)cohort》的检测报告,本技术所述的相对端粒长度(t/s)检测结果表明,上述样本均来自20-30岁人群端粒长度的范围之内,与实际情况相符,表明本技术所述的基因及其引物组合物的检测准确性较好。
[0118]
以上仅为本发明的实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明
构思的前提下,还可以做出若干变形和改进,这些均属于本发明的保护范围。
