三萜制备
1.引言
2.皂皮酸是在位置3和16处具有羟基基团、在位置23处具有醛基团且在位置28处具有羧酸的五环三萜类化合物(图1),并且已被证明具有有用的药用性质,例如rodr
í
guez-d
í
az m等人,topical anti-inflammatory activity of quillaic acid from quillaja saponaria mol.and some derivatives.jpharm pharmacol.2011may;63(5):718-24。皂皮酸的化学合成或生物合成途径均未知,并且因此,对皂皮酸制备方法的需求未得到满足。
3.发明概述
4.本发明提供了用于制备β-香树素氧化产物,诸如皂皮酸、皂皮酸前体及其还原和氧化形式的方法、组合物和系统,诸如工程化细胞。
5.一方面,本发明提供了一种制备氧化三萜的方法,其包括在其中c28氧化酶、c16氧化酶和c23氧化酶分别将β-香树素的c28、c16和c23碳分别氧化成羧基、羟基和甲酰基(醛)的条件下,孵育表达β-香树素合酶、细胞色素p450还原酶、细胞色素p450 c28氧化酶、细胞色素p450 c16氧化酶和细胞色素c23氧化酶的工程化微生物细胞或使其生长,以形成氧化三萜。
6.在实施方案中:
7.微生物细胞是酵母细胞,诸如酿酒酵母(saccharomyces cerevisiae)、巴斯德毕赤酵母(pichia pastoris)、或多形汉逊酵母(hansenula polymorpha);
8.微生物细胞是产油酵母细胞,诸如解脂耶氏酵母(yarrowia lipolytica)、圆红冬孢酵母(rhodosporidium toruloides)或斯达油脂酵母(lipomyces starkey);
9.微生物细胞是细菌细胞,诸如大肠杆菌(escherichia coli)、枯草芽孢杆菌(bacillus subtilis)、或链霉菌属细菌(streptomyces spp.);
10.将微生物细胞工程化以表达植物β-香树素合酶以使类异戊二烯或天然甾醇生物合成途径转向;
11.细胞色素p450还原酶选自:拟南芥细胞色素p450还原酶(atatr1)和百脉根(lotus japonicus)细胞色素p450还原酶(ljcpr);
12.细胞色素p450 c16氧化酶选自:cyp87d16和cyp716y1;
13.细胞色素p450 c23氧化酶选自:cyp72a68和cyp714e19;
14.细胞色素p450 c28氧化酶选自:cyp716a1、cyp716a12、cyp716a15、cyp716a17、cyp716a44、cyp716a46、cyp716a52v2、cyp716a75、cyp716a78、cyp716a79、cyp716a80、cyp716a81、cyp716a83、cyp716a86、cyp716a154、cyp716a110、cyp716a140、cyp716a 141、cyp716a179、cyp716a252和cyp716a253;
15.细胞色素p450还原酶、c28氧化酶、c16氧化酶和c23氧化酶中的1、2、3种或全部是植物的,特别是拟南芥(arabidopsis thaliana)、百脉根(lotus japonicus)、积雪草(centella asiatica)、蒺藜苜蓿(medicago truncatula)、柴胡(bupleurum falcatum)或披针形杜茎山(maesa lanceolate)的;
16.细胞色素p450还原酶、c28氧化酶、c16氧化酶和c23氧化酶独立地是拟南芥
(arabidopsis thaliana)、百脉根(lotus japonicus)、积雪草(centella asiatica)、蒺藜苜蓿(medicago truncatula)、柴胡(bupleurum falcatum)或披针形杜茎山(maesa lanceolate)的;
17.c16氧化酶和c23氧化酶是:cyp72a68(c23)和cyp716y1(c16);
18.细胞色素p450还原酶、c28氧化酶、c16氧化酶和c23氧化酶选自组合:ljcpr+cyp72a68(c23)+cyp716y1(c16)+cyp716a83(c28);ljcpr+cyp72a68(c23)+cyp716y1(c16)+cyp716a12(c28);和atrcpr+cyp72a68(c23)+cyp716y1(c16)+cyp716a12(c28),
19.氧化三萜选自皂皮酸、常春藤皂苷元(hederagenin)、葳岩仙皂苷元(caulophylogenin)、丝石竹皂苷元(gypsogenin)、丝石竹酸(gypsosenic acid)和氧化皂皮酸;和/或
20.c23碳被氧化成酸,并且任选地随后将该酸还原回醛,或者c23碳被氧化成醇,并且任选地随后将该醇氧化成醛,如此以形成皂皮酸。
21.一方面,本发明提供了一种用于制备氧化三萜的工程化微生物细胞,该细胞表达β-香树素合酶、细胞色素p450还原酶、细胞色素p450 c28氧化酶、细胞色素p450 c16氧化酶和细胞色素c23氧化酶,其中c28氧化酶、c16氧化酶和c23氧化酶分别将β-香树素的c28、c16和c23碳分别氧化成羧基、羟基和甲酰基(醛),形成氧化三萜。
22.本发明涵盖本文所列举的具体实施方案的所有组合,如同每个组合都已被着意列举一样。
附图说明
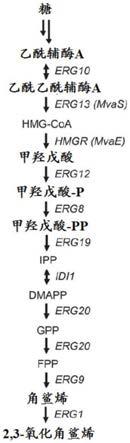
23.图1a.酿酒酵母(saccharomyces cerevisiae)中2,3-氧化角鲨烯制备的生物合成途径。
24.图1b.在皂苷合成的最后糖基化步骤之前,通过表达异源蛋白进行下游结构官能化以产生三萜。实线箭头:相应的酶已经被鉴定;虚线箭头:酶还有待被发现。
25.图2.工程化的酿酒酵母(s.cerevisiae.)中的皂皮酸生物合成途径的简化概述。示出了用于合成皂皮酸的交替途径,其中在右上角列出其相应的酶。示出了c16、c23和c28的氧化步骤。
26.图3.在酵母中体内组合制备皂皮酸和其他中间体。在表达atatr1、cyp72a68、cyp716y1和cyp716a12的工程化菌株中标准品的lc-ms色谱图的叠加(1:葳岩仙皂苷元,2:皂皮酸,3:丝石竹酸,4:16-羟基齐墩果酸,5:常春藤皂苷元,6:丝石竹皂苷元)。
27.发明具体实施方式的描述
28.除非另外禁用或说明,否则在这些描述和整个说明书中,术语“一(a)”和“一(an)”意指一或多,术语“或”意指和/或。本文所描述的实施例和实施方案仅用于说明性目的,并且将向本领域技术人员提示根据其的各种修改或变化,并且根据其的各种修改或变化将被包括在本技术的精神和范围以及所附权利要求书的范围内。本文引用的所有出版物、专利和专利申请,包括其中的引文,出于所有目的通过引用以其整体特此并入。
29.我们公开了使用在菌株中共表达异源蛋白质的组合策略,通过从工程化微生物,包括酵母,诸如酿酒酵母(saccharomyces cerevisiae)发酵制备氧化三萜。研究了来自各种植物来源的细胞色素p450还原酶和p450的组合。由于三萜构成具有各种工业和药物应用
的大且结构多样的一类天然产物,并且p450催化的结构修饰对于三萜支架的多样化和官能化是关键的,因此我们的策略提供了简单而通用的平台,以在工程化酵母中提供三萜及其p450官能化产物的可再生供应。
30.组合的氧化酶和萜环化酶表达策略与三萜制备菌株一起还提供了制备其他种类的具有生物活性但难以提取和/或纯化的天然存在的三萜的平台。
31.实施例:通过异源蛋白质的组合研究的皂皮酸生物合成
32.在本实施例中,我们提供了通过使用在具有高β-香树素产率的菌株中共表达异源蛋白质的组合策略,从工程化酿酒酵母(saccharomyces cerevisiae)发酵制备皂皮酸。证明了来自各种植物来源的细胞色素p450还原酶和p450的组合。由于酶的高特异性,p450可以选择性地官能化所选择的碳位置,而不需要绕道合成步骤以确保立体选择性和化学选择性。同样的策略也可以用于制备其他种类的天然存在的三萜,包括氧化的β-香树素产物。
33.由于天然的皂皮酸生物合成途径仍是未知的,从拟南芥(arabidopsis thaliana)、百脉根(lotus japonicus)、积雪草(centella asiatica)、蒺藜苜蓿(medicago truncatula)、柴胡(bupleurum falcatum)、披针形杜茎山(maesa lanceolate)中已表征了二十五种p450并且已证实了它们对作为底物的β-香树素的酶活性,它们被选择用于组合研究。在表达植物β-香树素合酶的工程化酵母菌株中由高拷贝数质粒表达三种p450的组合,所述p450包括一种用于在每个碳位置(c16、c23和c28)上进行官能化的酶,以使天然甾醇生物合成途径转向;参见例如,图2和kirby,romanini,paradise and keasling,febs journal 275(8)apr 2008,第1852-1859页,“engineering triterpene production in saccharomyces cerevisiaeβ-amyrin synthase from artemisia annua”。从培养基和糖的协调、培养基类型、发酵时间、添加剂的使用等方面验证了皂皮酸的制备过程。我们的结果确认了可以协同地将β-香树素转化为皂皮酸的功能酶。
34.选择液相色谱-质谱法(lc-ms)作为表征方法,以鉴定和纯化从酵母工厂制备的皂皮酸。表达atatr1、cyp72a68、cyp716y1和cyp716a12的菌株的体内制备水平提供了由其他不同酵母构建体制备的实例。在图3中,将来自酵母菌株的提取物的lc-ms色谱图与包括皂皮酸(2)以及其他氧化中间体:葳岩仙皂苷元(1),丝石竹酸(3),16-羟基齐墩果酸(4),常春藤皂苷元(5),丝石竹皂苷元(6)的真实样品进行比较。虽然观察到中间体3-6的积累,但在10.01min处存在对应于酵母提取物中的皂皮酸的洗脱峰明确地证实了其在体内制备。
35.我们还已经在酿酒酵母(saccharomyces cerevisiae)中验证了来自皂皮树(quillaja saponaria)的天然p450(cyp716a224,qs28氧化酶;cyp714e52,qs23氧化酶)。cyp716a297、qs16氧化酶反应性也得到证实;这些序列是公众可获得的。
