一种cu3zn(oh)6br2晶体及其制备方法
技术领域
1.本发明属于磁性材料制备的技术领域,特别涉及一种简单、新颖、高效的制备cu3zn(oh)6br2晶体的方法。
背景技术:
2.最近提出herbertsmithite这种材料以矿物学家赫伯特
·
史密斯的名字命名,是一种掺有杂质的氯铜矿化合物家族成员。这些材料最近在凝聚态物理界引起了许多关注,因为它们是研究量子磁体中挫折效应的优秀候选者。对于凝聚态物理领域的探索具有重要的研究意义。kapellasite作为herbertsmithite的亚稳多晶型,其化学式为cu3zn(oh)6cl2,于2008年发现。
3.随着科研技术的不断进步与发展,潜在的量子自旋液体材料(cu3m(oh)6x2)在磁学的研究领域备受关注(其中m=zn,ni,co,fe,cd,mg和x=cl,br,或i)。量子自旋液体的实验实现是物理学的一个长期目标,因为它们代表了物质的新状态。量子自旋液体不能用与常规基态相关的对称性来描述。自旋液体在描述高转变温度超导体的理论中有突出的作用,这些状态的拓扑性质可能在量子信息中有应用。致使潜在的量子自旋液体材料(cu3m(oh)6x2)的研究领域也日益增加。文献大量报道过合成cu3zn(oh)6cl2晶体。2008年在克里斯托弗
·
英戈尔德实验室合成了与herbertsmithite(cu3zn(oh)6cl2)化学式相同,但是晶体结构不同的kapellasite晶体(cu3zn(oh)6cl2)。文献报道,kriti gupta等人介绍过的cu3zn(oh)6cl2晶体晶型结构。shaoyan chu等人研究了cu3zn(oh)6cl2磁学性质。r.h.colman等人介绍了kapellasite的制备方法、磁学性质等。但对于cu3zn(oh)6br2制备方法的研究,至今也没有报道。本发明在制备cu3zn(oh)6br2晶体的方法具有一定的独创性。
技术实现要素:
4.本发明要解决的技术问题是,提供一种制备cu3zn(oh)6br2晶体材料的方法。
5.具体技术方案如下:
6.一种cu3zn(oh)6br2晶体,呈现薄厚均匀的条形块状结构,具有kapellasite结构,空间群为p-3m1,是潜在的量子自旋液体材料。
7.一种cu3zn(oh)6br2晶体的制备方法,以碱式碳酸铜粉末、溴化锌粉末为原料,首先将质量比为0.5:0.63的碱式碳酸铜粉末和溴化锌粉末加入醇水体系中,所述的醇水体系是体积比为2:1的乙醇和水的混合溶液,用量为每克碱式碳酸铜粉末使用30毫升,在磁力搅拌器中搅拌10分钟,形成均匀的混浊液,将此混浊液置于反应釜中在180~200摄氏度下密封反应4~8小时;待其冷却至室温,将固液分离、研磨后得到cu3zn(oh)6br2晶体材料。
8.制备尺寸均匀、晶型完整的cu3zn(oh)6br2晶体的最佳反应温度为180摄氏度;反应时间优选4小时。
9.有益效果:
10.本发明合成出cu3zn(oh)6br2晶体,呈现薄厚均匀的条形块状结构;操作简单易行、
重复性好、成本低廉;制备出的cu3zn(oh)6br2晶体的产量高、纯度高。本发明为合成的cu3zn(oh)6br2晶体提供了一种新方法。
附图说明
11.图1是实施例1制得的cu3zn(oh)6br2晶体的sem图。
12.图2是实施例1制得的cu3zn(oh)6br2晶体的edx图。
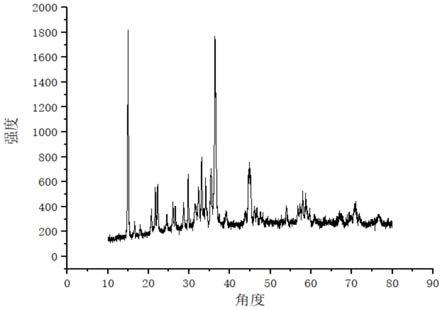
13.图3是实施例1制得的cu3zn(oh)6br2晶体的xrd谱图。
14.图4是实施例1制得的cu3zn(oh)6br2晶体的sem图。
15.图5是实施例2制得的cu3zn(oh)6br2晶体的sem图。
16.图6是实施例2制得的cu3zn(oh)6br2晶体的xrd谱图。
17.图7是实施例3制得的cu3zn(oh)6br2晶体的sem图。
18.图8是实施例3制得的cu3zn(oh)6br2晶体的xrd谱图。
19.图9是实施例4制得的cu3zn(oh)6br2晶体的sem图。
20.图10是实施例4制得的cu3zn(oh)6br2晶体的xrd谱图。
21.图11是实施例5制得的cu3zn(oh)6br2晶体的sem图。
具体实施方式
22.实施例1
23.以碱式碳酸铜粉末、无水溴化锌粉末为原料。首先取0.5克的碱式碳酸铜(cu2(oh)2co3)和0.63克氯化锌(znbr2)放入干净的烧杯中,加入15毫升乙醇和水的混合溶液(醇水体积比为2:1),并在磁力搅拌器中搅拌10分钟,使原料充分反应,得到混合溶液;将混合溶液倒入聚四氟乙烯内衬,放入不锈钢高压反应釜中密封,反应温度为180摄氏度下密封反应4小时;反应结束后,待其冷却至室温,将固液分离然后沉淀倒入干净的瓷盅,放在室温中干燥后进行研磨、收集,得到深绿色粉末状的cu3zn(oh)6br2样品。
24.本实施例是最佳实施例。
25.图1给出了上述条件制备的cu3zn(oh)6br2晶体的sem图,图2出上述条件下制备的cu3zn(oh)6br2晶体的edx图,可以得出纳米晶体只由cu、zn、o、h、br五种元素组成(其中h元素为无法测试的元素)。图3给出上述条件下制备的cu3zn(oh)6br2晶体的xrd谱图,证明合成的cu3zn(oh)6br2样品结晶性好,产物纯度高。图4给出所制备的cu3zn(oh)6br2晶体的扫描电镜,可以看出所制备的样品都是薄厚均匀的条形块状结构,粒径尺寸均一。
26.实施例2
27.以碱式碳酸铜粉末、无水溴化锌粉末为原料。首先取0.5克的碱式碳酸铜(cu2(oh)2co3)和0.63克氯化锌(znbr2)放入干净的烧杯中,加入15毫升去离子水,并在磁力搅拌器中搅拌10分钟,使原料充分反应,得到混合溶液;将混合溶液倒入聚四氟乙烯内衬,放入不锈钢高压反应釜中密封,反应温度为180摄氏度下密封反应4小时;反应结束后,待其冷却至室温,将固液分离然后沉淀倒入干净的瓷盅,放在室温中干燥后进行研磨、收集,得到深绿色粉末状的cu3zn(oh)6br2样品。
28.图5给出所制备的cu3zn(oh)6br2晶体的扫描电镜,大部分形貌呈现堆叠层状,与cu3zn(oh)6br2形貌不符。图6给出上述条件下制备的cu3zn(oh)6br2晶体的xrd谱图,杂质峰
多且结晶性不好。
29.本实施例是作为对比的反例,说明当反应体系不合适时无法制备出良好结晶的cu3zn(oh)6br2晶体。
30.实施例3
31.以碱式碳酸铜粉末、无水溴化锌粉末为原料。首先取0.5克的碱式碳酸铜(cu2(oh)2co3)和0.63克氯化锌(znbr2)放入干净的烧杯中,加入15毫升乙醇和水的混合溶液(醇水体积比为2:1),并在磁力搅拌器中搅拌10分钟,使原料充分反应,得到混合溶液;将混合溶液倒入聚四氟乙烯内衬,放入不锈钢高压反应釜中密封,反应温度为180摄氏度下密封反应8小时;反应结束后,待其冷却至室温,将固液分离然后沉淀倒入干净的瓷盅,放在室温中干燥后进行研磨、收集,得到深绿色粉末状的cu3zn(oh)6br2样品。
32.图7给出所制备的cu3zn(oh)6br2晶体的扫描电镜,可以看出所制备的样品都是条形块状形状。图8给出上述条件下制备的cu3zn(oh)6br2晶体的xrd谱图。
33.实施例4
34.以碱式碳酸铜粉末、无水溴化锌粉末为原料。首先取0.5克的碱式碳酸铜(cu2(oh)2co3)和0.63克氯化锌(znbr2)放入干净的烧杯中,加入15毫升乙醇和水的混合溶液(醇水体积比为2:1),并在磁力搅拌器中搅拌10分钟,使原料充分反应,得到混合溶液;将混合溶液倒入聚四氟乙烯内衬,放入不锈钢高压反应釜中密封,反应温度为200摄氏度下密封反应4小时;反应结束后,待其冷却至室温,将固液分离然后沉淀倒入干净的瓷盅,放在室温中干燥后进行研磨、收集,得到深绿色粉末状的cu3zn(oh)6br2样品。
35.图9给出所制备的cu3zn(oh)6br2晶体的扫描电镜,可以看出所制备的样品都是条形块状形状,但是形貌大小不均一。图10给出上述条件下制备的cu3zn(oh)6br2晶体的xrd谱图。
36.实施例5
37.以碱式碳酸铜粉末、无水溴化锌粉末为原料。首先取0.5克的碱式碳酸铜(cu2(oh)2co3)和0.63克氯化锌(znbr2)放入干净的烧杯中,加入15毫升乙醇和水的混合溶液(醇水体积比为2:1),并在磁力搅拌器中搅拌10分钟,使原料充分反应,得到混合溶液;将混合溶液倒入聚四氟乙烯内衬,放入不锈钢高压反应釜中密封,反应温度为200摄氏度下密封反应8小时;反应结束后,待其冷却至室温,将固液分离然后沉淀倒入干净的瓷盅,放在室温中干燥后进行研磨、收集,得到深绿色粉末状的cu3zn(oh)6br2样品。
38.图11给出所制备的cu3zn(oh)6br2晶体的扫描电镜,可以看出所制备的样品都是条形块状形状,但是形貌大小不均一。
