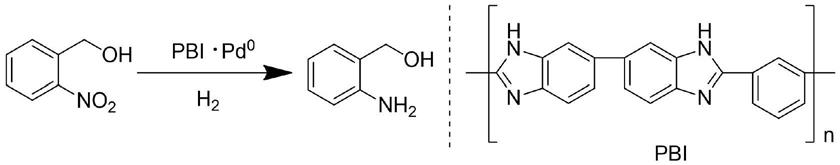
1.本发明属于有机合成技术领域,具体涉及一种邻氨基苯甲醇类化合物的合成方法。
背景技术:
2.邻氨基苯甲醇类化合物是一种重要化工中间体,在有机化学和药物合成中有广泛的用途,特别是在杂环化合物的合成中起着重要的作用。当前,国内生产邻氨基苯甲醇类化合物主要为化学还原法,但是该工艺操作繁琐,废水量大。与化学还原法相比,催化氢化具有原子经济性高、设备通用性强、高效绿色生产工艺等特点,目前国内外催化氢化制备邻氨基苯甲醇类化合物的合成工艺主要有以下四种方法:
3.(一)1985年jean m.j.frechet报道的邻硝基苯甲醇氢化合成路线(j.chem.soc.,chem.commun.1985,16,1100-1101),该路线催化剂制备复杂,底物单一。
[0004][0005]
(二)matthias beller课题组在2017年报道的在碳材料负载的纳米co-co3o4@carbon-700选择性氢化硝基化合物制备邻氨基苯甲醇(chemsuschem 2017,10,3035-3039),该路线避免使用贵金属,但是反应周期长,氢气压力高,效率低。
[0006][0007]
(三)rhett kempez课题组报道的可回收的ni@sicn或fe@sicn催化剂选择性氢化硝基化合物制备邻氨基苯甲醇(chemcatchem2016,8,2461-2465;chem.eur.j.2018,24,8989-8993),二条路线的优点是催化剂可回收,但催化剂制备复杂,反应收率低。
[0008][0009]
(四)2017年肖丰收教授报道合成了一种pd@beta催化剂,能很好实现硝基的选择性氢化,但氢化过程需要贵金属钯(angew.chem.int.ed.2017,56,9747-9751)。
[0010]
因此,研发绿色环保,成本低的氢化合成方法,对于邻氨基苯甲醇类化合物的绿色工业化生产具有重要意义。而邻氨基苯甲醇类化合物是合成杂环化合物重要的中间体,因此,研发绿色环保、操作简便且成本低的氢化合成方法,对于杂环化合物的绿色工业化生产具有重要意义。
技术实现要素:
[0011]
本发明是为了解决上述问题而进行的,目的在于提供一种绿色环保、操作简便且成本低的邻氨基苯甲醇类化合物的合成方法。
[0012]
本发明提供了一种邻氨基苯甲醇类化合物的合成方法,其特征在于:以邻硝基苯甲酸酯类化合物为原料,在催化剂、碱和溶剂的条件下,在80℃~120℃的温度,10bar~50bar的氢气压力下反应5h~12h制得邻氨基苯甲醇类化合物,反应方程式如下:
[0013][0014]
其中,所述催化剂由[mn(co)5br]和配体l制备得到,
[0015]
邻硝基苯甲酸酯类化合物具有通式ⅰ所示的结构,所述配体l为磷氮氮,配体l具有通式ⅱ所示的结构,
[0016][0017]
通式ⅰ中,r1为c1~c
10
烷基,c3~c
12
环烷基,含有n、s、o、p中一种或二种以上官能团的c1~c
10
烷基,含有n、s、o、p中一种或二种以上官能团的c3~c
10
环烷基,c6~c
30
内的芳香基团,卤素原子中任一种;r2为甲基、乙基、异丙基中任一种,
[0018]
通式ⅱ中,ar为c6~c
60
内的芳香基团,含氮杂环基团为:吡啶、咪唑、喹啉、噻唑、苯并咪唑或苯并噻唑中的任一种。
[0019]
最优的,反应温度为90℃~110℃,氢气压力为20bar~40bar,反应时间为6h。
[0020]
进一步,在本发明提供的邻氨基苯甲醇类化合物的合成方法中,还可以具有这样的特征:反应的溶剂为乙醇、甲醇、异丙醇中的任一种。最优的,溶剂选择乙醇。
[0021]
进一步,在本发明提供的邻氨基苯甲醇类化合物的合成方法中,还可以具有这样的特征:碱为叔丁醇钾、叔丁醇钠、碳酸铯、碳酸钾、碳酸钠、碳酸氢钠中的一种或多种。最优的,碱选择叔丁醇钾。
[0022]
进一步,在本发明提供的邻氨基苯甲醇类化合物的合成方法中,还可以具有这样的特征:邻硝基苯甲酸酯类化合物和碱的摩尔比为(5~20):1;
[0023]
邻硝基苯甲酸酯类化合物和催化剂中mn原子的摩尔比为(5~200):1。
[0024]
最优的,邻硝基苯甲酸酯类化合物和碱的摩尔比为(10~15):1;
[0025]
邻硝基苯甲酸酯类化合物和催化剂中mn原子的摩尔比为(50~100):1。
[0026]
进一步,在本发明提供的邻氨基苯甲醇类化合物的合成方法中,还可以具有这样的特征:所述催化剂由[mn(co)5br]和配体l在溶剂中原位生成。
[0027]
进一步,在本发明提供的邻氨基苯甲醇类化合物的合成方法中,还可以具有这样的特征:首先由[mn(co)5br]和配体l在溶剂中原位生成催化剂,然后加入邻硝基苯甲酸酯
类化合物、碱和溶剂后置入高压反应釜中,通入氢气,反应完成后,冷却,慢慢释放氢气,除去溶剂后用硅胶柱分离得到产物邻氨基苯甲醇类化合物,其中,生成催化剂所用溶剂和反应所用溶剂相同。
[0028]
进一步,在本发明提供的邻氨基苯甲醇类化合物的合成方法中,还可以具有这样的特征:置入高压反应釜之前的操作中需要在氮气的保护下进行。
[0029]
进一步,在本发明提供的邻氨基苯甲醇类化合物的合成方法中,还可以具有这样的特征:置入高压反应釜后需要用氢气置换至少三次,然后再通入氢气至需要的压力。
[0030]
本发明提供了如下优点:
[0031]
本发明所涉及的邻氨基苯甲醇类化合物的合成方法与现有的化学还原法工艺相比,通过氢化邻硝基苯甲酸酯制备邻氨基苯甲醇类化合物,可以显著降低能耗,降低生产时间,降低成本,减少三废。成功地解决了氢化过程需要贵金属、效率低等问题,具有很好的工业实用性。
附图说明
[0032]
图1是本发明中实施例一中产物的核磁共振氢谱图;
[0033]
图2是本发明中实施例一中产物的核磁共振碳谱图;
[0034]
图3是本发明中实施例十中产物的核磁共振氢谱图;
[0035]
图4是本发明中实施例十中产物的核磁共振碳谱图;
[0036]
图5是本发明中实施例十一中产物的核磁共振氢谱图;
[0037]
图6是本发明中实施例十一中产物的核磁共振碳谱图;
[0038]
图7是本发明中实施例十二中产物的核磁共振氢谱图;
[0039]
图8是本发明中实施例十二中产物的核磁共振碳谱图;
[0040]
图9是本发明中实施例十三中产物的核磁共振氢谱图;
[0041]
图10是本发明中实施例十三中产物的核磁共振碳谱图;
[0042]
图11是本发明中实施例十四中产物的核磁共振氢谱图;
[0043]
图12是本发明中实施例十四中产物的核磁共振碳谱图;
[0044]
图13是本发明中实施例十五中产物的核磁共振氢谱图;
[0045]
图14是本发明中实施例十五中产物的核磁共振碳谱图。
具体实施方式
[0046]
为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,以下实施例结合附图对本发明的邻氨基苯甲醇类化合物的合成方法作具体阐述。
[0047]
《实施例一》
[0048]
制备2-氨基-4-甲基苯甲醇。以2-硝基-4-甲基苯甲酸甲酯为原料。配体l为磷氮氮配体,在本实施例中,配体l的结构如下所示:
[0049][0050]
以2-硝基-4-甲基苯甲酸甲酯为原料制备2-氨基-4-甲基苯甲醇的反应方程式如
下:
[0051][0052]
2-氨基-4-甲基苯甲醇的制备方法为:
[0053]
在氮气保护下,将[mn(co)5br](0.005mmol,1mol%),膦氮氮配体l(0.0055mmol,1.1mol%)溶于乙醇(1ml),室温下搅拌30分钟,加入底物2-硝基-4-甲基苯甲酸甲酯(0.5mmol)及叔丁醇钾(0.025mmol,5mol%),再加入乙醇(1ml),将其置于高压反应釜中,氢气换气三次,然后通入氢气至20bar,100℃下反应6小时。冷却,慢慢释放氢气,除去溶剂后用硅胶柱分离得到66.5毫克产物,收率97%。
[0054]
《实施例二》
[0055]
本实施例与实施例一相同的部分省略,与实施例一不同的是,在本实施例中,底物2-硝基-4-甲基苯甲酸甲酯与催化剂中mn原子的摩尔比为200:1,即:[mn(co)5br]的物质的量为0.0025mmol,膦氮氮配体l的物质的量为0.00275mmol。底物2-硝基-4-甲基苯甲酸甲酯与叔丁醇钾的摩尔比为5:1,即叔丁醇钾用量为0.1mmol。反应时间为5小时。反应温度为120℃。氢气换气四次。
[0056]
最终得54.8毫克产物,收率80%。
[0057]
《实施例三》
[0058]
本实施例与实施例一相同的部分省略,与实施例一不同的是,在本实施例中,底物2-硝基-4-甲基苯甲酸甲酯与催化剂中mn原子的摩尔比为50:1,即:[mn(co)5br]的物质的量为0.01mmol,膦氮氮配体l的物质的量为0.011mmol。碱为碳酸铯,底物2-硝基-4-甲基苯甲酸甲酯与碳酸铯的摩尔比为10:1,即碳酸铯用量为0.05mmol。反应时间为12小时。反应温度为110℃。最终得61.7毫克产物,收率90%。
[0059]
《实施例四》
[0060]
本实施例与实施例一相同的部分省略,与实施例一不同的是,在本实施例中溶剂为甲醇。底物2-硝基-4-甲基苯甲酸甲酯与催化剂中mn原子的摩尔比为80:1,即:[mn(co)5br]的物质的量为0.06mmol,膦氮氮配体l的物质的量为0.066mmol。底物2-硝基-4-甲基苯甲酸甲酯与叔丁醇钾的摩尔比为12:1,即叔丁醇钾用量为0.042mmol。最终得65.2毫克产物,收率95%。
[0061]
《实施例五》
[0062]
本实施例与实施例一相同的部分省略,与实施例一不同的是,在本实施例中,底物2-硝基-4-甲基苯甲酸甲酯与催化剂中mn原子的摩尔比为5:1,即:[mn(co)5br]的物质的量为0.1mmol,膦氮氮配体l的物质的量为0.11mmol。碱为叔丁醇钠,底物2-硝基-4-甲基苯甲酸甲酯与叔丁醇钠的摩尔比为15:1,即叔丁醇钠用量为0.0333mmol。反应时间为8小时。反应温度为80℃。最终得61毫克产物,收率89%。
[0063]
《实施例六》
[0064]
本实施例与实施例一相同的部分省略,与实施例一不同的是,在本实施例中,高压
反应釜中氢气压力为10bar。反应温度90℃。碱为碳酸氢钠。配体l的结构如下所示:
[0065][0066]
最终得58.3毫克产物,收率85%。
[0067]
《实施例七》
[0068]
本实施例与实施例一相同的部分省略,与实施例一不同的是,在本实施例中,溶剂为异丙醇。高压反应釜中氢气压力为30bar。碱为碳酸钾。配体l的结构如下所示:
[0069][0070]
最终得61.8毫克产物,收率90%。
[0071]
《实施例八》
[0072]
本实施例与实施例一相同的部分省略,与实施例一不同的是,在本实施例中,高压反应釜中氢气压力为40bar。碱为碳酸钠。配体l的结构如下所示:
[0073][0074]
最终得48毫克产物,收率70%。
[0075]
《实施例九》
[0076]
本实施例与实施例一相同的部分省略,与实施例一不同的是,在本实施例中,高压反应釜中氢气压力为50bar。以2-硝基-4-甲基苯甲酸乙酯为原料。最终得65.8毫克产物,收率96%。
[0077]
对实施例一至实施例九的产物进行检测分析,经检测实施例一至实施例九的产物均为2-氨基-4-甲基苯甲醇。
[0078]
在本文本中仅提供实施例一中的nmr数据和谱图,实施例一中nmr谱图如图1、图2所示,实施例一中nmr数据如下所示:
[0079]1h nmr(400mhz,dmso)δ6.91(d,j=7.5hz,1h),6.44(s,1h),6.33(d,j=7.5hz,1h),4.89(t,j=5.3hz,1h),4.81(s,2h),4.34(d,j=5.2hz,2h),2.15(s,3h).
13
c nmr(101mhz,dmso)δ146.76(s),137.02(s),128.33(s),123.12(s),117.05(s),115.64(s),99.99(s),61.51(s),21.41(s).
[0080]
《实施例十》
[0081]
本实施例与实施例一的制备方法相同,相同的部分省略,与实施例一不同的是,在本实施例中,以2-硝基-3-甲基苯甲酸甲酯为原料,制备2-氨基-3-甲基苯甲醇。最终得65.9毫克产物,收率96%。
[0082]
对产物进行检测分析,本实施例中,nmr谱图如图3、图4所示,nmr数据如下所示:
[0083]1h nmr(400mhz,dmso)δ7.05
–
6.79(m,2h),6.48(dd,j=7.0,3.3hz,1h),5.03(d,j=4.1hz,1h),4.68(s,2h),4.54
–
4.34(m,2h),2.09(d,j=2.6hz,3h).
[0084]
13
c nmr(101mhz,dmso)δ144.74(s),129.48(s),126.30(s),125.28(s),121.60(s),116.07(s),99.99(s),62.19(s),17.93(s).
[0085]
经检测,产物为:2-氨基-3-甲基苯甲醇。
[0086]
《实施例十一》
[0087]
本实施例与实施例一的制备方法相同,相同的部分省略,与实施例一不同的是,在本实施例中,以2-硝基-5-氟苯甲酸甲酯为原料,制备2-氨基-5-氟苯甲醇。最终得67毫克产物,收率95%。
[0088]
对产物进行检测分析,本实施例中,nmr谱图如图5、图6所示,nmr数据如下所示:
[0089]1h nmr(400mhz,dmso)δ7.05(d,j=8.0hz,1h),6.65(s,1h),6.52(dd,j=8.0,1.6hz,1h),5.20(s,2h),5.06(t,j=5.1hz,1h),4.35(d,j=4.6hz,2h).
13
c nmr(101mhz,dmso)δ148.20(s),132.27(s),129.39(s),124.67(s),115.47(s),113.90(s),60.77(s).
[0090]
经检测,产物为:2-氨基-5-氟苯甲醇。
[0091]
《实施例十二》
[0092]
本实施例与实施例一的制备方法相同,相同的部分省略,与实施例一不同的是,在本实施例中,以2-硝基-5-甲氧基苯甲酸甲酯为原料,制备2-氨基-5-甲氧基苯甲醇。最终得73.5毫克产物,收率96%。
[0093]
对产物进行检测分析,本实施例中,nmr谱图如图7、图8所示,nmr数据如下所示:
[0094]1h nmr(400mhz,dmso)δ6.73(d,j=2.2hz,1h),6.57(dd,j=7.2,5.5hz,2h),5.02(t,j=5.1hz,1h),4.46(s,2h),4.36(d,j=4.7hz,2h),3.63(s,3h).
13
c nmr(101mhz,dmso)δ151.29(s),140.13(s),127.47(s),116.01(s),113.75(s),113.38(s),61.30(s),55.73(s).
[0095]
经检测,产物为:2-氨基-5-甲氧基苯甲醇。
[0096]
《实施例十三》
[0097]
本实施例与实施例一的制备方法相同,相同的部分省略,与实施例一不同的是,在本实施例中,以2-硝基-5-甲基苯甲酸甲酯为原料,制备2-氨基-5-甲基苯甲醇。最终得65.8毫克产物,收率96%。
[0098]
对产物进行检测分析,本实施例中,nmr谱图如图9、图10所示,nmr数据如下所示:
[0099]1h nmr(400mhz,dmso)δ6.86(s,1h),6.77(d,j=7.9hz,1h),6.52(d,j=7.9hz,1h),4.94(s,1h),4.67(s,2h),4.35(d,j=5.1hz,2h),2.14(s,3h).
13
c nmr(101mhz,dmso)δ144.28(s),128.80(s),128.46(s),125.97(s),124.56(s),115.21(s),61.66(s),20.66(s).
[0100]
经检测,产物为:2-氨基-5-甲基苯甲醇。
[0101]
《实施例十四》
[0102]
本实施例与实施例一的制备方法相同,相同的部分省略,与实施例一不同的是,在本实施例中,以2-硝基-5-溴苯甲酸甲酯为原料,制备2-氨基-5-溴苯甲醇。最终得96毫克产物,收率95%。
[0103]
对产物进行检测分析,本实施例中,nmr谱图如图11、图12所示,nmr数据如下所示:
[0104]1h nmr(400mhz,dmso)δ7.21(d,j=2.3hz,1h),7.07(dd,j=8.5,2.4hz,1h),6.56(d,j=8.5hz,1h),5.11(t,j=5.5hz,1h),5.06(s,2h),4.34(d,j=5.5hz,2h).
13
c nmr
(101mhz,dmso)δ145.69(s),130.15(s),129.74(s),128.37(s),116.72(s),106.96(s),60.46(s)。
[0105]
经检测,产物为:2-氨基-5-溴苯甲醇。
[0106]
《实施例十五》
[0107]
本实施例与实施例一的制备方法相同,相同的部分省略,与实施例一不同的是,在本实施例中,以2-硝基-6-甲基甲酸甲酯为原料,制备2-氨基-6-甲基苯甲醇。最终得63.8毫克产物,收率93%。
[0108]
对产物进行检测分析,本实施例中,nmr谱图如图13、图14所示,nmr数据如下所示:
[0109]1h nmr(400mhz,cdcl3)δ7.00(t,j=7.7hz,1h),6.74
–
6.47(m,2h),4.73(s,2h),3.23(s,3h),2.32(s,3h).
13
c nmr(101mhz,cdcl3)δ146.40(s),136.78(s),128.83(s),123.33(s),120.80(s),114.43(s),59.00(s),19.55(s).
[0110]
经检测,产物为:2-氨基-6-甲基苯甲醇。
[0111]
本发明所涉及的邻氨基苯甲醇类化合物的合成方法并不限于具体实施例的范围。以上内容仅为本发明的基本说明,而依据本发明的技术方案所作的任何等效变换,均应属于本发明的保护范围。
