甘草中具有抗结直肠癌活性的化合物制备及其应用
一、技术领域
1.本发明属于中药技术领域,涉及一种化合物制备及其应用,具体地说是一种甘草中具有抗结直肠癌活性的化合物制备及其应用。
二、
背景技术:
2.甘草是豆科甘草属植物,全世界约有20多个种,主要分布于东欧至东亚。在中国,该属共有8个种,大部分发现于华北地区,如河北、河南、山西、陕西、山东、内蒙古和新疆。其中乌拉尔甘草glycyrrhiza uralensis fisch.、胀果甘草glycyrrhiza inflata bat.、光果甘草glycyrrhiza glabra l.在中药中作为甘草用于治疗咳嗽、流感、糖尿病、癌症等多种疾病。植物化学研究表明,它含有多种活性天然产物,目前已从甘草中分离鉴定出400多种化学成分,如三萜皂苷、黄酮类化合物、甾醇、多糖和香豆素。其中黄酮类化合物作为主要活性成分,具有抗肿瘤、抗病原微生物、抗前列腺炎等活性。
3.结直肠癌(colorectal cancer,crc)是一种严重威胁人类健康的恶性肿瘤,尽管最近在用于治疗结直肠癌的放疗,化疗和手术技术方面取得了很好的进展,但结直肠癌患者的总生存率仍然很低。化疗是一种必不可少的治疗方式,常用于抑制癌症复发和延长患者生命。然而,尽管具有独特的抗癌特性,但化疗的副作用和选择性限制了其使用范围。有趣的是,越来越多的证据表明crc不是单一的、统一的疾病类型,而是由一组以一系列基因组和表观基因组改变为特征的分子异质性疾病。此外,来自癌症基因组图谱(tcga)的数据表明,wnt/β-catenin信号通路在93%的非超突变crc和97%的超突变crc中被激活,因此,该信号是一个合适的药物靶点,具有治疗crc的潜力。天然产物与wnt/β-catenin信号通路密切相关,从天然产物中寻找具有抗结直肠癌活性的化合物具有重要意义。
三、
技术实现要素:
4.本发明的目的在于分离出一种从光果甘草中提取的具有抗结直肠癌活性的化合物及其应用,所述式1,式2化合物对人结直肠癌ht-29和rko细胞具有较高的抑制作用,因此本发明提供甘草中单体化合物在抗结直肠癌药物中的应用。
5.为实现上述目的,本发明所述化合物,其特征在于:所述化合物为异黄酮类化合物包括具有如式1所示结构的组分:
[0006][0007][0008]
或其药学上可接受的盐。
[0009]
所述化合物为二氢异黄酮类化合物包括具有如式2和式3所示结构的组分:
[0010][0011]
或其药学上可接受的盐。
[0012]
所述式3的化合物:
[0013][0014]
或其药学上可接受的盐。
[0015]
所述化合物或其药学上可接受的盐的剂型为片剂,胶囊,散剂,微粒,颗粒剂,糖浆剂,溶液剂,透皮贴剂,栓剂的任一种剂型。
[0016]
所述化合物有效成分在制备治疗结直肠癌药物中的应用。
[0017]
所述化合物具有抑制的作用。
[0018]
所述化合物的提取方法,实现步骤如下:
[0019]
(1)称取光果甘草3kg,用70%甲醇浸泡,浸泡滤液减压浓缩干燥得甲醇浸膏,加2500ml水混悬,用等体积的有机溶剂萃取,得到有机溶剂提取物;
[0020]
(2)取有机溶剂提取物用硅胶柱色谱分离:
[0021]
首先,采用石油醚-乙酸乙酯100:1-0:100梯度洗脱,得到15部分(fr.a-o);
[0022]
然后,fr.f用石油醚-乙酸乙酯硅胶柱色谱梯度洗脱,得到6部分(fr.f1-f6);fr.f3用二氯甲烷-甲醇硅胶柱色谱梯度洗脱,得到6部分(fr.f3a-f3f);
[0023]
最后fr.f3b经甲醇-水开放ods柱色谱梯度洗脱、ptlc和半制备hplc 75%甲醇纯化,得到异黄酮类化合物;fr.f3c经甲醇-水开放ods柱色谱梯度洗脱、ptlc和半制备hplc 75%甲醇纯化,得到二氢异黄酮类化合物。
[0024]
所述提取原料为光果甘草的根及根茎。
[0025]
所述步骤(1)中用70%甲醇提取次数为4次,70%甲醇用量为甘草根茎重量的8倍;所述步骤(1)中有机溶剂为乙酸乙酯;所述步骤(1)中有机溶剂萃取步骤为:用等体积的乙酸乙酯萃取4次。
[0026]
本发明所述一种甘草中具有抗结直肠癌活性的化合物制备及其应用,其有益效果在于:本发明得到的化合物为新化合物,所述新化合物为具有抗结直肠癌活性的异黄酮类化合物和二氢异黄酮类化合物,及其药学上可接受的盐。本发明以光果甘草的根及根茎为原料,其提取方法操作简单,且提取得到的化合物纯度高,用途较广,效果较好。所述化合物
对人结直肠癌ht-29和rko细胞具有较好的抑制作用,在研发新型抗结直肠癌药和合理利用甘草资源方面前景良好。
四、附图说明
[0027]
图1本发明所述3个新化合物对ht-29细胞的抑制作用。
[0028]
图2本发明所述3个新化合物对rko细胞的抑制作用。
五、具体实施方式
[0029]
实施例1
[0030]
本发明所述一种甘草中具有抗结直肠癌活性的化合物制备,操作步骤如下:
[0031]
1、仪器与材料
[0032]
avance av iii-400核磁共振波谱仪(瑞士布鲁克公司);超高效二维液相色谱仪-气相谱仪-四级杆飞行时间离子淌度质谱仪(美国安捷伦公司);半制备型高效液相色谱仪(上海通威分析技术有限公司);easyseptm-1050半制备液相色谱仪专用溶剂输液泵;easyseptm-1050半制备液相色谱仪专用紫外/可见光检测器;制备型色谱柱(cosmosil-pack 5c18-ms
‑ⅱ
);薄层色谱硅胶gf254和柱色谱硅胶(200-300目,青岛海洋化工有限公司);所用试剂均为分析纯(天津市富宇精细化工有限公司)。
[0033]
2、提取与分离:
[0034]
称取干燥的光果甘草根及根茎3kg,用70%甲醇浸泡过夜,重复4次,合并滤液,减压浓缩干燥得甲醇浸膏,加适量水混悬,用等体积的乙酸乙酯萃取4次,得到乙酸乙酯提取物67.27g。
[0035]
取乙酸乙酯提取物67.27g用硅胶柱色谱分离,采用石油醚-乙酸乙酯(100:1-0:100,v/v)梯度洗脱,得到15部分(fr.a-o);然后,fr.f用石油醚-乙酸乙酯硅胶柱色谱梯度洗脱,得到6部分(fr.f1-f6);fr.f3用二氯甲烷-甲醇硅胶柱色谱梯度洗脱,得到6部分(fr.f3a-f3f);最后fr.f3b经甲醇-水开放ods柱色谱梯度洗脱、ptlc和半制备hplc 75%甲醇纯化,得到异黄酮类化合物,所述得到的异黄酮类化合物为化合物1(式1);fr.f3c经甲醇-水开放ods柱色谱梯度洗脱、ptlc和半制备hplc 75%甲醇纯化,得到二氢异黄酮类化合物,所述得到二氢异黄酮类化合物为化合物2(式2)、化合物3(式3)。
[0036]
3、结构与鉴定:
[0037]
化合物1:淡黄色粉末;分子式c
25h22
o6;hr-esi-ms m/z:417.1416[m-h]-;1h-nmr(400mhz,dmso-d6)δ:8.23(1h,s,h-2),6.27(1h,s,h-6),6.44(1h,d,j=8.0hz,h-5'),6.93(1h,d,j=8.0hz,h-6'),6.69(1h,d,j=10.0hz,h-1”),5.79(1h,d,j=10.0hz,h-2”),1.45(3h,s,h-4”),1.45(3h,s,h-5”),6.61(1h,d,j=10.0hz,d,j=10.0hz,h-1”'),5.65(1h,d,j=10.0hz,h-2”'),1.31(3h,s,h-4”'),1.31(3h,s,h-5”');
13
c-nmr(100mhz,dmso-d6)δ:155.7(c-2),120.7(c-3),180.9(c-4),154.0(c-5),99.9(c-6),161.8(c-7),101.3(c-8),159.2(c-9),105.7(c-10),109.7(c-1'),151.9(c-2'),109.5(c-3'),152.1(c-4'),107.8(c-5'),131.7(c-6'),114.4(c-1”),128.7(c-2”),78.7(c-3”),28.2(c-4”),28.2(c-5”),117.2(c-1”'),129.1(c-2”'),76.3(c-3”'),27.9(c-4”'),27.9(c-5”')。
[0038]
化合物2:淡黄色粉末;分子式c
25h28
o6;hr-esi-ms m/z:423.1813[m-h]-;1h-nmr
(400mhz,dmso-d6)δ:4.50(1h,dd,j=10.8,10.8hz,h-2α),4.45(1h,dd,j=10.8,5.6hz,h-2β),4.15(1h,dd,j=10.8,5.6hz,h-3),5.85(1h,s,h-6),6.31(1h,d,j=8.0hz,h-5'),6.76(1h,d,j=8.0hz,h-6'),2.55(1h,t,j=6.8hz,h-1”),1.77(1h,t,j=6.8hz,h-2”),1.31(3h,s,h-4”),1.28(3h,s,h-5”),2.48(1h,t,j=6.8hz,h-1”'),1.68(1h,t,j=6.8hz,h-2”'),1.16(3h,s,h-4”'),1.13(3h,s,h-5”');
13
c-nmr(100mhz,dmso-d6)δ:70.6(c-2),47.2(c-3),198.5(c-4),160.4(c-5),96.8(c-6),162.1(c-7),100.7(c-8),161.4(c-9),103.0(c-10),113.6(c-1'),152.4(c-2'),108.9(c-3'),155.7(c-4'),106.1(c-5'),128.7(c-6'),16.2(c-1”),31.6(c-2”),76.5(c-3”),27.4(c-4”),26.5(c-5”),17.4(c-1”'),31.9(c-2”'),74.3(c-3”'),27.3(c-4”'),25.9(c-5”')。
[0039]
化合物3,淡黄色粉末;分子式c
25h28
o6;hr-esi-ms m/z:423.1818[m-h]-;1h-nmr(400mhz,dmso-d6)δ:4.41(1h,dd,j=10.4,10.4hz,h-2α),4.38(1h,dd,j=10.4,6.4hz,h-2β),4.09(1h,dd,j=10.4,6.4hz,h-3),5,98(1h,s,h-6),6.29(1h,d,j=8.0hz,h-5'),6.75(1h,d,j=8.0hz,h-6'),3.10(2h,t,j=7.2hz,h-1”),5.10(1h,t,j=7.2hz,h-2”),1.62(3h,s,h-4”),1.67(3h,s,h-5”),2.51(1h,t,j=6.8hz,h-1”'),1.70(1h,t,j=6.8hz,h-2”'),1.15(3h,s,h-4”'),1.12(3h,s,h-5”');
13
c-nmr(100mhz,dmso-d6)δ:70.5(c-2),47.2(c-3),198.3(c-4),162.0(c-5),95.9(c-6),164.9(c-7),107.3(c-8),160.2(c-9),102.6(c-10),114.0(c-1'),152.3(c-2'),108.9(c-3'),155.6(c-4'),106.0(c-5'),128.6(c-6'),21.6(c-1”),123.5(c-2”),130.6(c-3”),25.9(c-4”),18.1(c-5”),17.4(c-1”'),31.9(c-2”'),74.2(c-3”'),27.4(c-4”'),25.9(c-5”')。
[0040]
实施例2
[0041]
抑制人结直肠癌ht-29和rko细胞活性评价:
[0042]
分别用含10%胎牛血清的rpmi-1640培养基和含13%胎牛血清的mem培养基,在37℃、5%co2条件下培养人结直肠癌细胞ht-29和rko细胞。取对数生长期的细胞,用胰酶消化后收集细胞,调整细胞密度为5
×
103ml-1
,取100μl于96孔板中,分别设置空白组,阴性对照组,5-fu组和实验组,每组设置3个复孔;待细胞贴壁后,弃去培养基,加入不同药物浓度(10μm、20μm、40μm)的培养基,培养24h后,加入mtt 20μl,培养4h后,吸去培养基,每孔加入dmso 150μl,置于恒温振荡器中使甲瓚结晶充分溶解,用酶标仪在570nm下测定各孔的吸光度,实验重复3次
[0043]
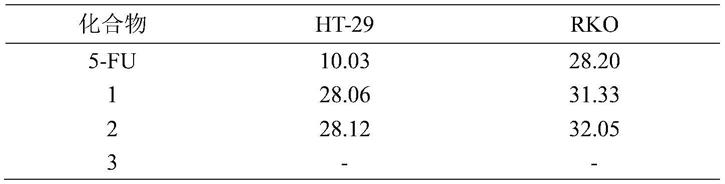
实验结果如表1显示,与阳性对照5-fu相比,式1和式2具有较好的抑制人结直肠癌ht-29和rko细胞的作用。
[0044]
表1:化合物在24h的半数有效浓度(μm)
[0045]
