一种dna纳米结构、构建方法及应用
技术领域
1.本发明属于纳米结构技术领域,尤其涉及一种dna纳米结构、构建方法及应用。
背景技术:
2.目前,rna自组装是广泛存在,如rna四边形、四面体、k-turn、prna-3wj,病毒ires模型,因为它们的高多样性,长rna链难于预测。相反,dna链是可编程的且可以人工折叠。基于watson-crick碱基配对,dna无疑是最具有前景的自组装能力的分子。dna可以自组装成2d和3d纳米结构(如dna三角形、dna四面体和其他合理设计下的重组dna几何形状),这让它们在多种应用中更有潜在使用价值。一个长dna支架可以被dna订书钉链折叠成不同的纳米结构,即dna折纸。在计算的帮助下,人们发现了dna折纸技术,dna 纳米结构发展成了一个自上而下的构建方法,如dna表情、dna盒子等。程序化的dna纳米体在纳米结构、分子器械应用和纳米医学的研究中具有重要意义,被dna或rna订书钉链折叠的rna脚手架链也用于开发这些应用。
3.由于dna脚手架链和dna订书钉链形成的dna纳米结构常常伴随着纳米结构构型错误(例如高浓度时聚合)、低产率和低效率。另外,rna的成本相对较高,而在制备较大的dna纳米结构时,需要引入一段dna来参入配对,相对应的大的dna纳米结构组装效率较低。这些挑战是dna纳米结构和纳米技术应用中主要的阻碍。因此,亟需一种新型的dna纳米结构的构建方法。
4.通过上述分析,现有技术存在的问题及缺陷为:由于rna的成本相对较高,且需要引入一段dna参入配对,故制备较大dna纳米结构的组装效率较低。
5.解决以上问题及缺陷的难度为:大的dna纳米结构需要较长的dna和rna链,制备较长的dna和rna单链的成本较高且纯度相对要低,也更容易被核酸酶降解,而且较长的核酸链会更容易产生碱基的错误配对,进一步制约了大的dna纳米结构的组装效率。
6.解决以上问题及缺陷的意义为:通过引入2
’‑
ome-rna能够帮助提高 dna-rna纳米结构的稳定性,获得高纯度的大dna纳米结构能够推动其在新型材料、药物递送系统、分子传感器、细胞成像等领域的广泛应用。
技术实现要素:
7.针对现有技术存在的问题,本发明提供了一种dna纳米结构、构建方法及应用,尤其涉及一种rna夹子引导dna纳米结构的形成方法。
8.本发明是这样实现的,一种dna纳米结构的构建方法,所述dna纳米结构的构建方法包括:
9.利用rna和修饰的rna通过折叠支架dna链来形成dna纳米结构。
10.进一步,所述修饰的rna为2
’‑
ome-rna。
11.进一步,所述dna纳米结构的构建方法,还包括:
12.将外链作为rna夹子,将含3~5个折叠单位的dna脚手架链分别折叠成三角形、四
边形和五边形;其中,一个rna夹子折叠形成的dna纳米结构包括两个高组装效率的寡核苷酸组分。
13.进一步,所述dna纳米结构的构建方法,还包括:
14.利用具有特殊结构的rna作为夹子来折叠dna支架链得dna纳米结构。
15.进一步,所述dna纳米结构的构建方法,还包括:
16.改变dna支架链的rna夹子结合位点数量,得到不同形状的dna纳米结构。
17.进一步,所述dna纳米结构的构建方法,还包括:
18.利用2
’‑
ome修饰的rna作为夹子折叠dna支架连得到dna纳米结构。
19.进一步,所述dna纳米结构的构建方法,还包括:
20.通过引入一段dna到rna折叠的dna纳米结构中,得到更大的dna纳米结构。
21.进一步,所述dna纳米结构的构建方法,还包括:
22.用部分dna取代rna得到的dna-rna杂合链作为夹子折叠dna,得到 dna纳米结构;和/或通过延长的dna夹子链稳定的折叠dna支架链得到dna 纳米结构。
23.本发明的另一目的在于提供一种应用所述的dna纳米结构的构建方法构建得到的新型dna纳米结构,所述新型dna纳米结构通式为:
[0024][0025]
本发明的另一目的在于提供一种所述的新型dna纳米结构在分子器械和纳米医学中的应用。
[0026]
结合上述的所有技术方案,本发明所具备的优点及积极效果为:本发明提供的dna纳米结构的构建方法,即用短的rna链作为夹子来引导dna纳米结构的形成,rna和修饰的rna(2
’‑
ome-rna)可以折叠支架dna链来形成dna纳米结构,丰富了dna纳米结构的构建方法,同时相比以往的dna 折纸术得到的dna纳米结构,rna折叠得到的dna纳米结构纯度更高,为 dna纳米结构的广泛应用提供了良好的基础。
[0027]
本发明用短rna夹子(包括修饰过的rna)可以高效地将dna脚手架链组装成设计好的形状和结构,因为短rna价格低廉且2-甲基修饰后化学稳定性较好,所以短rna是dna自组装纳米材料的理想支架夹子。本发明用rna夹子折叠dna的策略为折叠多种复杂的dna纳米材料提供了一个建筑学平台,一个rna夹子折叠形成的dna纳米结构包括两个高组装效率的寡核苷酸组分,这让构建dna纳米结构变得容易。
[0028]
本发明首次利用具有特殊结构的rna作为夹子来折叠dna支架链得dna 纳米结构;改变dna支架链的rna夹子结合位点数量,可以得到不同形状的 dna纳米结构;利用2
’‑
ome修饰的rna作为夹子可以折叠dna支架连得到效率更高,稳定性更好的dna纳米结构;通过引入一段dna到rna折叠的 dna纳米结构中,可以得到更大的dna纳米结构。
[0029]
在常规rna自组装情况下,当rna链较长时容易形成难以预测的复杂结构,不利于对其进行设计改造,本发明利用短的rna链来折叠长的dna链很好的避免了这个问题;在常规的dna折纸术或dna自组装的纳米结构,往往由于dna 结构多样性不足,容易导致组装效率较低,从而导致需要更多的dna链来完成组装,较多dna链又容易导致dna的错误组装,最终还是会引起组装效率较低。本发明巧妙地利用的rna的结构多样性和dna的易编程性的特点,利用两条核酸链就能形成纯度较高的dna纳米结构。
附图说明
[0030]
为了更清楚地说明本发明实施例的技术方案,下面将对本发明实施例中所需要使用的附图做简单的介绍,显而易见地,下面所描述的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下还可以根据这些附图获得其他的附图。
[0031]
图1是本发明实施例提供的新型dna纳米结构示意图。
[0032]
图2是本发明实施例提供的dna正方形可以通过rna夹子来折叠形成示意图。
[0033]
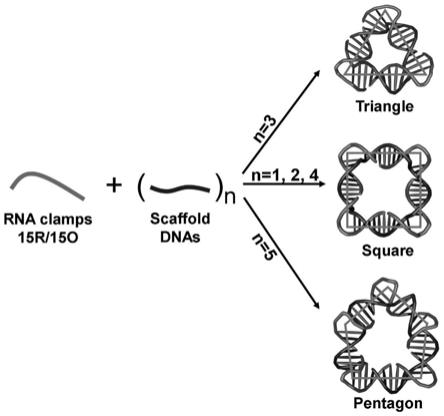
图3是本发明实施例提供的rna夹子折叠dna的三角形、方形和五边形纳米结构示意图。
[0034]
图4是本发明实施例提供的扩大的三角形、正方形和五边形dna纳米结构的设计和电镜成像示意图。
具体实施方式
[0035]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0036]
针对现有技术存在的问题,本发明提供了一种dna纳米结构、构建方法及应用,下面结合附图对本发明作详细的描述。
[0037]
本发明实施例提供的dna纳米结构的构建方法包括:利用rna和修饰的 rna通过折叠支架dna链来形成dna纳米结构。
[0038]
下面结合术语解释对本发明的技术方案作进一步描述。
[0039]
本发明中,dna纳米结构(dnananostructure):人为的基于核酸碱基互补配对来设计的核酸结构。rna夹子(rna clamp)具有特殊结构的一段短的rna 链,可以和dna支架链配对和组装形成特定的形状。
[0040]
下面结合具体实施例对本发明的技术方案作进一步描述。
[0041]
为了解决现有技术存在的问题,本发明用短rna夹子而非dna订书钉链,利用了rna的结构多样性和双链稳定性。实际上,有特殊结构的短rna链依然可以使rna-dna相互作用并有稳定性,不像双链dna订书钉链,短rna 夹子有更强的结合能力和更多样的构像,原则
上可以引导dna脚手架链形成多种形状。本发明用短rna夹子(包括修饰过的rna)可以高效地将dna脚手架链组装成设计好的形状和结构,因为短rna价格低廉且2-甲基修饰后化学稳定性较好,所以短rna是dna自组装纳米材料的理想支架夹子。
[0042]
本发明首先报道了rna夹子可高效地将dna脚手架链折叠成许多形状,如 dna三角形、四边形和五角形,而相应的dna无法有效完成。这种rna夹子是来自丙型肝炎病毒rna基因组的ires结构域2α,这个结构域被两个重叠序列剪切成一个角,在x-射线晶体确认下,四个角可以组装成的rna四边形。在实验设计中,本发明将外链作为rna夹子,将dna脚手架链(含3-5个折叠单位)分别折叠成三角形、四边形和五边形。这些dna纳米结构已经成功地组装成了更大的dna纳米结构,一些多边形纳米结构(dna三角形、四边形、五边形)设计成更加复杂的纳米结构的建筑基石。本发明用rna夹子折叠dna的策略为折叠多种复杂的dna纳米材料提供了一个建筑学平台,一个rna夹子折叠形成的 dna纳米结构包括两个高组装效率的寡核苷酸组分,这让构建dna纳米结构变得容易。
[0043]
本发明的结构示意图如图1所示,rna和修饰的rna(2
’‑
ome-rna)可以折叠支架dna链来形成dna纳米结构。
[0044]
本发明首次利用具有特殊结构的rna作为夹子来折叠dna支架链得dna 纳米结构;改变dna支架链的rna夹子结合位点数量,可以得到不同形状的 dna纳米结构;利用2
’‑
ome修饰的rna作为夹子可以折叠dna得到效率更高,稳定性更好的dna纳米结构;通过引入一段dna到rna折叠的dna纳米结构中,可以得到更大的dna纳米结构。
[0045]
在常规rna自组装情况下,当rna链较长时容易形成难以预测的复杂结构,不利于对其进行设计改造,本发明利用短的rna链来折叠长的dna链很好的避免了这个问题;
[0046]
在常规的dna折纸术或dna自组装的纳米结构,往往由于dna结构多样性不足,容易导致组装效率较低,从而导致需要更多的dna链来完成组装,较多 dna链又容易导致dna的错误组装,最终还是会引起组装效率较低。本发明巧妙地利用的rna的结构多样性和dna的易编程性的特点,利用两条核酸链就能的纯度较高的dna纳米结构。
[0047]
本发明的替代方案为:(1)由于rna和2
’‑
ome-rna具有较好的结构多样性,用部分dna来取代rna得到的dna-rna杂合链作为夹子同样可以折叠dna来得到dna纳米结构;(2)同样由于短的dna作为夹子时,多样性不足,无法稳定的折叠dna支架链,通过延长的dna夹子链可以稳定折叠dna的支架链得到 dna纳米结构。
[0048]
rna外链(15r)在rna四边形稳定组装中起关键性作用,本发明探索相应的dna链是否也能形成dna四边形。本发明用相应的dna(10d和15d)分别替换了rna四边形的内链(10r)和外链(15r),让内链(10r和10d)与外链(15r 和15d)组装。正如非变形聚丙烯酰胺凝胶电泳(page;图2a)所示,rna四边形(10r+15r)成功组装,但dna四边形(10d+15d)组装情况不佳,dna四边形(10r+15d)也没有形成。但是在有15r的情况下,dna-rna四边形(10d+15r) 组装成功了。这些结果表明,相较于对应的dna,15r在纳米组装中有更好的多样性和结合亲和力。因此,本发明发现具有更好多样性的rna外链,可以做 rna夹子,能够把dna链折叠成各种纳米结构。
[0049]
图2dna正方形可以通过rna夹子来折叠形成。15r:rna正方形的外链rna(15nt);10r:rna正方形的内链rna(10nt);15d:15r对应的dna; 10d:10r对应的dna;20d:10d两次重复的dna;40d:10d四次重复的 dna。这些纳米结构的组装通过非变性胶进行分析。(a)内链
(10r和10d) 和外链(15r和15d)的组装;(b)用rna夹子(15r)折叠dna支架(10d、 20d和40d)。
[0050]
为了探究rna夹子是否能将dna折叠成纳米结构,本发明设计了一些 dna链,包括相应的dna内链(10d,一个折叠单元)和它有2-、4-折叠单位的重复dna链,分别是20d和40d。有意思的是,本发明发现这种rna夹子可以将10d、20d和40d折叠成dna四边形,这也提高了dna四边形组装效率(图2b)。
[0051]
为了进一步研究rna夹子是否能将dna链折叠成纳米结构,本发明设计了带3-和5-折叠单位的dna链,分别为30d和50d。本发明发现rna夹子分别用30d、40d和50d组装形成了三角形、四边形、五边形的dna纳米结构(图3a)。特别是在有2-甲基化对应rna夹子存在时,所有的纳米结构都可以高效折叠,在三角形(98.5%vs 95.1%)四边形(96.0%vs 91.2%)和五边形(84.3%vs62.1%)中,折叠dna链比15r效率更高。结果表明组装效率按照dna五边形 (理论角度:108
°
)、四边形(90
°
)、三角形(60
°
)依次增加,这证明rna夹子(15r) 更倾向于形成小角度(60
°
)的紧密结构,但对应的dna(15d)不能折叠成任何纳米结构(图3c)。和大多数带有4个寡核苷酸的rna-dna杂交纳米结构不同的是,每个rna夹子折叠形成的dna纳米结构都只包括两个寡核苷酸,这平衡了 rna夹子的多样性和双重稳定性,但是dna订书钉链不能兼顾这两者。
[0052]
图3 rna夹子折叠dna的三角形、方形和五边形纳米结构,通过变性page 和ms研究证实。15o:15r对应的的2'-甲基化rna;在三角形(98.5%vs95.1%)、正方形(96.0%vs91.2%)和五边形(84.3%vs62.1%)的纳米形状中,15o折叠 dna支架链效果优于15r;30d:具有10d三次重复的dna;50d:具有10d 五次重复的dna;p10d:5'端磷酸化的10d;p30d:5'端磷酸化的30d;p40d: 5'端磷酸化40d;p50d:5'端磷酸化50d;c30d:环化的30d;c40d:环化的 40d;c50d:环化的50d。(a),(b)和(c)dna三角形、正方形和五边形经 15r、15o和15d折叠后的组装的非变性page分析。(d)变性page分析有无 t4 dna连接酶连接的三角形(30d+15r)、正方形(10d+15r、40d+15r)和五边形(50d+15r),(e)三角形、正方形和五边形组装的esi-ms分析。用t4 dna连接酶将折叠的dna三角形、正方形和五边形连接起来,然后用esi-ms 检测连接的三角形、正方形和五边形。
[0053]
表1 环状dna支架链的 esi-ms数据
[0054]
因为15r可以折叠纳米材料,并形成缺口,在5-磷酸化的dna脚手架链存在时,用t4 dna连接酶将c30d、c40d和c50d连接起来,形成环化单链dna 链。可以基于这些环化的dna链的迁移率在变性page下检测出来(图3d)。对于page分析,可用ssdna环化连接酶合成环化的p30d、p40d和p50d,作为阳性marker(c30d、c40d、c50d),这些纳米结构可以在电喷雾质谱 (esi-ms,图3e)下得到进一步证实。通过变性page分析,不管是连接还是没有连接的折叠纳米结构,结果都与esi-ms数据一致(图3d和图3e)。
[0055]
详细来说,10d、30d、40d和50d的5端磷酸化,依次得到p10d、p30d、 p40d和p50d。在
用tadna连接酶组装连接后,p10d+15r形成c30d和c40d,并同时用ms检测(图3d和3e)。因为有p10d+15r的存在,没有观察到p20d 和p30d的组装和连接现象,本发明怀疑三角形和四边形是先形成再连接形成 c30d和c40d。如图所示(图3e,表1),3-unitdna(p30d+15r)的组装反应形成了折叠的p30d,之后t4 dna连接酶连接产生环化的30d(c30d); 4-unitdna(p40d+15r)的组装反应形成了折叠的p40d,随之连接形成环化的 40d(c40d)(图3e,表1));5-unitdna(p50d+15r)的组装反应得到折叠的p50d,然后连接生成环化的50d(c50d)(图3e,表1)。为了研究在没有15r夹子的情况下,环形纳米dna是否可以形成,本发明将这些磷酸化支架(p10d、p30d、 p40、p50d)进行无15r的连接,作为阴性对照。就如本发明预期的那样,没有观察到有环状dna的存在,这表示它们的形成需要rna夹子的引导。
[0056]
此外,为了证实并观察到15r夹子折叠的环状dna纳米结构,本发明采用了原子力显微镜(afm),但因为它们尺寸太小(约4nm),所以它们的形状难以确认。另外本发明增加了纳米结构的大小,以观察到它们并验证本发明rna夹子引导下的dna纳米结构的构建策略。因此,本发明用21-bp的双链dna(21d;图4a)插入了三角形、四边形和五边形的每一条边,组装了更大尺寸的多边形。扩展的dna三角形包括93-nt的dna(93d),并有三个相同结合单元21d和15r。扩大的dna四边形包含124-nt的dna(124d),并带有四个相同的21d和15r 结合单元,扩大的dna五边形包含155-nt的dna(155d),带五个相同的21d 和15r结合单元(图4a)。正如在非变性page上所示(图4b),15r夹子成功地引导形成了纳米结构(扩大的dna三角形、四边形和五边形),而在非变性page 显示,扩大的四边形有更详细的组装过程,最后,通过负染色em成像并确认了扩大的三角形、四边形和五边形(图4c)。本发明的方法为利用特异性和多样性的rna单元和rna夹子构建dna纳米结构提供了一种可行的策略。
[0057]
图4扩大的三角形、正方形和五边形dna纳米结构的设计和电镜成像。21d:插入纳米结构两侧的dna(21nt);93d、124d和155d是dna(分别含有93、 124和155个nt),分别具有21d的三、四和五个配对序列。(a)通过环扩张设计新的三角形、正方形和五边形纳米结构。三角形、正方形和五边形的每边为 31bp。(b)和(c)dna纳米结构的非变性page分析和电镜图像。
[0058]
总而言之,rna夹子可以成功折叠形成dna三角形、四边形和五边形,rna 夹子也可以用一个、两个或者四个折叠单元将dna脚手架链折叠成相同的四边形形状。相反,对应的dna无法做到,这说明结构单链rna可以提供充足的结构多样性、稳定性和高组装效率,以形成稳定的dna纳米结构。在本发明的这种策略下,rna夹子可以折叠形成扩大的dna纳米形状并在em成像在得到确认,这为使用简单的dna纳米结构作为构建单元,组装成复杂的dna纳米结构提供了一个平台。为了稳定rna引导的dna纳米结构,2-甲基化的rna链可以提高折叠效率和化学稳定性,是理想的替代品。本发明的实验结果证明了一个新的策略:有结构多样性的短rna夹子可以通过稳定的双链和rna夹子的二级结构,引导dna脚手架链形成多种形状。
[0059]
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,都应涵盖在本发明的保护范围之内。
