1.本发明涉及含有机有效成分的医药制品,具体涉及异黄酮类中药单体刺芒柄花素在制备防治脓毒症损伤的药物中的应用。
背景技术:
2.脓毒症(sepsis)被定义为由于宿主在机体感染后做出一系列应答,导致致命的器官功能障碍。脓毒症最主要的表现是全身的过度炎症、免疫平衡的紊乱。脓毒症的发病率和死亡率随着医学的发展和人民生活水平的提高有所下降,但因为其病情发展迅速,发病机制复杂,具有高度异质性,在重症病房(icu)仍是患者死亡的重要原因,数据显示病死率高至30%~50%。临床上,主要依靠抗感染和临床重症监护治疗脓毒症,辅以液体复苏、营养支持、抗凝治疗、糖皮质激素等手段,但是这些西医上的对症治疗手段的疗效并不乐观,如应用抗生素导致细菌耐药等,给治疗增加了很大难度。中医注重整体观,强调辩证论治,近年来,在研发脓毒症治疗药物方面,研究者开始将目光看向中药有效成分,并在脓毒症的治疗中取得了一定进展。在此专利中,我们要说明的是一种异黄酮中药单体刺芒柄花素在防治脓毒症损伤中的作用。
3.刺芒柄花素(formononetin,fmn)为灰白色结晶粉末,易溶于甲醇、乙酸乙酯、乙醚等有机溶剂以及稀碱溶液,难溶于水,不易发生分解,但易被氧化,其分子式为c
16h12
o4,化学结构式如下图所示。刺芒柄花素是一种异黄酮类植物雌激素,也被称为7-羟基-4
’‑
甲氧基异黄酮、芒柄花黄素、芒柄花素,是豆科植物红车轴草的主要活性成分,也是一些常用中草药(如当归、黄芪、葛根、鸡血藤等)的活性成分之一。刺芒柄花素可通过浸提、超声波、微波等方法从天然植物中提取,也可人工合成和改构。
[0004][0005]
有许多研究证明刺芒柄花素及其衍生物具有多种生物学功能,如抗癌、抗炎、抗氧化、抗病毒、调节血脂、促进创伤修复等等。有大量的研究关注刺芒柄花素的抗癌作用,其能促进细胞凋亡和防止细胞增殖,抑制肿瘤的转移和生长,可对抗多种癌症,包括乳腺癌、结肠直肠癌和前列腺癌等。有研究表明刺芒柄花素的抗氧化和神经保护功能对治疗阿尔茨海默病有一定作用。还有研究表明刺芒柄花素对过敏性哮喘的气道炎症和氧化应激方面具有治疗作用。考虑到刺芒柄花素的抗炎、抗氧化、促进创伤修复等功能,而且目前关于刺芒柄花素在防治因机体感染导致的脓毒症损伤中的作用尚无明确报道,我们探索了刺芒柄花素在脓毒症治疗中的作用。
技术实现要素:
[0006]
本发明所要解决的技术问题是中药单体刺芒柄花素在医学上的新用途。
[0007]
本发明第一方面提供刺芒柄花素在制备防治脓毒症损伤的药物中的应用。
[0008]
本发明第二方面提供防治脓毒症损伤的药物,所述防治脓毒症损伤的药物中含有刺芒柄花素。
[0009]
本发明第三方面提供刺芒柄花素在制备含有以下任一项或多项作用的产品中的用途:(1)减缓作用对象器官损伤;(2)减缓作用对象全身炎症作用;(3)提高作用对象生存率。
[0010]
本发明的有益效果为:
[0011]
本发明发现了刺芒柄花素的新用途,扩展了刺芒柄花素的应用范围。本发明发现刺芒柄花素可提高脓毒症模型小鼠生存率,改善脓毒症模型小鼠器官损伤和减轻全身炎症反应。目前脓毒症缺乏针对病因的治疗药物,而刺芒柄花素对脓毒症模型小鼠的组织损伤具有缓解作用,可用于制备防治脓毒症损伤的药物。
附图说明
[0012]
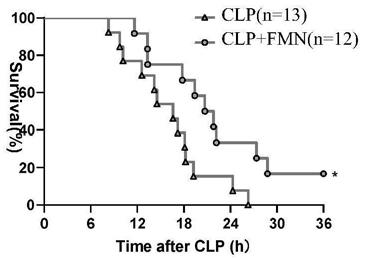
图1是刺芒柄花素对clp脓毒症模型小鼠生存率的影响的统计图,数据采用t检验分析,*p《0.05。
[0013]
图2是刺芒柄花素改善脓毒症模型小鼠肝脏组织损伤病理结果图。其中a图为clp组肝脏组织形态学变化he染色图,b图为clp+fmn组肝脏组织形态学变化he染色图,标尺为100μm,c图为肝脏病理损伤统计图,数据采用t检验分析,*p《0.05。
[0014]
图3是刺芒柄花素改善脓毒症模型小鼠肾脏组织损伤病理结果图。其中a图为clp组肾脏组织形态学变化he染色图,b图为clp+fmn组肾脏组织形态学变化he染色图,标尺为100μm,c图为肾脏病理损伤统计图,数据采用t检验分析,*p《0.05。
[0015]
图4是刺芒柄花素改善脓毒症模型小鼠肺脏组织损伤病理结果图。其中a图为clp组肺脏组织形态学变化he染色图,b图为clp+fmn组肺脏组织形态学变化he染色图,标尺为100μm,c图为肺脏病理损伤统计图,数据采用t检验分析,*p《0.05。
[0016]
图5是刺芒柄花素对脓毒症模型小鼠脏器损伤的影响的结果统计图。其中a图为血浆中alt的含量统计图,b图为血浆中ast的含量统计图,c图为血浆中cr的含量统计图,数据采用t检验分析,*p《0.05。
[0017]
图6是刺芒柄花素对脓毒症模型小鼠全身性炎症的影响的结果统计图。a图为血浆中il-6的含量统计图,b图为血浆中il-1β的含量统计图,c图为血浆中tnf-α的含量统计图,数据采用t检验分析,*p《0.05。
具体实施方式
[0018]
在进一步描述本发明具体实施方式之前,应理解,本发明的保护范围不局限于下述特定的具体实施方案;还应当理解,本发明实施例中使用的术语是为了描述特定的具体实施方案,而不是为了限制本发明的保护范围。下列实施例中未注明具体条件的试验方法,通常按照常规条件,或者按照各制造商所建议的条件。当实施例给出数值范围时,应理解,除非本发明另有说明,每个数值范围的两个端点以及两个端点之间任何一个数值均可选用。除非另外定义,本发明中使用的所有技术和科学术语与本技术领域技术人员通常理解的意义相同。除实施例中使用的具体方法、设备、材料外,根据本技术领域的技术人员对现有技术的掌握及本发明的记载,还可以使用与本发明实施例中所述的方法、设备、材料相似
或等同的现有技术的任何方法、设备和材料来实现本发明。
[0019]
除非另外说明,本发明中所公开的实验方法、检测方法、制备方法均采用本技术领域常规的分子生物学、生物化学、染色质结构和分析、分析化学、细胞培养、重组dna技术及相关领域的常规技术。
[0020]
本发明一实施例为刺芒柄花素在制备防治脓毒症损伤的药物中的应用。
[0021]
可选的,刺芒柄花素作为防治脓毒症损伤的药物的唯一有效成分或有效成分之一。
[0022]
上述刺芒柄花素在制药中的新应用具体为,刺芒柄花素在制备提高脓毒症生存率、治疗脓毒症器官损伤和减轻全身炎症的药物中的应用。
[0023]
所述的防治脓毒症损伤的药物中,刺芒柄花素为异黄酮类中药单体,刺芒柄花素的药物剂量为15mg/kg。
[0024]
可选的,所述的防治脓毒症损伤的药物还包含药学上可接受的载体或辅料。
[0025]“药学上可接受的”是指当分子本体和组合物适当地给予动物或人时,它们不会产生不利的、过敏的或其它不良反应。
[0026]“药学上可接受的载体或辅料”应当与所述有效成分相容,即能与其共混而不会在通常情况下大幅度降低药物的效果。可作为药学上可接受的载体或辅料的一些物质的具体例子是糖类,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和土豆淀粉;纤维素及其衍生物,如甲基纤维素钠、乙基纤维素和甲基纤维素;西黄蓍胶粉末;麦芽;明胶;滑石;固体润滑剂,如硬脂酸和硬脂酸镁;硫酸钙;植物油,如花生油、棉籽油、芝麻油、橄榄油、玉米油和可可油;多元醇,如丙二醇、甘油、山梨糖醇、甘露糖醇和聚乙二醇;海藻酸;乳化剂,如tween;润湿剂,如月桂基硫酸钠;着色剂;调味剂;压片剂、稳定剂;抗氧化剂;防腐剂;无热原水;等渗盐溶液;和磷酸盐缓冲液等。这些物质根据需要用于帮助配方的稳定性或有助于提高活性或它的生物有效性或在口服的情况下产生可接受的口感或气味。
[0027]
本发明中,除非特别说明,药物剂型并无特别限定,例如,所述的防治脓毒症损伤的药物形式选自片剂、胶囊剂、颗粒剂、混悬剂、乳剂、溶液剂、糖浆剂、喷剂或注射剂。
[0028]
本发明一实施例提供防治脓毒症损伤的药物,所述防治脓毒症损伤的药物中含有刺芒柄花素。
[0029]
刺芒柄花素作为防治脓毒症损伤的药物的唯一有效成分或有效成分之一。
[0030]
所述的防治脓毒症损伤的药物中,刺芒柄花素为异黄酮类中药单体,刺芒柄花素的药物剂量为15mg/kg。
[0031]
可选的,所述的防治脓毒症损伤的药物还包含药学上可接受的载体或辅料。本发明一实施例提供刺芒柄花素在制备含有以下任一项或多项作用的产品中的用途:(1)减缓作用对象器官损伤;(2)减缓作用对象全身炎症作用;(3)提高作用对象生存率。
[0032]
实施例1:刺芒柄花素能够提高脓毒症模型小鼠的生存率
[0033]
1实验材料
[0034]
1.1实验动物:8~10周雌性c57bl/6j小鼠,体重20~22g,购买于广州市言诚生物科技有限公司。
[0035]
1.2试剂和仪器:刺芒柄花素(aladdin,f111388);芝麻油(源叶生物)。
[0036]
2实验方法和结果
[0037]
2.1动物实验
[0038]
刺芒柄花素称取15mg,加入芝麻油10ml,37℃水浴超声30min,现配现用。将25只c57bl/6j小鼠随机均分为2组,分别为盲肠结扎穿孔组(clp组)、盲肠结扎穿孔+刺芒柄花素组(clp+fmn组)。进行盲肠结扎中度实验,缝合之后,clp组腹腔注射芝麻油200μl,clp+fmn组腹腔注射刺芒柄花素,剂量15mg/kg,注射体积200μl。在补液后记录clp完成的时间,观察和记录小鼠死亡时间。
[0039]
2.2实验结果
[0040]
结果如图1所示,clp+fmn组小鼠的生存时间与clp组相比延长(p《0.05),说明刺芒柄花素能够提高脓毒症模型小鼠的生存率。
[0041]
实施例2:刺芒柄花素减缓脓毒症模型小鼠肝脏、肾脏、肺脏组织的损伤
[0042]
1实验材料
[0043]
1.1实验动物:8~10周雌性c57bl/6j小鼠,体重20~22g,购买于广州市言诚生物科技有限公司。
[0044]
1.2试剂和仪器刺芒柄花素(aladdin,f111388);芝麻油(源叶生物);磷酸盐缓冲液(pbs);he染液(北京雷根生物公司);4%多聚甲醛(北京雷根生物公司);肌酐(cr)检测试剂盒(南京建成生物工程研究所);丙氨酸氨基转移酶(alt)检测试剂盒(南京建成生物工程研究所);天冬氨酸氨基转移酶(ast)检测试剂盒(南京建成生物工程研究所);多功能酶标仪(美国moleculardevices);mouse il-1βelisa检测试剂盒(深圳欣博盛生物科技有限公司);mouse il-6elisa检测试剂盒(深圳欣博盛生物科技有限公司);mouse tnf-αelisa检测试剂盒(深圳欣博盛生物科技有限公司)。
[0045]
2实验方法和结果
[0046]
2.1动物实验
[0047]
刺芒柄花素称取15mg,加入芝麻油10ml,37℃水浴超声30min,现配现用。将16只c57bl/6j小鼠随机均分为2组,分别为盲肠结扎穿孔组(clp组)、盲肠结扎穿孔+刺芒柄花素组(clp+fmn组)。进行盲肠结扎中度实验,缝合之后,clp组腹腔注射芝麻油200μl,clp+fmn组腹腔注射刺芒柄花素,剂量15mg/kg,注射体积200μl。于术后12h,分离小鼠肝脏、肾脏、肺脏组织,进行病理形态学变化检测;下腔静脉采血,edta抗凝,13,000g于4℃离心10min,收集血浆待检测。根据试剂说明书检测alt、ast、cr,以及tnf-α、il-1β、il-6。
[0048]
2.2肝脏、肾脏、肺脏组织形态学变化检测
[0049]
2.2.1石蜡切片和he染色
[0050]
切取相同部位合适大小的组织块,置于4%多聚甲醛固定24h后,在自动脱水仪器仪器上设置好程序进行脱水;包埋;石蜡切片厚度为3μm。然后he染色:切片放置60℃烤箱1h;置于二甲苯10min两次进行脱腊;置于梯度乙醇溶液脱二甲苯,无水乙醇i5 min,无水乙醇ii5 min,95%乙醇3min,70%乙醇3min;苏木精染液染5min,水洗1min;1%盐酸乙醇溶液分化,水洗1min;0.2%氨水的反蓝1min;1%伊红染液染30s;乙醇脱水,95%乙醇30s,无水乙醇1min,无水乙醇1min;二甲苯透明两次,每次1min。中性树胶封片,光学显微镜观察拍照,每张片随机选取至少6个视野。
[0051]
2.2.2实验结果
[0052]
he染色及评分结果如图2-图4所示,clp模型组可见肝脏中央静脉周围炎症细胞浸
润,肝实质细胞空泡化严重,clp+fmn组炎症浸润减轻(图2)。clp模型组肾小管扩张,clp+fmn组小鼠肾损伤有所改善(图3)。clp模型组中可见肺间隔增厚,毛细血管充血,clp+fmn组肺损伤有所改善(图4)。上述数据说明刺芒柄花素能够减缓脓毒症模型小鼠肝脏、肾脏、肺脏组织的病理形态学变化。
[0053]
2.3生化指标检测
[0054]
2.3.1检测血浆中的alt、ast、cr的变化
[0055]
根据试剂说明书检测血浆中alt、ast、cr的含量。
[0056]
2.3.2实验结果
[0057]
结果如图5所示,clp+fmn组血浆中alt、ast、cr的含量与clp组相比明显减少(p《0.05)。说明刺芒柄花素能够减轻脓毒症模型小鼠肝脏、肺脏和肾脏的损伤。
[0058]
2.4炎症因子指标检测
[0059]
2.4.1检测血浆中的il-6、il-1β、tnf-α的变化
[0060]
检测il-6时血浆稀释500倍,检测il-1β、tnf-α时血浆稀释20倍。根据试剂说明书通过elisa检测血浆中il-6、il-1β、tnf-α的含量。
[0061]
2.4.2实验结果
[0062]
结果如图6所示,其中,图6a表明,clp+fmn组血浆中il-6的含量与clp组相比明显减少(p《0.05);图6b表明,中、clp+fmn组血浆中il-1β的含量与clp组相比减少(p《0.05);图6c表明,clp+fmn组血浆中tnf-α含量与clp组相比减少(p=0.06)。说明刺芒柄花素能够减轻脓毒症模型小鼠的全身炎症反应,具有抗炎作用。
