一种唾液乳杆菌jyls-372在制备解酒护肝产品中的应用
技术领域
1.本发明涉及益生菌技术领域,具体涉及一种唾液乳杆菌jyls-372在制备解酒护肝产品中的应用。
背景技术:
2.肝脏,人体的五脏之一,主要负责机体的代谢功能。肝脏一旦受到损伤,便会对人的身体健康造成极大威胁。长期饮酒是可能导致肝损伤的诱因之一,有研究显示,每天摄入超过20g酒精就会对肝脏造成损害。
3.为降低因喝酒所造成的肝脏损伤,部分人群选择服用保健品、酵素饮料或中药饮液。玉米低聚肽是目前市面上宣传较广的解酒护肝保健品之一,属于小分子肽,但其解酒护肝的分子作用机理并不明确,而且玉米低聚肽并不能完全对任何醉酒患者产生效果,实际应用过程中,大量人群并没有表现出快速解酒效果。酵素饮料是根据中医传统理论,挑选具有解酒作用的药食同源食品进行微生物发酵后获得的产品,其具有一定的解酒护肝效果,但该方式具有很大的局限性,不能满足当下人群的需求。根据中药解酒配方选取药材熬制的中药饮液也具有一定的解酒醒酒、保护肝脏的效果,但中医方法通常比较繁琐,需要耗费较大的人力和物力。
4.基于此,有必要提供一种作用机理更明确、服用更加方便的解酒护肝产品。
技术实现要素:
5.针对现有解酒护肝产品作用机理不明确或使用繁琐、具有局限性的技术问题,本发明提供一种唾液乳杆菌jyls-372的应用,该唾液乳杆菌jyls-372有较强的过胃肠存活率及肠道定植能力,能够将乙醇转化为乳酸乙酯,以其制备的产品服用方法,解酒护肝效果明显。
6.本发明技术方案如下:一种唾液乳杆菌jyls-372在制备解酒护肝产品中的应用,所述唾液乳杆菌(lactobacillus salivarius)jyls-372已于2019年6月27日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc no.18044,并公开于中国专利申请cn110791452a中。
7.进一步的,所述解酒护肝产品为将乙醇转化为乳酸乙酯的产品。
8.进一步的,所述唾液乳杆菌jyls-372以菌粉剂型存在于解酒护肝产品中。
9.进一步的,菌粉的制备方法包括如下步骤:(1)唾液乳杆菌jyls-372首先在mrs平板培养基上活化;(2)将活化后的唾液乳杆菌jyls-372接种到mrs液体培养基上培养,获得菌液;(3)菌液离心收集菌体,用无菌生理盐水洗涤后重悬于15wt%的复原脱脂乳中,获得悬浊液;(4)调整悬浊液的浓度为1.0-2.0
×
10
10
cfu/ml,获得菌悬液,将菌悬液冷冻干燥
后,获得菌粉。
10.进一步的,步骤(1)mrs平板培养基的原料包括:蛋白胨10g、牛肉粉5g、三水醋酸钠5g、七水磷酸氢二钾2g、吐温80 1ml、四水硫酸锰0.05g、柠檬酸三铵2g、葡萄糖20g、七水硫酸镁0.2g、琼脂15g、蒸馏水1000ml;制备方法为将上述原料混合,自然ph下搅拌,然后在121℃、0.1mpa下灭菌20min,将灭菌的培养基倒入平皿中,放凉后待用。
11.进一步的,步骤(2)mrs液体培养基的原料包括:蛋白胨10g、牛肉粉5g、三水醋酸钠5g、七水磷酸氢二钾2g、吐温80 1ml、四水硫酸锰0.05g、柠檬酸三铵2g、葡萄糖20g、七水硫酸镁0.2g、蒸馏水1000ml;制备方法为将上述原料混合,调ph值为6.8,搅拌,然后在121℃、0.1mpa下灭菌20min,即得。
12.进一步的,步骤(2)培养条件为37℃、24h。
13.进一步的,所述解酒护肝产品中还包括低聚异麦芽糖。
14.本发明的有益效果在于:本发明利用唾液乳杆菌jyls-372较强的胃肠道存活率和肠道定植能力和可直接将乙醇反应为乳酸乙酯,从而消耗人体中摄入的乙醇含量的特性,制备解酒护肝产品,并经过实验数据和小鼠实验,验证了产品的有效性。
15.同时,以唾液乳杆菌jyls-372制备解酒护肝产品节约成本,简单直接,且没有任何副作用。
附图说明
16.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,对于本领域普通技术人员而言,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
17.图1是实施例4中培养时间为10h的培养基上清液的气相色谱图。
18.图2是乳酸纯品用乙醇+叔丁醇作溶剂的气相色谱图。
19.图3是乳酸乙酯纯品用乙醇+叔丁醇作溶剂的气相色谱图。
具体实施方式
20.为了使本技术领域的人员更好地理解本发明中的技术方案,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
21.本发明具体实施方式中使用的低聚异麦芽糖购自保龄宝生物股份有限公司。
22.本发明具体实施方式中使用的mrs平板培养基的原料包括:蛋白胨10g、牛肉粉5g、三水醋酸钠5g、七水磷酸氢二钾2g、吐温80 1ml、四水硫酸锰0.05g、柠檬酸三铵2g、葡萄糖20g、七水硫酸镁0.2g、琼脂15g、蒸馏水1000ml;制备方法为将上述原料混合,自然ph下搅拌,然后在121℃、0.1mpa下灭菌20min,
将灭菌的培养基倒入平皿中,放凉后待用。
23.本发明具体实施方式中使用的mrs液体培养基的原料包括:蛋白胨10g、牛肉粉5g、三水醋酸钠5g、七水磷酸氢二钾2g、吐温80 1ml、四水硫酸锰0.05g、柠檬酸三铵2g、葡萄糖20g、七水硫酸镁0.2g、蒸馏水1000ml;制备方法为将上述原料混合,调ph值为6.8,搅拌,然后在121℃、0.1mpa下灭菌20min,即得。
24.本发明具体实施方式中使用的模拟胃液按照如下方法配制:用9.5%盐酸加蒸馏水稀释至ph值为1.5,每100ml加入1.0g胃蛋白酶,混匀后用0.22μm无菌滤膜过滤,现配现用。
25.本发明具体实施方式中使用的模拟肠液按照如下方法配制:将6.8g的磷酸二氢钾溶于500ml蒸馏水中,加入3g胆盐和10g胰蛋白酶,用浓度为4g/l的氢氧化钠溶液调节溶液ph值至6.8,用蒸馏水定容至1l后,混匀后用0.22μm无菌滤膜过滤,现配现用。
26.本发明具体实施方式中使用的pbs缓冲液按照如下方法配制:磷酸二氢钾0.27g、磷酸氢二钠1.42g、氯化钠8g、氯化钾0.2g,加去离子水约800ml充分搅拌溶解,加浓盐酸调ph值至7.4,加去离子水定容至1l,于121℃灭菌20min,即得。
27.本发明具体实施方式中使用的ph8.0的磷酸氢二钾缓冲液按照如下方法配制:取磷酸氢二钾5.59g与磷酸二氢钾0.41g,加水使溶解成1000ml,即得。
28.实施例1按照产品中唾液乳杆菌jyls-372的菌数为100亿、150亿、200亿cfu/g,对唾液乳杆菌jyls-372菌粉和低聚异麦芽糖进行复配,得到三种不同菌数规格的解酒护肝产品。
29.其中,唾液乳杆菌jyls-372菌粉由如下制备方法制得:(1)唾液乳杆菌jyls-372首先在mrs平板培养基上活化;(2)将活化后的唾液乳杆菌jyls-372按1%(v/v)的接种量接种到mrs液体培养基上37℃培养24h,获得菌液;(3)菌液离心收集菌体,用无菌生理盐水洗涤后重悬于15wt%的复原脱脂乳中,获得悬浊液;(4)调整悬浊液的浓度为1.0-2.0
×
10
10
cfu/ml,获得菌悬液,将菌悬液冷冻干燥后,获得菌粉。
30.实施例2称取若干份实施例1解酒护肝产品作为样品,每份样品重量为1g,转移至预热的装有9ml模拟胃液试管中,分别于37℃、80r/min下处理1h、2h、3h、4h,每个处理3个重复。
31.称取若干份实施例1解酒护肝产品作为样品,每份样品重量为1g,转移至装有9ml模拟肠液试管中,分别于37℃、80r/min下处理1h、2h、3h、4h,每个处理3个重复。
32.对处理后的样品溶液进行梯度稀释,使用倾注法做活菌计数,计算存活率:存活率=(处理后菌数/原始菌数)
×
100%。
33.计算结果如表1所示,可以看出唾液乳杆菌jyls-372在体外模拟胃肠环境下的存活率非常高,在胃液和肠液中4h,存活率依然在90%以上。可以为后续菌种定植肠道,发挥功能作用垫定基础。
34.表1 唾液乳杆菌jyls-372在体外模拟胃肠环境下的存活率
实施例3将caco-2细胞置于含10%热灭活新生牛血清和双抗(青霉素浓度100u/ml、链霉素1.0μg/ml)的dmem培养液(购自gibco公司)中,于37℃、5%co2、相对湿度95%的二氧化碳培养箱中孵育,每天换1次培养液,3~4天传代1次,18天后将细胞接种于24孔培养板中,接种密度约为5
×
105cfu/ml,待细胞长至单层后进行黏附试验。
35.将活化好的唾液乳杆菌jyls-372按1%(v/v)的接种量接种于mrs液体培养基中,37℃培养12h,然后在4000g、4℃条件下对发酵液离心10min,收集菌体并用无菌pbs缓冲液洗涤3次,将菌体重悬于无菌pbs缓冲液中,得到浓度为2
×
108cfu/ml的jyls-372菌悬液。
36.将已长成单层的caco-2细胞用无菌pbs缓冲液漂洗2次,每孔加入0.5ml的jyls-372菌悬液和0.5ml新鲜的dmem培养液,于37℃、5%co2、相对湿度95%的二氧化碳培养箱中孵育1h,然后用无菌pbs缓冲液漂洗细胞5次,以除去未黏附的细菌。漂洗完后,用甲醛固定,革兰染色,镜检,倒置显微镜下计算20个随机视野下100个细胞上黏附的细菌数,根据公式:粘附率=(初始菌数-漂洗下的菌数)/初始菌数
×
100%计算粘附率。每个处理做3个平行。
37.经计算,唾液乳杆菌jyls-372在caco-2细胞上的粘附个数为680个,粘附率为84%,表明唾液乳杆菌jyls-372在细胞定植方面有较强的能力。
38.实施例4将活化好的唾液乳杆菌jyls-372按5%(v/v)的接种量分别接种至五个mrs液体培养基中,并向各mrs液体培养基中加入5%的乙醇(v/v),37℃下培养,五个培养基的培养时间分别为8h、9h、10h、11h、12h。培养结束后,在4000g、4℃条件下对发酵液离心20min,收集离心液待用,将收集的菌体用灭活生理盐水冲洗3次,将菌泥和ph8.0的磷酸氢二钾缓冲液以1:5的质量比制成悬浊液。悬浊液首先于0℃条件下超声破碎20min,再于4000rpm、4℃条件下离心20min,再次收集上清液,合并两次离心得到的上清液,备用。
39.取合并后上清液1μl用乙醇+叔丁醇作溶剂混合后,进行高效气相色谱检测,其中气相检测采用内标检测方式。以5%二苯基1%乙烯基94%二甲基聚硅氧烷为填料的弱极性毛细管柱,载气为氦气,分流比为3.5~4.0,升温程序为70℃保持10min,10~30min内以2.5~3.0℃/min的速度升温至180℃,30~60min内以5.5~6.5℃/min的速度升温至250℃,然后以250℃保持30min。
40.对比图1-图3,保留时间3min之前的峰为叔丁醇和乙醇的峰,乳酸乙酯的保留时间约为4.4min,乳酸的保留时间约为5.8min,表明本发明使用的唾液乳杆菌jyls-372在含乙醇的培养基中培养10h后,能够产生乳酸乙酯。
41.五个培养基上清液中乙醇与乳酸乙酯含量如表2所示,可以看出随时间变化,乙醇含量逐渐降低,乳酸乙酯含量逐渐升高,表明唾液乳杆菌jyls-372能够将乙醇反应为乳酸乙酯。
42.表2 上清液中乙醇与乳酸乙酯含量随培养时间的变化情况(单位:质量%)实施例5取30只小鼠,随机均分为空白对照组、低剂量组和高剂量组三组。空白对照组小鼠不服用唾液乳杆菌菌粉,低剂量组小鼠每次白酒灌胃后30分钟服用实施例1产品(菌数100亿cfu/g)2g,高剂量组小鼠每次白酒灌胃后30分钟服用实施例1产品(菌数100亿cfu/g)4g。
43.各组灌胃白酒30分钟后,立即将小鼠放在垂直的金属网上,观察小鼠活动情况并记录小鼠掉落下金属网为止的攀附时间。随后将小鼠翻转放置在水平平板上,观察记录其翻正反射消失时间(即将其翻转放置,若背向下的姿势保持30s以上,则判为翻正反射消失)和醉酒持续时间(即小鼠翻正反射消失到翻正反射恢复的时间)。
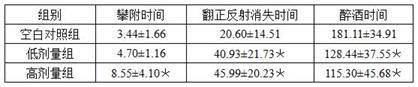
44.结果如表3所示,与空白对照组相比,高剂量组小鼠的攀附时间明显延长(p《0.05),低、高剂量组小鼠的翻正反射消失时间显著延长(p《0.05)、醉酒时间显著缩短(p《0.05),表明唾液乳杆菌能明显改善小鼠醉酒后的行为学指标。同时,从攀附时间对比来看,唾液乳杆菌jyls-372的剂量越高,其解酒效果越好。
45.表3 唾液乳杆菌jyls-372对醉酒小鼠行为学指标的影响(单位:min)注:*表示与空白对照组相比较,p《0.05。
46.实施例6 人群解酒的实验验证随机选取实验对象30人(17男、13女),年龄分布40-50岁。实验时间为一周时间,在这一周时间中,实验对象喝酒前半小时服用实施例1产品(菌数200亿cfu/g)4g。研究实验对象的酒后感触并与以前未服用实施例1产品时对比。对比结果如下表4所示。
47.表4 人群解酒实验结果(单位:人)表4中,有明显效果指与以前未服用实施例1产品相比喝酒量有所提高(尤其啤酒较之前可多喝200-500ml),喝酒期间无明显心率加速现象,喝酒期间脸白或脸红现象程度较以前未服用时有明显减轻,酒后无一例头痛现象;有效果指酒量无明显变化,但酒后口渴程度较之前大大减轻,酒后情绪较之前大为平稳,波动较小。
48.由表4可以看出,通过人群试验验证,本发明使用唾液乳杆菌jyls-372制备的益生菌产品具有一定的解酒效果。
49.尽管通过参考附图并结合优选实施例的方式对本发明进行了详细描述,但本发明并不限于此。在不脱离本发明的精神和实质的前提下,本领域普通技术人员可以对本发明
的实施例进行各种等效的修改或替换,而这些修改或替换都应在本发明的涵盖范围内/任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到变化或替换,都应涵盖在本发明的保护范围之内。
