芋螺毒素肽类似物以及用于治疗疼痛和炎性病况的用途
1.对电子提交的序列表的引用
2.本发明申请作为参考并入了作为于2019年1月3日创建并且大小为66,707字节的标题为“seq_listing_14520-002-228.txt”的文本文件与本发明申请一起提交的序列表。
1.技术领域
3.本文提供了α-芋螺毒素肽类似物,包括共价连接至聚乙二醇(peg)的α-芋螺毒素肽类似物和这些α-芋螺毒素肽类似物的药物组合物。本文还提供了有助于通过抑制受试者中含有α9的烟碱乙酰胆碱受体(nachr)(例如,nachr的α9α10亚型)的治疗或预防的治疗或预防病况的方法
2.
背景技术:
4.芋螺属(conus)中的掠食性海蜗牛具有富含神经药理学活性肽(芋螺毒素肽或芋螺毒素)的毒液(olivera等人,1990,science 249:257-263)。芋螺属中大约有500个种,且在迄今为止已调查的那些种中,保守特征为其毒液中存在α-芋螺毒素肽。天然α-芋螺毒素肽是具有c1-c3和c2-c4二硫桥模式的高度二硫键交联的肽(azam and mcintosh,2009,acta pharmacol.sin.30:771-783)。
5.α-芋螺毒素肽通常显示为烟碱乙酰胆碱受体(nachr)拮抗剂(nicke等人,2004,eur.j.biochem.271:2305-2319)。nachr是由一或多个α亚基(α1-α10)单独或与一或多个非-α亚基(β1-β4)一起组装的五聚体配体门控离子通道(sine and engel,2006,nature440:448-455)。
6.α9α10nachr亚基在不同组织中表达。在内耳中,α9α10nachr介导传出的橄榄耳蜗纤维和耳蜗毛细胞之间的突触传递(vetter等人,1999,neuron 23:93-103)。α9α10亚基还存在于脊神经后根神经节神经元(lips等人,2002,neuroscience 115:1-5)、淋巴细胞(peng等人,2004,life.sci.76:263-280)、皮肤角化细胞(nguyen等人,2000,am.j.pathol.157:1377-1391)和垂体结节部中(elgoyhen等人,1994,cell 79:705-715;zuo等人,1999,proc.natl.acad.sci.usa 96:14100-14105)。
7.具有包括α9α10拮抗剂活性的药理学谱的化合物预防或减弱一些啮齿类动物模型中的疼痛表现,包括由化疗、创伤性神经损伤及糖尿病所引起的神经性疼痛(参见hone and mcintosh,2018,febs lett.592:1045-1062)。
8.天然芋螺毒素肽rgia具有氨基酸序列gly-cys-cys-ser-asp-pro-arg-cys-arg-tyr-arg-cys-arg(seq id no:1)(ellison等人,2008,j.mol.biol.377:1216-1227)。α-芋螺毒素肽rgia已显示阻断α9α10nachr活性(romero等人,2017,proc.natl.acad.sci.usa 14:e1825-e1832)。
9.rgia属于α-芋螺毒素的α-4/3家族。rgia的天然结构的特征在于两个紧密的半胱氨酸内环,其由在cys2-cys8(有时称为cysi-cysiii)与cys3-cys12(有时称为cysii-cysiv)之间所形成的两个二硫键限定(ellison等人,2008,j.mol.biol.377:1216-1227;
armishaw,2010,toxins 2:1471-1499)。在α-芋螺毒素中,第一和第二半胱氨酸残基始终相邻,但第二和第三半胱氨酸之间以及第三和第四半胱氨酸残基之间的氨基酸残基数可以不同。这产生了两个中间氨基酸环,表示为环1或m-环和环2或n-环。在rgia中,环1含有4个氨基酸且环2含有3个氨基酸。α-芋螺毒素的二硫键以及因此的二级结构不稳定并且经受重排(armishaw,2010,toxins 2:1471-1499)。
10.α-芋螺肽的两个二硫键经受重排并且可以形成替代立体结构,包括带状形式(二硫键cys-2-cys12和cys3-cys8)以及珠粒形式(二硫键cys2-cys3和cys8-cys12)。尽管肽的天然或球状形式对α9α10-nachr具有活性,但带状或珠粒形式均认为不具有活性(dekan等人,2011,j.am.chem.soc.133:15866-15869;armishaw等人,2006,j.bio.chem.281:14136-14143)。
11.hargittai等人评价了α-芋螺毒素si的四种内酰胺-桥接衍生物,并且这四种内酰胺-桥接衍生物中仅一种在与bc3h1细胞的结合中未丧失显著活性(hargittai等人,2000,j.med.chem.43:4787-4792)。bondebjerg等人评价了α-芋螺毒素gi的合成硫醚模拟物,并且发现所测试的两种异构物的药理学活性显著低于天然肽(bondebjerg等人,2003,chembiochem 4:186-194)。评价了α-imi的非还原二碳杂类似物,并且在两种情况下均发现药理学活性降低大约10-倍(macraild等人,2009,j.med.chem.52:755-762)。imi的某些特定硒代半胱氨酸和丙氨酸丁氨酸硫醚衍生物保留了阻断大鼠α7nachr的活性(dekan等人,2011,j.am.chem.soc.133:15866-15869;armishaw等人,2006,j.bio.chem.281:14136-14143)。
12.van lierop评价了α-芋螺毒素vc1.1的二硫键的二碳杂取代并且发现[2,8]-顺式及[2,8]-反式二碳杂类似物对大鼠α9α10nachr不具有活性,而vc1.1的[3,16]-顺式及[3,16]-反式异构体对大鼠α9α10nachr的活性极大地降低(10-100倍)(van lierop等人,2013,acs chemical biology 8:1815-1821)。yu等人产生了vc1.1的n末端至c末端肽连接的衍生物,其具有被his或phe替换的一或多个半胱氨酸残基。相对于天然vc1.1,这些衍生物对人α9α10nachr的效力显著降低(低20至40-倍)(yu等人2015,sci.rep.5:13264)。在同一研究组的单独研究中,在不存在n末端至c末端环化的情形下,vc1.1中的cys2被his的取代和cys8被phe的取代还导致对人α9α10nachr的活性丧失,尽管分析证实了二级结构的保留(tabassum等人2017,acs omega2:4621
–
4631)。
[0013]
已开展了类似的工作来使用二碳杂键替换rgia中的二硫键(chhabra等人,2014,j.med.chem.57:993-9944)。尽管该研究发现rgia的二碳杂类似物在合成上可行,但基于nmr的天然rgia与二碳杂类似物的结构比较证实在所述肽的第二环中具有显著结构差异。与这些结构差异以及来自相关vc1.1的观察结果一致,rgia的[2,8]-顺式和[2,8]-反式二碳杂类似物对大鼠α9α10nachr不具有活性,而[3,12]-顺式及[3,12]-反式异构体二者对乙酰胆碱-引起的α9α10电流的抑制均降低>100-倍。chhabra等人未评价二碳杂桥接的rgia类似物对人α9α10nachr的活性。
[0014]
knuhtsen等人(knuhtsen等人,chemical science,2019,advance article)研究α-芋螺毒素gi的类似物,其中cys2-cys7或cys3-cys13二硫键被1,5-二取代的1,2,3-三唑桥替换。
[0015]
天然rgia对人α9α10nachr的亲和力较大鼠α9α10nachr低大约300-倍,并且这种亲
合力差异已反映在rgia结合口袋内α9亚基的氨基酸序列中的变异(azam等人,2015,mol.pharmacol.87:855-864)。
[0016]
已报道了rgia的芋螺毒素肽类似物(wo 2008/011006;romero等人,2017,proc.natl.acad.sci.usa 14:e1825-e1832;wo 2016/073949)。
[0017]
研究已证实了在rgia的环2中更大程度的结构柔性,特别是在羧基末端周围,以及环2残基在人受体结合相互作用中的重要性(clark等人,2008,febs lett.582(5):597-602)。nmr光谱学还表明rgia的cys12可以与野生型或天然肽中的tyr10相互作用(ellison等人,2008,j.mol.biol.377:1216-1227;armishaw,2010,toxins2:1471-1499)。
[0018]
芋螺毒素肽及其类似物是α9α10nachr的竞争性抑制剂,并且它们在ach结合位点处,即在相邻亚基之间的界面处结合。亚基界面埋藏至的探针半径,表面积为~其中这些芋螺毒素与亚基间包含小于的距离的残基相互作用(hansen等人,2005,embo j.,24(20):3635-3646)。
[0019]
与其它已知的nachr亚基的氨基酸比较显示α9α10nachr与α7nachr密切相关(elgoyhen等人,1994,cell 79(4):705-715;lustig等人,2001,genomics,73(3):272-283;sgard等人,2002,mol.pharmacol.61(1):150-159)。α7nachr在神经系统中具有多向性效应(ellison等人,2008,j.mol.biol.377:1216-1227;armishaw,2010,toxins2:1471-1499)。
[0020]
非共价或共价连接至聚乙二醇聚合物(peg化)可以改变生物分子,如肽的物理和化学性质,如其构象、静电结合及疏水性(veronese and mero,2008,biodrugs,22:315-329;还参见harris等人,2001,clin.pharmacokinet.40:539-551)。
[0021]
由于peg聚合物对药物-靶标结合相互作用的空间位阻,因此治疗性蛋白的peg化通常导致其结合亲和力的丧失(fishburn,2008,j.pharm.sci.97:4167-4183)。peg化的治疗性蛋白可以通过位阻效应或通过peg与蛋白质内疏水结构域之间的疏水-疏水相互作用而丧失生物活性或效力(parrott and desimone,2011,nat.chem.4:13-14)。
[0022]
研究已表明含α9的nachr的拮抗剂在神经性疼痛动物模型中显示出止痛活性(hone等人,2018,british journal of pharmacology,175:1915-1927)。研究还显示啮齿类动物中的α9α10nachr的抑制预防了化疗-引起的神经性疼痛(romero等人,2018,proc.natl.acad.sci.usa 114(10):e1825-e1832)。还参见,mohammadi and christie,2014,molecular pain,10:64-72;simard等人,2013,immunology and cell biology,91:195-200。
[0023]
对于具有提高的代谢稳定性同时维持对含有α9的nachr的足够的拮抗活性的芋螺毒素肽类似物的医疗需求尚未满足。本发明的芋螺毒素肽类似物满足了这些需求。
[0024]
本文中对参考文献的引用不应视为承认这些参考文献是本发明公开的现有技术。
3.
技术实现要素:
[0025]
本发明公开提供了化学式(i)所示的芋螺毒素肽类似物(seq id no:93):
[0026][0027]
或其药物可用的盐,
[0028]
其中
[0029]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且x
aa2
是n-me-gly、d-tyr或者n-me-tyr;
[0030]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基。
[0031]
在具体的实施方式中,三唑桥为
[0032]
其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素肽类似物的c2碳的连结点;并且其中x为1、2、3或4;并且y为2、3或4。
[0033]
在具体的实施方式中,其中所述三唑桥为
[0034]
在具体的实施方式中,所述三唑桥为
[0035]
在具体的实施方式中,x为1、2或3。
[0036]
在具体的实施方式中,x为1。
[0037]
在具体的实施方式中,y为2或3。
[0038]
在具体的实施方式中,y为3。
[0039]
在具体的实施方式中,x为1、2或3,且y为2或3。
[0040]
在具体的实施方式中,x为1且y为3。
[0041]
在具体的实施方式中,x为2且y为3。
[0042]
在具体的实施方式中,x为2且y为2。
[0043]
在具体的实施方式中,x为1且y为3。
[0044]
在具体的实施方式中,x为2且y为2。
[0045]
在具体的实施方式中,所述三唑桥为其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素
肽类似物的c2碳的连结点。
[0046]
在具体的实施方式中,x是x
aa1
。
[0047]
在具体的实施方式中,x是x
aa1
x
aa2
。
[0048]
在具体的实施方式中,x
aa1
选自tyr,d-tyr和phe。
[0049]
在具体的实施方式中,x是tyr。
[0050]
在具体的实施方式中,芋螺毒素肽类似物的c末端是oh。
[0051]
在具体的实施方式中,芋螺毒素肽类似物的c末端是nh2。
[0052]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ia)(seq id no:94)
[0053][0054]
其中r1是oh或nh2。
[0055]
在具体的实施方式中,r1是oh。
[0056]
在具体的实施方式中,r1是nh2。
[0057]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ig)(seq id no:30):
[0058]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ih)(seq id no:33):
[0059]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ii)(seq id no:36):
[0060][0061]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ik)(seq id no:42):
[0062]
在具体的实施方式中,芋螺毒素肽类似物是化学式(il)(seq id no:45):
[0063]
在具体的实施方式中,芋螺毒素肽类似物是化学式(im)(seq id no:48)
[0064][0065]
在具体的实施方式中,芋螺毒素肽类似物是化学式(in)(seq id no:51)
[0066][0067]
在具体的实施方式中,芋螺毒素肽类似物是化学式(io)(seq id no:54)
[0068][0069]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ip)(seq id no:57)
[0070][0071]
本文还提供了peg化的芋螺毒素肽类似物或其药物可用的盐,其中所述芋螺毒素肽类似物具有化学式(i)(seq id no:93):
[0072][0073]
其中
[0074]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且
x
aa2
是n-me-gly、d-tyr或者n-me-tyr;
[0075]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基;和
[0076]
其中所述芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个聚乙二醇(peg)聚合物。
[0077]
在具体的实施方式中,所述三唑桥为
[0078]
其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素肽类似物的c2碳的连结点;并且其中x为1、2、3或4;并且y为2、3或4。
[0079]
在具体的实施方式中,其中所述三唑桥为
[0080]
在具体的实施方式中,所述三唑桥为
[0081]
在具体的实施方式中,x是1,2或3。
[0082]
在具体的实施方式中,x是1。
[0083]
在具体的实施方式中,y是2或3。
[0084]
在具体的实施方式中,y是3。
[0085]
在具体的实施方式中,x是1,2或3且y是2或3。
[0086]
在具体的实施方式中,x是1且y是3。
[0087]
在具体的实施方式中,x是2且y是3。
[0088]
在具体的实施方式中,x是2且y是2。
[0089]
在具体的实施方式中,x是1且y是3。
[0090]
在具体的实施方式中,x是2且y是2。
[0091]
在具体的实施方式中,所述三唑桥为其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素肽类似物的c2碳的连结点。
[0092]
在具体的实施方式中,x是x
aa1
。
[0093]
在具体的实施方式中,x是x
aa1
x
aa2
。
[0094]
在具体的实施方式中,x
aa1
选自tyr,d-tyr和phe。
[0095]
在具体的实施方式中,x是tyr。
[0096]
在具体的实施方式中,芋螺毒素肽类似物的c末端是oh。
[0097]
在具体的实施方式中,芋螺毒素肽类似物的c末端是nh2。
[0098]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ia)(seq id no:94)
[0099][0100]
在具体的实施方式中,r1是oh。
[0101]
在具体的实施方式中,r1是nh2。
[0102]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ig)(seq id no:30):
[0103]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ih)(seq id no:33):
[0104]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ii)(seq id no:36):
[0105]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ik)(seq id no:42):
[0106][0107]
在具体的实施方式中,芋螺毒素肽类似物是化学式(il)(seq id no:45):
[0108][0109]
在具体的实施方式中,芋螺毒素肽类似物是化学式(im)(seq id no:48)
[0110][0111]
在具体的实施方式中,芋螺毒素肽类似物是化学式(in)(seq id no:51)
[0112][0113]
在具体的实施方式中,芋螺毒素肽类似物是化学式(io)(seq id no:54)
[0114][0115]
在具体的实施方式中,芋螺毒素肽类似物是化学式(ip)(seq id no:57)
[0116][0117]
在具体的实施方式中,所述芋螺毒素肽类似物共价连接至一个peg聚合物。
[0118]
在具体的实施方式中,所述peg聚合物共价连接至芋螺毒素肽类似物的n-末端。
[0119]
在具体的实施方式中,所述peg聚合物共价连接至芋螺毒素肽类似物的c-末端。
[0120]
在具体的实施方式中,所述peg聚合物共价连接至非芋螺毒素肽类似物的n-末端或c-末端的氨基酸残基位置。
[0121]
在具体的实施方式中,所述peg聚合物通过连接基团共价连接至芋螺毒素肽类似物。
[0122]
在具体的实施方式中,所述连接基团是具有以下化学式的戊酸酯接头:
[0123]
在具体的实施方式中,所述连接基团是亚丁基。
[0124]
在具体的实施方式中,所述连接基团是羰基。
[0125]
在具体的实施方式中,所述peg聚合物是直链或支链peg聚合物。
[0126]
在具体的实施方式中,所述peg聚合物是直链peg聚合物。
[0127]
在具体的实施方式中,所述peg聚合物具有10kda至40kda的范围内的分子量。
[0128]
在具体的实施方式中,所述peg聚合物是直链30kda的peg聚合物。
[0129]
在具体的实施方式中,所述peg聚合物是直链30kda mpeg聚合物。
[0130]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iia)(seq id no:83):
[0131][0132]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iig)(seq id no:95):
[0133][0134]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iih)(seq id no:96):
[0135][0136]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iii)(seq id no:97):
[0137][0138]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iik)(seq id no:98):
[0139][0140]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iil)(seq id no:99):
[0141][0142]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iim)(seq id no:100):
[0143][0144]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iin)(seq id no:101):
[0145][0146]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iio)(seq id no:102):
[0147]
[0148]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iip)(seq id no:103):
[0149][0150]
本文还提供了化学式(ib)所示的芋螺毒素肽类似物(seq id no:104):
[0151][0152]
或其药物可用的盐,
[0153]
其中r2为oh或nh2。
[0154]
在具体的实施方式中,r2是oh。
[0155]
在具体的实施方式中,r2是nh2。
[0156]
本文还提供了peg化的芋螺毒素肽类似物或其药物可用的盐,其中所述芋螺毒素肽类似物具有化学式(ib)(seq id no:104):
[0157][0158]
其中r2为oh或nh2;和
[0159]
其中所述芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个聚乙二醇(peg)聚合物。
[0160]
在具体的实施方式中,r2是oh。
[0161]
在具体的实施方式中,r2是nh2。
[0162]
在具体的实施方式中,所述芋螺毒素肽类似物共价连接至一个peg聚合物。
[0163]
在具体的实施方式中,所述peg聚合物共价连接至芋螺毒素肽类似物的n-末端。
[0164]
在具体的实施方式中,所述peg聚合物共价连接至芋螺毒素肽类似物的c-末端。
[0165]
在具体的实施方式中,所述peg聚合物共价连接至非芋螺毒素肽类似物的n-末端或c-末端的氨基酸残基位置。
[0166]
在具体的实施方式中,所述peg聚合物通过连接基团共价连接至芋螺毒素肽类似物。
[0167]
在具体的实施方式中,所述连接基团是具有以下化学式的戊酸酯接头:
[0168]
在具体的实施方式中,所述连接基团是亚丁基。
[0169]
在具体的实施方式中,所述连接基团是羰基。
[0170]
在具体的实施方式中,所述peg聚合物是直链或支链peg聚合物。
[0171]
在具体的实施方式中,所述peg聚合物是直链peg聚合物。
[0172]
在具体的实施方式中,所述peg聚合物具有10kda至40kda的范围内的分子量。
[0173]
在具体的实施方式中,所述peg聚合物是直链30kda的peg聚合物。
[0174]
在具体的实施方式中,所述peg聚合物是直链30kda mpeg聚合物。
[0175]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iib)(seq id no:105):
[0176][0177]
本文还提供了选自芋螺毒素肽类似物ia、ia’、ib、ib’、ic、id、ie、if、ig、ih、ii、ij、ik、il、im、in、io、ip、iq、ir、is、it、iu和iv的芋螺毒素肽类似物,或其药物可用的盐。
[0178]
在具体的实施方式中,所述芋螺毒素肽类似物选自芋螺毒素肽类似物ia、ia’、ib、ib’、ig、ih、ii、ik、il、im、in、io和ip。
[0179]
在具体的实施方式中,所述芋螺毒素肽类似物选自芋螺毒素肽类似物ia、ia’、ib和ib’。
[0180]
本文还提供了包含本文所述的芋螺毒素肽类似物或其药物可用的盐或者peg化的芋螺毒素肽类似物或其药物可用的盐和任选地药物可用的载体的药物组合物。
[0181]
本文还提供了有助于通过抑制受试者中含有α9的烟碱乙酰胆碱受体(nachr)的治疗或预防的治疗或预防病况的方法,其包括向所述受试者施用治疗有效量的芋螺毒素肽类似物或其药物可用的盐,或者peg化的芋螺毒素肽类似物或其药物可用的盐,或者本文所述的药物组合物。
[0182]
本文还提供了治疗或预防受试者中与含有α9的烟碱乙酰胆碱受体(nachr)的激活有关的病况的方法,其包括向所述受试者施用治疗有效量的芋螺毒素肽类似物或其药物可用的盐,或者peg化的芋螺毒素肽类似物或其药物可用的盐,或者本文所述的药物组合物。
[0183]
在具体的实施方式中,有助于通过抑制含有α9的nachr的治疗或预防的病况是疼痛或炎症。
[0184]
在具体的实施方式中,所述包括是疼痛。
[0185]
在具体的实施方式中,所述疼痛选自全身疼痛、慢性疼痛、神经性疼痛、伤害性疼痛、炎症性疼痛、内脏疼痛、体细胞疼痛、由周围神经损伤所引起的疼痛、由炎性病症所引起的疼痛、由代谢病症所引起的疼痛、由癌症所引起的疼痛、由化疗所引起的疼痛、由手术程序所引起的疼痛和由烧伤所引起的疼痛。
[0186]
在具体的实施方式中,所述疼痛是癌症-相关慢性疼痛。
[0187]
在具体的实施方式中,有助于通过抑制含有α9的nachr的治疗或预防的病况是炎性病况。
[0188]
在具体的实施方式中,所述炎性病况选自炎症、慢性炎症、风湿性疾病、败血病、纤维性肌痛、炎性肠病、结节病、子宫内膜异位、子宫纤维瘤、炎性皮肤病、炎性肺病、与神经系统炎症有关的疾病、牙周病和心血管疾病。
[0189]
在具体的实施方式中,所述炎性病况是受免疫细胞介导的。
[0190]
在具体的实施方式中,所述炎性病况是损伤后的长期炎症和/或周围神经病。
[0191]
在具体的实施方式中,有助于通过抑制含有α9的nachr的治疗或预防的病况是疼痛和炎症。
[0192]
在具体的实施方式中,有助于通过抑制含有α9的nachr的治疗或预防的病况是炎症和神经病。
[0193]
在具体的实施方式中,有助于通过抑制含有α9的烟碱乙酰胆碱受体(nachr)的治疗或预防的病况是有助于通过抑制nachr的α9α10亚型的治疗或预防的病况。
[0194]
在具体的实施方式中,所述受试者是人。
[0195]
本文还提供了治疗或预防受试者中疼痛或炎症的方法,其包括向所述受试者施用治疗有效量的芋螺毒素肽类似物或其药物可用的盐,或者peg化的芋螺毒素肽类似物或其药物可用的盐,或者本文所述的药物组合物。
[0196]
本文还提供了芋螺毒素肽类似物或其药物可用的盐,或者peg化的芋螺毒素肽类似物或其药物可用的盐,或者本文所述的药物组合物用于在有助于通过抑制受试者中含有α9的烟碱乙酰胆碱受体(nachr)的治疗或预防的病况的治疗或预防中的使用。
[0197]
本文还提供了包含芋螺毒素肽类似物或其药物可用的盐,或者peg化的芋螺毒素肽类似物或其药物可用的盐的药物组合物用于在有助于通过抑制受试者中含有α9的烟碱乙酰胆碱受体(nachr)的治疗或预防的病况的治疗或预防中的使用。
[0198]
本文还提供了芋螺毒素肽类似物或其药物可用的盐,或者peg化的芋螺毒素肽类似物或者其药物可用的盐,或者本文所述的药物组合物在制备用于治疗或预防有助于通过抑制受试者中含有α9的烟碱乙酰胆碱受体(nachr)的治疗或预防的病况的药剂中的使用。
[0199]
本文还提供了芋螺毒素肽类似物或其盐,其中所述芋螺毒素肽类似物的氨基酸序列为
[0200]
gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-trp-gln-x
aa12-x(seq id no:106),其中
[0201]
x
aa3
选自(s)-炔丙基甘氨酸、(s)-叠氮基丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮
双高炔丙基甘氨酸;
[0252]
其中当x
aa3
选自(s)-炔丙基甘氨酸、(s)-高炔丙基甘氨酸和(s)-双高炔丙基甘氨酸时,x
aa12
为(s)-叠氮基高丙氨酸或(s)-叠氮基缬氨酸;并且当x
aa3
选自(s)-叠氮基丙氨酸、(s)-叠氮基高丙氨酸和(s)-叠氮基缬氨酸时,x
aa12
为(s)-高炔丙基甘氨酸或者(s)-双高炔丙基甘氨酸;
[0253]
x如以上对于化学式(i)所示的芋螺毒素肽类似物所定义的;和
[0254]
其中中间体芋螺毒素肽类似物的c-末端如以上对于化学式(i)所示的芋螺毒素肽类似物所定义的;和
[0255]
其中在所述三唑形成条件下,x
aa3
与x
aa12
反应以在化学式(i)所示的芋螺毒素肽类似物中形成三唑桥。
[0256]
本文还提供了制备化学式(ib)所示的芋螺毒素肽类似物(seq id no:104)或其药物可用的盐的方法,
[0257][0258]
其中化学式(ib)所示的芋螺毒素肽类似物的c-末端为羧酸或酰胺基,
[0259]
其包括使中间体芋螺毒素肽类似物或其盐经受三唑形成条件,其中所述中间体芋螺毒素肽类似物的氨基酸序列为gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-x
aa10-gln-x
aa12-tyr(seq id no:107),
[0260]
其中
[0261]
x
aa3
为(s)-炔丙基甘氨酸;
[0262]
x
aa9
为瓜氨酸;
[0263]
x
aa10
为3-碘-tyr;
[0264]
x
aa12
为(s)-叠氮基缬氨酸;和
[0265]
其中中间体芋螺毒素肽类似物的c-末端如以上对于化学式(ib)所示的芋螺毒素肽类似物所定义的;和
[0266]
其中在所述三唑形成条件下,x
aa3
与x
aa12
反应以形成如化学式(ib)所示的芋螺毒素肽类似物中所示的三唑桥。
[0267]
本文还提供了制备peg化的芋螺毒素肽类似物或其药物可用的盐的方法,其包括在反应条件下,使芋螺毒素肽类似物或其盐接触一种或多种反应性聚乙二醇(peg)聚合物以形成peg化的芋螺毒素肽类似物,其中所述反应性peg聚合物分别包括任选地通过连接基团共价连接至peg聚合物的反应基团,并且其中每个反应基团在所述反应条件下反应以与芋螺毒素肽类似物形成共价键,借此芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个peg聚合物,
[0268]
其中所述芋螺毒素肽类似物的氨基酸序列为gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-trp-gln-x
aa12-x(seq id no:106),
[0269]
其中
[0270]
x
aa3
选自(s)-炔丙基甘氨酸、(s)-叠氮基丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基高丙氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸;
[0271]
x
aa9
为瓜氨酸;
[0272]
x
aa12
选自(s)-叠氮基高丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸;
[0273]
其中当x
aa3
选自(s)-炔丙基甘氨酸、(s)-高炔丙基甘氨酸和(s)-双高炔丙基甘氨酸时,x
aa12
为(s)-叠氮基高丙氨酸或(s)-叠氮基缬氨酸;并且当x
aa3
选自(s)-叠氮基丙氨酸、(s)-叠氮基高丙氨酸和(s)-叠氮基缬氨酸时,x
aa12
为(s)-高炔丙基甘氨酸或者(s)-双高炔丙基甘氨酸;
[0274]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且x
aa2
是n-me-gly、d-tyr或n-me-tyr;和
[0275]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基。
[0276]
本文还提供了制备peg化的芋螺毒素肽类似物或其药物可用的盐的方法,其包括在反应条件下,使芋螺毒素肽类似物或其盐接触一种或多种反应性聚乙二醇(peg)聚合物以形成peg化的芋螺毒素肽类似物,其中所述反应性peg聚合物分别包括任选地通过连接基团共价连接至peg聚合物的反应基团,并且其中每个反应基团在所述反应条件下反应以与芋螺毒素肽类似物形成共价键,借此芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个peg聚合物,
[0277]
其中所述芋螺毒素肽类似物的氨基酸序列为gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-x
aa10-gln-x
aa12-tyr(seq id no:107),
[0278]
其中
[0279]
x
aa3
为(s)-炔丙基甘氨酸;
[0280]
x
aa9
为瓜氨酸;
[0281]
x
aa10
为3-碘-tyr;
[0282]
x
aa12
为(s)-叠氮基缬氨酸;
[0283]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基。
4.附图说明
[0284]
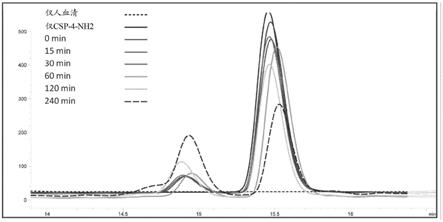
图1a-图1d:人血清中csp-4-nh2的二硫键改组。图1a:将csp-4-nh2加样至人血清中并在37℃下培育指定时间段,然后将样品冷冻,通过沉淀和过滤进行纯化并通过rp-hplc进行分析。观察到主峰向具有更快保留时间的次峰的时间依赖性转化。图1b:分析了合成构建的csp-4-nh2带状、珠粒和天然异构体以及分离自人血清的csp-4-nh2样品的各个注射剂。血清来源的峰的共迁移显示天然形式向带状异构体的转化。图1c:血清来源的化合物csp-4-nh2的分离,然后冷冻干燥和质谱分析显示天然及带状异构体二者均具有相同的质荷比。图1d:通过csp-4-nh2的谷胱甘肽还原使球状转化为带状形式,这表明二硫键改组是异构化的基础。
[0285]
图2a-图2b:大鼠血浆中芋螺毒素肽类似物ia和芋螺毒素肽类似物csp-4-nh2的反相hplc分析。图2a:在0h、8h和24h对芋螺毒素肽类似物ia的反相hplc分析(黑线:0h;深灰色线:8h;浅灰色线:24h)。图2b:在0h、8h及24h对大鼠血浆中芋螺毒素肽类似物csp-4-nh2(“天然”形式,由两个二硫键组成,一个位于cys2与cys8之间,第二个位于cys3与cys12之间)的反相hplc分析(黑线:0h;深灰色线:8h;浅灰色线:24h)。
[0286]
图3a-图3b:芋螺毒素肽类似物抑制人α9α10nachr中的ach-门控电流的浓度-反应曲线。图3a:芋螺毒素肽类似物ia、ia’及ib’抑制人α9α10nachr中的ach-门控电流的浓度-反应曲线(
●
:ia;
▲
:ia’;
□
:ib’)。图3b:芋螺毒素肽类似物csp-4-nh2和csp-4-oh抑制人α9α10nachr中的ach-门控电流的浓度-反应曲线(
●
:csp-4-nh2;
▲
:csp-4-oh)。
[0287]
图4:rgia(seq id no:1)、imi(seq id no:2)及vc1.1(seq id no:3)的氨基酸序列比较。
[0288]
图5a-图5b:芋螺毒素肽类似物抑制人α9α10nachr中的ach-门控电流的浓度-反应曲线。图5a:芋螺毒素肽类似物csp-4-oh和csp-4-destyr-oh抑制人α9α10nachr中的ach-门控电流的浓度-反应曲线(
▲
:csp-4-oh;
■
:csp-4-destyr-oh)。图5b:芋螺毒素肽类似物1a及1q抑制人α9α10nachr中的ach-门控电流的浓度-反应曲线(
●
:1a;
■
:1q)。
[0289]
图6a-图6b:来自注射了人(左)或大鼠(右)α9α10nachr的卵母细胞的代表性迹线。暴露于化合物peg化的芋螺毒素肽类似物iia前后的ach-门控电流。图6a:人α9α10nachr对ach的反应。图6b:大鼠α9α10nachr对ach的反应。
[0290]
图7a-图7b:peg化的芋螺毒素肽类似物在大鼠中的药物动力学谱。以1mg/kg向大鼠静脉内和皮下施用的peg化的芋螺毒素肽类似物iia和芋螺毒素肽类似物ia的平均浓度vs.时间的谱图(n=3)。图7a:peg化的芋螺毒素肽类似物iia的药物动力学谱(1mg/kg iv施用;1mg/kg sc施用)。图7b:芋螺毒素肽类似物ia的药物动力学谱(1mg/kg iv施用;1mg/kg sc施用)。
[0291]
图8:peg化的芋螺毒素肽类似物iia在猴中的药物动力学谱。以1mg/kg向食蟹猕猴(cynomolgus macaque)静脉内和皮下施用的化合物21的平均浓度vs时间的谱图(n=3)。(1mg/kg iv施用;1mg/kg sc施用)。
[0292]
图9:芋螺毒素肽类似物ib’在大鼠慢性压迫性损伤(cci)模型中的止痛效力及作用持续时间(
■
:0.1mg/kg/天芋螺毒素肽类似物ib’;
●
:媒介物)。
[0293]
图10a-图10c:芋螺毒素肽类似物csp-4-nh2和csp-4-nh2的peg化衍生物在大鼠cipn模型中的止痛效力及作用持续时间。图10a:通过randall-selitto测试测量机械性痛觉过敏,其表明在剂量后96h内csp-4-nh2和peg化的芋螺毒素肽viii及x在大鼠cipn模型中的止痛效力(归一化反应)。图10b:通过randall-selitto测试测量机械性痛觉过敏,其表明在剂量后96h内csp-4-nh2和peg化的芋螺毒素肽vii、ix、xi和xii在大鼠cipn模型中的止痛效力(归一化反应)。图10c:csp-4-nh2及csp-4-nh2的peg化衍生物的效力持续时间的汇总图显示效力持续时间与peg化缀合化学(支链vs.直链)以及缀合的peg聚合物的大小二者相关。
[0294]
图11a-图11c:芋螺毒素肽类似物ia’、ia及peg化的芋螺毒素肽类似物iia在大鼠化疗引起的周围神经病(cipn)模型中的止痛效力及作用持续时间。图11a:与媒介物处理的对照动物相比,在引起神经病后14天向患有奥沙利铂-引起的周围神经病的大鼠施用单次
0.5mg/kg剂量的芋螺毒素肽类似物ia’使得机械性痛觉过敏统计学显著降低长达24h。(
■
:0.5mg/kg芋螺毒素肽类似物ia’;
●
:媒介物)。图11b:与媒介物处理的对照动物相比,在外科手术引起模型后第14天向患有保留性神经损伤的大鼠施用单次0.5mg/kg剂量的ia’使得机械性痛觉过敏统计学显著降低长达24h。(
■
:0.5mg/kg芋螺毒素肽类似物ia’;
●
:媒介物)。图11c:与媒介物处理的对照动物相比,在引起神经病后14天向患有奥沙利铂-引起的周围神经病的大鼠施用单次0.5mg/kg剂量的芋螺毒素肽类似物ia或者peg化的芋螺毒素肽类似物iia使得剂量后机械性痛觉过敏统计学显著降低长达4h(芋螺毒素肽类似物ia)或者72h(芋螺毒素肽类似物ia)。(媒介物;芋螺毒素肽类似物ia;peg化的芋螺毒素肽类似物iia)。通过randall selitto缩爪阈值(以克计)测量机械性痛觉过敏。所有研究的终点为randall siletto缩爪阈值(以克计)。双向方差分析,*p《0.05,**p《0.01,***p《0.001。
[0295]
5.详细说明
[0296]
应理解本发明公开不局限于本文所述的具体实施方式,并且还应理解本文所使用的术语仅出于描述具体实施方式的目的,并且不意欲限制。
[0297]
本文提供了α-芋螺毒素肽类似物,包括共价连接至聚乙二醇(peg)的α-芋螺毒素肽类似物和这些α-芋螺毒素肽类似物的药物组合物。本文还提供了有助于通过抑制受试者中含有α9的烟碱乙酰胆碱受体(nachr)(例如,nachr的α9α10亚型)的治疗或预防的治疗或预防病况的方法
[0298]
5.1.本文所使用的缩写
[0299][0300][0301]
将理解在整个发明公开中,根据单字母或3字母代码表示氨基酸。形成全部或部分肽的氨基酸可以来自已知的21种天然存在的氨基酸,通过它们的单字母缩写和它们常见的三字母缩写表示所述氨基酸。在本文所提供的肽序列中,常规的氨基酸残基具有它们常规的含义。因此,“leu”为亮氨酸,“ile”为异亮氨酸,“nle”为正亮氨酸等。为了帮助读者,常规的氨基酸以及它们相应的3字母和单字母缩写如下所示:
[0302]
丙氨酸ala(a)精氨酸arg(r)天门冬酰胺asn(n)门冬氨酸asp(d)半胱氨酸cys(c)
谷氨酸glu(e)谷氨酰胺gln(q)甘氨酸gly(g)组氨酸his(h)异亮氨酸ile(i)亮氨酸leu(l)赖氨酸lys(k)蛋氨酸met(m)苯丙氨酸phe(f)脯氨酸pro(p)丝氨酸ser(s)苏氨酸thr(t)色氨酸trp(w)酪氨酸tyr(y)缬氨酸val(v)
[0303]
在本文所提供的肽序列中,其它氨基酸和它们相应的3字母缩写如下所示:
[0304]
(s)-5-叠氮基缬氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
5-叠氮基nva
[0305]
(s)-炔丙基甘氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
pra
[0306]
(s)-3-叠氮基-丙氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
3-叠氮基ala
[0307]
(s)-高炔丙基甘氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
高pra
[0308]
(s)-γ-叠氮基-高丙氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀ
叠氮基高ala
[0309]
(s)-双-高炔丙基甘氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双高pra
[0310]
瓜氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
cit
[0311]
5.2.芋螺毒素肽rgia类似物
[0312]
在一个方面,本文提供了化学式(i)所示的芋螺毒素肽类似物(seq id no:93):
[0313][0314]
或其药物可用的盐,
[0315]
其中
[0316]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且x
aa2
是n-me-gly、d-tyr或者n-me-tyr;
[0317]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基。
[0318]
化学式(i)中c1和c2碳附近的“(s)”表示法指明了c1和c2碳的绝对构型。
[0319]
在多个实施方式中,所述三唑桥为其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素肽类似物的c2碳的连结点;并且其中x为1、2、3或4;y为2、3或4。在具体的实施方式中,所述三唑桥为在具体的实施方式中,所述三唑桥为
[0320]
在具体的实施方式中,x是1,2,3或4。在一个优选的实施方式中,x是1,2或3。在具体的实施方式中,x是1或2。在一个实施方式中,x是1。在另一个实施方式中,x是2。
[0321]
在具体的实施方式中,y是2,3或4。在具体的实施方式中,y是2或3。在一个实施方式中,y是3。在另一个实施方式中,y是2。
[0322]
在具体的实施方式中,x是1,2或3且y是2或3。在具体的实施方式中,x是1,2或3且y是2。在具体的实施方式中,x是1,2或3且y是3。在具体的实施方式中,x是1或2且y是2或3。在具体的实施方式中,x是1或3且y是2或3。在具体的实施方式中,x是2或3且y是2或3。在具体的实施方式中,x是1且y是2或3。在具体的实施方式中,x是2且y是2或3。在具体的实施方式中,x是3且y是2或3。在一个优选的实施方式中,x是1且y是3。在一个优选的实施方式中,x是2且y是3。在一个优选的实施方式中,x是2且y是2。
[0323]
在具体的实施方式中,所述三唑桥为其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素肽类似物的c2碳的连结点。
[0324]
在具体的实施方式中,所述三唑桥为其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素肽类似物的c2碳的连结点。
[0325]
在具体的实施方式中,x是x
aa1
。在具体的实施方式中,x是x
aa1
x
aa2
。
[0326]
在具体的实施方式中,x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体。在具体的实施方式中,x
aa1
是tyr,phe或trp。在具体的实施方式中,x
aa1
是tyr,d-tyr或phe。在具体的实施方式中,x
aa1
是tyr或d-tyr。在具体的实施方式中,x
aa1
是tyr或phe。在具体的实施方式中,x
aa1
是d-tyr或phe。在具体的实施方式中,x
aa1
是phe。在具体的实施方式中,x
aa1
是d-phe。在具体的实施方式中,x
aa1
是trp。在具体的实施方式中,x
aa1
是d-trp。在具体的实施方式中,x
aa1
是d-tyr。在一个优选的实施方式中,x
aa1
是tyr。
[0327]
在具体的实施方式中,x
aa2
是n-me-gly,d-tyr或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly或d-tyr。在具体的实施方式中,x
aa2
是d-tyr或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly。在具体的实施方式中,x
aa2
是n-me-tyr。在具体的实施方式中,x
aa2
是d-tyr。在具体的实施方式中,x
aa2
是任选地存在的。在具体的实施方式中,x
aa2
是存在的。在具体的实施方式中,x
aa2
是不存在的。
[0328]
在具体的实施方式中,x选自tyr,phe,d-tyr,(tyr)-(d-tyr)、(tyr)-(n-me-gly)、(tyr)-(n-me-tyr)、n-me-tyr、d-arg、n-me-d-tyr、β-tyr和n-me-arg。在具体的实施方式中,x选自tyr、phe、d-tyr、(tyr)-(d-tyr)、(tyr)-(n-me-gly)和(tyr)-(n-me-tyr)。在具体的实施方式中,x选自tyr、phe和d-tyr。在具体的实施方式中,x选自(tyr)-(d-tyr)、(tyr)-(n-me-gly)和(tyr)-(n-me-tyr)。在具体的实施方式中,x选自n-me-tyr、d-arg、n-me-d-tyr、β-tyr和n-me-arg。在具体的实施方式中,x是tyr。在具体的实施方式中,x是phe。在具体的实施方式中,x是d-tyr。在具体的实施方式中,x是(tyr)-(d-tyr)。在具体的实施方式中,x是(tyr)-(n-me-gly)。在具体的实施方式中,x是(tyr)-(n-me-tyr)。在具体的实施方式中,x是n-me-tyr。在具体的实施方式中,x是d-arg。在具体的实施方式中,x是n-me-d-tyr。在具体的实施方式中,x是β-tyr。在具体的实施方式中,x是n-me-arg。
[0329]
在具体的实施方式中,芋螺毒素肽类似物的c末端是羧酸或酰胺基。在一个优选的实施方式中,芋螺毒素肽类似物的c末端是oh。在具体的实施方式中,芋螺毒素肽类似物的c末端是nh2。
[0330]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ia)(seq id no:94):
[0331][0332]
其中r1是oh或nh2。在具体的实施方式中,r1是oh。在具体的实施方式中,r1是nh2。
[0333]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ig)(seq id no:30):
[0334][0335]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有
化学式(ih)(seq id no:33):
[0336][0337]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ii)(seq id no:36):
[0338][0339]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ik)(seq id no:42):
[0340][0341]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(il)(seq id no:45):
[0342]
[0343]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(im)(seq id no:48):
[0344][0345]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(in)(seq id no:51):
[0346][0347]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(io)(seq id no:54):
[0348][0349]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ip)(seq id no:57):
[0350][0351]
在另一个方面,本文提供了化学式(ib)所示的芋螺毒素肽类似物(seq id no:104):
[0352][0353]
或其药物可用的盐,
[0354]
其中r2为oh或nh2。
[0355]
在具体的实施方式中,r2是oh。在具体的实施方式中,r2是nh2。
[0356]
在另一个方面,本文提供了选自芋螺毒素肽类似物ia、ia’、ib、ib’、ic、id、ie、if、ig、ih、ii、ij、ik、il、im、in、io、ip、iq、ir、is、it、iu和iv的芋螺毒素肽类似物或其药物可用的盐。
[0357]
在具体的实施方式中,所述芋螺毒素肽类似物选自芋螺毒素肽类似物ia、ia’、ib、ib’、ig、ih、ii、ik、il、im、in、io和ip。
[0358]
在具体的实施方式中,所述芋螺毒素肽类似物选自芋螺毒素肽类似物ia、ia’、ib和ib’。在一个优选的实施方式中,所述芋螺毒素肽类似物是芋螺毒素肽类似物ia或ia’。在一个优选的实施方式中,所述芋螺毒素肽类似物是芋螺毒素肽类似物ia。
[0359]
5.3.peg化的芋螺毒素肽rgia类似物
[0360]
在一个实施方式中,将本发明的芋螺毒素肽类似物peg化,具体地共价连接至一个或多个peg聚合物。
[0361]
在具体的实施方式中,将芋螺毒素肽类似物共价连接至一个peg聚合物。在具体的实施方式中,将芋螺毒素肽类似物共价连接至不止一个peg聚合物。在具体的实施方式中,将芋螺毒素肽类似物共价连接至两个peg聚合物。在具体的实施方式中,将芋螺毒素肽类似物共价连接至3个peg聚合物。
[0362]
在优选的实施方式中,将peg聚合物共价连接至芋螺毒素肽类似物的n-末端,最优选地将一个peg聚合物仅附接至n-末端。在具体的实施方式中,将peg聚合物共价连接至芋螺毒素肽类似物的c-末端。在具体的实施方式中,将peg聚合物共价连接至非芋螺毒素肽类
似物的n-末端或c-末端的氨基酸残基位置。
[0363]
在具体的实施方式中,所述peg聚合物通过连接基团共价连接至芋螺毒素肽类似物。在具体的实施方式中,将peg聚合物直接共价连接至芋螺毒素肽类似物。
[0364]
在一个优选的实施方式中,所述连接基团是具有以下化学式的戊酸酯接头:在具体的实施方式中,所述连接基团是亚丁基。在具体的实施方式中,所述连接基团是亚丁基。在具体的实施方式中,所述连接基团是羰基。
[0365]
在具体的实施方式中,所述peg聚合物是直链或支链peg聚合物。在具体的实施方式中,所述peg聚合物是支链peg聚合物。在一个优选的实施方式中,所述peg聚合物是直链peg聚合物。
[0366]
在具体的实施方式中,所述peg聚合物具有10kda至40kda的范围内的分子量。在一个优选的实施方式中,所述peg聚合物是30kda peg聚合物。在具体的实施方式中,所述peg聚合物是直链30kda peg聚合物。在具体的实施方式中,所述peg聚合物是直链30kda mpeg聚合物。
[0367]
在优选的实施方式中,将一个peg聚合物附接至芋螺毒素肽类似物的氨基末端,并且将peg聚合物通过连接基团附接至芋螺毒素肽类似物,并且所述连接基团是具有以下化学式的戊酸酯接头:并且所述peg聚合物是直链30kda mpeg聚合物。
[0368]
在具体的实施方式中,本文提供了peg化的芋螺毒素肽类似物或药物可用的盐,其中所述芋螺毒素肽类似物是化学式(i)(seq id no:93):
[0369][0370]
其中
[0371]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且x
aa2
是n-me-gly、d-tyr或者n-me-tyr;
[0372]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基;和
[0373]
其中所述芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个聚乙二醇(peg)聚合物。
[0374]
在多个实施方式中,所述三唑桥为其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三
唑桥与芋螺毒素肽类似物的c2碳的连结点;并且其中x为1、2、3或4;y为2、3或4。在具体的实施方式中,所述三唑桥为在具体的实施方式中,所述三唑桥为
[0375]
在具体的实施方式中,x是1、2、3或4。在一个优选的实施方式中,x是1、2或3。在具体的实施方式中,x是1或2。在一个实施方式中,x是1。在另一个实施方式中,x是2。
[0376]
在具体的实施方式中,y是2、3或4。在具体的实施方式中,y是2或3。在一个实施方式中,y是3。在另一个实施方式中,y是2。
[0377]
在具体的实施方式中,x是1、2或3且y是2或3。在具体的实施方式中,x是1、2或3且y是2。在具体的实施方式中,x是1、2或3且y是3。在具体的实施方式中,x是1或2且y是2或3。在具体的实施方式中,x是1或3且y是2或3。在具体的实施方式中,x是2或3且y是2或3。在具体的实施方式中,x是1且y是2或3。在具体的实施方式中,x是2且y是2或3。在具体的实施方式中,x是3且y是2或3。在一个优选的实施方式中,x是1且y是3。在一个优选的实施方式中,x是2且y是3。在一个优选的实施方式中,x是2且y是2。
[0378]
在具体的实施方式中,所述三唑桥为其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素肽类似物的c2碳的连结点。
[0379]
在具体的实施方式中,所述三唑桥为其中单波浪线表示三唑桥与芋螺毒素肽类似物的c1碳的连结点,而双波浪线表示三唑桥与芋螺毒素肽类似物的c2碳的连结点。
[0380]
在具体的实施方式中,x是x
aa1
。在具体的实施方式中,x是x
aa1
x
aa2
。
[0381]
在具体的实施方式中,x
aa1
是tyr、phe、trp或者tyr、phe或trp的d-异构体。在具体的实施方式中,x
aa1
是tyr、phe或trp。在具体的实施方式中,x
aa1
是tyr、d-tyr或phe。在具体的实施方式中,x
aa1
是tyr或d-tyr。在具体的实施方式中,x
aa1
是tyr或phe。在具体的实施方式中,x
aa1
是d-tyr或phe。在具体的实施方式中,x
aa1
是phe。在具体的实施方式中,x
aa1
是d-phe。在具体的实施方式中,x
aa1
是trp。在具体的实施方式中,x
aa1
是d-trp。在具体的实施方式中,x
aa1
是d-tyr。在一个优选的实施方式中,x
aa1
是tyr。
[0382]
在具体的实施方式中,x
aa2
是n-me-gly、d-tyr或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly或d-tyr。在具体的实施方式中,x
aa2
是d-tyr或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly。在具体的实施方式中,x
aa2
是n-me-tyr。在具体的实施方式中,x
aa2
是d-tyr。在具体的实施方式中,x
aa2
是任选地存在的。在具体的实施方式中,x
aa2
是存在的。在具体的实施方式中,x
aa2
是不存在的。
[0383]
在具体的实施方式中,x选自tyr、phe、d-tyr、(tyr)-(d-tyr)、(tyr)-(n-me-gly)、(tyr)-(n-me-tyr)、n-me-tyr、d-arg、n-me-d-tyr、β-tyr和n-me-arg。在具体的实施方式中,x选自tyr、phe、d-tyr、(tyr)-(d-tyr)、(tyr)-(n-me-gly)和(tyr)-(n-me-tyr)。在具体的实施方式中,x选自tyr、phe和d-tyr。在具体的实施方式中,x选自(tyr)-(d-tyr)、(tyr)-(n-me-gly)和(tyr)-(n-me-tyr)。在具体的实施方式中,x选自n-me-tyr、d-arg、n-me-d-tyr、β-tyr和n-me-arg。在具体的实施方式中,x是tyr。在具体的实施方式中,x是phe。在具体的实施方式中,x是d-tyr。在具体的实施方式中,x是(tyr)-(d-tyr)。在具体的实施方式中,x是(tyr)-(n-me-gly)。在具体的实施方式中,x是(tyr)-(n-me-tyr)。在具体的实施方式中,x是n-me-tyr。在具体的实施方式中,x是d-arg。在具体的实施方式中,x是n-me-d-tyr。在具体的实施方式中,x是β-tyr。在具体的实施方式中,x是n-me-arg。
[0384]
在具体的实施方式中,芋螺毒素肽类似物的c末端是羧酸或酰胺基。在一个优选的实施方式中,芋螺毒素肽类似物的c末端是oh。在具体的实施方式中,芋螺毒素肽类似物的c末端是nh2。
[0385]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ia)(seq id no:94):
[0386][0387]
其中r1是oh或nh2。在具体的实施方式中,r1是oh。在具体的实施方式中,r1是nh2。
[0388]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ig)(seq id no:30):
[0389][0390]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ih)(seq id no:33):
[0391][0392]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ii)(seq id no:36):
[0393][0394]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ik)(seq id no:42):
[0395][0396]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(il)(seq id no:45):
[0397]
[0398]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(im)(seq id no:48):
[0399][0400]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(in)(seq id no:51):
[0401][0402]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(io)(seq id no:54):
[0403][0404]
在具体的实施方式中,化学式(i)所示的芋螺毒素肽类似物或药物可用的盐具有化学式(ip)(seq id no:57):
[0405][0406]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iia)(seq id no:83):
[0407][0408]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iig)(seq id no:95):
[0409][0410]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iih)(seq id no:96):
[0411][0412]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iii)(seq id no:97):
[0413][0414]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iik)(seq id no:98):
[0415][0416]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iil)(seq id no:99):
[0417][0418]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iim)(seq id no:100):
[0419][0420]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iin)(seq id no:101):
[0421]
[0422]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iio)(seq id no:102):
[0423][0424]
在具体的实施方式中,所述peg化的芋螺毒素肽类似物具有化学式(iip)(seq id no:103):
[0425][0426]
在另一个方面,本文提供了peg化的芋螺毒素肽类似物或其药物可用的盐,其中所述芋螺毒素肽类似物是化学式(ib)(seq id no:104):
[0427][0428]
其中r2为oh或nh2;和
[0429]
其中所述芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个聚乙二醇(peg)聚合物。
[0430]
在化学式(ib)的具体实施方式中,r2为oh。在化学式(ib)的具体实施方式中,r2为nh2。
[0431]
在具体的实施方式中,peg化的芋螺毒素肽类似物具有化学式(iib)(seq id no:105):
[0432][0433]
5.4.药物组合物
[0434]
本文还提供了“药物组合物”,其包括本文所提供的芋螺毒素肽类似物或者本文所提供的peg化的芋螺毒素肽类似物,和一个或多个药物可用的载体。在具体的实施方式中,芋螺毒素肽类似物以治疗有效量存在。在具体的实施方式中,芋螺毒素肽类似物以预防有效量存在。可以根据本文所提供的方法和用途来使用所述药物组合物。因此,例如,可以将所述药物组合物施用于受试者以实践本文所提供的治疗或预防方法和用途。可以配制本文所提供的药物组合物以适合于预期施用方法或途径;在本文中说明了示例性施用途径。
[0435]
药物组合物通常包括治疗有效量的本文所提供的芋螺毒素肽类似物或peg化的芋螺毒素肽类似物中的至少一种和药物可用的载体。适合的药物可用的载体包括(但不限于)抗氧化剂(例如,抗坏血酸)、防腐剂(例如,苯甲醇、对羟基苯甲酸甲酯、p-羟基苯酸酯)、乳化剂、助悬剂、分散剂、溶剂、缓冲剂、润滑剂、填充剂和/或稀释剂。例如,适合的媒介物可以是生理盐溶液。可以使用的典型的缓冲剂包括(但不限于)药物可用的弱酸、弱碱或其混合物。缓冲剂组分还可以包括水溶性试剂,如磷酸、酒石酸、琥珀酸、柠檬酸、乙酸及其盐。
[0436]
媒介物可以含有改变或维持药物组合物的ph、渗透性、粘度或稳定性的其它药物可用的赋形剂。在具体的实施方式中,所述媒介物是水性缓冲剂。在具体的实施方式中,媒介物包括(例如)氯化钠。
[0437]
本文所提供的药物组合物可以含有用于改变或维持本文所述的芋螺毒素肽类似物的释放速率的其它药物可用的制剂。这些制剂包括(例如)本领域技术人员已知的制备缓释或控释制剂的那些物质。对于药物可用的制剂,参见,例如,remington's pharmaceutical sciences,第18版(1990,mack publishing co.,easton,pa.18042)第1435-1712页,和the merck index,第12版(1996,merck publishing group,whitehouse,nj)。
[0438]
在具体的实施方式中,在无菌小瓶中作为溶液、混悬液、凝胶、乳液或者脱水或冻干粉末提供药物组合物。这些组合物可以(例如)以即可使用形式、使用前需要复原的冻干形式或者使用前需要稀释的液体形式储存。在具体的实施方式中,在一次性容器(例如,一次性小瓶、安瓿瓶、注射器或自注射器(autoinjector))中提供药物组合物。在具体的实施方式中,在多用途容器(例如,多用途小瓶或药筒(cartridge))中提供药物组合物。任何药物递送设备可以用于递送本文所述的芋螺毒素肽类似物或peg化的芋螺毒素肽类似物或药物组合物,包括植入物(例如,可植入泵)和导管。在具体的实施方式中,可以使用积存注射来在限定的一段时间内释放本文所述的芋螺毒素肽类似物或peg化的芋螺毒素肽类似物或药物组合物。通常皮下或肌内施用积存注射。
[0439]
可以配制药物组合物以与如本文所述的预定施用途径相容。
[0440]
药物组合物可以处于无菌可注射水混悬液的形式。可以使用本领域技术人员已知
相关慢性疼痛。在具体的实施方式中,所述疼痛是与神经病有关的疼痛,举例来说,它可以是药物(例如,癌症化疗剂)-引起的神经病或者感染-引起的神经病。在具体的实施方式中,所述疼痛是神经痛,其包括(但不限于)带状疱疹神经痛,例如,由于带状疱疹所造成的带状疱疹神经痛。
[0453]
在具体的实施方式中,有助于通过抑制含有α9的烟碱乙酰胆碱受体,例如,nachr的α9α10亚型的治疗或预防的病况是炎性病况。在具体的实施方式中,所述炎性病况选自炎症、慢性炎症、风湿性疾病、败血病、纤维性肌痛、炎性肠病、结节病、子宫内膜异位、子宫纤维瘤、炎性皮肤病、炎性肺病、与神经系统炎症有关的疾病、牙周病和心血管疾病。在具体的实施方式中,所述炎性病况受免疫细胞介导。在具体的实施方式中,所述炎性病况是损伤后的长期炎症和/或周围神经病。
[0454]
在具体的实施方式中,与含有α9的烟碱乙酰胆碱受体,例如,nachr的α9α10亚型有关的病况是疼痛和炎症。在具体的实施方式中,与nachr的α9α10亚型病况有关的病况是炎症和神经病。
[0455]
在另一个方面,本文提供了治疗或预防受试者中与含有α9的nachr,例如,nachr的α9α10亚型的激活有关的病况的方法,其包括向所述受试者施用治疗有效量的如本文所述的芋螺毒素肽类似物或其药物可用的盐,或者如本文所述的peg化的芋螺毒素肽类似物或其药物可用的盐,或者如本文所述的药物组合物。
[0456]
在另一个方面,本文提供了治疗或预防受试者中疼痛或炎症的方法,其包括向所述受试者施用治疗有效量的如本文所述芋螺毒素肽类似物或其药物可用的盐,或者如本文所述的peg化的芋螺毒素肽类似物或其药物可用的盐,或者如本文所述的药物组合物。在治疗或预防疼痛的方法的具体实施方式中,所述疼痛是与神经病有关的疼痛,举例来说,它可以是药物(例如,癌症化疗剂)-引起的神经病或者感染-引起的神经病。在具体的实施方式中,所述疼痛是神经痛,其包括(但不限于)带状疱疹神经痛,例如,由于带状疱疹所造成的带状疱疹神经痛。
[0457]
在具体的实施方式中,本文所提供的方法是治疗疼痛或炎症的方法。在具体的实施方式中,本文所提供的方法是治疗疼痛的方法。在具体的实施方式中,本文所提供的方法是治疗炎症的方法。
[0458]
在具体的实施方式中,本文所提供的方法是预防疼痛或炎症的方法。在具体的实施方式中,本文所提供的方法是预防疼痛的方法。在具体的实施方式中,本文所提供的方法是预防炎症的方法。
[0459]
在具体的实施方式中,预防疼痛的方法是预防与神经病有关的疼痛。在这些方法的具体实施方式中,与神经病有关的疼痛是神经痛。在具体的实施方式中,所述神经痛是带状疱疹神经痛。在具体的实施方式中,预防疼痛的方法是预防通过癌症化疗所引起的疼痛(并因此在向患者施用癌症化疗剂之前,向患者施用芋螺毒素肽类似物或其药物可用的盐)。在具体的实施方式中,预防疼痛的方法是预防通过手术程序所引起的疼痛;在这些方法的具体实施方式中,在手术程序之前和/或同时施用芋螺毒素肽类似物或其药物可用的盐,具体地,其中合理地预期所述手术程序将造成疼痛和/或炎症。
[0460]
在另一个方面,本文提供了抑制受试者中含有α9的烟碱乙酰胆碱受体(nachr),例如,nachr的α9α10亚型的方法,其包括向所述受试者施用治疗有效量的如本文所述的芋螺
毒素肽类似物或其药物可用的盐,或者如本文所述的药物组合物。
[0461]
在具体的实施方式中,“治疗”等表示在已诊断、观察到疾病、病症或病况或其症状等后起始以暂时或永久消除、减少、抑制、减轻或改善造成受试者所经受的疾病、病症或病况的潜在原因中的至少一种或者与受试者所经受的疾病、病症或病况有关的症状中的至少一种的动作(如施用芋螺毒素肽类似物或其药物可用的盐或者包含芋螺毒素肽类似物或其药物可用的盐的药物组合物)。因此,治疗可以包括抑制(即终止疾病、病症或病况或者与之有关的临床症状的发展或进一步发展)活动性疾病。
[0462]
在其中实施预防方法的本发明的具体实施方式中,预防不需要是完全的;在具体的实施方式中,所述预防是相对于在不存在芋螺毒素肽类似物或药物可用的盐的施用情况下,另外将预期发生的疾病、病况或病症,疾病、病况或病症中的部分抑制或部分预防或降低。
[0463]
在具体的实施方式中,所述施用可以通过向患者注射或另外物理递送芋螺毒素肽类似物,如通过粘膜、皮内、静脉内、肌内递送和/或本文所述的或本领域中已知的任何其它物理递送方法。当疾病、病症或病况或其症状正在治疗时,芋螺毒素肽类似物或其药物可用的盐的施用通常发生在疾病、病症或病况或其症状发病后。当疾病、病症或病况或其症状正在预防时,芋螺毒素肽类似物或其药物可用的盐的施用通常发生在疾病、病症或病况或其症状发病之前。在具体的实施方式中,在疼痛和/或炎症发病之前和之后施用芋螺毒素肽类似物或其药物可用的盐以预防和治疗疼痛和/或炎症。
[0464]
在多个实施方式中,在本文所提供的任何方法中使用如本文所述的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或者药物组合物。例如,可以在本文所述的疾病或病症或病况的治疗或预防方法中使用本文所提供的芋螺毒素肽类似物,其包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物。因此,本文所提供的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物可以用作药剂。本文所提供的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物可以用于治疗或预防有助于通过抑制含有α9的烟碱乙酰胆碱受体(nachr),例如,nachr的α9α10亚型的治疗或预防的病况的方法。本文所提供的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物可以用于治疗或预防有助于通过抑制含有α9的烟碱乙酰胆碱受体(nachr),例如,nachr的α9α10亚型的治疗或预防的病况的方法。例如,本文所提供的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物可以用于疼痛或炎症的治疗或预防方法。
[0465]
5.6.施用途径和剂量
[0466]
可以将如本文所述的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物通过任何多种途径施用于患者。这些包括(但不限于)肠胃外、关节内、鼻内、气管内、口服、皮内、局部、肌内、腹膜内、透皮、静脉内、肿瘤内、结膜、皮下和肺部途径。在具体的实施方式中,通过皮下施用来施用本文所述的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物。在具体的实施方式中,通过静脉内施用来施用本文所述的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物。在具体的实施方式中,通过关节内
施用来施用本文所述的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物。
[0467]
向患者施用的芋螺毒素肽类似物,包括(但不限于)peg化的芋螺毒素肽类似物或其药物可用的盐的量将取决于疾病性质和患者状况,并且可以通过标准临床技术和医师的认识来确定。
[0468]
在组合物中使用的准确剂量和方案还将取决于施用途径和疾病严重程度,并且应根据医师的判断和每位患者的情况来决定。可以通过医学领域的技术人员确定适当的剂量。可以将总每日剂量划分并在一天内以几个部分或者通过提供连续递送的方式施用。
[0469]
在具体的实施方式中,以0.01至约50mg/kg体重的剂量向人受试者施用芋螺毒素肽类似物或其药物可用的盐。在具体的实施方式中,以约0.5mg/kg体重的剂量向人受试者施用芋螺毒素肽类似物,例如,peg化的芋螺毒素肽类似物或其药物可用的盐。在具体的实施方式中,所述人剂量为1至1000mg/天。在具体的实施方式中,所述人日剂量为1至750mg/天;或者10至500mg/天。
[0470]
可以一次或以一定时间间隔多次施用本文所公开的芋螺毒素肽类似物,例如,peg化的芋螺毒素肽类似物或其药物可用的盐或药物组合物。应理解准确的剂量和治疗持续时间可以随要治疗的患者的年龄、体重和状况而改变,并且可以使用已知的测试规程或者通过体内或体外测试或诊断数据外推来经验性地确定。应进一步理解对于任何具体的个体,可以根据个人需要和施用或监管制剂施用的人员的专业判断,随时间调整具体的剂量方案。
[0471]
5.7.患者
[0472]
在本发明公开中所提及的患者可以是(但不限于)人或非人脊椎动物,如野生、家养或农畜动物。在具体的实施方式中,所述患者是哺乳动物,例如,人、牛、狗、猫、山羊、马、绵羊、猪、兔、大鼠或小鼠。在优选的实施方式中,所述患者是人患者。
[0473]
在具体的实施方式中,所述人患者为成年人(至少16岁)。在另一个具体的实施方式中,所述人患者为青年(12-15岁)。在另一个具体的实施方式中,所述患者为儿童(12岁以下)。
[0474]
5.8.制备芋螺毒素肽类似物的方法
[0475]
本发明公开提供了制备芋螺毒素肽类似物的方法,其中使中间体芋螺毒素肽类似物(三唑桥形成前)经受三唑形成条件以形成本发明的芋螺毒素肽类似物。
[0476]
5.8.1.中间体芋螺毒素肽类似物
[0477]
本发明公开提供了通过三唑桥用于合成芋螺毒素肽类似物的中间体芋螺毒素肽类似物的合成。可以(例如)使用固相肽合成来合成中间体芋螺毒素肽类似物。当进行固相肽合成时,可以将具有适合于形成三唑桥的反应基团(例如,叠氮基或乙炔基)的必需氨基酸引入肽(例如,rgia的芋螺毒素肽)中。可以在rgia的芋螺毒素肽类似物的3-和12-位引入必需氨基酸。
[0478]
将具有乙炔基的氨基酸残基(例如,(s)-炔丙基甘氨酸、(s)-高炔丙基甘氨酸或者(s)-双高炔丙基甘氨酸)进入3-和12-位之一,并且将具有叠氮基的氨基酸(例如,(s)-叠氮基丙氨酸、(s)-叠氮基高丙氨酸、(s)-叠氮基缬氨酸)引入另一个位置,借此当使中间体芋螺毒素肽经受三唑形成条件时,相同中间体芋螺毒素肽内的乙炔基和叠氮基可以形成三唑
环,借此在所产生的芋螺毒素肽类似物中形成三唑桥。
[0479]
在具体的实施方式中,用于形成三唑桥的必需氨基酸(例如)选自(s)-炔丙基甘氨酸、(s)-叠氮基丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基高丙氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸。
[0480]
在另一个方面,本文提供了中间体芋螺毒素肽类似物或其盐,其中所述芋螺毒素肽类似物的氨基酸序列为
[0481]
gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-trp-gln-x
aa12-x(seq id no:106),
[0482]
其中
[0483]
x
aa3
选自(s)-炔丙基甘氨酸、(s)-叠氮基丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基高丙氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸;
[0484]
x
aa9
为瓜氨酸;
[0485]
x
aa12
选自(s)-叠氮基高丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸;
[0486]
其中当x
aa3
选自(s)-炔丙基甘氨酸、(s)-高炔丙基甘氨酸和(s)-双高炔丙基甘氨酸时,x
aa12
为(s)-叠氮基高丙氨酸或(s)-叠氮基缬氨酸;并且当x
aa3
选自(s)-叠氮基丙氨酸、(s)-叠氮基高丙氨酸和(s)-叠氮基缬氨酸时,x
aa12
为(s)-高炔丙基甘氨酸或者(s)-双高炔丙基甘氨酸;
[0487]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且x
aa2
是n-me-gly、d-tyr或n-me-tyr;和
[0488]
其中所述中间体芋螺毒素肽类似物的c-末端为羧酸或酰胺基。
[0489]
在具体的实施方式中,x
aa3
为(s)-炔丙基甘氨酸或者(s)-叠氮基丙氨酸。在具体的实施方式中,其中x
aa12
为(s)-叠氮基缬氨酸或(s)-双高炔丙基甘氨酸。在具体的实施方式中,x
aa3
为(s)-炔丙基甘氨酸且x
aa12
为(s)-叠氮基缬氨酸。在具体的实施方式中,x
aa3
为(s)-高炔丙基甘氨酸且x
aa12
为(s)-叠氮基缬氨酸。在具体的实施方式中,x
aa3
为(s)-高炔丙基甘氨酸且x
aa12
为(s)-叠氮基高丙氨酸。在具体的实施方式中,x
aa3
为(s)-叠氮基高丙氨酸且x
aa12
为(s)-高炔丙基甘氨酸。在具体的实施方式中,x
aa3
为(s)-叠氮基高丙氨酸且x
aa12
为(s)-高炔丙基甘氨酸。
[0490]
在具体的实施方式中,x是x
aa1
。在具体的实施方式中,x是x
aa1
x
aa2
。
[0491]
在具体的实施方式中,x
aa1
是tyr、phe、trp或者tyr、phe或trp的d-异构体。在具体的实施方式中,x
aa1
是tyr、phe或trp。在具体的实施方式中,x
aa1
是tyr、d-tyr或phe。在具体的实施方式中,x
aa1
是tyr或d-tyr。在具体的实施方式中,x
aa1
是tyr或phe。在具体的实施方式中,x
aa1
是d-tyr或phe。在具体的实施方式中,x
aa1
是phe。在具体的实施方式中,x
aa1
是d-phe。在具体的实施方式中,x
aa1
是trp。在具体的实施方式中,x
aa1
是d-trp。在具体的实施方式中,x
aa1
是d-tyr。在优选的实施方式中,x
aa1
是tyr。
[0492]
在具体的实施方式中,x
aa2
是n-me-gly、d-tyr或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly或d-tyr。在具体的实施方式中,x
aa2
是d-tyr或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly或n-me-tyr。在具体的实施方式中,x
aa2
是n-me-gly。在具体的实施方式中,x
aa2
是n-me-tyr。在具体的实施方式中,x
aa2
是d-tyr。在具体的实施方式中,x
aa2
是任选地存在的。在具体的实施方式中,x
aa2
是存在的。在具体的实施方式中,x
aa2
是不存在的。
[0493]
在具体的实施方式中,x选自tyr、phe、d-tyr、(tyr)-(d-tyr)、(tyr)-(n-me-gly)、(tyr)-(n-me-tyr)、n-me-tyr、d-arg、n-me-d-tyr、β-tyr和n-me-arg。在具体的实施方式中,x选自tyr、phe、d-tyr、(tyr)-(d-tyr)、(tyr)-(n-me-gly)和(tyr)-(n-me-tyr)。在具体的实施方式中,x选自tyr、phe和d-tyr。在具体的实施方式中,x选自(tyr)-(d-tyr)、(tyr)-(n-me-gly)和(tyr)-(n-me-tyr)。在具体的实施方式中,x选自n-me-tyr、d-arg、n-me-d-tyr、β-tyr和n-me-arg。在具体的实施方式中,x是tyr。在具体的实施方式中,x是phe。在具体的实施方式中,x是d-tyr。在具体的实施方式中,x是(tyr)-(d-tyr)。在具体的实施方式中,x是(tyr)-(n-me-gly)。在具体的实施方式中,x是(tyr)-(n-me-tyr)。在具体的实施方式中,x是n-me-tyr。在具体的实施方式中,x是d-arg。在具体的实施方式中,x是n-me-d-tyr。在具体的实施方式中,x是β-tyr。在具体的实施方式中,x是n-me-arg。
[0494]
在具体的实施方式中,芋螺毒素肽类似物的c末端是羧酸或酰胺基。在一个优选的实施方式中,芋螺毒素肽类似物的c末端是oh。在具体的实施方式中,芋螺毒素肽类似物的c末端是nh2。
[0495]
在具体的实施方式中,x
aa3
为(s)-炔丙基甘氨酸,x
aa12
为(s)-叠氮基缬氨酸,x为tyr。在一个实施方式中,所述芋螺毒素肽类似物的c-末端为羧基。在另一个实施方式中,所述芋螺毒素肽类似物的c-末端为酰胺基。
[0496]
在具体的实施方式中,x
aa3
为(s)-高炔丙基甘氨酸,x
aa12
为(s)-叠氮基缬氨酸,x为tyr;并且其中所述芋螺毒素肽类似物的c-末端为羧基。
[0497]
在具体的实施方式中,x
aa3
为(s)-高炔丙基甘氨酸,x
aa12
为(s)-叠氮基高丙氨酸,x为tyr;并且其中芋螺毒素肽类似物的c-末端为羧基。
[0498]
在具体的实施方式中,x
aa3
为(s)-叠氮基高丙氨酸,x
aa12
为(s)-高炔丙基甘氨酸,x为tyr;并且其中芋螺毒素肽类似物的c-末端为羧基。
[0499]
在具体的实施方式中,x
aa3
为(s)-叠氮基丙氨酸,x
aa12
为(s)-双高炔丙基甘氨酸,x为tyr;并且其中芋螺毒素肽类似物的c-末端为羧基。
[0500]
在具体的实施方式中,x
aa3
为(s)-炔丙基甘氨酸,x
aa12
为(s)-叠氮基缬氨酸,x为phe;并且其中芋螺毒素肽类似物的c-末端为羧基。
[0501]
在具体的实施方式中,x
aa3
为(s)-炔丙基甘氨酸,x
aa12
为(s)-叠氮基缬氨酸,x为d-tyr;并且其中芋螺毒素肽类似物的c-末端为羧基。
[0502]
在具体的实施方式中,x
aa3
为(s)-炔丙基甘氨酸,x
aa12
为(s)-叠氮基缬氨酸,x为tyr-n-me-gly;并且其中芋螺毒素肽类似物的c-末端为羧基。
[0503]
在具体的实施方式中,x
aa3
为(s)-炔丙基甘氨酸,x
aa12
为(s)-叠氮基缬氨酸,x为tyr-d-tyr;并且其中芋螺毒素肽类似物的c-末端为羧基。
[0504]
在具体的实施方式中,x
aa3
为(s)-炔丙基甘氨酸,x
aa12
为(s)-叠氮基缬氨酸,x为tyr-n-me-tyr;并且其中芋螺毒素肽类似物的c-末端为羧基。
[0505]
在另一个方面,本文提供了中间体芋螺毒素肽类似物或其盐,其中所述芋螺毒素肽类似物的氨基酸序列为
[0506]
gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-x
aa10-gln-x
aa12-tyr(seq id no:107),其中
[0507]
x
aa3
为(s)-炔丙基甘氨酸;
[0508]
x
aa9
为瓜氨酸;
[0509]
x
aa10
为3-碘-tyr;
[0510]
x
aa12
为(s)-叠氮基缬氨酸;
[0511]
其中所述中间体芋螺毒素肽类似物的c-末端为羧酸或酰胺基。
[0512]
在具体的实施方式中,中间体芋螺毒素肽类似物的c-末端为羧基。
[0513]
在具体的实施方式中,中间体芋螺毒素肽类似物的c-末端为酰胺基。
[0514]
5.8.2.三唑桥形成
[0515]
在3-和12-位具有形成三唑桥所必需的基团的中间体芋螺毒素肽(分别具有一个乙炔基和一个叠氮基)的合成后,乙炔基和叠氮基在三唑形成条件下反应以提供三唑,借此在所产生的芋螺毒素肽类似物中形成三唑桥。
[0516]
在具体的实施方式中,本文提供了制备化学式(i)所示的芋螺毒素肽类似物(seq id no:93)或其药物可用的盐的方法,
[0517][0518]
其中
[0519]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且x
aa2
是n-me-gly、d-tyr或n-me-tyr;和
[0520]
其中化学式(i)所示的芋螺毒素肽类似物的c-末端为羧酸或酰胺基;
[0521]
其包括使中间体芋螺毒素肽类似物或其盐经受三唑形成条件,其中所述中间体芋螺毒素肽类似物的氨基酸序列为gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-trp-gln-x
aa12-x(seq id no:106),
[0522]
其中
[0523]
x
aa3
选自(s)-炔丙基甘氨酸、(s)-叠氮基丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基高丙氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸;
[0524]
x
aa9
为瓜氨酸;
[0525]
x
aa12
选自(s)-叠氮基高丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸;
[0526]
其中当x
aa3
选自(s)-炔丙基甘氨酸、(s)-高炔丙基甘氨酸和(s)-双高炔丙基甘氨酸时,x
aa12
为(s)-叠氮基高丙氨酸或(s)-叠氮基缬氨酸;并且当x
aa3
选自(s)-叠氮基丙氨酸、(s)-叠氮基高丙氨酸和(s)-叠氮基缬氨酸时,x
aa12
为(s)-高炔丙基甘氨酸或者(s)-双高炔丙基甘氨酸;
[0527]
x如以上对于化学式(i)所示的芋螺毒素肽类似物所定义的;和
[0528]
其中中间体芋螺毒素肽类似物的c-末端如以上对于化学式(i)所示的芋螺毒素肽类似物所定义的;和
[0529]
其中在所述三唑形成条件下,x
aa3
与x
aa12
反应以在化学式(i)所示的芋螺毒素肽类似物中形成三唑桥。
[0530]
在另一个方面,本文提供了制备化学式(ib)所示的芋螺毒素肽类似物(seq id no:104)或其药物可用的盐的方法,
[0531][0532]
其中化学式(ib)所示的芋螺毒素肽类似物的c-末端为羧酸或酰胺基,
[0533]
其包括使中间体芋螺毒素肽类似物或其盐经受三唑形成条件,其中所述中间体芋螺毒素肽类似物的氨基酸序列为gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-x
aa10-gln-x
aa12-tyr(seq id no:107),
[0534]
其中
[0535]
x
aa3
为(s)-炔丙基甘氨酸;
[0536]
x
aa9
为瓜氨酸;
[0537]
x
aa10
为3-碘-tyr;
[0538]
x
aa12
为(s)-叠氮基缬氨酸;和
[0539]
其中中间体芋螺毒素肽类似物的c-末端如以上对于化学式(ib)所示的芋螺毒素肽类似物所定义的;和
[0540]
其中在所述三唑形成条件下,x
aa3
与x
aa12
反应以形成如化学式(ib)所示的芋螺毒素肽类似物中所示的三唑桥。
[0541]
在具体的实施方式中,所述三唑形成条件是在hein等人,pharm.res.2008,25(10):2216-2230中所述的“点击化学”条件(即叠氮化物和末端炔烃的1,3-偶极环化加成)。在具体的实施方式中,所述三唑形成条件包括铜催化剂的存在。在具体的实施方式中,所述三唑形成条件包括铜催化剂和还原剂的存在。在一个实施方式中,铜催化剂是cu(ii)盐。在一个实施方式中,铜催化剂为cuso4。在一个实施方式中,还原剂为l-抗坏血酸。在另一个实施方式中,所述还原剂为抗坏血酸钠。在一个实施方式中,所述三唑形成条件包括钌催化剂的存在。在一个实施方式中,所述钌催化剂是cp*rucl(pph3)。在某些实施方式中,所述三唑形成条件是无催化剂条件。
[0542]
在具体的实施方式中,化学式(i)或(ib)所示的芋螺毒素肽类似物的盐可以经受盐交换步骤以提供药物可用的盐。在一个实施方式中,例如,化学式(i)所示的芋螺毒素肽类似物的tfa盐与水溶液(ph 7.0-8.0)中的碱反应,然后与适当的酸反应以提供化学式(i)所示的芋螺毒素肽类似物的药物可用的盐。在一个实施方式中,所述碱为nh4hco3(水溶液)。在一个实施方式中,在与水溶液中的碱反应后,芋螺毒素肽类似物与乙酸反应以提供芋螺毒素肽类似物的乙酸盐。
[0543]
5.8.3.peg化
[0544]
可以将合成的芋螺毒素肽类似物进一步共价缀合至一个或多个聚乙二醇(peg)聚合物。所述芋螺毒素肽类似物可以(例如)直接或通过连接基团附接至一个或多个peg聚合物。
[0545]
在具体的实施方式中,本文提供了制备peg化的芋螺毒素肽类似物或其药物可用的盐的方法,其包括在反应条件下,使芋螺毒素肽类似物或其盐接触一种或多种反应性聚乙二醇(peg)聚合物以形成peg化的芋螺毒素肽类似物,其中所述反应性peg聚合物分别包括任选地通过连接基团共价连接至peg聚合物的反应基团,并且其中每个反应基团在所述反应条件下反应以与芋螺毒素肽类似物形成共价键,借此芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个peg聚合物。在一个实施方式中,所述芋螺毒素肽类似物是化学式(i)所示的芋螺毒素肽类似物(seq id no:93):
[0546][0547]
其中
[0548]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且x
aa2
是n-me-gly、d-tyr或者n-me-tyr;
[0549]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基;和
[0550]
其中所述芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个聚乙二醇(peg)聚合物。
[0551]
在具体的实施方式中,本文提供了制备peg化的芋螺毒素肽类似物或其药物可用的盐的方法,其包括在反应条件下,使芋螺毒素肽类似物或其盐接触一种或多种反应性聚乙二醇(peg)聚合物以形成peg化的芋螺毒素肽类似物,其中所述反应性peg聚合物分别包括任选地通过连接基团共价连接至peg聚合物的反应基团,并且其中每个反应基团在所述反应条件下反应以与芋螺毒素肽类似物形成共价键,借此芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个peg聚合物,
[0552]
其中所述芋螺毒素肽类似物是化学式(ib)所示的芋螺毒素肽类似物(seq id no:104):
[0553][0554]
其中r2为oh或nh2。
[0555]
在具体的实施方式中,本文提供了制备peg化的芋螺毒素肽类似物或其药物可用的盐的方法,其包括在反应条件下,使芋螺毒素肽类似物或其盐接触一种或多种反应性聚乙二醇(peg)聚合物以形成peg化的芋螺毒素肽类似物,其中所述反应性peg聚合物分别包括任选地通过连接基团共价连接至peg聚合物的反应基团,并且其中每个反应基团在所述反应条件下反应以与芋螺毒素肽类似物形成共价键,借此芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个peg聚合物,
[0556]
其中所述芋螺毒素肽类似物的氨基酸序列为gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-trp-gln-x
aa12-x(seq id no:106),
[0557]
其中
[0558]
x
aa3
选自(s)-炔丙基甘氨酸、(s)-叠氮基丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基高丙氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸;
[0559]
x
aa9
为瓜氨酸;
[0560]
x
aa12
选自(s)-叠氮基高丙氨酸、(s)-高炔丙基甘氨酸、(s)-叠氮基缬氨酸和(s)-双高炔丙基甘氨酸;
[0561]
其中当x
aa3
选自(s)-炔丙基甘氨酸、(s)-高炔丙基甘氨酸和(s)-双高炔丙基甘氨酸时,x
aa12
为(s)-叠氮基高丙氨酸或(s)-叠氮基缬氨酸;并且当x
aa3
选自(s)-叠氮基丙氨酸、(s)-叠氮基高丙氨酸和(s)-叠氮基缬氨酸时,x
aa12
为(s)-高炔丙基甘氨酸或者(s)-双高炔丙基甘氨酸;
[0562]
x是x
aa1
或x
aa1
x
aa2
;其中x
aa1
为tyr、phe、trp,或者tyr、phe或trp的d-异构体,并且x
aa2
是n-me-gly、d-tyr或n-me-tyr;和
[0563]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基。
[0564]
在另一个方面,本文提供了制备peg化的芋螺毒素肽类似物或其药物可用的盐的方法,其包括在反应条件下,使芋螺毒素肽类似物或其盐接触一种或多种反应性聚乙二醇(peg)聚合物以形成peg化的芋螺毒素肽类似物,其中所述反应性peg聚合物分别包括任选地通过连接基团共价连接至peg聚合物的反应基团,并且其中每个反应基团在所述反应条件下反应以与芋螺毒素肽类似物形成共价键,借此芋螺毒素肽类似物直接或通过连接基团共价连接至一个或多个peg聚合物,
[0565]
其中所述芋螺毒素肽类似物的氨基酸序列为gly-cys-x
aa3-thr-asp-pro-arg-cys-x
aa9-x
aa10-gln-x
aa12-tyr(seq id no:107),
[0566]
其中
[0567]
x
aa3
为(s)-炔丙基甘氨酸;
[0568]
x
aa9
为瓜氨酸;
[0569]
x
aa10
为3-碘-tyr;
[0570]
x
aa12
为(s)-叠氮基缬氨酸;
[0571]
其中芋螺毒素肽类似物的c-末端为羧酸或酰胺基。
[0572]
在具体的实施方式中,所述反应条件是标准peg化条件。在一个实施方式中,所述反应条件是标准酰胺形成条件。在valeur and bradley,chemical society reviews,2009,38:606-631中描述了某些标准酰胺形成条件。在一个实施方式中,所述酰胺形成条件包括偶联剂,如二环己基碳二亚胺(dcc)、1-羟基-1h-苯并三唑(hobt)、1-乙基-3-(3-二甲基氨丙基)碳二亚胺(edc)或者1-[双(二甲基氨)亚甲基]-1h-1,2,3-三唑并[4,5-b]3-氧化六氟磷酸吡啶鎓(hatu)的存在。在另一个实施方式中,所述反应条件是标准胺形成条件。在一个实施方式中,所述胺形成条件是还原胺化条件。
6.实施例
[0573]
以下非限制性实施例公开了芋螺毒素rgia的芋螺毒素肽类似物以及芋螺毒素rgia的peg化的芋螺毒素肽类似物的制备和测试。
[0574]
应理解以下实施例是说明性的且不是限制性的。
[0575]
6.1.实施例1:rgia芋螺毒素肽类似物csp-4-oh及csp-4-nh2的二硫键改组
[0576]
rgia芋螺毒素肽类似物csp-4-oh和csp-4-nh2具有氨基酸序列gly-cys-cys-thr-asp-pro-arg-cys-(cit)-(3-碘代-tyr)-gln-cys-tyr;其中csp-4-oh(seq id no:4)在c末端具有羧酸基团并且csp-4-nh2在c末端具有酰胺基团。csp-4-destyr-oh具有氨基酸序列gly-cys-cys-thr-asp-pro-arg-cys-(cit)-(3-碘代-tyr)-gln-cys(seq id no:5)其在c末端具有羧酸。
[0577]
当在人和大鼠血浆和血清中培育时,发现芋螺毒素肽类似物csp-4-oh和csp-4-nh2对二硫键改组敏感。这种二硫键重排导致形成rgia衍生物的异构体,其丧失了对α9α10nachr的活性。
[0578]
csp-4-nh2的活性构象由两个二硫键组成,一个位于cys2与cys8之间,而第二个位于cys3与cys12之间。csp-4-nh2的cys2-8、cys3-12“天然”形式对人和大鼠α9α10nachr两者均具有活性。一旦暴露于人和大鼠血清或血浆,则csp-4-nh2的天然形式的大部分经历异构化成含有替代二硫键cys2-cys12和cys3-cys8的“带状”形式和含有替代cys2-cys3和cys8-cys12二硫键的“珠粒”形式。
[0579]
在血浆和血清样品中,csp-4-nh2主要在天然形式和带状形式之间异构化,珠粒形成极少(图1a,b)。带状或珠粒形式对人或大鼠α9α10nachr均不具有活性,这表明二硫键改组有助于降低所述分子的效力。此外,相对于csp-4-oh中的c末端羧酸,csp-4-nh2中c末端酰胺的存在不会降低异构化。最后,在向sprague dawley大鼠静脉内和皮下注射1mg/kg剂量的化合物6后,还在体内发生了二硫键异构化。注射后1h,通过hplc-ms/ms分析,仅40-50%从血液回收的肽保持天然形式,这表明二硫键异构化在体内的发生类似于体外观察结果。
[0580]
通过使所述肽在来自sprague dawley大鼠和人的血清或血浆中以0.1-0.5mg/ml
的最终浓度,在37℃体外培育长达24h证实了芋螺毒素肽类似物csp-4-oh和csp-4-nh2的二硫键改组。用抗凝血剂,包括柠檬酸盐、k2edta和肝素处理血浆样品。在几个时间点除去培育的样品并且对于每个时间点,通过蛋白质沈淀(3体积的甲醇)、然后通过millipore ultrafree-mc gv离心过滤器以10,000
×
g使沉淀样品离心,从基质提取所产生的肽异构体。回收所产生的澄清样品,并在装有phenomenex aeris c-18柱(2.1
×
150mm,3.6μm)的agilent 1260infinity hplc上进样5μl。通过利用在45min内,0%至50%b,以0.3ml/min梯度洗脱将肽分离;流动相a(19:1:0.01h2o/ch3cn/tfa)和流动相b(具有0.05%tfa的ch3cn)。在这些条件下,csp-4-nh2的多种异构体的相对保留时间如下所示:带状<珠粒<天然(图1b)。
[0581]
利用氧化型谷胱甘肽和还原型谷胱甘肽的1:1混合物(各10mm)处理csp-4-nh2(40μg/ml)1h,然后利用8%的甲酸处理(淬灭),从而导致形成了与在血清或血浆中所观察到的产物具有相同质量和色谱保留时间的带状异构体,这表明二硫键异构化介导了肽在生物基质中的不稳定性(图1d)。谷胱甘肽还原导致产生了天然和带状形式的混合物。
[0582]
在如上所述的每个hplc峰的分离、收集和冷冻干燥后,使用orbitrap elite上的lc-ms分析来确定每个csp-4-oh和csp-4-nh2异构体的属性(identity)(图1c)。将非还原样品的等份在水:乙腈:甲酸(98:2:0.1%)中1:100稀释至1.2-1.5pmol/μl的估计浓度。通过easy-nlc ii hplc系统(thermo scientific)将10μl进样至与2cm长、100μm i.d.integrafrit
tm
阱(new objective)偶联的75μm i.d.picotip
tm 25cm长熔融石英纳米柱(new objective)上。将所述柱和阱配置为开放构造(licklider等人,analytical chemistry,2002,74,3076-3082),其中所述柱装填有5μm大小的magic c18 aq反相介质(孔径,michrom bioresources,auburn,ca)并且所述阱装填有相同材料(孔径,michrom)。使用由流动相a[超纯级水/甲酸(0.1体积%)]和流动相b[乙腈/甲酸(0.1体积%)]组成的梯度以400nl/min的流速根据以下条件在所述柱上分离样品:以95%“a”和5%“b”开始,0至2分钟,此时流动相“b”自5%升至7%,然后7%“b”经60分钟升至35%“b”,然后35%“b”经2分钟升至50%“b”,此时将“b”保持1分钟,然后50%“b”经5分钟升至90%“b”并保持8分钟,并且最后是经1分钟使“b”降回至5%的一段时间以重新平衡至起始条件。质谱仪是以数据依赖模式在400-1800m/z的范围内运行的。对于仪器的每个循环,从前体扫描(precursor scan)选择前3个丰度最高的离子(其中以轮廓模式,将轨道阱(orbitrap)分辨率设置为120k)。使用与如上所列相同的设置以质心模式采集ms/ms数据,除了将分离宽度设置为2.0m/z以外。所使用的动态排除设置如下:重复计数为1,计数持续时间为15秒,排除列表大小为500且排除持续时间为30秒。如使用质谱所确定的,天然和条带异构体具有相同的质荷比,这表明两个hplc峰具有相同属性(图1c)。
[0583]
据发现分离的csp-4-nh2的带状异构体对人α9α10nachr不具有阻断活性。如以上所描述的,将csp-4-nh2在人血清中培育1小时,然后进行制备hplc并收集对应于带状异构体的峰。还利用cys2-cys12和cys3-cys8二硫键连结性来化学合成带状异构体。使用双电极电压钳电生理学来测试化学合成的带状异构体和在人血清中培育后分离的异构体对人α9α10nachr的活性。
[0584]
测量每种类似物在非洲蟾蜍(xenopus)卵母细胞中阻断乙酰胆碱-引起的α9α10nachr电流的能力。如表1所示,浓度100nm的天然csp-4-nh2阻断>99%的ach-引起的电
cit-trp(boc)-gln(trt)-5-叠氮基-nva-tyr(tbu)-o-(2-氯三苯甲基)在聚苯乙烯载体上的固相肽合成(spps)(2):将负载了fmoc-tyr(otbu)的2-氯三苯甲基树脂(1,17.3g,5mmol)用dmf(100ml)清洗,然后完全排液。通过用1:4的哌啶/dmf处理(2
×
100ml,每次15min),从连接的tyr基团除去fmoc基团,然后用dmf(6
×
100ml)清洗树脂。然后,添加在dmf(100ml)中的hatu(3.80g,10mmol)、hoat(1.35g,10mmol)和dipea(2.5ml,15mmol)以及fmoc-5-叠氮基-nva-oh(cas#1097192-04-5,3.80g,10mmol)。将反应容器振荡至少2.5h,随后用dmf(6
×
100ml)清洗。通过茚三酮测试确定反应完成性。如果为阴性(无色),则认为偶联完成并继续合成。如果为阳性(蓝色),则使用如上所述的树脂和hatu/hoat(10mmol/10mmol)偶联dmf(100ml)中的第二当量的相同fmoc-氨基酸(10mmol)。一旦茚三酮测试表明反应完成,则从每个顺序添加的氨基酸除去fmoc,然后在如上所述的肽序列中顺序偶联fmoc-氨基酸-oh。使用下列物质,按以下顺序来顺序进行:fmoc-gln(trt)-oh(cas#132327-80-1,6.1g,10mmol)、fmoc-trp(boc)-oh(cas#143824-78-6,5.2g,10mmol)、fmoc-cit-oh(cas#133174-15-9,3.9g,10mmol)、fmoc-cys(trt)-oh(cas#103213-32-7,5.8g,10mmol)、fmoc-arg(pbf)-oh(cas#154445-77-9,6.4g,10mmol)、fmoc-pro-oh(cas#71989-31-6,3.3g,10mmol)、fmoc-asp(otbu)-oh(cas#71989-14-5,4.1g,10mmol)、fmoc-thr(tbu)-oh(cas#71989-35-0,3.9g,10mmol)、fmoc-pra-oh(cas#198561-07-8,3.3g,10mmol)、fmoc-cys(trt)-oh(5.8g,10mmol)和fmoc-gly-oh(cas#29022-11-5,2.9g,10mmol)。在直链肽偶联完成后,将树脂用dmf(100ml
×
6)清洗,随后用meoh(100ml
×
2)并最终用et2o(100ml
×
2)清洗,然后真空干燥2h。
[0594]
氨基酸序列h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-tyr-oh(3)(seq id no:7)的树脂切割:向烧瓶中的干燥树脂(2,28.0g,5.0mmol)中添加230ml切割溶液(tfa/edt/苯硫基甲烷/苯甲醚:90:3:5:2),并将混合物在室温下振荡2h。在此之后,过滤树脂并用tfa(2
×
50ml)清洗。合并滤液,并加入10-倍体积的冷(0℃)et2o,这导致肽沉淀。将沉淀的肽以5,000rpm离心10min,并用冷(0℃)et2o(3
×
50ml)清洗。将粗产物真空干燥2h以获得3(6.8g,4.2mmol,84%),其在下一步使用时未进一步纯化。
[0595]
半胱氨酸二硫键形成以产生h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-tyr-oh,(cys2
→
cys8)二硫键(4)(seq id no:8):将肽3(2.0g,1.2mmol)溶于ch3cn(100ml)、dmso(100ml)和h2o(1800ml)。然后,滴加h2o2(30%在h2o中,0.25ml)并在室温下搅拌该混合物1.5h。在此之后,过滤混合物,并通过hplc方法j纯化滤液以提供800mg白色固体状的标题化合物4(得率:38%,tfa盐)。lc-ms(esi)m/z:540.7[m+3h]/3
+
,810.3[m+2h]/2
+
,纯度95%(214nm)。将剩余4.8g的3分成两批,并且如所述的氧化和纯化以获得总计2.5g的4(总得率:35%)。
[0596]
1,3-偶极环化/点击反应(三唑桥形成)以生产芋螺毒素肽类似物ia:将肽4(400mg,0.25mmol)溶于iproh(100ml)和h2o(300ml)。然后,添加cuso4(157mg,1mmol)在h2o(2ml)中的溶液,随后滴加l-抗坏血酸(176mg,1mmol)在h2o(2ml)中的溶液。将混合物在室温下搅拌2h。然后,将溶液直接加载到快速色谱塔(例如,snap ultra c18,120g)上并用水(0.1%tfa)和ch3cn洗脱。合并含有芋螺毒素肽类似物ia的洗脱液部分并冻干以获得305mg白色固体状的芋螺毒素肽类似物ia的tfa盐(305mg,tfa盐,得率:69%)。lc-ms(esi)m/z:540.7[m+3h]/3
+
,810.3[m+2h]/2
+
,纯度90%(214nm)。将剩余2.1g的4分成3批,并
分别用如上所述的条件处理,从而提供了1.7g标题芋螺毒素肽类似物ia(整体合并得率:61%,tfa盐)。
[0597]
将所获得的芋螺毒素肽类似物ia的tfa盐(1.0g)溶于h2o(20ml)和ch3cn(2ml)。然后,滴加20mm nh4hco3的(水)溶液以调节ph 7.0-8.0。然后,使用hplc方法h纯化混合物。将含有产物的部分冻干以提供白色固体状的芋螺毒素肽类似物ia的乙酸盐(650mg,乙酸盐,总得率:62%)。以相同方式,将剩余700mg芋螺毒素肽类似物ia-tfa盐纯化并转化为乙酸盐以提供350mg(48%,乙酸盐)。所得的整体合并的量为1.0g的芋螺毒素肽类似物ia的乙酸盐(56%)。lc-ms(esi-tof)m/z:540.2[m+3h]/3
+
,810.0[m+2h]/2
+
,1617.66[m+h]/
+
;hplc方法a;保留时间:10.1min;纯度95.7%。
[0598]
方案1中显示了芋螺毒素肽类似物ia的合成。
[0599][0600]
step:步骤;repeated for each amino acid:对每个氨基酸重复
[0601]
实施例1.2芋螺毒素肽类似物ia’(l-酪氨酰胺,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:9):
[0602][0603]
中间体芋螺毒素肽类似物ya’(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-tyr-nh2)(seq id no:10):通过使用rink amide树脂mfcd00677976代替2-氯三苯甲基氯树脂mfcd00040399,使用对化合物3所述的相同程序合成了中间体芋螺毒素肽类似物ya'。
[0604]
中间体芋螺毒素肽类似物za’(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-tyr-nh2,(cys2
→
cys8)二硫键)(seq id no:11):通过使用中间体芋螺毒素肽类似物ya'代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物za'。
[0605]
通过使用芋螺毒素肽类似物za'代替化合物4,使用对芋螺毒素肽类似物ia'所述的相同程序合成了芋螺毒素肽类似物ia'。lc-ms(单四级杆esi)m/z:1617.5(m+1h)/
+
(计算mw:1616.5);hplc方法e;保留时间:14.0min;纯度96.9%。
[0606]
实施例1.3芋螺毒素肽类似物ib(l-酪氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-3-碘代酪氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:12):
[0607][0608]
中间体芋螺毒素肽类似物yb(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-3-i-tyr-gln-5-叠氮基nva-tyr-oh)(seq id no:13):通过在10-位残基的肽合成中,使用fmoc-3-i-tyr-oh代替fmoc-trp(boc)-oh,使用对化合物3所述的相同程序合成了中间体芋螺毒素肽类似物yb。
[0609]
中间体芋螺毒素肽类似物zb(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-3-i-tyr-gln-5-叠氮基nva-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:14):通过使用中间体芋螺毒素肽类似物yb代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zb。
cit-3-i-tyr-gln-cys-tyr-nh2)(seq id no:19):通过在固相肽合成中使用fmoc-cys(trt)-oh代替fmoc-5-叠氮基-nva-oh(12-位残基),fmoc-5-叠氮基-nva-oh代替fmoc-cys(trt)-oh(8-位残基),fmoc-cys(trt)-oh代替fmoc-pra-oh(3-位残基)和fmoc-pra-oh代替fmoc-cys(trt)-oh(2-位残基),使用对中间体芋螺毒素肽类似物yb'所述的相同程序合成了中间体芋螺毒素肽类似物yc。
[0619]
中间体芋螺毒素肽类似物zc(h-gly-pra-cys-thr-asp-pro-arg-5-叠氮基nva-cit-3-i-tyr-gln-cys-tyr-nh2,(cys3
→
cys12)二硫键)(seq id no:20):通过使用中间体芋螺毒素肽类似物yc代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zc。
[0620]
通过使用中间体芋螺毒素肽类似物zc代替中间体芋螺毒素肽类似物zb',使用对芋螺毒素肽类似物ib'所述的相同程序合成了芋螺毒素肽类似物ic。lc-ms(esi-tof)m/z:574.2[m+3h]/3
+
,860.7[m+2h]/2
+
(计算mw:1719.55);hplc方法b;保留时间:10.2min;纯度98.3%。
[0621]
实施例1.5芋螺毒素肽类似物id(l-酪氨酰胺,甘氨酰基-l-正缬氨酰基-l-半胱氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-丙氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-3-碘代酪氨酰基-l-谷氨酰胺酰基-l-半胱氨酰基-环25,8
3-(1h-1,2,3-三唑-1,4-二基)-环-(3
→
12)-二硫化物)(seq id no:21):
[0622][0623]
中间体芋螺毒素肽类似物yd(h-gly-5
‑ꢀ
叠氮基nva-cys-thr-asp-pro-arg-pra-cit-3-i-tyr-gln-cys-tyr-nh2)(seq id no:22):通过在固相肽合成中使用fmoc-cys(trt)-oh代替fmoc-5-叠氮基-nva-oh(12-位残基),fmoc-pra-oh代替fmoc-cys(trt)-oh(8-位残基),fmoc-cys(trt)-oh代替fmoc-pra-oh(3-位残基)和fmoc-5-叠氮基-nva-oh代替fmoc-cys(trt)-oh(2-位残基),使用对中间体芋螺毒素肽类似物yb'所述的相同程序合成了中间体芋螺毒素肽类似物yd。
[0624]
中间体芋螺毒素肽类似物zd(h-gly-5-叠氮基nva-cys-thr-asp-pro-arg-pra-cit-3-i-tyr-gln-cys-tyr-nh2,(cys3
→
cys12)二硫键)(seq id no:23):通过使用中间体芋螺毒素肽类似物yd代替中间体芋螺毒素肽类似物yb',使用对中间体芋螺毒素肽类似物zb'所述的相同程序合成了中间体芋螺毒素肽类似物zd。
[0625]
通过使用中间体芋螺毒素肽类似物zd代替中间体芋螺毒素肽类似物zb',使用对芋螺毒素肽类似物ib'所述的相同程序合成了芋螺毒素肽类似物id。lc-ms(esi-tof)m/z:860.7[m+2h]/2
+
(计算mw:1719.55);hplc方法b;保留时间:10.2min;纯度99.2%。
[0626]
实施例1.6芋螺毒素肽类似物ie(l-酪氨酰胺,甘氨酰基-l-半胱氨酰基-l-正缬氨
酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-3-碘代酪氨酰基-l-谷氨酰胺酰基-l-丙氨酰基-环(2
→
8)-二硫化物-环35,12
3-(1h-1,2,3-三唑-1,4-二基))(seq id no:24):
[0627][0628]
中间体芋螺毒素肽类似物ye(h-gly-cys-5-叠氮基nva-thr-asp-pro-arg-cys-cit-3-i-tyr-gln-pra-tyr-nh2)(seq id no:25):通过在固相肽合成中使用fmoc-pra-oh代替fmoc-5-叠氮基-nva-oh(12-位残基)并且使用fmoc-5-叠氮基-nva-oh代替fmoc-pra-oh(3-位残基),使用对中间体芋螺毒素肽类似物yb'所述的相同程序,合成了中间体芋螺毒素肽类似物ye。
[0629]
中间体芋螺毒素肽类似物ze(h-gly-cys-5-叠氮基nva-thr-asp-pro-arg-cys-cit-3-i-tyr-gln-pra-tyr-nh2,(cys2
→
cys8)二硫键)(seq id no:26):通过使用中间体芋螺毒素肽类似物ye代替中间体芋螺毒素肽类似物yb',使用对中间体芋螺毒素肽类似物zb'所述的相同程序合成了中间体芋螺毒素肽类似物ze。
[0630]
通过使用中间体芋螺毒素肽类似物ze代替中间体芋螺毒素肽类似物zb',使用对芋螺毒素肽类似物ib'所述的相同程序合成了芋螺毒素肽类似物ie。lc-ms(esi-tof)m/z:574.4[m+3h]/3
+
,861.1[m+2h]/2
+
(计算mw:1719.55);hplc方法c;保留时间:12.6min;纯度92.1%。
[0631]
实施例1.7芋螺毒素肽类似物if(l-酪氨酰胺,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-3-碘代酪氨酰基-l-谷氨酰胺酰基-l-丙氨酰基-环(2
→
8)-二硫化物-环33,12
3-(1h-1,2,3-三唑-4,1-二基))(seq id no:27):
[0632]
二硫化物-环34,12
4-(1h-1,2,3-三唑-4,1-二基))(seq id no:33):
[0642][0643]
中间体芋螺毒素肽类似物yh(h-gly-cys-高pra-thr-asp-pro-arg-cys-cit-trp-gln-叠氮基高ala-tyr-oh)(seq id no:34):通过在固相肽合成中使用fmoc-高炔丙基甘氨酸代替fmoc-pra-oh(3-位残基)并且使用fmoc-γ-叠氮基-高丙氨酸代替fmoc-5-叠氮基-nva-oh(12-位残基),使用对化合物3所述的相同程序,合成了中间体芋螺毒素肽类似物yh。
[0644]
中间体芋螺毒素肽类似物zh(h-gly-cys-高pra-thr-asp-pro-arg-cys-cit-trp-gln-叠氮基高ala-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:35):通过使用中间体芋螺毒素肽类似物yh代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zh。
[0645]
通过使用中间体芋螺毒素肽类似物zh代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物ih。lc-ms(单四级杆esi)m/z:540.6[m+3h]/3
+
,809.9[m+2h]/2
+
(计算mw:1617.66);hplc方法a;保留时间:12.4min;纯度83.9%。
[0646]
实施例1.10芋螺毒素肽类似物ii(l-酪氨酸,甘氨酰基-l-半胱氨酰基-(2s)-2-氨基丁酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-(2s)-2-氨基丁酰基-环(2
→
8)-二硫化物-环34,12
4-(1h-1,2,3-三唑-1,4-二基))(seq id no:36):
[0647][0648]
中间体芋螺毒素肽类似物yi(h-gly-cys-叠氮基高ala-thr-asp-pro-arg-cys-cit-trp-gln-高pra-tyr-oh)(seq id no:37):通过在固相肽合成中使用fmoc-γ-叠氮基-高丙氨酸代替fmoc-pra-oh(3-位残基)并且使用fmoc-高炔丙基甘氨酸代替fmoc-5-叠氮基-nva-oh(12-位残基),使用对化合物3所述的相同程序,合成了中间体芋螺毒素肽类似物yi。
[0649]
中间体芋螺毒素肽类似物zi(h-gly-cys-叠氮基高ala-thr-asp-pro-arg-cys-cit-trp-gln-高pra-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:38):通过使用中间体芋螺毒素肽类似物yi代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zi。
[0650]
通过使用中间体芋螺毒素肽类似物zi代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物ii。lc-ms(单四级杆esi)m/z:540.7[m+3h]/3
+
,810.5[m+2h]/2
+
(计算mw:1617.66);hplc方法a;保留时间:12.3min;纯度85.8%。
[0651]
实施例1.11芋螺毒素肽类似物ij(l-酪氨酸,甘氨酰基-l-半胱氨酰基-(2s)-2-氨基戊酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-3-碘代酪氨酰基-l-谷氨酰胺酰基-l-丙氨酰基-环(2
→
8)-二硫化物-环35,12
3-(1h-1,2,3-三唑-4,1-二基))(seq id no:39):
[0652][0653]
中间体芋螺毒素肽类似物yj(h-gly-cys-双高pra-thr-asp-pro-arg-cys-cit-trp-gln-3-叠氮基ala-tyr-oh)(seq id no:40):通过在固相肽合成中使用fmoc-双-高炔丙基甘氨酸代替fmoc-pra-oh(3-位残基)并且使用fmoc-3-叠氮基-ala-oh代替fmoc-5-叠氮基-nva-oh(12-位残基),使用对化合物3所述的相同程序,合成了中间体芋螺毒素肽类似物yj。
[0654]
中间体芋螺毒素肽类似物zj(h-gly-cys-双高pra-thr-asp-pro-arg-cys-cit-trp-gln-3-叠氮基ala-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:41):通过使用中间体芋螺毒素肽类似物yj代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zj。
[0655]
通过使用中间体芋螺毒素肽类似物zj代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物ij。lc-ms(单四级杆esi)m/z:540.5[m+3h]/3
+
,810.1[m+2h]/2
+
(计算mw:1617.66);hplc方法a;保留时间:12.04min;纯度97.6%。
[0656]
实施例1.12芋螺毒素肽类似物ik(l-酪氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-(2s)-2-氨基戊酰基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-1,4-二基))(seq id no:42):
[0657][0658]
中间体芋螺毒素肽类似物yk(h-gly-cys-3-叠氮基ala-thr-asp-pro-arg-cys-cit-trp-gln-双高pra-tyr-oh)(seq id no:43):通过在固相肽合成中使用fmoc-3-叠氮基-ala-oh代替fmoc-pra-oh(3-位残基)并且使用fmoc-双-高炔丙基甘氨酸代替fmoc-5-叠氮基-nva-oh(12-位残基),使用对化合物3所述的相同程序,合成了中间体芋螺毒素肽类似物yk。
[0659]
中间体芋螺毒素肽类似物zk(h-gly-cys-3-叠氮基ala-thr-asp-pro-arg-cys-cit-trp-gln-双高pra-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:44):通过使用中间体芋螺毒素肽类似物yk代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zk。
[0660]
通过使用中间体芋螺毒素肽类似物zk代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物ik。lc-ms(单四级杆esi)m/z:540.6[m+3h]/3
+
,810.0[m+2h]/2
+
(计算mw:1617.66);hplc方法a;保留时间:12.24min;纯度97.6%。
[0661]
实施例1.13芋螺毒素肽类似物il(l-苯丙氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:45):
[0662][0663]
2-氯三苯甲基树脂负载的fmoc-phe(otbu)-oh(5):通过使用fmoc-phe(otbu)-oh代替fmoc-tyr(otbu)-oh,使用对2-氯三苯甲基树脂1所述的相同程序,合成了2-氯三苯甲基树脂负载的fmoc-phe(otbu)-oh。
[0664]
中间体芋螺毒素肽类似物yl(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-phe-oh)(seq id no:46):通过在固相肽合成中使用fmoc-phe(otbu)-oh-负载的2-氯三苯甲基树脂负载的fmoc-phe(otbu)-oh(5)代替fmoc-tyr(otbu)-负载的2-氯三苯甲基树脂(1)作为c-末端起点,使用对化合物3所述的相同程序合成了中间体芋螺
毒素肽类似物yl。
[0665]
中间体芋螺毒素肽类似物zl(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-phe-oh,(cys2
→
cys8)二硫键)(seq id no:47):通过使用中间体芋螺毒素肽类似物yl代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zl。
[0666]
通过使用中间体芋螺毒素肽类似物zl代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物il。lc-ms(单四级杆esi)m/z:535.2[m+3h]/3
+
,802.2[m+2h]/2
+
(计算mw:1601.66);hplc方法a;保留时间:13.47min;纯度95.6%。
[0667]
实施例1.14芋螺毒素肽类似物im(d-酪氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:48):
[0668][0669]
2-氯三苯甲基树脂负载的fmoc-d-tyr(otbu)-oh(6):通过使用fmoc-d-tyr(otbu)-oh代替fmoc-tyr(otbu)-oh,使用对2-氯三苯甲基树脂1所述的相同程序,合成了2-氯三苯甲基树脂负载的fmoc-d-tyr(otbu)-oh。
[0670]
中间体芋螺毒素肽类似物ym(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-d-tyr-oh)(seq id no:49):通过在固相肽合成中使用fmoc-d-tyr(otbu)-oh-负载的2-氯三苯甲基树脂(6)代替fmoc-tyr(otbu)-负载的2-氯三苯甲基树脂(1)作为c-末端起点,使用对化合物3所述的相同程序合成了中间体芋螺毒素肽类似物ym。
[0671]
中间体芋螺毒素肽类似物zm(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-d-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:50):通过使用中间体芋螺毒素肽类似物ym代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zm。
[0672]
通过使用中间体芋螺毒素肽类似物zm代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物im。lc-ms(单四级杆esi)m/z:540.6[m+3h]/3
+
,810.0[m+2h]/2
+
(计算mw:1617.66);hplc方法a;保留时间:12.07min;纯度86.6%。
[0673]
实施例1.15芋螺毒素肽类似物in(甘氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-l-酪氨酰-n-甲基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:51):
gln-5-叠氮基nva-tyr-d-tyr-oh)(seq id no:55):通过使用fmoc-d-tyr(otbu)-oh-负载的2-氯三苯甲基树脂,使用对化合物3所述的相同程序以顺序添加氨基酸,从而合成了中间体芋螺毒素肽类似物yo,合成按以下顺序进行:fmoc-tyr(otbu)-oh、fmoc-5-叠氮基-nva-oh、fmoc-gln(trt)-oh、fmoc-trp(boc)-oh、fmoc-cit-oh、fmoc-cys(trt)-oh、fmoc-arg(pbf)-oh、fmoc-pro-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-oh、fmoc-pra-oh、fmoc-cys(trt)-oh和fmoc-gly-oh。
[0682]
中间体芋螺毒素肽类似物zo(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-tyr-d-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:56):通过使用中间体芋螺毒素肽类似物yo代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zo。
[0683]
通过使用中间体芋螺毒素肽类似物zo代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物io。lc-ms(单四级杆esi)m/z:595.0[m+3h]/3
+
,891.7[m+2h]/2
+
(计算mw:1780.72);hplc方法a;保留时间:12.43min;纯度97.4%。
[0684]
实施例1.17芋螺毒素肽类似物ip(l-酪氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-l-酪氨酰-n-甲基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:57):
[0685][0686]
2-氯三苯甲基树脂负载的fmoc-n-me-tyr-oh(8):通过使用fmoc-n-me-tyr-oh代替fmoc-tyr(otbu)-oh,使用对2-氯三苯甲基树脂1所述的相同程序,合成了2-氯三苯甲基树脂负载的fmoc-n-me-tyr-oh。
[0687]
中间体芋螺毒素肽类似物yp(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-tyr-n-me-tyr-oh)(seq id no:58):通过使用fmoc-n-me-tyr-oh-负载的2-氯三苯甲基树脂(8),使用对化合物3所述的相同程序以顺序添加氨基酸,从而合成了中间体芋螺毒素肽类似物yp,合成按以下顺序进行:fmoc-tyr(otbu)-oh、fmoc-5-叠氮基-nva-oh、fmoc-gln(trt)-oh、fmoc-trp(boc)-oh、fmoc-cit-oh、fmoc-cys(trt)-oh、fmoc-arg(pbf)-oh、fmoc-pro-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-oh、fmoc-pra-oh、fmoc-cys(trt)-oh和fmoc-gly-oh。
[0688]
中间体芋螺毒素肽类似物zp(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-tyr-n-me-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:59):通过使用中间体芋螺毒素肽类似物yp代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zp。
[0689]
通过使用中间体芋螺毒素肽类似物zp代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物ip。lc-ms(单四级杆esi)m/z:599.7[m+3h]/3
+
,898.7[m+2h]/2
+
(计算mw:1794.74);hplc方法a;保留时间:12.56min;纯度95.5%。
[0690]
实施例1.18芋螺毒素肽类似物iq(l-缬氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:60):
[0691][0692]
2-氯三苯甲基树脂负载的fmoc-5-叠氮基-nva-oh(9):通过使用fmoc-5-叠氮基-nva-oh代替fmoc-tyr(otbu)-oh,使用对2-氯三苯甲基树脂1所述的相同程序,合成了2-氯三苯甲基树脂负载的fmoc-5-叠氮基-nva-oh。
[0693]
中间体芋螺毒素肽类似物yq(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-oh)(seq id no:61):通过使用fmoc-5-叠氮基-nva-oh-负载的2-氯三苯甲基树脂(9),使用对化合物3所述的相同程序以顺序添加氨基酸,从而合成了中间体芋螺毒素肽类似物yq,合成按以下顺序进行:fmoc-gln(trt)-oh、fmoc-trp(boc)-oh、fmoc-cit-oh、fmoc-cys(trt)-oh、fmoc-arg(pbf)-oh、fmoc-pro-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-oh、fmoc-pra-oh、fmoc-cys(trt)-oh和fmoc-gly-oh。
[0694]
中间体芋螺毒素肽类似物zq(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-oh,(cys2
→
cys8)二硫键)(seq id no:62):通过使用中间体芋螺毒素肽类似物yq代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zq。
[0695]
通过使用中间体芋螺毒素肽类似物zq代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物iq。lc-ms(esi-tof)m/z:1455.5[m+1h]/
+
(计算mw:1454.59);hplc方法a;保留时间:11.4min;纯度95.0%。
[0696]
实施例1.19芋螺毒素肽类似物ir(l-酪氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-n-甲基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:63):
l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:72):
[0714][0715]
2-氯三苯甲基树脂负载的fmoc-β-tyr-oh(12):通过使用fmoc-β-tyr-oh代替fmoc-tyr(otbu)-oh,使用对2-氯三苯甲基树脂1所述的相同程序,合成了2-氯三苯甲基树脂负载的fmoc-β-tyr-oh。
[0716]
中间体芋螺毒素肽类似物yu(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-β-tyr-oh)(seq id no:73):通过使用fmoc-β-tyr-oh-负载的2-氯三苯甲基树脂(12),使用对化合物3所述的相同程序以顺序添加氨基酸,从而合成了中间体芋螺毒素肽类似物yu,合成按以下顺序进行:fmoc-5-叠氮基-nva-oh、fmoc-gln(trt)-oh、fmoc-trp(boc)-oh、fmoc-cit-oh、fmoc-cys(trt)-oh、fmoc-arg(pbf)-oh、fmoc-pro-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-oh、fmoc-pra-oh、fmoc-cys(trt)-oh和fmoc-gly-oh。
[0717]
中间体芋螺毒素肽类似物zu(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-β-tyr-oh,(cys2
→
cys8)二硫键)(seq id no:74):通过使用中间体芋螺毒素肽类似物yu代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zu。
[0718]
通过使用中间体芋螺毒素肽类似物zu代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物iu。lc-ms(单四级杆esi)m/z:544.5[m+3h]/3
+
,816.3[m+2h]/2
+
(计算mw:1631.67);hplc方法a;保留时间:10.28min;纯度98.8%。
[0719]
实施例1.23芋螺毒素肽类似物iv(l-精氨酸,甘氨酰基-l-半胱氨酰基-l-丙氨酰基-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-色氨酰基-l-谷氨酰胺酰基-l-正缬氨酰基-n-甲基-环(2
→
8)-二硫化物-环33,12
5-(1h-1,2,3-三唑-4,1-二基))(seq id no:75):
[0720]
[0721]
2-氯三苯甲基树脂负载的fmoc-n-me-arg-oh(13):通过使用fmoc-n-me-arg-oh代替fmoc-tyr(otbu)-oh,使用对2-氯三苯甲基树脂1所述的相同程序,合成了2-氯三苯甲基树脂负载的fmoc-n-me-arg-oh。
[0722]
中间体芋螺毒素肽类似物yv(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-n-me-arg-oh)(seq id no:76):通过使用fmoc-n-me-arg-oh-负载的2-氯三苯甲基树脂(13),使用对化合物3所述的相同程序以顺序添加氨基酸,从而合成了中间体芋螺毒素肽类似物yv,合成按以下顺序进行:fmoc-5-叠氮基-nva-oh、fmoc-gln(trt)-oh、fmoc-trp(boc)-oh、fmoc-cit-oh、fmoc-cys(trt)-oh、fmoc-arg(pbf)-oh、fmoc-pro-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-oh、fmoc-pra-oh、fmoc-cys(trt)-oh和fmoc-gly-oh。
[0723]
中间体芋螺毒素肽类似物zv(h-gly-cys-pra-thr-asp-pro-arg-cys-cit-trp-gln-5-叠氮基nva-n-me-arg-oh,(cys2
→
cys8)二硫键)(seq id no:77):通过使用中间体芋螺毒素肽类似物yv代替化合物3,使用对化合物4所述的相同程序合成了中间体芋螺毒素肽类似物zv。
[0724]
通过使用中间体芋螺毒素肽类似物zv代替化合物4,使用对芋螺毒素肽类似物ia所述的相同程序合成了芋螺毒素肽类似物iv。lc-ms(单四级杆esi)m/z:542.9[m+3h]/3
+
,813.5[m+2h]/2
+
(计算mw:1624.71);hplc方法a;保留时间:9.29min;纯度95.9%。
[0725]
实施例1.24芋螺毒素肽类似物iw(l-酪氨酰胺,甘氨酰基-l-半胱氨酰基-l-谷氨酰-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-3-碘代酪氨酰基-l-谷氨酰胺酰基-l-赖氨酰-环(2
→
8)-二硫化物-环-(3
→
12)-内酰胺)(seq id no:78):
[0726][0727]
直链肽中间体(x1)(seq id no:79)的合成:用dmf(10ml)清洗fmoc-tyr(otbu)-负载的rink酰胺mbha树脂(1.7g,0.5mmol),然后完全排干。通过用1:4的哌啶/dmf处理(2
×
10ml,每次15min),从连接的tyr基团除去fmoc基团,然后用dmf(6
×
10ml)清洗树脂。然后,将hatu(cas#148893-10-1,0.38g,1mmol)、hoat(cas#39968-33-7,0.14g,1mmol)和dipea(0.25ml,1.5mmol)与fmoc-lys(ivdde)-oh(cas#204777-78-6,0.57g,1mmol)一起添加到dmf(10ml)中。将反应容器振荡至少2.5h,随后用dmf(6
×
10ml)清洗。通过茚三酮测试确定反应完成性。如果为阴性(无色),则认为偶联完成并继续合成。如果为阳性(蓝色),则使用如上所述的树脂和hatu/hoat(1mmol/1mmol)偶联dmf(10ml)中的第二当量的相同fmoc-氨基酸(1mmol)。一旦茚三酮测试表明反应完成,则从每个顺序添加的氨基酸除去fmoc,然后
在如上所述的肽序列中顺序偶联fmoc-氨基酸-oh。使用下列物质,按以下顺序来顺序进行:fmoc-gln(trt)-oh(cas#132327-80-1,0.61g,1mmol)、fmoc-(3-i-tyr)-oh(cas#134486-00-3,0.53g,1mmol)、fmoc-cit-oh(cas#133174-15-9,0.39g,1mmol)、fmoc-cys(trt)-oh(cas#103213-32-7,0.58g,1mmol)、fmoc-arg(pbf)-oh(cas#154445-77-9,0.64g,1mmol)、fmoc-pro-oh(cas#71989-31-6,0.33g,1mmol)、fmoc-asp(otbu)-oh(cas#71989-14-5,0.41g,1mmol)、fmoc-thr(tbu)-oh(cas#71989-35-0,0.39g,1mmol)、fmoc-glu(odmab)(cas#268730-86-5,0.68g,1mmol)、fmoc-cys(trt)-oh(0.58g,1mmol)和fmoc-gly-oh(cas#29022-11-5,0.29g,1mmol)。在直链肽偶联完成后,将树脂用dmf(10ml
×
6)清洗,随后用meoh(10ml
×
2)并最终用et2o(10ml
×
2)清洗,然后真空干燥2h。
[0728][0729]
内酰胺形成以在树脂上产生中间体x2(seq id no:80):为了从lys12及glu3残基分别除去ivdde和odmab保护基,用dmf(10ml)洗涤肽树脂,然后完全排干,然后将树脂与2%水合肼一起在dmf(10ml)中在室温下培育1h。随后用dmf(6
×
10ml)清洗树脂,然后再混悬于dmf(10ml)中,然后利用hatu(0.38g,1mmol)、hoat(0.14g,1mmol)和dipea(0.25ml,1.5mmol)进行处理。将反应容器振荡至少2.5h,然后用dmf(6
×
10ml)清洗,然后用meoh(10ml
×
2)并最终用et2o(10ml
×
2)清洗,然后真空干燥2h。
[0730][0731]
从树脂切割以提供中间体x3(seq id no:81):通过将中间体x2在23ml切割溶液(tfa/edt/苯硫基甲烷/苯甲醚:30:3:5:2)中培育使内酰胺从树脂上切割,并将混合物在室温下振荡2h。在此之后,过滤树脂并用tfa(2
×
5ml)清洗。合并滤液,并加入10-倍体积的冷(0℃)et2o,这导致肽沉淀。将沉淀的肽以5,000rpm离心10min,并用冷(0℃)et2o(3
×
5ml)清
洗。将粗产物x3真空干燥2h以获得粗单环3
→
12内酰胺肽中间体(x3,mw=1727.7g/mol,0.4g,0.23mmol,46%),其使用时未进一步纯化。
[0732][0733]
二硫键形成以提供芋螺毒素肽类似物iw:将中间体x3(0.4g,0.23mmol)溶于ch3cn(10ml)、dmso(10ml)和h2o(180ml)。然后,滴加h2o2(30%在h2o中,25μl)并在室温下搅拌该混合物1.5h。在此之后,过滤混合物,并通过hplc方法j纯化滤液以提供50mg白色固体状的芋螺毒素肽类似物iw(mw=1725.6g/mol,29μmol,该步得率:12.6%,tfa盐)。纯度82%(230nm)。
[0734]
根据对于芋螺毒素肽类似物ia所述的方法,通过制备hplc在将tfa阴离子交换为乙酸盐的同时进一步纯化所述肽。芋螺毒素肽类似物iw(乙酸盐)的分离得率为20mg(12μmol,总得率2.4%)。lc-ms(单四级杆esi)m/z:576.1[m+3h]/3
+
,863.5[m+2h]/2
+
,(计算mw:1723.56);hplc方法k;保留时间:7.0min;纯度97%。
[0735]
实施例1.25芋螺毒素肽类似物ix(l-酪氨酰胺,甘氨酰基-l-半胱氨酰基-l-赖氨酰-l-苏氨酰基-l-α-天门冬氨酰基-l-脯氨酰基-l-精氨酰基-l-半胱氨酰基-n5-(氨甲酰基)-l-鸟氨酰基-l-3-碘代酪氨酰基-l-谷氨酰胺酰基-l-谷氨酰-环(2
→
8)-二硫化物-环-(3
→
12)-内酰胺)(seq id no:82):
[0736][0737]
通过使用fmoc-glu(odmab)代替fmoc-lys(ivdde)-oh并且使用fmoc-lys(ivdde)-oh代替fmoc-glu(odmab),使用对芋螺毒素肽类似物iw所述的相同程序合成了芋螺毒素肽类似物ix。lc-ms(esi-离子阱)m/z:862.9[m+2h]/2
+
,1724.3[m+h]/
+
,(计算mw:1723.56);hplc方法k;保留时间:7.1min;纯度95%。
[0738]
6.3.实施例2:peg化的芋螺毒素肽类似物的制备
[0739]
实施例2.1peg化的芋螺毒素肽类似物iia(seq id no:83)(30kda-mpeg-戊酸酯
(va)-芋螺毒素肽类似物ia):
[0740][0741]
将芋螺毒素肽类似物ia的乙酸盐(25mg,0.015mmol)溶于pbs缓冲液(ph=8.0,12.5ml),随后添加在h2o(20ml)中mpeg-30kda-va-nhs酯(560mg,0.018mmol;nof america,sunbright me-300hs;最终接头=戊酸酰胺(“va”);平均值n=675)。在室温下将反应容器振荡2h后,使用分析型hplc监测反应进程。如通过hplc分析所确定的,当>90%的芋螺毒素肽类似物ia已消耗时,通过hplc方法i纯化所产生的peg化的肽(peg化的芋螺毒素肽类似物iia)以除去未反应的芋螺毒素肽类似物ia(rt=5.0min)。将peg化的芋螺毒素肽类似物iia的hplc峰分成三份,并且通过hplc方法i利用elsd检测(在线,uv检测器后)分析每个部分以确定肽纯度(uv rt=16.65min,elsd保留时间=16.75min)、残余游离peg的量(elsd rt=17.00min)。将基于elsd信号(游离peg相对于肽的elsd信号)含有<5%的游离peg的肽纯度>95%的部分合并并冻干。总体分离得率为0.21g(44%);hplc方法i:纯度:95%(uv 214nm),97%(elsd)。peg化的芋螺毒素肽类似物iia的表征数据列于下表2中。
[0742]
表2.peg化的芋螺毒素肽类似物iia的表征数据
[0743][0744]
实施例2.2 peg化的芋螺毒素肽类似物iva(seq id no:84)(30kda-mpeg-bamine-芋螺毒素肽类似物ia):
[0745][0746]
将芋螺毒素肽类似物ia的乙酸盐(25mg,0.013mmol)溶于meoh(10ml),然后添加mpeg-30kda-丁醛(cas no.9004-74-4,414mg,0.013mmol)在meoh(10ml)中的溶液。将混合物在室温下振荡3h。在此之后,添加ppts(3.3mg,0.013mmol)在meoh(0.1ml)中的溶液,然后添加nacnbh3(1.6mg,0.026mmol)在meoh(0.1ml)中的溶液。继续振荡12h,此后通过制备hplc方法g直接纯化反应混合物以提供peg化的芋螺毒素肽类似物iva的tfa盐(92mg,总得率21%,tfa盐)。hplc纯度:95.7%(uv 214nm)。
[0747]
通过将来自以上的peg化的芋螺毒素肽类似物iva的tfa盐(92mg,0.0027mmol)溶于3ml水中以实现后续盐交换。向该溶液中滴加nh4hco3(水溶液)以将ph调整为7.0-8.0。然后,通过制备rp-hplc(流动相:a:0.1%acoh在水中的溶液,b:0.1%acoh在acn中的溶液)直接纯化混合物并冻干以提供白色固体状的peg化的芋螺毒素肽类似物iva的乙酸盐(31mg,总得率7%,乙酸盐)。lc/ms纯度:95.5%(uv 214nm),98.7%(elsd)。peg化的芋螺毒素肽类似物iva的表征数据列于下表3中。
[0748]
表3.peg化的芋螺毒素肽类似物iva的表征数据
[0749][0750]
实施例2.3 c-末端peg化的芋螺毒素肽类似物va(seq id no:85)(芋螺毒素肽类似物ia-30kda-peg)
[0751][0752]
n末端n-乙酰基芋螺毒素肽类似物ia中间体(14):将芋螺毒素肽类似物ia(75mg,46μmol)溶于无水dmf(35ml)中,然后添加ac2o(7.5μl,0.3mmol)和无水吡啶(32μl,0.4mmol)。将溶液在室温下搅拌2h。然后,通过制备hplc方法g(表7)纯化产物。在将含有产
物的部分冻干后,获得黄白色固体状的化合物14(44.5mg,27μmol,98%纯度,59%得率)。lc-ms(esi)m/z:554.6[m+3h]/3
+
,831.0[m+2h]/2
+
,纯度98%(uv 214nm)。
[0753]
c-末端peg化的芋螺毒素肽类似物va:将化合物14(15mg,9.0μmol)溶于无水dmf(2.5ml)中,并添加30kda-mpeg-丙胺(300mg,10μmol,1.1当量)在无水dmf(2.5ml)中的溶液。然后,分别添加hbtu(3.7mg,9.7μmol)在dmf(0.3ml)中的溶液和dipea(458μl,26μmol)在无水dmf(45ml)中的溶液。将混合物在室温下搅拌2h,然后通过hplc方法g(表7)纯化。将纯化产物冻干得到c末端peg化的芋螺毒素肽类似物va的tfa盐(100mg,3.1μmol,35%得率),其为tfa盐(在214nm下纯度为91%)。然后,将该tfa盐溶于h2o:ch3cn(3ml:1ml)中,然后滴加nh4hco3稀溶液(水溶液)以获得ph=7.0-8.0。然后,通过hplc方法h(表7)纯化混合物以提供c末端聚peg化的芋螺毒素肽类似物va的乙酸盐。在冻干后,获得白色固体(50mg,得率:15.8μmol,17.5%,乙酸盐)。lc-纯度:90.4%(uv 214nm),99.3%(elsd)。peg化的芋螺毒素肽类似物va的表征数据列于下表4中。
[0754]
表4.peg化的芋螺毒素肽类似物va的表征数据
[0755][0756][0757]
实施例2.4 7-arg-peg化的芋螺毒素肽类似物via(seq id no:86)(ac-芋螺毒素肽类似物ia(arg7-va-30kda-peg)
[0758][0759]
将n-末端n-乙酰基芋螺毒素肽类似物ia中间体14(15mg,9.0μmol)溶于无水dmf(2.5ml)中,并添加mpeg-30kda-戊酸-nhs酯试剂(0.54g,18μmol)在无水dmf(2.5ml)中的溶液。然后,添加dbu(4μl,27μmol)在dmf(0.3ml)中的溶液。将混合物加热至40℃持续4h,然后通过hplc方法g(表7)纯化产物。随后冻干得到35mg 7-arg-peg化的芋螺毒素肽类似物via的乙酸盐(表6;35mg,1.1μmol,12.2%,tfa盐)。纯度80%(uv 214nm)。如所述的实施盐交换以提供白色固体状的7-arg-peg化的芋螺毒素肽类似物via的乙酸盐(28mg,9.8%的总得率,乙酸盐)。纯度:99.1%(uv 214nm),81.4%(elsd)。peg化的芋螺毒素肽类似物via的表征数据列于下表5中。
[0760]
表5.peg化的芋螺毒素肽类似物via的表征数据
[0761][0762]
表6.peg化试剂
[0763][0764][0765]
下表7总结了本文所描述的hplc方法。
[0766]
表7:hplc方法的总结
[0767][0768][0769]
6.4.稳定性分析
[0770]
为了解决rgia衍生物中二硫键的不稳定性,合成了二硫桥被三唑桥取代的芋螺毒素肽类似物并且在人和sprague dawley大鼠血浆和血清中对其进行了评价。
[0771]
来自每个三唑-稳定的芋螺毒素肽类似物的样品的反相hplc分析显示了与所述肽的天然构象一致的单一分离的峰。例如,图2a显示芋螺毒素肽类似物ia在大鼠血浆中,在0h、8h和24h在反相hplc上显示出单一分离的峰。无二硫键重排的迹象,这表明一个天然二硫键被三唑模拟物的替换足以防止rgia衍生物在血浆中的二硫键改组(disulfide shuffling)。
[0772]
相反,如图2b中的芋螺毒素肽类似物csp-4-nh2的反相hplc迹线所示,芋螺毒素肽类似物csp-4-nh2(“天然”形式,由两个二硫键组成,一个在cys2和cys8之间并且第二个在cys3和cys12之间)的显著部分经历了成为含有替代的二硫键cys2-cys12和cys3-cys8的“带状(ribbon)”形式和含有替代的cys2-cys3和cys8-cys12二硫键的“珠粒”形式的异构化。在血浆和血清样品中,芋螺毒素肽类似物csp-4-nh2主要在天然形式和带状形式之间异构化,珠粒形成极少(图2b)。
[0773]
6.5.生物测定
[0774]
6.5.1.大鼠和人nachr的两电极电压钳法
[0775]
实施例4.1
[0776]
测定:
[0777]
将爪蟾(xenopus laevis)卵母细胞(非洲蟾蜍属1,mi)用于异源表达克隆的大鼠或人nachr亚型。注射后1-5天进行记录。简要地,将卵母细胞置于sylgard制造的100μl室(4mm直径,62mm深)中并以恒定流量(2ml/min)重力-灌注nd96(96mm nacl,1.8mm cacl2,2.0mm kcl,1.0mm mgcl2,5mm hepes,ph 7.1-7.5)。使用geneclamp500两电极电压钳放大器将卵母细胞的膜电位保持在-70mv。每分钟用100μm乙酰胆碱(ach)1-sec脉冲刺激nachr一次并且采集ach-门控电流。在使用nd96实现ach脉冲的稳定基线后,将溶液转换为含有多种化合物浓度的nd96并观察ach脉冲的阻断反应。在肽应用后,将nachr对ach的反应计算为基线所观察的值的“反应%”。通过非线性回归分析并且使用底部等于0且顶部等于100的约束,将每个卵母细胞的数据对hill方程:反应%=100/{1+([毒素]/ic
50
}
nh
}拟合(graphpad prism),产生了ach-门控电流抑制的浓度-反应曲线。对每个卵母细胞拟合独立的浓度反应曲线并将ic
50
值取平均值。将ic
50
的平均值报告为平均值
±
sem。将双尾非配对t检验用于显著性差异(graphpad prism)。
[0778]
结果:
[0779]
6.5.1.1.对大鼠和人nachr两者,用三唑桥替换二硫桥改善了稳定性并且维持了充分的活性
[0780]
表8.芋螺毒素肽rgia及其类似物对大鼠和人α9α10烟碱乙酰胆碱受体(nachr)的抑制
[0781][0782]
注:nt=未测试。
[0783]
确定了在6.2和6.3节中制备的芋螺毒素肽类似物和peg化的芋螺毒素肽类似物对大鼠和人nachr两者的活性并且分别在表8和9中总结了结果。
[0784]
如表8所示,csp-4-nh2对大鼠和人nachr两者显示出纳摩尔活性(ic
50
:对大鼠α9α10nachr为0.4
±
0.2nm,并且对人α9α10nachr为3.5
±
1.5nm)。尽管如此,由于csp-4-nh2具有两个二硫桥(一个二硫桥在2-和8-位的半胱氨酸残基之间;另一个二硫桥在3-和8-位的半胱氨酸残基之间),因此csp-4-nh2经受了二硫键改组问题并且具有不良的稳定性(参见图1a-图1d和图2b)。
[0785]
如表8所示,3-和12-位的二硫桥被内酰胺桥取代的芋螺毒素肽类似物iw和ix未对人α9α10nachr维持足够的活性。芋螺毒素肽类似物iw和ix分别显示出》300nm和123
±
22nm的ic
50
。具有在3-位的pra和12-位的叠氮基nva之间形成的三唑桥的某些芋螺毒素肽类似物对人α9α10nachr维持了足够的生物活性(例如,ic
50
《100nm)。例如,芋螺毒素肽类似物ia和
ia'对人α9α10nachr的ic
50
的测量结果分别为0.7
±
0.03nm和26
±
4nm。中间体芋螺毒素肽类似物ib和ib'对人α9α10nachr的ic
50
的测量结果分别为37
±
1.3nm和48
±
9nm。在c-末端具有羧酸的芋螺毒素肽类似物ia和ib以及在c-末端具有酰胺基的芋螺毒素肽类似物ia'和ib'维持了足够的活性。两者在c-末端均具有酰胺基的芋螺毒素肽类似物ia和ib分别显示出比在c-末端具有羧酸的相应芋螺毒素肽类似物低的ic
50
(ia vs.ia'和ib vs.ib')。
[0786]
相反,具有在2-和8-位之间形成的三唑桥的芋螺毒素肽类似物ic和id对人α9α10nachr未维持足够的活性。芋螺毒素肽类似物ic和id的ic
50
的测量结果分别为152
±
71nm和≥1000nm。仍相反,具有在3-和12-位之间形成形成三唑桥,但是具有在12-位分别由pra或叠氮基ala形成的三唑桥的芋螺毒素肽类似物if和ij对人α9α10nachr未维持足够的活性。芋螺毒素肽类似物if和ij的ic
50
的测量结果分别为1521
±
116nm和152
±
71nm。
[0787]
先前已表明rgia的末端氨基酸的缺失以及被酰胺(cys12-酰胺)的替换对肽与大鼠α9α10nachr的结合没有显著影响(ellison等人,2008,j.mol.biol.377:1216-1227;armishaw,2010,toxins 2:1471-1499;us 20120220539 a1)。此外,其它α-芋螺毒素,如vc1.1和imi在13位不具有氨基酸(参见图4),这表明该残基对于通道结合将不是必须的。
[0788]
然而,意外地发现在芋螺毒素肽类似物ia的背景中,c末端氨基酸缺失或替换影响人α9α10nachr效力。具体地,如表8所示,当13-位的tyr被phe(芋螺毒素肽类似物il)或d-tyr(芋螺毒素肽类似物im)替换时,效力降低。芋螺毒素肽类似物il和im的ic
50
的测量结果分别为11
±
1.4nm和50
±
1.2nm。相反,当13-位的tyr缺失(芋螺毒素肽类似物iq),被n-me-tyr替换(芋螺毒素肽类似物ir)、被d-arg替换(芋螺毒素肽类似物is)、被n-me-d-tyr替换(芋螺毒素肽类似物it)、被β-tyr替换(芋螺毒素肽类似物iu)或者被n-me-arg替换(芋螺毒素肽类似物iv)时,它提供了对人α9α10nachr具有低效力的芋螺毒素肽类似物。
[0789]
相对于csp-4-oh(具有3-和12-二硫桥的相应的芋螺毒素肽类似物)的13-位残基的缺失的影响,评价了具有在3-和12-位之间所形成的三唑桥的芋螺毒素肽类似物的13-位处的氨基酸残基的缺失对它们对人α9α10nachr的效力的影响。意外地,相对于csp-4-oh(cys3,12二硫桥),据发现tyr在13-位的缺失导致对人α9α10nachr的结合亲合力降低了大于20-倍(图5a)。然而,相对于芋螺毒素肽类似物1a(具有3-和12-位之间的三唑桥的替换),氨基酸13的缺失导致对大鼠通道活性约10-倍的损失和对人通道的活性大于100-倍的损失(芋螺毒素肽类似物1a vs 1q)(表8,图5b)。这些数据显示氨基酸在c-末端(位置13)的缺失降低了在3-和12-位之间具有三唑桥的芋螺毒素肽类似物的活性,但是不会降低在3-和12-位之间具有二硫桥的那些。这些数据表明在稳定的二硫键模拟物的背景中,在整个肽的环2和羧基末端中的相互作用对于确定人通道效力是重要的,并且环2和羧基末端的二级结构的改变在芋螺毒素肽rgia类似物和α9α10nachr之间产生了不可预测的相互作用。
[0790]
此外,一个其它氨基酸(例如,n-me-gly、d-tyr或者n-me-tyr)向芋螺毒素肽类似物ia的c-末端的添加提供了具有14个残基的芋螺毒素肽类似物in、io和ip,它们维持了对人α9α10nachr的效力。如表8所示,例如,芋螺毒素肽类似物in(与ia相比,在14-位具有另外的n-me-gly)、io(与ia相比,在14-位具有另外的d-tyr)和ip(与ia相比,在14-位具有另外的n-me-tyr)的ic
50
的测量结果分别为37
±
15nm,59nm和26
±
1.4nm。
[0791]
通道结合的选择性:在涉及88种受体、转运蛋白、酶和激酶的潜在脱靶影响的评价中,含有三唑的芋螺毒素肽类似物ia'和ib'表明除了α7nachr的部分抑制(分别为52%和
56%)外,在10μm无脱靶影响。在这方面,芋螺毒素肽rgia中的二硫桥的三唑桥替换未显著改变芋螺毒素肽类似物的选择性。
[0792]
6.5.1.2.芋螺毒素肽类似物ia在n-末端的peg化意外地保留了对大鼠和人nachr两者的足够的活性
[0793]
30kda戊酸酯-直链peg(n末端酰基化)向芋螺毒素肽类似物ia的n-末端的添加导致产生了peg化的芋螺毒素肽类似物iia。当评价它对人和大鼠nachr的活性时,peg化的芋螺毒素肽类似物iia以低纳摩尔效力对大鼠和人α9α10nachr(图6a和图6b)产生了类似的阻断。对人α9α10nachr,peg化的芋螺毒素肽类似物iia导致产生了与未缀合的芋螺毒素肽类似物ia(0.7
±
0.03nm)几乎相等的ic
50
(表9;0.7
±
0.1nm)。与peg化将潜在产生结构限制,从而导致肽对啮齿类和人通道的结合效力降低的文献教导内容(fishburn,2008,j.pharm.sci.97:4167-4183;parrott and desimone,2011,nat.chem.4:13-14)相反,通过附接至peg聚合物,分子量增加约18.5-倍的peg化的芋螺毒素肽类似物iia意外地保留了芋螺毒素肽ia的效力(对人α9α10nachr,0.7
±
0.1nm)。
[0794]
表9.芋螺毒素肽类似物ia及其peg化的芋螺毒素肽类似物iia、iiia、iva、va和via对大鼠和人α9α10烟碱乙酰胆碱受体(nachr)的抑制
[0795][0796]
注:nt=未测试。
[0797]
通过测试peg化的芋螺毒素肽类似物va(其中将直链mpeg聚合物共价连接至芋螺毒素肽类似物ia的c-末端)和via(其中将直链mpeg聚合物共价连接至芋螺毒素肽类似物ia的7-位处的精氨酸)对人α9α10nachr的活性,评价了在不同连接位置的peg化的影响。与具有共价连接至芋螺毒素肽类似物ia的n-末端的直链mpeg聚合物的peg化的芋螺毒素肽类似物iia(ic
50
=0.7
±
0.1nm)相比,对peg化的芋螺毒素肽类似物va(ic
50
=~300nm)和via(ic
50
=300nm)两者观察到了对人nachr显著较低的ic
50
。在芋螺毒素肽类似物ia的c-末端(va)或者位置7(via)缀合至peg不会提供具有足够的活性的peg化的芋螺毒素肽类似物。
[0798]
还研究了使用不同接头的peg化的芋螺毒素肽类似物的效力。测试了具有通过亚丁基接头附接至芋螺毒素肽类似物ia的n-末端的直链mpeg聚合物的peg化的芋螺毒素肽类似物iva对人α9α10nachr的活性。如表9所示,peg化的芋螺毒素肽类似物iva的ic
50
比其中通过戊酸酯接头将peg聚合物附接至所述肽(芋螺毒素肽类似物ia)的n-末端的peg化的芋螺毒素肽类似物iia(ic
50
=0.7
±
0.1nm)的ic
50
高100-倍以上(ic
50
=~100nm)。这些结果表明接头类型和peg聚合物所附接的肽上的位置的选择对于保留其对人α9α10nachr的效力的芋
螺毒素肽类似物ia的peg化衍生化是至关重要的。意外地,据发现具有通过戊酸酯接头共价连接至芋螺毒素肽类似物ia的n-末端的30kda直链mpeg的peg化的芋螺毒素肽类似物iia是最优的peg化的芋螺毒素肽类似物。
[0799]
还通过peg化的csp-4-oh证明了类似的意外结果。通过戊酸酯接头向csp-4-oh的n-末端添加30kda peg,所产生的peg化的芋螺毒素肽类似物xi(直链30kda mpeg-va-csp-4-nh2)对大鼠α9α10nachr维持了低纳摩尔效力(ic
50
=6.0
±
0.1nm),这表明这些肽的n-末端允许添加大的分子,同时不会显著改变它们的体外生物效力。
[0800]
6.5.2.芋螺毒素肽类似物和peg化的芋螺毒素肽类似物在大鼠中的药物动力学研究
[0801]
芋螺毒素肽类似物ia在大鼠中的药物动力学研究:将芋螺毒素肽类似物ia以1mg/kg在媒介物(10mm磷酸钠、0.8%氯化钠、0.05%吐温20,ph 6.0)中静脉内或皮下注射到10周大的雄性sprague dawley大鼠(n=3只每组)中。在不同时间点(剂量前和剂量后0.083至24小时)通过尾静脉将血液采集到k2edta收集管、离心并将血浆在-60至-90℃存储直至分析。使用如以下所描述的肽特异性lc-ms/ms测定确定芋螺毒素肽类似物1a的浓度。产生原始数据并通过graphpad prism,使用具有s形剂量-反应(可变斜率)的非线性回归作图。使用pksolver 2.0软件计算药物动力学参数。
[0802]
芋螺毒素肽类似物1a的血浆pk样品的lc-ms/ms分析:使用shimadzu液相色谱系统(shimadzu uflc-xr)和ab sciex api 5000三重四极杆串联质谱仪进行芋螺毒素肽类似物1a的样品分析。hplc系统由配备有两个lc-20ac xr泵、cbm-20a通信模块、sil-20ac xr自动进样器、cto-20a柱温箱和在线spd-20a uv检测器的shimadzu液相色谱系统组成。在thermo scientific fluophase pfp柱(2.1
×
50mm,5μm,)上,以40℃进行色谱分离。流动相a是具有0.05%的乙酸的水,流动相b是具有0.05%的乙酸的乙腈。以0.3ml/min的流速,在0-6min应用b(5%-90%)的线性梯度,然后在6.0-7.8min保持90%,然后2min回到5%b进行柱平衡。将样品在4℃保持在自动进样器中,并且对于每个分析,将5μl体积进样到hplc系统中。
[0803]
在配备有以负电离模式运行的涡流离子喷雾源的三重四极杆串联质谱仪api 5000上进行质谱检测。优化ms的操作条件,如下所示:离子喷雾电压设置为-4500kv,离子源温度保持在500℃;碰撞能设置为-35v。将氮气用作碰撞气体。气帘气、离子源气体1和气体2的流速分别设置为10、40和40l/min。使用analyst 2.1软件(ab sciex)进行lc-ms/ms的操作和数据分析。通过使用m/z 809.0/792.5的芋螺毒素肽类似物ia转换的多反应监控(mrm)模式获得定量数据。
[0804]
在来自使用hp d300数字分配器(tecan)准确称量的、纯度正确的肽在dmso中的1.0mg/ml储液的k2edta大鼠血浆(bioreclamation)中制备芋螺毒素肽类似物ia的标准曲线(10-5000ng/ml)。将50μl pk样品血浆、芋螺毒素肽类似物ia标准品和芋螺毒素肽类似物ia qc样品等分到phree磷脂除去板(phree phospholipid removal plate)(phenomenex)上,用450μl甲醇(1:10稀释)处理并彻底混合。然后,通过真空歧管将样品通过phree板过滤到96-深孔样品板中并使用所述lc-ms/ms法分析。通过ab-sciex multiquant软件,使用单参数非线性回归从标准曲线获得芋螺毒素肽类似物ia的浓度,并且使用pksolver 2.0软件计算pk参数。
[0805]
peg化的芋螺毒素肽类似物iia在大鼠中的药物动力学(pk)研究:将peg化的芋螺毒素肽类似物iia以1mg/kg(核心肽含量,~19mg/kg peg化的肽含量)在媒介物(10mm磷酸钠、0.8%氯化钠、0.05%吐温20,ph 6.0)中静脉内(“iv”)或皮下(“sc”)注射到10周大的雄性sprague dawley大鼠(n=3只每组)中。在不同时间点(剂量前和剂量后0.083-120小时)通过尾静脉将血液采集到k2edta收集管、离心并将血浆在-60至-90℃存储直至分析。通过如以下所描述的peg-缀合物特异性elisa测定定量芋螺毒素肽类似物iia的量。通过graphpad prism,使用具有s形剂量-反应(可变斜率)的非线性回归产生所获得的血浆浓度(净肽)。使用pksolver 2.0软件计算pk参数。
[0806]
用于peg化的芋螺毒素肽类似物iia pk样品分析的elisa抗体、试剂和方法:通过用缀合至klh载体蛋白的芋螺毒素肽类似物ia免疫未处理过的nzw兔产生兔多克隆抗-芋螺肽捕获抗体,并用芋螺毒素肽类似物ia加强。然后,使用亲合蛋白g琼脂糖(ge healthcare life sciences)重力柱,然后使用pbs作为流动相在16/600superdex 75pg尺寸-排阻色谱(sec)柱(ge healthcare life sciences)上精制和缓冲液更换,从免疫血清纯化多克隆igg抗体。将含有纯化抗体的sec部分混合并通过二辛可宁酸测定(bca测定)计算浓度。纯化的多克隆抗体已证明了识别芋螺毒素肽类似物ia和芋螺毒素肽类似物iia的交叉反应性。在4℃,用50μl每孔在涂覆缓冲液(0.1m nahco3 ph 9.6)中的捕获抗体(纯化的抗-芋螺毒素肽类似物ia 7626r pab,批次#26r-1-d54-0618,5μg/ml)涂覆微量滴定板孔12h,或者在37℃振荡1h,然后在室温下用200μl每孔在pbs中的5%bsa封闭2h。重复两次加载血浆样品、qc样品和标准品(50μl)并在室温下边振荡边培育1.5-2h,然后添加50μl每孔在稀释剂缓冲液(在pbs中的0.5%bsa)中的抗-peg抗体(1ug/ml),并在室温下振荡另外1h。将50μl每孔在稀释剂缓冲液中1:200稀释的抗生蛋白链菌素hrp加入至板中并在室温下边振荡边培育1h,然后添加50μl发色底物(tmb),并将其在室温下培育5-6min。用100μl h2so4终止反应,并使用elisa酶标仪测量450nm的吸光值。每个步骤后,用清洗缓冲液(pbst,ph 7.4,含有0.1%(v/v)吐温20)将板清洗3次,然后用pbs清洗3-6次。作为定量参考,通过peg化的芋螺毒素肽类似物iia在10%k2edta血浆(大鼠或猴)中的连续稀释(400ng/ml-0.06ng/ml,基于核心肽含量的重量)建立标准曲线。通过将样品信号外推至标准曲线的线性范围(信号vs浓度),定量每个样品中peg化的芋螺毒素肽类似物iia的量。
[0807]
结果:如以下所讨论的,芋螺毒素肽类似物ia的peg化显示延长了其循环时间。在大鼠中评价了peg化的芋螺毒素肽iia的药物动力学谱并与芋螺毒素肽类似物ia的pk谱和清除相比较。图7a和图7b中显示了在单一1mg/kg iv或sc剂量后,血浆中芋螺毒素肽类似物ia和peg化的芋螺毒素肽iia的平均浓度相对于时间的图。当将peg-缀合物pk谱图与单独的未缀合的芋螺毒素肽类似物ia的谱图相比较时,由于peg化的两种提高是显然的:(i)通过添加peg基团,芋螺毒素肽类似物ia的半衰期显著提高,和(ii)peg化的芋螺毒素肽iia的总暴露比未缀合的芋螺毒素肽类似物ia要大得多。对于sc施用的化合物,peg化的芋螺毒素肽iia的消除半衰期比未缀合的芋螺毒素肽类似物ia长约42-倍(分别地,21h相对于0.5h)。还改善了peg化的芋螺毒素肽iia的cmax和auc,其中peg化的芋螺毒素肽iia的cmax是未缀合的芋螺毒素肽类似物ia的接近四倍,并且peg化的芋螺毒素肽iia的auc比芋螺毒素肽类似物ia的auc大接近140-倍(cmax:peg化的芋螺毒素肽iia:2518ng/ml;芋螺毒素肽类似物ia:648ng/ml)(auc
0-t
:peg化的芋螺毒素肽iia:137729ng/ml*hr;芋螺毒素肽类似物ia:981ng/
ml*hr)。芋螺毒素肽类似物ia和peg化的芋螺毒素肽iia在大鼠中的药物动力学(pk)和药效学(pd)参数如下表10所示。
[0808]
表10.芋螺毒素肽类似物ia和peg化的芋螺毒素肽iia在大鼠中的药物动力学(pk)和药效学(pd)参数
[0809][0810]
还在猴中观察到了通过芋螺毒素肽类似物ia的peg化的pk谱图的增强。对雄性食蟹猕猴(cynomolgus macaque)iv和sc施用1mg/kg(净肽浓度)的peg化的芋螺毒素肽iia以用于pk研究。在iv施用后,peg化的芋螺毒素肽iia的最高暴露为在剂量后0.083h,其cmax为42,200ng/ml并在剂量后168h降低至109ng/ml。auc为603,594ng/ml*h。在sc施用后,peg化的芋螺毒素肽iia的最高暴露为剂量后24h,其cmax为7,867ng/ml并在剂量后168h降低至216ng/ml。auc为453,077ng/ml*h并且sc剂量施用后peg化的芋螺毒素肽iia的生物利用度为75%。图8和表11中显示了peg化的芋螺毒素肽iia在猴中的pk谱图和参数。
[0811]
表11.在猴中单一1mg/kg剂量施用(iv或sc)后,peg化的芋螺毒素肽iia的药物动力学参数
[0812][0813]
注:nt=未测试。
[0814]
6.5.3.动物疼痛模型中的止痛活性
[0815]
慢性压迫性损伤(cci)模型是通过连接至坐骨神经所引起的单神经病模型(bennett and xie,1988,pain,33(1):87-107)。涉及周围神经的损害,以及肥大细胞、粒性白细胞、巨噬细胞和t淋巴细胞的浸润。这些细胞通过炎症介质(例如,促炎细胞因子和趋化因子)的分泌可以有助于神经性疼痛的产生和维持。cci是周围神经损伤的常见模型之一。
[0816]
测定:在第0天,在吸气室中使用5%的异氟烷(o2,以1l/min)使雄性sprague dawley大鼠麻醉。一旦已达到适当的麻醉平面,通过鼻锥施用3%的维持水平的恒定异氟烷流。在平行于股骨的左后肢产生2cm皮肤切口。暴露坐骨神经,并且在坐骨神经的三根分叉部附近,以约1mm的间隔系扎4根松散的4-0铬肠线结扎线。使肌肉和皮肤靠近,并使动物恢复。在手术当天开始并且在此后14天中的每一天,通过皮下注射施用在由10mm磷酸钠、0.8%nacl、0.05%吐温20组成的媒介物中的0.1mg/kg芋螺毒素肽类似物1b'。
[0817]
结果:将来自用芋螺毒素肽类似物1b'处理的动物的数据与用媒介物对照处理的动物相比较。在手术后7和14天,使用ugo basile痛觉测量计在左后爪中测量机械性痛觉过敏(n=3次)。通过双向方差分析进行统计分析。如图9所示,在两个测量日,相对于媒介物-处理的对照动物,用0.1mg/kg芋螺毒素肽类似物1b'每天处理导致缩爪阈值统计学显著改善。这些数据表明三唑-替换的rgia类似物有效地治疗了大鼠cci模型中的神经性疼痛。
[0818]
6.5.4.化疗引起的周围神经病模型
[0819]
测定:化疗引起的周围神经病(cipn)在经历铂盐化疗的患者中是常见的。通过用2.4mg/kg静脉内(i.v.)奥沙利铂每周处理两次,处理3周(6次i.v.注射),在雄性sprague dawley大鼠中引起了化疗引起的神经病。用痛觉测量计(ugo basile,varese,italy)确定大鼠中的疼痛阈值。简要地,使用钝锥形探针,将持续升高的压力应用于后爪背侧的小区域中。提高机械压力,直至发声或发生退避反射。以克表示发声或退避反射阈值。对于止痛测量,在120g终止机械压力应用。在研究期间,实验员对注射化合物的属性不知情。使用dunnett多重比较检验,通过单因素方差分析分析数据(graphpad prism)。在芋螺毒素肽类似物的单次皮下剂量(例如,0.5mg/kg)施用后14天,测量神经性疼痛。
[0820]
6.5.4.1.使用不同peg聚合物的peg化的芋螺毒素肽类似物衍生物的评价
[0821]
制备了csp-4-nh2的不同的peg化衍生物,包括直链20kda mpeg-va-csp-4-nh2(peg化的芋螺毒素肽类似物vii,化学式(vii),seq id no:87)、直链20kda mpeg-bamine-csp-4-nh2(peg化的芋螺毒素肽类似物viii,化学式(viii),seq id no:88)、支链2
×
10kda mpeg-胺-csp-4-nh2(peg化的芋螺毒素肽类似物ix,化学式(ix),seq id no:89)、支链2
×
10kda mpeg-碳酸酯-csp-4-nh2(peg化的芋螺毒素肽类似物x,化学式(x),seq id no:90)、直链30kda mpeg-va-csp-4-nh2(peg化的芋螺毒素肽类似物xi,化学式(xi),seq id no:91)和直链40kda mpeg-va-csp-4-nh2(peg化的芋螺毒素肽类似物xii,化学式(xii),seq id no:92)。
[0822][0823]
评价了csp-4-nh2的多种peg化衍生物在大鼠cipn模型中的止痛效果的持续时间。所测试的peg化衍生物大小(20kda至40kda)和构造(共价连接至直链或支链peg聚合物)不同。在单次500μg/kg皮下剂量的csp-4-nh2、peg化的芋螺毒素vii、viii、ix、x、xi和xii后,在大鼠cipn模型中确定了止痛效力和药效作用的持续时间。在剂量施用后30min、5h、24h、48h、72h和96h测试了止痛效力。通过randall-selitto测试测量了机械性痛觉过敏。在每周两次iv施用奥沙利铂之后疼痛阈值随时间降低,在奥沙利铂剂量施用后第7天显著引起了机械性痛觉过敏并持续增加至第14天。在第14天,测试了csp-4-nh2和csp-4-nh2的peg-衍生物在降低机械性痛觉过敏中的效力。在药物施用后0.5-5h,机械性痛觉过敏测量达到化疗前的水平。随着所添加的peg的分子量提高至高达30kda直链peg,止痛效力的持续时间延长。使用正丁基接头的peg化的csp-4-nh2(viii)的效力的持续时间比通过戊酸接头的peg化的csp-4-nh2(vii)、(xi)、(xii)的效力的持续时间显著更短(图10a-10c)。通过用大于30kda直链peg的peg分子(xii)或者用支链peg(ix和x)缀合并未获得额外的益处(图10c)。
[0824]
6.5.4.2.芋螺毒素肽类似物ia和ia'以及peg化的芋螺毒素肽类似物iia的效力评价
[0825]
如图11a所示,芋螺毒素肽类似物ia'的单次皮下剂量(0.5mg/kg)导致机械性痛觉过敏在剂量后0.5h、4h和24h统计学显著改善。如图11b所示,芋螺毒素肽类似物ia'的单次皮下注射导致机械性痛觉过敏在剂量后0.5h、4h和24h相对于媒介物处理的动物统计学显著改善。图11c显示在奥沙利铂-诱导的周围神经病的诱导后14天,单次0.5mg/kg剂量的芋螺毒素肽类似物ia或peg化的芋螺毒素肽类似物iia向大鼠的施用导致机械性痛觉过敏显著降低(对于ia,长达4h,或者对于iia,长达72h)。这些数据进一步表明了使用这些三唑稳定的rgia衍生物对于治疗或预防神经性疼痛的治疗潜能。
[0826]
7.作为参考并入
[0827]
本文所引用的所有参考文献以好象每个单个专利公开或专利或专利申请具体且单独表明出于所有目的以其全部作为参考并入的相同程度以其全部内容并且出于所有目的作为参考并入本文。
[0828]
可以在不背离其精神和范围的情况下对本发明做出多种修改和改变,如将对本领域技术人员显而易见的。仅通过举例说明提供了本文所述的具体实施方式,并且本发明仅限于所附权利要求项以及这些权利要求所赋予的等价形式的全部范围。
