1.本发明涉及化学生产技术领域,具体为一种三氯化铁溶液制备工艺。
背景技术:
2.三氯化铁分为无水三氯化铁和六水合三氯化铁,被广泛用于水处理剂、印刷制版、电子线路图版的腐蚀剂、冶金工业的氧化剂、染料工业的氧化剂和媒染剂、有机合成工业的催化剂和氧化剂、还有制造其他颜料的原料(铁颜料、珠光颜料包膜材料等)领域,在化工生产中,有些有机合成反应使用三氯化铁作为催化剂,铁催化剂在使用一定时间后出现“中毒”现象,即铁被氧化生成氧化铁而失去活性,需要更换新的铁催化剂,失去活性的铁催化剂通常采用在一定温度下进行酸浸(如盐酸、硫酸)的方法回收,利用铁“聚合”现象,铁不能与酸完全反应,回收率低(30-40%),而且会造成二次污染。
3.在已有的三氯化铁生产方法中技术文献中,专利文献(申请号:200810110685.x)公开了一种制备高纯度三氯化铁的方法,该方法包括如下步骤:首先以有机铁为原料经升华或蒸馏提纯有机铁,接着再在一定温度下将有机铁炭化成fe/c粉,接着再与高纯度盐酸和氧化剂反应生成含炭粉的三氯化铁水溶液,再经过滤分离炭粉,滤液浓缩得高纯度三氯化铁,该法非常简洁,使用的原料为有机铁,铁元素的含量比较低,会影响产出量,再者碳粉的过滤是一个比较麻烦的问题,但专利内容中没有提及,因此其实用性还有待商榷。
4.有鉴于此,针对现有的问题予以研究改良,提供一种三氯化铁溶液制备工艺,来解决传统的三氯化铁的生产中存在稳定性差有效成分损失大、污染严重、生产成本高等缺陷,旨在通过该技术,达到解决问题与提高实用价值性的目的。
技术实现要素:
5.本发明旨在解决现有技术或相关技术中存在的技术问题之一。
6.为此,本发明所采用的技术方案为:一种三氯化铁溶液制备工艺,包括以下步骤:
7.s1:取质量比为1:0.24-0.35的三氯化铁和结晶葡萄糖加入高速分散器并加热,调节高速分散器的搅拌速度15-25节,反应时间20-25min;
8.s2:当溶液呈绿色并无气泡产生时,静止3-5min观察反应器底部状态,若溶液底部没有三氯化铁沉淀则三氯化铁完全反应,冷却至室温制得氯化亚铁溶液;
9.s3:在制得氯化亚铁溶液中再加入稀盐酸溶液控制ph值≤2,按设定速度加入三氯化铁质量的1.6-1.65倍的双氧水;
10.s4:最后在反应过程中用滴管从反应器中取样于点滴板上,加0.01mol/l的k3[fe(cn)3]溶液2滴检测,如果不产生蓝色沉淀,则fecl2被完全氧化成fecl3,得到fecl3水溶液,若产生蓝色沉淀则继续添加双氧水,直至检测结果不产生蓝色沉淀,加入40-65%净水剂,完成配制。
[0011]
本发明在一较佳示例中可以进一步配置为:步骤s1中所述稀盐酸溶液溶度为18
±
1%。
[0012]
通过采用上述技术方案,由于质量分数较高的hci浓度较高,其挥发性大,从而导致生产所用hcl较多,对环境污染大,现有技术中不采用浓hci也是考虑这个原因,由于质量分数较低的hcl,反应时间较长,在长时间作用中其挥发出的hci气体相对较多,从而导致实验所用hcl较多,对环境污染也大,质量分数为18
±
1%的hcl为最佳hcl浓度。
[0013]
本发明在一较佳示例中可以进一步配置为:步骤s1中高速分散器的加热温度为85
±
5℃。
[0014]
通过采用上述技术方案,适宜的反应高温有利于节约hcl原料和提高生产效率,且过高的反应温度易加剧hcl气体的挥发,从而导致环境污染和原料的浪费。
[0015]
本发明在一较佳示例中可以进一步配置为:在步骤s3中双氧水加入速度0.5-1ml/min,反应温度55℃。
[0016]
通过采用上述技术方案,由于环境温度与反应温度相差较大,导致在反应过程中有部分热量损失.而双氧水氧化fecl2,时会放出热量,所以控制好双氧水的加入速度就能控制好溶液的反应温度;h2o2加入速度在0.5-1ml/min时,双氧水用量、溶液温度变化和反应时间适中,有利于节约双氧水用量提高生产效率。
[0017]
本发明在一较佳示例中可以进一步配置为:在步骤s1、s2和s3中反应容器选择三口瓶,三口瓶的一端插入用于实时监测反应温度的温度计,三口瓶的顶端连接有冷凝管,冷凝管中通入冷凝液用于将高温挥发的hcl气体冷凝呈稀盐酸回落继续参与反应。
[0018]
本发明所取得的有益效果为:
[0019]
1.本发明中,通过采用稀盐酸置换氧化法制备三氯化铁溶液,利用特定稀盐酸和特定温度条件下的反应以及双氧水氧化剂的加入速度,多方面提高三氯化铁的生产效率控制原材料用量,达到降低投入成本提高产出比的效果,从而提高该制备工艺的经济效益。
[0020]
2.本发明中,通过采用双氧水作为强氧化剂将二价铁离子氧化形成三价铁成为稳定的三氯化铁溶液,根据双氧水的强氧化氢和反应后生成水的特性,提高该反应的制备效率和环保性,且相较于传统氯气、硝酸、和次氯化钠等氧化剂其反应更加安全污染性低。
[0021]
3.本发明中,通过双氧水在酸性环境下产生大量游离态氢根离子抑制氢氧根与三价铁离子形成絮状fe(oh)3沉淀析出,可有效保证三氯化铁溶液的稳定存续,提高溶液中三氯化铁含量。
具体实施方式
[0022]
为使本发明的目的、技术方案和优点更加清楚明了,下面结合具体实施方式,对本发明进一步详细说明。需要说明的是,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
[0023]
该理解,这些描述只是示例性的,而并非要限制本发明的范围。
[0024]
下面描述本发明的一些实施例提供的一种三氯化铁溶液制备工艺。
[0025]
实施例1:
[0026]
本发明提供的一种三氯化铁溶液制备工艺,包括以下步骤:
[0027]
s1:取质量比为1:0.24-0.35的三氯化铁和结晶葡萄糖,优选采用1:0.3的三氯化铁和结晶葡萄糖加入高速分散器并加热,调节高速分散器的搅拌速度15-25节,反应时间20-25min;
[0028]
s2:当溶液呈绿色并无气泡产生时,静止3-5min观察反应器底部状态,若溶液底部没有三氯化铁沉淀则三氯化铁完全反应,冷却至室温制得氯化亚铁溶液;
[0029]
s3:在制得氯化亚铁溶液中再加入稀盐酸溶液控制ph值≤2,按设定速度加入三氯化铁质量的1.6-1.65倍的双氧水;
[0030]
s4:最后在反应过程中用滴管从反应器中取样于点滴板上,加0.01mol/l的k3[fe(cn)3]溶液2滴检测,如果不产生蓝色沉淀,则fecl2被完全氧化成fecl3,得到fecl3水溶液,若产生蓝色沉淀则继续添加双氧水,直至检测结果不产生蓝色沉淀,加入40-65%净水剂,完成配制。
[0031]
在该实施例中,步骤s1中稀盐酸溶液溶度为18
±
1%。
[0032]
具体的,由于质量分数较高的hci浓度较高,其挥发性大,从而导致生产所用hcl较多,对环境污染大,现有技术中不采用浓hci也是考虑这个原因,由于质量分数较低的hcl,反应时间较长,在长时间作用中其挥发出的hci气体相对较多,从而导致实验所用hcl较多,对环境污染也大,质量分数为18
±
1%的hcl为最佳hcl浓度。
[0033]
在该实施例中,步骤s1中高速分散器的加热温度为85
±
5℃。
[0034]
具体的,适宜的反应高温有利于节约hcl原料和提高生产效率,且过高的反应温度易加剧hcl气体的挥发,从而导致环境污染和原料的浪费。
[0035]
在该实施例中,在步骤s3中双氧水加入速度0.5-1ml/min,反应温度55℃。
[0036]
具体的,由于环境温度与反应温度相差较大,导致在反应过程中有部分热量损失.而双氧水氧化fecl2,时会放出热量,所以控制好双氧水的加入速度就能控制好溶液的反应温度;h2o2加入速度在0.5-1ml/min时,双氧水用量、溶液温度变化和反应时间适中,有利于节约双氧水用量提高生产效率。
[0037]
在该实施例中,在步骤s1、s2和s3中反应容器选择三口瓶,三口瓶的一端插入用于实时监测反应温度的温度计,三口瓶的顶端连接有冷凝管,冷凝管中通入冷凝液用于将高温挥发的hcl气体冷凝呈稀盐酸回落继续参与反应。
[0038]
对比例1:
[0039]
提供一种三氯化铁溶液制备工艺,包括以下步骤:
[0040]
s1:取质量比为1:0.3的三氯化铁和结晶葡萄糖,加入高速分散器并加热,调节高速分散器的搅拌速度15-25节,反应时间20-25min;
[0041]
s2:当溶液呈绿色并无气泡产生时,静止3-5min观察反应器底部状态,若溶液底部没有三氯化铁沉淀则三氯化铁完全反应,冷却至室温制得氯化亚铁溶液;
[0042]
s3:在制得氯化亚铁溶液中再加入稀盐酸溶液控制ph值≤2,按设定速度加入三氯化铁质量的1.6-1.65倍的双氧水;
[0043]
s4:最后在反应过程中用滴管从反应器中取样于点滴板上,加0.01mol/l的k3[fe(cn)3]溶液2滴检测,如果不产生蓝色沉淀,则fecl2被完全氧化成fecl3,得到fecl3水溶液,若产生蓝色沉淀则继续添加双氧水,直至检测结果不产生蓝色沉淀,加入40-65%净水剂,完成配制。
[0044]
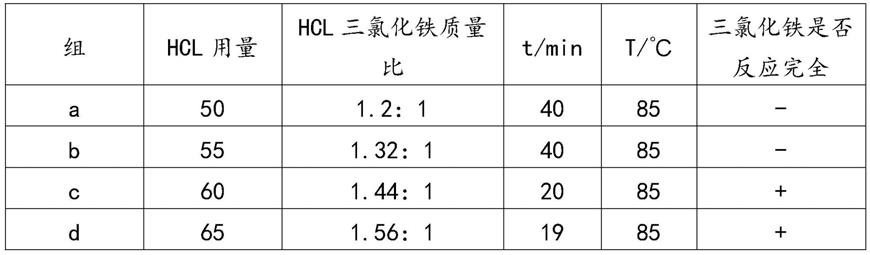
与实施例1的区别在于,该方案中采用质量分数为24%的稀盐酸溶液进行反应测试试验,结果如下表1:
[0045][0046]
表1(质量分数为24%的稀盐酸溶液不同质量比和温度条件下实验结果)
[0047]
由上表可得由于质量分数为24%的hci浓度较高,其挥发性大,从而导致生产所用hcl挥发浪费较多,相同质量比的三氯化铁未完全参与反应有剩余,而挥发出的hcl对环境污染大,因此本方案中采用质量分数为18
±
1%的hcl为最佳hcl浓度。
[0048]
对比例2:
[0049]
提供一种三氯化铁溶液制备工艺,包括以下步骤:
[0050]
s1:取质量比为1:0.3的三氯化铁和结晶葡萄糖加入高速分散器并加热,调节高速分散器的搅拌速度15-25节,反应时间20-25min;
[0051]
s2:当溶液呈绿色并无气泡产生时,静止3-5min观察反应器底部状态,若溶液底部没有三氯化铁沉淀则三氯化铁完全反应,冷却至室温制得氯化亚铁溶液;
[0052]
s3:在制得氯化亚铁溶液中再加入稀盐酸溶液控制ph值≤2,按设定速度加入三氯化铁质量的1.6-1.65倍的双氧水;
[0053]
s4:最后在反应过程中用滴管从反应器中取样于点滴板上,加0.01mol/l的k3[fe(cn)3]溶液2滴检测,如果不产生蓝色沉淀,则fecl2被完全氧化成fecl3,得到fecl3水溶液,若产生蓝色沉淀则继续添加双氧水,直至检测结果不产生蓝色沉淀,加入40-65%净水剂,完成配制。
[0054]
与实施例1的区别在于,该方案中采用18%的稀盐酸浓度,反应温度分别采用75℃和95℃进行试验,结果如下表2:
[0055][0056][0057]
表2(质量分数为28%的稀盐酸溶液不同温度条件下实验结果)
[0058]
由上表可得温度升到75℃时,反应开始特别剧烈,随着反应的进行反应速率也慢慢下降,经过搅拌,三氯化铁与hcl会反应完全,但时间会稍微延长;当温度升到95c时,反应开始特别剧烈,但由于过高的温度加剧hci气体的挥发,从而导致相同量的hci与三氯化铁反应不完全,因此本方案中特定温度85℃左右条件下的反应效率较高且反应完全充分。
[0059]
对比例3:
[0060]
提供一种三氯化铁溶液制备工艺,包括以下步骤:
[0061]
s1:取质量比为1:0.24-0.35的三氯化铁和结晶葡萄糖加入高速分散器并加热,调
节高速分散器的搅拌速度15-25节,反应时间20-25min;
[0062]
s2:当溶液呈绿色并无气泡产生时,静止3-5min观察反应器底部状态,若溶液底部没有三氯化铁沉淀则三氯化铁完全反应,冷却至室温制得氯化亚铁溶液;
[0063]
s3:在制得氯化亚铁溶液中再加入稀盐酸溶液控制ph值≤2,按设定速度加入氧化剂;
[0064]
s4:最后在反应过程中用滴管从反应器中取样于点滴板上,加0.01mol/l的k3[fe(cn)3]溶液2滴检测,如果不产生蓝色沉淀,则fecl2被完全氧化成fecl3,得到fecl3水溶液,若产生蓝色沉淀则继续添加双氧水,直至检测结果不产生蓝色沉淀,加入40-65%净水剂,完成配制。
[0065]
与实施例1的区别在于,该方案中采用氧化剂为氯气、稀硝酸和次氯酸钠,实验结果如下表3:
[0066]
组氧化剂生成物污染尾气gcl2fecl3cl2、hclhhno3fecl3、no、h2ono、hclinaclofecl3、nacl、h2onacl、hcl
[0067]
表3(不同氧化剂相同反应条件下实验结果)
[0068]
由上表可得采用氧化剂为氯气、稀硝酸和次氯酸钠反应生成物和尾气测判断,采用双氧水作为强氧化剂将二价铁离子氧化形成三价铁成为稳定的三氯化铁溶液相较于传统氯气、硝酸、和次氯化钠等氧化剂其反应更加安全污染性低。
[0069]
在本发明中,术语“多个”则指两个或两个以上,除非另有明确的限定。本文所使用的术语“及/或”包括一个或多个相关的所列项目的任意的和所有的组合。术语“安装”、“相连”、“连接”、“固定”等术语均应做广义理解,例如,“连接”可以是固定连接,也可以是可拆卸连接,或一体地连接;“相连”可以是直接相连,也可以通过中间媒介间接相连。对于本领域的普通技术人员而言,可以根据具体情况理解上述术语在本发明中的具体含义。
[0070]
需要说明的是,当元件被称为“装配于”、“安装于”、“固定于”或“设置于”另一个元件,它可以直接在另一个元件上或者也可以存在居中的元件。当一个元件被认为是“连接”另一个元件,它可以是直接连接到另一个元件或者可能同时存在居中元件。本文所使用的术语“垂直的”、“水平的”、“上”、“下”、“左”、“右”以及类似的表述只是为了说明的目的,并不表示是唯一的实施方式。
[0071]
在本说明书的描述中,术语“一个实施例”、“一些实施例”、“具体实施例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或实例。而且,描述的具体特征、结构、材料或特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
[0072]
尽管已经示出和描述了本发明的实施例,本领域的普通技术人员可以理解,在不脱离本发明的原理和宗旨的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由权利要求及其等同物限定。
