微生物的治疗性和预防性应用
1.相关申请
2.本技术要求于2018年12月27日递交的第62/785,640号美国临时专利申请的优先权,其内容在此通过引用整体并入本文中,用于所有目的。
3.发明背景
4.粪便微生物群移植(fmt)是一种非常有效的治疗各种病况的方法,包括胃肠道病症和艰难梭菌(clostridium difficile)感染(cdi),特别是在患有复发性cdi的患者中。fmt也称为粪便移植,其涉及将含有微生物的粪便物质从健康个体移植到受体的胃肠道中的过程。fmt的目标是通过经输注健康个体的粪便的各种方式,例如通过结肠镜、灌肠、口胃管,或者以含有冷冻干燥的获自健康供体的物质的胶囊形式通过口引入(或重新引入)健康的细菌群,而修复由于诸如cdi的病症破坏的肠微生物区系。除cdi外,fmt被越来越多地用于治疗其他肠内和肠外疾病,包括其他胃肠疾病,如炎性肠病(ibd)、耐抗生素的细菌感染、腹泻、便秘、肠易激综合征、自闭症、抑郁症、肥胖、糖尿病、脱发等。另外,fmt已被用于治疗某些神经性病况,如多发性硬化和帕金森氏病。最近的研究已揭示出,用于fmt的供体物质中存在的某些微生物,如某些细菌和真菌,会显著影响fmt的功效,并直接影响是否可能赋予fmt受体与代谢调节有关的另外的健康益处。考虑到人类群体中可通过fmt治疗的各种病况和疾病的流行性及其重大的经济影响,存在对开发新的和改进的方法的迫切需求,以提高fmt的治疗功效和优化治疗结果,特别是在供体和/或受体特异性的基础上。本发明满足了此需求及其他相关的需求。
5.发明概述
6.本发明涉及新的方法和组合物,其可用于优化粪便微生物群移植(fmt)治疗,特别是最大化赋予fmt受体健康益处。特别地,本发明人发现,当在用于fmt受体的移植物中,并随后于接受fmt治疗后在受体的胃肠(gi)道中存在某些微生物(例如细菌、真菌、病毒)(特别是以升高的水平)时,可以在fmt受体中实现显著的健康益处,如体重减轻、较高的胰岛素敏感性、较低的血胆固醇、减少的耐多药细菌的存在、减轻的造血干细胞移植后不良状况如急性移植物抗宿主病(agvhd)、以及减轻的gi道病况如溃疡性结肠炎(uc)或炎性肠病(ibd)或克罗恩病;而在fmt受体gi道中存在(特别是以较高的水平)的某些其他的微生物与此类性质的健康益处的缺乏或大大减少或者与基本上无效的治疗效果有关。这些发现允许发明人设计能够提高关于这些健康益处的fmt效力的方法和组合物。因此,本发明提供了新的鉴定合适的fmt供体的方法,所述供体提供了在适当处理后用于fmt的粪便物质。方法包括确定获自fmt供体候选者的粪便样品中表1a、1b、2、3a、3b、4、5、6a、6b、7a、7b、8a、8b、10a、10b、11、15或16中所示的一种或多种细菌、真菌或病毒的水平的步骤。
7.在第一个方面,本发明提供了鉴定合适的fmt供体的方法,包括确定获自候选者的粪便样品中表1a、4、6a、10b、11或15所示的一种或多种细菌的水平的步骤。在一些实施方案中,一种或多种细菌的水平为百分比相对丰度。在一些实施方案中,当发现一种或多种细菌的水平为大于0.1%时,则候选者被认为是合适的fmt供体。在一些实施方案中,表1b、6b或10a中所示的一种或多种细菌的水平为不大于0.01%。在一些实施方案中,方法还包括从用
于fmt的合适的候选者获取粪便物质的步骤。在一些实施方案中,方法还包括确定粪便样品中的总细菌载荷的步骤。在一些实施方案中,当1b、6b或10a中所示的一种或多种细菌的水平为大于0.01%时,候选者被鉴定为是不合适的fmt供体。
8.在一些实施方案中,确定获自第一候选者的第一粪便样品和获自第二候选者的第二粪便样品中的表1a、1b、4、6a、6b、10a、10b、11、15或16中所示的一种或多种细菌的水平。在一些实施方案中,第一候选者比第二候选者具有更高水平的表1a、4、6a、10b、11或15中所示的一种或多种细菌,并且被认为是比第二候选者更合适的fmt供体。在一些实施方案中,第一候选者比第二候选者具有更低水平的表1b、6b或10a中所示的一种或多种细菌,并且被认为是比第二候选者更合适的fmt供体。
9.在一个实例中,当针对其作为合适的fmt供体的潜能对供体进行筛选时,特别是为了帮助受体减轻体重的目的,其粪便样品中存在的有益菌如两歧双歧杆菌(bifidobacterium bifidum)、肠道罗斯拜瑞氏菌(roseburia intestinalis)和华德萨特菌(sutterella wadsworthensis)应当达到或超过一定的相对量阈值:例如,至少约0.3%或至少0.7%的两歧双歧杆菌、至少约3.5%或至少约6%的肠道罗斯拜瑞氏菌,或者至少约1%的华德萨特菌。相反,有害菌如氢营养布劳特氏菌(blautia hydrogenotrophica)或消化链球菌科菌的存在优选为尽可能低(例如,小于约0.001%)或甚至检测不到。另一方面,如果候选者供体在其粪便样品中具有不足量的有益菌(例如,少于约0.1%的两歧双歧杆菌、肠道罗斯拜瑞氏菌和华德萨特菌中的每种),但太多的有害菌(例如,至少约0.01%、至少约0.05%或至少约0.07%的氢营养布劳特氏菌或消化链球菌科菌),则其应被排除用作供体,特别是当体重减轻是提议的fmt过程中的一个目标时。
10.在相关的方面,提供了提高fmt效力的方法,所述方法包括于fmt之前将有效量的表1a、4、6a、10b、11或15中所示的一种或多种细菌引入旨在用于移植的组合物中。在一些实施方案中,在引入步骤之后,表1a、4、6a、10b、11或15中所示的一种或多种细菌中的每种的水平为大于组合物中的总细菌的0.1%。在一些实施方案中,方法还包括使用组合物进行fmt的步骤。在一些实施方案中,方法还包括在组合物中引入有效量的抑制表1b、6b或10a中所示的一种或多种细菌的生长的抗细菌剂的步骤。在一些实施方案中,在引入步骤之后,表1b、6b、10a中所示的一种或多种细菌中的每种的水平为小于组合物中的总细菌的0.01%。在一些实施方案中,方法还包括使用组合物进行fmt的步骤。
11.在另一相关的方面,提供了通过在fmt之前给予fmt受体有效量的抑制表1b、6b或10a中所示的一种或多种细菌的生长的抗细菌剂,而提高fmt效力的方法。在一些实施方案中,在给予抗细菌剂之前确定来自fmt受体的粪便样品中的表1b、6b或10a中所示的一种或多种细菌的水平。在一些实施方案中,在给予抗细菌剂之后确定来自fmt受体的粪便样品中的表1b、6b或10a中所示的一种或多种细菌的水平。在一些实施方案中,方法还包括在fmt之前给予受体有效量的能减少在fmt之前取自受体的粪便样品中的总细菌载荷的试剂的步骤。
12.在又一相关的方面,提供了试剂盒,其包含:(1)包含供体粪便的第一组合物;和(2)包含以下物质的第二组合物:(i)有效量的表1a、4、6a、10b、11、15或16中所示的一种或多种细菌;或(ii)有效量的抑制表1b、6b或10a中所示的一种或多种细菌的生长的抗细菌剂。在一些实施方案中,第一组合物包含已被干燥、冷冻并放入用于口服的胶囊中的供体粪
便。在一些实施方案中,试剂盒还包含在第二组合物中的有效量的抑制表1b、6b或10a中所示的一种或多种细菌的生长的抗细菌剂,或在第三组合物中的有效量的减少总细菌载荷的抗细菌剂。另外,试剂盒可以包含印刷的说明书来指导用户正确地使用试剂盒。
13.在一些实施方案中,在上述方法中,通过定量聚合酶链式反应(pcr)确定表1a、1b、4、6a、6b、10a、10b、11或15中所示的一种或多种细菌的水平。
14.在第二方面,本发明提供了鉴定合适的fmt供体的方法。方法包括确定获自候选者的粪便样品中的表2、3a、5、7a或16中所示的一种或多种真菌的水平的步骤。在一些实施方案中,一种或多种真菌的水平为百分比相对丰度。在一些实施方案中,表2、3a、5、7a或16中所示的一种或多种真菌的水平为大于0.5%,并且候选者被鉴定为合适的fmt供体。在一些实施方案中,表3b或7b中所示的一种或多种真菌的水平为不大于0.05%。在一些实施方案中,方法还包括从用于fmt的合适的候选者获取粪便物质的步骤。在一些实施方案中,表3b或7b中所示的一种或多种真菌的水平为大于0.05%,并且候选者被鉴定为不合适的fmt供体。在一些实施方案中,方法还包括确定粪便样品中的总真菌载荷的步骤。
15.在一些实施方案中,确定获自第一候选者的第一粪便样品和获自第二候选者的第二粪便样品中的表2、3a、3b、5、7a、7b或16中所示的一种或多种真菌的水平。在一些实施方案中,第一候选者比第二候选者具有更高水平的表2、3a、5、7a或16中所示的一种或多种真菌,并被认为是比第二候选者更合适的fmt供体。在一些实施方案中,第一候选者比第二候选者具有更低水平的表3b或7b中所示的一种或多种真菌,并被认为是比第二候选者更合适的fmt供体。
16.在一个相关的方面,提供了提高fmt效力的方法,所述方法包括于fmt之前将有效量的表2、3a、5、7a或16中所示的一种或多种真菌引入旨在用于移植的组合物中。在一些实施方案中,在引入步骤之后,表2、3a、5、7a或16中所示的一种或多种真菌的水平为大于组合物中的总真菌的0.5%。在一些实施方案中,方法还包括使用组合物进行fmt的步骤。在一些实施方案中,方法还包括在组合物中引入有效量的抑制表3b或7b中所示的一种或多种真菌的生长的抗真菌剂的步骤。在一些实施方案中,在引入步骤之后,表3b或7b中所示的一种或多种真菌的水平为小于组合物中的总真菌的0.05%。在一些实施方案中,方法还包括使用组合物进行fmt的步骤。
17.在另一相关的方面,提供了提高fmt效力的方法,所述方法包括在fmt之前给予fmt受体有效量的抑制表3b或7b中所示的一种或多种真菌的生长的抗真菌剂。在一些实施方案中,在给予抗真菌剂之前确定来自fmt受体的粪便样品中的表3b或7b中所示的一种或多种真菌的水平。在一些实施方案中,在给予抗真菌剂之后确定来自fmt受体的粪便样品中的表3b或7b中所示的一种或多种真菌的水平。在一些实施方案中,方法还包括在fmt之前给予受体有效量的能减少在fmt之前取自受体的粪便样品中的总真菌载荷的试剂的步骤。
18.在又一相关的方面,提供了试剂盒,其包含:(1)包含供体粪便的第一组合物;和(2)包含以下物质的第二组合物:(i)有效量的表2、3a、5、7a或16中所示的一种或多种真菌;或(ii)有效量的抑制表3b或7b中所示的一种或多种真菌的生长的抗真菌剂。在一些实施方案中,第一组合物包含已被干燥、冷冻并放入用于口服的胶囊中的供体粪便。在一些实施方案中,试剂盒还包含在第二组合物中的有效量的抑制表3b或7b中所示的一种或多种真菌的生长的抗真菌剂,或在第三组合物种的有效量的减少总真菌载荷的抗真菌剂。另外,试剂盒
可以包含印刷的说明书以指导用户正确使用试剂盒。
19.在一些实施方案中,在上述方法中,通过定量聚合酶链式反应(pcr)确定表2、3a、3b、5、7a、7b或16中所示的一种或多种真菌的水平。
20.在第三个方面,本发明提供了鉴定合适的fmt供体的方法。所述方法包括确定获自候选者的粪便样品中的表8b中所示的一种或多种病毒的水平的步骤。在一些实施方案中,一种或多种病毒的水平为百分比相对丰度。在一些实施方案中,表8b中所示的一种或多种病毒的水平为大于0.1%,且候选者被鉴定为合适的fmt供体。在一些实施方案中,表8a中所示的一种或多种病毒的水平为不大于0.1%。在一些实施方案中,方法还包括从候选者获取粪便物质以用于fmt的步骤。在一些实施方案中,方法还包括从候选者获取粪便物质以用于fmt的步骤。在一些实施方案中,表8a中所示的一种或多种病毒的水平为大于0.1%,且候选者被鉴定为不合适的fmt供体。在一些实施方案中,方法还包括确定粪便样品中的总病毒载荷的步骤。
21.在一些实施方案中,确定获自第一候选者的第一粪便样品和获自第二候选者的第二粪便样品中的表8a或8b中所示的一种或多种病毒的水平。在一些实施方案中,第一候选者比第二候选者具有更高水平的表8b中所示的一种或多种病毒,且被认为是比第二候选者更合适的fmt供体。在一些实施方案中,第一候选者比第二候选者具有更低水平的表8a中所示的一种或多种病毒,且被认为是比第二候选者更合适的fmt供体。
22.在一个相关的方面,提供了提高fmt效力的方法。所述方法包括在fmt之前将有效量的表8b中所示的一种或多种病毒引入旨在用于移植的组合物中的步骤。在一些实施方案中,在引入步骤之后,表8b中所示的一种或多种病毒的水平为大于组合物中的总病毒的0.1%。在一些实施方案中,方法还包括使用组合物进行fmt的步骤。在一些实施方案中,方法还包括在组合物中引入有效量的抑制表8a中所示的一种或多种真菌的生长的抗真菌剂的步骤。在一些实施方案中,在引入步骤之后,表8a中所示的一种或多种真菌的水平为小于组合物中的总病毒的0.1%。在一些实施方案中,方法还包括使用组合物进行fmt的步骤。
23.在另一相关的方面,提供了提高fmt效力的方法,所述方法包括在fmt之前给予fmt受体有效量的抑制表8a中所示的一种或多种病毒的生长的抗病毒剂。在一些实施方案中,在给予抗病毒剂之前确定来自fmt受体的粪便样品中的表8a中所示的一种或多种病毒的水平。在一些实施方案中,在给予抗病毒剂之后确定来自fmt受体的粪便样品中的表8a中所示的一种或多种病毒的水平。在一些实施方案中,方法还包括在fmt之前给予受体有效量的能减少在fmt之前取自受体的粪便样品中的总病毒载荷的试剂的步骤。
24.在又一相关的方面,提供了试剂盒,其包含:(1)包含供体粪便的第一组合物;和(2)包含以下物质的第二组合物:(i)有效量的表8b中所示的一种或多种病毒;或(ii)有效量的抑制表8a中所示的一种或多种病毒的生长的抗病毒剂。在一些实施方案中,第一组合物包含已被干燥、冷冻并放入用于口服的胶囊中的供体粪便。在一些实施方案中,试剂盒还包含在第二组合物中的有效量的抑制表8a中所示的一种或多种病毒的生长的抗病毒剂,或在第三组合物中的有效量的减少总病毒载荷的抗病毒剂。另外,试剂盒可包含印刷的说明书以指导用户正确使用试剂盒。
25.在一些实施方案中,在上述方法中,通过定量聚合酶链式反应(pcr)确定表8a或8b中所示的一种或多种病毒的水平。
26.可用于fmt中的具有提高的效力的相关组合物可包含:(1)含有活的粪便微生物的供体粪便物质,和(2)抗细菌剂或抗真菌剂或抗病毒剂,其特异性抑制表1b、3b、6b、7b、8a或10a中所示的一种或多种细菌/真菌/病毒的生长或增殖,但对其他的细菌、真菌或病毒不显示这样的抑压性或抑制性效应。并非为广谱抗细菌剂、抗真菌剂或抗病毒剂,这样的特异性抗细菌剂、抗真菌剂、抗病毒剂可以为能够破坏表1b、3b、6b、7b、8a或10a中所示的一种或多种细菌、真菌或病毒的生命周期中的关键基因的表达的短多核苷酸性质(例如,小抑制性rna、微小rna、小rna、lncrna或反义寡核苷酸),其能够特异性地仅靶向这些物种,而不靶向其他密切相关的真菌。
27.另外,提供了用于治疗性应用的各种方法:例如,提供了用于对象体重减轻的方法,包括在对象的胃肠道中引入有效量的:(1)表1a中所示的一种或多种细菌,或(2)表2或3a中所示的一种或多种真菌的步骤。另一方面,提供了用于对象体重减轻的方法,包括在对象的胃肠道中引入有效量的抑制剂的步骤,其抑制:(1)表1b中所示的一种或多种细菌,或(2)表3b中所示的一种或多种真菌。在一些情形下,通过fmt的方式进行引入步骤。任选地,给予个体有效量的广谱抗细菌剂或抗真菌剂的步骤分别在引入有益细菌或真菌的步骤,如fmt进行之前进行。
28.同样,提供了抑制对象中的耐多药细菌的方法,包括在对象的胃肠道中引入有效量的:(1)表4或15中所示的一种或多种细菌,或(2)表5或16中所示的一种或多种真菌的步骤。在一些实施方案中,细菌为耐碳青霉烯的肠杆菌科(cre)。在一些实施方案中,细菌为耐万古霉素的肠球菌(vre)。在一些情形下,通过fmt的方式进行引入步骤。任选地,给予个体有效量的广谱抗细菌剂或抗真菌剂的步骤分别在引入有益细菌或真菌的步骤,如fmt进行之前进行。
29.此外,提供了治疗对象中的急性移植物抗宿主病(agvhd)的方法,包括在对象的胃肠道中引入有效量的:(1)表6a中所示的一种或多种细菌,或(2)表7a中所示的一种或多种真菌的步骤。另一方面,提供了治疗对象中的急性移植物抗宿主病(agvhd)的方法,包括在对象的胃肠道中引入有效量的抑制剂的步骤,其抑制:(1)表6b中所示的一种或多种细菌,或(2)表7b中所示的一种或多种真菌。在一些情形下,通过fmt的方式进行引入步骤。任选地,给予个体有效量的广谱抗细菌剂或抗真菌剂的步骤分别在引入有益细菌或真菌的步骤,如通过fmt进行之前进行。
30.另外,提供了治疗溃疡性结肠炎的方法,包括在对象的胃肠道中引入有效量的:(1)表10b中所示的一种或多种细菌,或(2)表8b中所示的一种或多种病毒的步骤。另一方面,提供了治疗溃疡性结肠炎的方法,包括在对象的胃肠道中引入有效量的抑制剂的步骤,其抑制:(1)表10a中所示的一种或多种细菌,或(2)表8a中所示的一种或多种病毒。在一些情形下,通过fmt的方式进行引入步骤。任选地,给予个体有效量的广谱抗细菌剂或抗病毒剂的步骤分别在引入有益细菌或病毒的步骤,如通过fmt进行之前进行。
31.此外,提供了治疗对象中的克罗恩病的方法,包括在对象的胃肠道中引入有效量的表11中所示的一种或多种真菌的步骤,例如,通过fmt的方式。任选地,给予个体有效量的广谱抗真菌剂的步骤在引入步骤,如通过fmt进行之前进行。
32.最后,提供了用于对象中的体重减轻的方法,包括在对象的胃肠道中引入有效量的华德萨特菌、肠道罗斯拜瑞氏菌或多酸光岗菌(mitsuokella multacida)中的任何一种、
两种或三种,例如,对象可接受所有三种,即有效量的华德萨特菌、肠道罗斯拜瑞氏菌和多酸光岗菌中的每种。还提供了减少对象中的总胆固醇和低密度脂蛋白胆固醇的方法,包括在对象的胃肠道中引入有效量的华德萨特菌、肠道罗斯拜瑞氏菌或多酸光岗菌中的任何一种、两种或三种,例如,对象可以接受所有三种,即有效量的华德萨特菌、肠道罗斯拜瑞氏菌和多酸光岗菌中的每种。该胆固醇降低方法可以在对象中独立于体重减轻,或与体重减轻同时实施。可以通过fmt的方式进行这些方法。任选地,在引入步骤如fmt进行之前进行给予对象有效量的广谱抗细菌剂如抗生素的步骤。对于在该方法中的应用,提供了包含有效量的华德萨特菌、肠道罗斯拜瑞氏菌或多酸光岗菌中的任何一种、两种或三种的组合物,例如,这样的组合物可以来源于供体粪便物质且已被干燥、冷冻并放入用于口服的胶囊中。
33.附图的简要说明
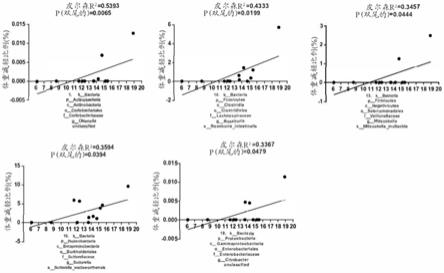
34.图1a通过相关性(线性回归)鉴定的用于诱导体重减轻的fmt供体中存在的“有利的”细菌。通过线性回归鉴定了5种物种与体重减轻呈正相关。这些物种提供在表1a中。图1b通过相关性(线性回归)鉴定的用于诱导体重减轻的fmt供体中存在的“不利的”细菌。从线性回归鉴定了17种物种与体重减轻呈负相关。这些物种提供在表1b中。图1c和1d通过lefse分析鉴定的用于诱导体重减轻的fmt供体中存在的“有利的”和“不利的”细菌。图1c使用中值作为截止点,lefse图显示在“有利的”和“较少有利的”供体中,丰度存在显著差异的细菌。图1d使用均值作为截止点,lefse图显示在“有利的”和“较少有利的”供体中,丰度存在显著差异的细菌。这些物种提供在表1a和表1b中。
35.图2用于诱导体重减轻的fmt供体中的“有利的”真菌。lefse图显示对照中的甜菜生尾孢(cercospora beticola)和纳加哈萨克斯坦酵母(kazachstania naganishii)的相对丰度比肥胖对象中的明显更高。这些物种提供在表2中。
36.图3与成功的和未成功的体重减轻相关的受体中的真菌。lefse图显示“体重减轻”或“非体重减轻”组中明显更高的真菌的相对丰度。这些物种提供在表3a和3b中。
37.图4a在横断面研究中鉴定的用于治疗cre的fmt供体中的“有利的”细菌。来自比较患有cre的患者和健康对照中的细菌特性的宏基因组测序的lefse分析的分类分支图。细菌特性与线性判别分析效应量(lefse)模型的比较。仅满足》2的线性判别分析(lda)阈值的分类被认为是显著的。健康对照中的33种物种(黑色)的相对丰度明显更高。这些物种提供在表4中。图4b在前瞻性的先导研究中鉴定的用于治疗cre的fmt供体中的“有利的”细菌。基于宏基因组测序比较fmt供体以及fmt之前的和fmt之后的受体中的细菌的分类特性。供体以及fmt之前的和fmt之后的受体的粪便样品中存在的细菌分类的相对丰度。r1和r2分别是指采自fmt受体1和2的粪便样品。柱通过字母d及后面的样品采集日进行标记,其中第一次fmt在第0天进行。这些物种提供在表4中。
38.图5在前瞻性的先导试验中鉴定的用于治疗cre的fmt的供体中的“有利的”真菌。基于宏基因组测序的fmt供体以及fmt之前的和fmt之后的具有cre的受体中的真菌的分类特性的比较。供体以及fmt之前的和fmt之后的受体的粪便样品中存在的真菌分类的相对丰度。r1和r2分别是指采自fmt受体1和2的粪便样品。柱通过字母d及随后的样品采集日进行标记,其中第一次fmt在第0天进行。选择的物种的详细的相对丰度显示在表5中。
39.图6a用于治疗急性移植物抗宿主病的fmt供体中的“有利的”和“不利的”细菌。基于宏基因组测序的fmt供体以及fmt之前的和fmt之后的患agvhd的受体中的细菌的分类特
性的比较。条形图表示来自供体以及fmt之前的和fmt之后的受体的粪便样品中的细菌分类的相对丰度。采自受体的粪便样品通过样品采集日进行标记,其中0表示第一次fmt的日期。来自用于fmt的供体的粪便样品标记为d4和d8。供体d8在不同的日期采集了5个样品。fmt之前在受体的肠细菌群落中由杰氏棒杆菌(corynebacterium jeikeium)(71.2%)占优,且其在第一次fmt之后大幅下降至《0.1%。在接受重复的fmt之后,在患者中观察到7种细菌的移植,且这些物种占据了患者细菌群落的较大比例。这些物种是alistipes onderdonkii、alistipes putredinis、鲍氏梭菌(clostridium bolteae)、系结梭菌(clostridium nexile)、共生梭菌(clostridium symbiosum)、未分类埃格特菌(eggerthella unclassified)、ruminococcus gnavu。这些物种在表6a和表6b中列出。图6b通过lefse分析鉴定的用于治疗急性移植物抗宿主病的fmt供体中的“有利的”和“不利的”细菌。lefse图显示了在患者具有腹泻或无腹泻时存在显著差异的4种细菌的相对丰度。在fmt之前和fmt之后,从患有agvhd的患者采集到总共22份粪便样品。根据患者在粪便采集日当天是否具有或不具有腹泻来对样品分类。腹泻定义为每天具有2次或更多次的排便(bowel opening),而非腹泻定义为每天具有0次或1次的排便。使用lefse分析来鉴定在来自“腹泻”或“非腹泻”组的粪便样品间存在显著差异的细菌。仅满足》2的lda阈值的分类被认为是显著的。腹泻组中的直肠真杆菌(eubacterium rectale)明显更高。非腹泻组中的alistipes putredinis、alistipes onderdonkii和哈撒韦梭菌(clostridium hathewayi)明显更高。这些物种在表6a和表6b中列出。
40.图7从热图鉴定的用于治疗agvhd的fmt供体中的“有利的”和“不利的”真菌。基于宏基因组测序的fmt供体以及fmt之前的和fmt之后的患agvhd的受体中的真菌的分类特性的比较。供体和fmt之前的和fmt之后的患agvhd的受体的粪便样品中存在的真菌分类的相对丰度。采自受体的粪便样品通过样品采集日进行标记,其中0表示第一次fmt的日期。来自用于fmt的供体的粪便样品标记为d4和d8。供体d8在不同的日期采集了5份样品。通过热图评估了在患有agvhd的患者fmt之后来自供体的真菌的移植。在患者fmt治疗之后移植了44种真菌。蓝色至红色色调表示如图例中所示的递增的相对丰度。图右侧的分类标记表示所指示的物种的标记。代表性的物种在表7a和7b中列出。
41.图8健康群体和患有uc的患者的粘膜之间的科、属和种水平上的差异病毒分类。通过具有fdr校正的deseq分析确定了健康和uc粘膜之间的差异性富集的病毒科(a)、属(b)和种(c)(仅显示了调整的p值《0.05且|log2(组间倍数变化)|》2的那些差异分类)。对于病毒分类名称,黑色的分类涂色表示原核病毒,而灰色的那些涂色表示真核病毒。对于病毒丰度箱形图,箱从第1四分位数延伸至第3四分位数(第25至第75百分位数),其中中值通过垂直线示出。这些分类在表8a和8b中列出。
42.图9健康群体和患有uc的患者中的粘膜病毒组肠型。图9a基于围绕中心点的划分(partition around medoids,pam)算法和主坐标分析(pcoa)的对来自健康群体和患有uc的患者的粘膜的病毒群落结构的病毒组肠型聚类。插图显示了每种肠型群体中的健康个体和uc对象的比率。图9b存在的对2种粘膜病毒组肠型的聚类有贡献的差异病毒的热图。通过协调性的(concordant)deseq和随机森林分析鉴定差别物种。病毒丰度根据log
10 rpkm值进行颜色加深。仅显示了通过deseq和随机森林算法协调性确定的效应量》2和fdr调整的p值《0.05的那些物种。这些物种在表9a和9b中列出。
43.图10uc粘膜中的改变的细菌微生物群。图10a对照和uc对象的粘膜中的基于辛普森多样性和chao1丰富度的细菌α多样性的比较。通过t检验确定统计显著性,*p《0.05,**p《0.01。对于箱形图,箱从第1四分位数延伸至第3四分位数(第25至第75百分位数),其中中值通过垂直线示出。将健康和uc粘膜中的细菌组成以门(b)、科(c)和属(d)水平上的相对丰度制图。e,通过具有fdr校正的lefse分析确定健康个体和uc对象的粘膜之间的差异富集的细菌分类。仅显示了调整的p值《0.05且lda效应量》2的那些分类。这些分类在表10a和10b中列出。
44.图11小鼠模型的研究时间线。对小鼠喂食高脂饮食1个月,然后喂食正常饮食1个月,并进行7天的抗生素处理。然后将小鼠分成3组,并经口服灌喂接受华德萨特菌、肠道罗斯拜瑞氏菌、多酸光岗菌、联合(以1*109cfu/ml的剂量)或培养基处理。
45.图12给予华德萨特菌显著减少了体重增加,而给予肠道罗斯拜瑞氏菌显示体重增加减少的趋势。在第15天后(在3次口服灌喂后)效应特别明显。缩写:sw-华德萨特菌;ri-肠道罗斯拜瑞氏菌
46.图13在第20天和第45天华德萨特菌和肠道罗斯拜瑞氏菌均减少了体重增加。体重增加减少在停止处理后持续20天(在第45天)。将第20天和第45天的体重与第0天进行比较,并提供为体重增加的百分比。缩写:sw-华德萨特菌;ri-肠道罗斯拜瑞氏菌
47.图14在给予联合、mm、ri和sw后平均食物摄取显示递减的趋势,这与仅给予培养基相反,其显示递增的趋势。食物摄取减少的效应在ri和sw中最为显著。平均食物摄取计算为克食物摄取/小鼠
·
天。
48.图15在15天后,相比给予培养基,给予联合、mm、ri和sw的小鼠中的平均食物效率减少。平均食物效率计算为每只小鼠的5天中的体重增加(克)/这5天中的总食物摄取(克)。
49.图16单独给予华德萨特菌减少了ldl-c、tc和tg。单独给予肠道罗斯拜瑞氏菌减少了ldl-c和tc。给予联合的华德萨特菌、肠道罗斯拜瑞氏菌和多酸光岗菌减少了ldl-c和tc。将第45天的所有结果均与给予培养基对照比较。缩写:sw-华德萨特菌;ri-肠道罗斯拜瑞氏菌;mm:多酸光岗菌;ldl-c:低密度脂蛋白胆固醇;tc:总胆固醇;tg:总甘油三酯。
50.图17供体和受体的样品采集时间线。示出了每个受体的cre的相对样品采集时间和结果。
51.图18fmt之前和fmt之后三个fmt受体及其相应的供体中的细菌瘤胃球菌(ruminococcus sp_5_1_39bfaa)、collinsella tanakaei和eubacterium sicaeum的相对丰度改变。瘤胃球菌(ruminococcus sp_5_1_39bfaa)、collinsella tanakaei和eubacterium sicaeum的相对丰度在fmt之前检测不到,且在fmt之后增加至与供体相似的水平或甚至更高。
52.图19比较fmt之前(黑色)和fmt之后(灰色)的细菌组成的lefse分析。示出了lda分数》2.0的显著不同的所有分类。
53.图20供体和受体的真菌组成的分析。(a)供体、受体和fmt之后的受体在不同时间的α多样性(香农多样性)。(b)受体的基于bray-curtis距离的主坐标分析(pcoa)。图显示了供体和cre受体之间的随时间的距离。(c)比较fmt之前(灰色)和fmt之后(黑色)的微生物组(mycobiome)组成的lefse分析。(d)显示fmt之前的和fmt之后的粪便样品中存在的显著占优的物种的热图。
54.定义
55.术语“粪便微生物群移植(fmt)”或“粪便移植”是指这样的医疗程序,其中将含有获自健康个体的活的粪便微生物(细菌、真菌、病毒等)的粪便物质转移到受体的胃肠道中以修复已被多种医学病况中的任何一种扰乱或破坏的健康肠微生物群。通常,首先将来自健康供体的粪便物质加工成适合移植的形式,这可以通过在下胃肠道中直接沉积,如通过结肠镜或通过鼻腔插管或通过口服含有处理过的(例如,干燥和冷冻的)粪便物质的封装物质来进行。fmt被用于治疗多种医学病况,包括肥胖、代谢综合征、胃肠疾病(如炎性肠病(ibd),包括溃疡性结肠炎(uc)和克罗恩病(cd))、耐抗生素菌感染(如艰难梭菌感染(cdi)或由包括耐碳青霉烯的肠杆菌科(cre)或耐万古霉素的肠球菌(vre)在内的耐多药生物体引起的病况),以及自闭症、抑郁症、肥胖、糖尿病、脱发、急性移植物抗宿主病(agvhd),并且还包括某些神经性病况,如多发性硬化症和帕金森氏病。
56.如本文中所用的术语“抑制(inhibiting)”或“抑制(inhibition)”是指对靶生物过程如靶基因的rna/蛋白表达、靶蛋白的生物学活性、细胞信号转导、细胞增殖等的任何可检测的负面影响。通常,抑制反映为当相比对照时,靶过程(例如,某些种类的微生物,例如,表1b、6b或10a中所示的细菌中的一种或多种;或表3b或7b中所示的真菌;或表8a中所示的病毒的生长或增殖),或上述的下游参数中的任一个的至少10%、20%、30%、40%、50%、60%、70%、80%、90%或更大的减少。“抑制”还包括100%的减少,即靶生物过程或信号的完全的清除或废除。其他相关的术语如“抑制(suppressing)”、“抑制(suppression)”、“减少(reducing)”和“减少(reduction)”在本公开中以类似的形式使用,是指不同水平的减少(例如,相比对照水平至少10%、20%、30%、40%、50%、60%、70%、80%、90%或更多的减少),直至完全清除靶生物过程或信号。另一方面,术语如“激活(activate)”、“激活(activating)”、“激活(activation)”、“增加(increase)”、“增加(increasing)”、“促进(promote)”、“促进(promoting)”、“提高(enhance)”、“提高(enhancing)”或“提高(enhancement)”在本公开中用于包括靶过程或信号的不同水平的正变化(例如,相比对照水平,例表1a、4、6a、10b、11或15中所示的细菌,或表2、3a、5、7a或16中所示的真菌,或表8b中所示的病毒中的一种或多种的对照水平,至少10%、20%、30%、40%、50%、60%、70%、80%、90%、100%、200%或更大,如3、5、8、10、20倍的增加)。
57.术语“抗细菌剂/抗真菌剂/抗病毒剂”是指能够分别抑制、压抑或防止细菌、真菌或病毒,特别是表1b、3b、6b、7b、8a和10a中所示的那些的生长或增殖的任何物质。已知的具有抗细菌活性的试剂包括广泛地抑制广谱的细菌的增殖的各种抗生素以及能够抑制特定细菌的增殖的诸如反应寡核苷酸、小抑制性rna的试剂。术语“抗细菌剂/抗真菌剂/抗病毒剂”类似地定义为包括分别具有杀死几乎所有细菌、真菌或病毒的广谱活性的试剂,以及分别特异性地抑制靶细菌、真菌或病毒的增殖的试剂。
58.当在描述分别与所有细菌或真菌或病毒有关的特定细菌或真菌或病毒(例如,表1-11中任一个中所示的那些中的任一种)的上下文中使用,在相同的环境中出现时,“百分比相对丰度”是指以百分比形式表示的细菌或真菌或病毒在所有细菌或真菌或病毒的量中的相对量。例如,可以通过比较一个给定样品中该物种特异性的dna的量(例如,通过定量聚合酶链式反应确定的)与相同样品中的所有真菌dna的量(例如,通过基于内部转录间隔子2或its2序列的定量聚合酶链式反应(pcr)和测序确定的),来确定一种特定真菌的百分比相
对丰度。
59.当在描述粪便中特定细菌或真菌或病毒(例如,表1-11、15和16中所示的那些中的任一种)的存在的上下文中使用时,“绝对丰度”是指粪便样品中的所有dna的量中,分别来源于细菌或真菌或病毒的dna的量。例如,可以通过比较一个给定样品中该真菌特异性的dna的量(例如,通过定量pcr确定的)与相同样品中的所有粪便dna的量来确定一种真菌的绝对丰度。
60.如本文中所用的粪便样品的“总细菌/真菌/病毒载荷”分别是指粪便样品中的所有dna的量中,所有细菌/真菌/病毒dna的量。例如,可以通过比较一个给定样品中的真菌特异性的dna的量(例如,通过定量pcr确定的18s rdna)与相同样品中的所有粪便dna的量,来确定真菌的绝对丰度。
61.如本文中所用的术语“有效量”是指产生所需效应的物质的量(例如,对使用或给予物质(例如,抗细菌剂)的一种或多种有害细菌或真菌或病毒(例如,表1b、6b或10a中所示的细菌)的生长或增殖的抑制性或压抑性效应。所述效应包括以任何可检测的程度防止、抑制或延迟细菌/真菌/病毒增殖过程中的任何相关的生物过程。准确的量将取决于物质(活性剂)的性质、使用/给予的方式以及施用的目的,并且将由本领域技术人员使用已知的技术以及本文中描述的那些来确定。在另一情形下,当在旨在用于fmt的组合物中人为引入“有效量”的一种或多种有益细菌或真菌或病毒(例如,表1a、2、3a、4、5、6a、7a、8b、10b、11、15或16中列出的那些)时,其意指引入的相关细菌/真菌/病毒的量足以赋予fmt受体健康益处,如体重减轻、提高的对胰岛素的敏感性、降低的血液胆固醇水平、耐药细菌感染的抑制,和/或急性移植物抗宿主病(agvhd)和gi道疾病如ibd的减轻。
62.如本文中所用的,术语“约”表示这样的值范围,即指定值的+/-10%。例如,“约10”表示9-11(10+/-1)的值范围。
63.发明详述
64.i.引言
65.本发明提供了在方案进行之前评估有效fmt的可能性以及在为受体赋予某些健康益处方面提高fmt程序的效力的新的方法。在其研究中,本发明人发现受体的胃肠道和供体的粪便中的某些细菌、真菌和病毒的存在和相对丰度均与fmt的结果直接相关。例如,发现表1a、4、6a、10b、11或15中所示的细菌的存在(特别是在升高的水平下),为fmt受体赋予了健康益处,而表1b、6b或10a中所示的细菌的存在(特别是在升高的水平下),倾向于不利地影响fmt结果。类似地,已经鉴定了某些真菌和病毒的存在和相对丰度与所需的fmt结果相关。因此,潜在供体的粪便中的诸表1a、2、3a、4、5、6a、7a、8b、10b、11、15或16中所示的那些的一种或多种“有益的”细菌/真菌/病毒的检测(特别是在升高的水平下),另一方面,诸表1b、3b、6b、7b、8a、10a或16中所示的那些的一种或多种“有害的”细菌/真菌/病毒的检测(特别是在升高的水平下),可用于指导供体选择,而fmt受体中的这些相关的细菌/真菌/病毒水平的分析可以确定对象是否直接准备好进行fmt,或者应当在fmt之前用抑制这样的不需要的微生物的抗细菌/真菌/病毒剂处理以优化治疗结果。ii.fmt供体/受体选择和准备
66.患有cdi,特别是复发性cdi的患者通常被认为是fmt治疗的受体。除cdi以外,其他的疾病和病况,包括消化系统或神经系统的那些,如结肠炎、肠易激综合征(ibs)、克罗恩病、急性移植物抗宿主病(agvhd)、由耐多药细菌如cre或vre引起的感染、多发性硬化症、帕
金森氏病、糖尿病和肥胖症,也适合进行fmt治疗。
67.fmt中使用的粪便物质获自健康供体,然后将其加工成适当的形式,以用于即将到来的fmt程序中的预期递送方式。直到最近,fmt供体的一般标准一直很简单,即供体为健康的个体,无任何已知的疾病或病症,特别是在消化道中,尽管通常优先考虑与受体同一家庭的成员。
68.本发明人在其研究中已发现受体的胃肠道或供体粪便(其在处理后被用于移植)中的一种或多种“有益的”细菌,表1a中所示的那些的升高的存在,在患者fmt治疗后可以赋予显著的健康益处,如受体中的体重减轻、提高的胰岛素敏感性、降低的血液/血清/血浆胆固醇水平。相反,当在受体的gi道或在用于fmt的供体粪便中发现其他“有害的”细菌,表1b中所示的那些的升高的存在时,在fmt治疗后不会赋予这样的健康益处。类似地,用于fmt的受体的胃肠道或供体粪便中的一种或多种“有益的”真菌,表2或3a中所示的那些的升高的存在,在fmt治疗后可以在患者中赋予相同的或相似的健康益处,而当在fmt之后受体的gi道或在用于fmt的供体粪便中发现“有害的”真菌,表3b中所示的那些的升高的存在时,不会获得这样的健康益处。
69.该启示使得能够初步筛选作为合适的fmt供体的个体,以及初步筛选作为成功的和有益的fmt治疗的可能候选者的患者,特别是在治疗肥胖症或代谢综合征,包括胰岛素不敏感和/或ii型糖尿病的情形下:如果候选供体的粪便含有最低或升高水平的表1a中所示的任何一种或多种细菌(例如,每种为大于总细菌的0.1%、0.2%、0.4%、0.6%、0.8%、1%、1.2%、1.5%、1.8%或2%),则候选者被认为适合作为fmt供体,且其粪便可以直接取回用于处理及随后用于fmt;另一方面,如果候选者的粪便样品显示无或仅低水平的这些有益细菌(例如,每种为不大于总细菌的0.1%、0.2%、0.4%、0.6%、0.8%、1%、1.2%、1.5%、1.8%或2%),则候选者被认为不是直接合适的fmt供体,且其粪便物质不应在可能的应用之前不进行必要的调整的情况下而被采集以用于fmt。在处理用于fmt之前改善供体粪便物质的一种可能的方式是人为引入一种或多种有益细菌(例如,表1a中的那些),以便增加这样的细菌在用于fmt的粪便物质中的存在(例如,每种物种为大于总细菌的0.1%、0.2%、0.4%、0.6%、0.8%、1%、1.2%、1.5%、1.8%或2%)。
70.相反,发明人也已揭示出用于fmt的粪便物质中的某些不需要的或有害的细菌,包括表1b中所示的那些中的一种或多种的缺失或减少的存在,在fmt治疗后倾向于在患者中产生显著的健康益处,如受体中的体重减轻、提高的胰岛素敏感性、降低的血液/血清/血浆胆固醇水平。因此,如果候选供体的粪便样品已经测试并显示含有减少的或检测不到的表1b中所示的一种或多种细菌水平(例如,每种为不大于总细菌的0.02%、0.04%、0.06%、0.08%、0.1%、0.2%、0.4%或0.5%),则个体被认为是合适的供体,且其粪便样品可以直接采集并处理用于fmt。另一方面,如果作为潜在供体的个体的粪便已经测试且发现其中含有表1b中所示的一种或多种细菌的大量存在(特别是以升高的水平)(例如,每种为大于总细菌的0.02%、0.04%、0.06%、0.08%、0.1%、0.2%、0.4%或0.5%),则其被认为不适合作为用于fmt的粪便物质的供体,因此其粪便样品不应被采集以用于fmt。
71.理想地,从供体粪便物质制备的且旨在用于治疗肥胖症或代谢综合征或ii型糖尿病的fmt的所需的fmt组合物具有高水平的一种或多种有益细菌(例如,表1a中所示的那些)和低水平的一种或多种有害的细菌(例如,表1b中所示的那些)。因此,虽然可以对旨在用于
fmt的组合物进行改善以分别解决有益细菌的水平不足和有害细菌的过量存在的问题,但一种可能的改善方式是增加一种或多种有益细菌(例如,表1a中所示的那些)的水平,例如,通过补充旨在用于fmt的转移物质或通过在受体的gi道中直接引入足量的此类有益细菌,任选地在同时抑制一种或多种有害的细菌(例如,表1b中所示的那些)的水平,以将受体从fmt程序可能获得的潜在健康益处最大化。
72.在有关fmt受体的范围内,如果患者被提议接受针对肥胖症或代谢综合征或ii型糖尿病的fmt治疗,并且其粪便样品显示升高的表1b中所示的一种或多种有害的细菌水平(例如,每种为大于0.02%、0.04%、0.06%、0.08%、0.1%、0.2%、0.4%或0.5%的总细菌),则患者可被认为不适合立即接受fmt,因为治疗可能具有减少的产生健康益处,如减少的体重、增加的胰岛素敏感性、减少的血液胆固醇的机会。患者可以在开始fmt治疗之前首先接受抗细菌剂处理以减少其胃肠道中的有害的细菌,特别是表1b中所示的那些的水平,其间患者将接受富集了一种或多种有益细菌(表1a中所示的那些)和/或具有抑制的一种或多种有害的细菌水平(例如,表1b中所示的那些)的供体粪便物质。另一方面,如果被提议接受fmt治疗的患者不具有表1b中所示的任何一种或多种细菌的大量的存在,特别是升高的存在(例如,每种为不大于总细菌的0.02%、0.04%、0.06%、0.08%、0.1%、0.2%、0.4%或0.5%),则患者可以立即开始fmt治疗,而无需进行其他的准备或预处理步骤。
73.另外,发明人还鉴定了用于针对肥胖症或代谢综合征或ii型糖尿病的fmt治疗的“有益的”和“有害的”真菌,这可以指导以与上述相同的方式选择合适的fmt供体和受体:例如,从供体粪便物质制备的且旨在用于治疗肥胖症或代谢综合征或ii型糖尿病的fmt的所需的fmt组合物具有升高的一种或多种有益的真菌水平(例如,表2或3a中所示的那些,每种为不小于总真菌的0.5%、1%、1.5%、2%、2.5%、3%、3.5%、4%、4.5%、5%、5.5%、6%、6.5%、7%、7.5%、8%、8.5%、9%、9.5%、10%、11%、12%、13%、14%或15%)和/或较低的一种或多种有害的细菌水平(例如,表3b中所示的那些,每种为不大于总真菌的0.05%、0.1%、0.2%、0.3%、0.4%、0.5%、0.6%、0.7%、0.8%、0.9%、1%、1.5%、2%、2.5%、3%或3.5%)。此外,可以进行针对fmt供体/供体粪便物质或受体的准备,以操纵有益真菌的水平(引起增加)和/或有害的真菌的水平(引起减少),以便将来自fmt程序的健康益处优化,这类似于上述的fmt之前有益和/或有害的细菌的操纵。
74.在用于抑制或根除耐多药细菌如耐碳青霉烯的肠杆菌科(cre)和耐万古霉素的肠球菌(vre)的fmt治疗的情形下,发明人已鉴定了“有益的”细菌和真菌,当其在fmt供体粪便中以升高的水平存在时,允许程序实现提高的治疗效力。这些细菌和真菌分别在表4和5中示出。从供体粪便物质制备的且旨在用于治疗耐多药细菌的fmt的所需的fmt组合物具有升高的一种或多种有益细菌或真菌水平(例如,表4、5、15或16中所示的那些,每种为不小于总细菌或总真菌的0.02%、0.05%、0.1%、0.5%、1%、1.5%、2%、2.5%或3%)。此外,可以进行针对fmt供体/供体粪便物质或受体的准备以操纵有益细菌或真菌的水平(引起增加),以便将来自fmt程序的效力和健康益处最大化,这类似于上述的fmt之前有益细菌的操纵,例如,通过在待用于fmt的转移物质中或直接向受体的gi道人为引入添加的和有效量的表4、5、15或16的一种或多种“有益的”细菌和/或真菌。
75.在用于细胞或组织移植相关的病况如急性移植物抗宿主病(agvhd)的fmt治疗的情形下,发明人已鉴定了某些“有益的”细菌和真菌,当其在fmt治疗之后在受体的粪便中以
升高的水平存在时,与提高的治疗性效力有关。这些细菌和真菌分别在表6a和7a中示出。另一方面,还鉴定了某些“有害的”细菌和真菌,参见表6b和7b。其在fmt治疗之后在受体的粪便中以升高的水平存在,这与减少的或不足的治疗性结果有关。因此,当选择潜在的fmt供体时,对于相比平均水平(例如,大于总细菌或总真菌的0.1%、0.2%、0.5%、0.8%、1%、1.5%、2%、2.5%、3%、3.5%、4%、4.5%、5%、5.5%、6%、6.5%、7%、7.5%、8%、8.5%、9%、9.5%、10%、11%、12%、13%、14%或15%)或在另一潜在供体的粪便样品中发现的相应水平,其粪便样品含有升高的任何一种或多种“有益的”细菌和/或真菌(表6a或7a中所示的)水平的供体,其将被认为是更合适的供体。相反,合适的供体在其粪便样品中还应具有较低水平的一种或多种或所有表6b或7b中所示的“有害的”细菌和/或真菌。此外,可以进行针对fmt供体/供体粪便物质或受体的准备,以操纵有益细菌或真菌的水平(引起增加)和/或有害的细菌或真菌的水平(引起减少),以便将来自fmt程序的效力和健康益处最大化,这类似于上述的在fmt之前有益细菌的操纵,例如,通过在待用于fmt的转移物质中或直接向受体的gi道人为引入添加的和有效量的表6a或7a的一种或多种“有益的”细菌和/或真菌。可以应用在fmt之后抑制,特别是特异性抑制受体的gi道中的一种或多种或所有表6b或7b中所示的有害的细菌和/或真菌的方式,以增加治疗效力或益处。
76.在gi道病症或病况如炎性肠病(ibd),特别是溃疡性结肠炎(uc)的情形下,发明人已鉴定了某些细菌和病毒,其存在,特别是以升高的水平存在,与疾病的存在相关联。这些细菌和病毒分别在表8a和10a中示出。另一方面,还鉴定了某些其他的细菌和病毒,分别参见表8b和10b,相比健康对比物,已在患有疾病的个体中观察到其缺失或以降低的水平存在。因此,这些特定的细菌和病毒可用于指导为提供用于治疗gi病症如ibd(其包括uc和cd)的物质的目的的fmt供体挑选:较低水平的表8a或10a中所示的一种或多种细菌和/或病毒倾向于指示候选者适合作为fmt供体。相反,较高水平的表8b或10b中所示的一种或多种细菌和/或病毒倾向于指示候选者适合作为fmt供体。此外,对于在其粪便样品中的表8a或10a中所示的一种或多种细菌和/或病毒的水平低于在另一候选者的粪便样品中发现的相应的水平的一个潜在供体,其将被认为是比第二候选者更合适的供体。另一方面,当一个潜在的供体在其粪便样品中的表8b或10b中所示的一种或多种细菌和/或病毒的水平高于在另一候选者的粪便样品中发现的相应的水平时,其将被认为是比第二候选者更合适的供体。例如,为引入另外的和有效量的表8b和10b中所示的一种或多种细菌和病毒,或为减少fmt物质和/或受体的gi道中的表8a和10a中所示的细菌和病毒的量,可以使用对fmt物质和/或受体的gi道中这些相关的细菌和/或病毒的进一步的操纵,以提高用于治疗ibd,特别是uc的fmt治疗策略的治疗效应。
77.在gi道病症或病况如克罗恩病(cd)(其为另一种类型的炎性肠病(ibd))的fmt治疗的情形下,发明人已鉴定了某些“有益的”细菌,当其在fmt供体粪便中以升高的水平存在时,允许程序实现提高的治疗效力。这些细菌示出在表11中。从供体粪便物质制备的且旨在用于治疗cd的fmt的所需的fmt组合物具有升高的一种或多种有益细菌水平(例如,表11中所示的那些,每种达到不小于总细菌的0.1%、0.2%或0.5%)。此外,可以进行针对fmt供体/供体粪便物质或受体的准备,以操纵一种或多种有益细菌的水平(引起增加),以便将来自fmt程序的效力和健康益处最大化,这类似于上述的在fmt之前有益细菌的操纵,例如,通过在待用于fmt的转移物质中或直接向受体的gi道人为引入添加的和有效量的表11的一种
或多种“有益的”细菌。
78.在文献中已报道了各种用于确定样品中的所有细菌或真菌或病毒的水平的方法,例如,利用通常共有的16s rdna细菌序列中的序列相似性的细菌多核苷酸序列扩增(例如,通过pcr)和测序。另一方面,可以通过对其独特基因组序列的扩增和测序来确定任何给定细菌的水平。百分比丰度常被用作指示细菌在给定环境中的相对水平的参数。
79.iii.利用有益微生物的治疗方法
80.本发明人的发现揭示了(1)个体的粪便或gi道或者来源于用于fmt的供体粪便的转移物质中的某些“有益的”细菌(例如,表1a、4、6a、10、11或15中所示的那些)、“有益的”真菌(例如,表2、3a、5、7a或16中所示的那些)、“有益的”病毒(例如,表8b中所示的那些),或者某些“有害的”细菌(例如,表1b、6b或10a中所示的那些)、“有害的”真菌(例如,表3b或7b中所示的那些)、“有害的”病毒(例如,表8a中所示的那些),与(2)疾病的存在/不存在或通过fmt治疗的方式向fmt受体赋予的显著的健康益处,如体重减轻、提高的胰岛素敏感性、降低的血液胆固醇水平、耐多药细菌如cre和vre的抑制、某些病症如agvhd、uc或cd的减轻的存在/缺失,之间存在着直接的相关性。该发现不仅允许设计初步的筛选过程来鉴定合适的供体和受体以获得来自fmt程序的治疗效力和/或健康益处,其还使得能够进行不同的方法,通过在fmt之前调节(增加或降低)供体粪便物质和受体中的如这里的表中所示的一种或多种有益的或有害的细菌、真菌或病毒的水平,来提高或优化fmt程序所赋予的潜在健康益处。
81.如上述章节中所论述的,当候选供体的粪便经测试且发现其中含有升高的诸表1b、3b、6b、7b、8a或10a中所示的那些的一种或多种有害的细菌或真菌或病毒水平(例如,每种物种分别为大于粪便样品中的总细菌、总真菌或总病毒的0.01%、0.02%、0.05%、0.1%、0.5%、1%、1.5%、2%、2.5%、3%或3.5%)时,候选者被认为不适合作为fmt供体,且其粪便不应被采集以用于fmt而不进行预处理或改善,因为如果不进行改善,这样的粪便物质不可能对fmt治疗的受体产生健康益处,如体重减轻、增加的胰岛素敏感性或降低的血液胆固醇、耐多药细菌的清除、agvhd、uc或cd的减轻。类似地,当提议的fmt供体其粪便经测试且发现其中含有不足的诸表1a、2、3a、4、5、6a、7a、8b、10b、11、15或16中所示的那些的一种或多种有益细菌或真菌或病毒水平(例如,每种为小于粪便样品中的总细菌、总真菌或总病毒的0.1%、0.2%、0.3%、0.4%、0.5%、1%、1.5%、2%、2.5%、3%、3.5%、4%、4.5%、5%、5.5%、6%、6.5%、7%、7.5%、8%、8.5%、9%、9.5%、10%、11%、12%、13%、14%或15%)时,所提议的供体被认为是旨在赋予健康益处,如体重减轻、对胰岛素反应敏感、降低的血液胆固醇水平、耐多药细菌的清除和agvhd、uc或cd的减轻的不合适的fmt供体,且其粪便物质不应被直接用于fmt,这是由于缺少赋予这样的有益健康效应的前景,除非对粪便物质进行充分的改善。在预期缺少来自fmt治疗的健康益处的这些情形下,可以基于本发明人的发现容易地进行改善,例如,可改善来自供体的粪便物质,以增加一种或多种有益细菌的水平(例如,通过引入额外量的此类细菌的方式将表1a、4、6a、10b、11或15中所示的一种或多种细菌的水平增加至大于总细菌的0.1%、0.2%、0.4%、0.6%、0.8%、1%、1.2%、1.5%、1.8%、2%、2.5%、3%、3.5%或4%),和/或降低一种或多种有害的细菌的水平(例如,通过使用此类细菌的特定抑制剂的方式将表1b、6b或10a中所示的一种或多种细菌的水平减少至小于总细菌的0.01%、0.02%、0.04%、0.05%、0.06%、0.08%、0.1%、0.2%、
0.3%、0.4%或0.5%)。可以采用具有类似预期目标的预处理方案来准备不久将接受fmt治疗的患者,以将其获得诸如上文和本文中所述的那些的健康益处的可能性最大化。
82.首先,对于已被考虑接受fmt但由于在其粪便样品中发现了升高的表1b、3b、6b、7b、8a或10a中所示的一种或多种有害的细菌或真菌或病毒水平(这指示减少的有益fmt结果机会)也已被认为是不合适的fmt受体的患者,可以在开始fmt之前采取措施来降低此类细菌或真菌或病毒的水平,以便可以获得fmt程序的大得多的实现有益结果的机会。例如,通常或具体而言,在开始旨在用于治疗肥胖症/患者体重操纵或用于治疗代谢综合征或用于治疗ii型糖尿病的fmt程序之前,可以给予患者有效量的能够抑制表1b中所示的细菌的生长或增殖的抗细菌剂,以便患者的消化道和粪便中的此类有害的细菌的水平被显著降低(例如,每种为不大于总细菌的0.01%、0.02%、0.04%、0.05%、0.06%、0.08%、0.1%、0.2%、0.3%、0.4%或0.5%)。类似地,通常或具体而言,在开始旨在用于治疗肥胖症/患者体重操纵或用于治疗代谢综合征或用于治疗ii型糖尿病的fmt程序之前,可以给予患者有效量的能够抑制表3b中所示的真菌的生长或增殖的抗真菌剂,以便患者的消化道和粪便中的此类有害的真菌的水平被显著降低(例如,每种为不大于总真菌的0.05%、0.1%、0.2%、0.3%、0.4%、0.5%、0.6%、0.7%、0.8%、0.9%、1%或1.5%)。
83.对于agvhd的治疗,通常或具体而言,在开始旨在用于治疗agvhd的fmt程序之前,可以给予患者有效量的能够抑制表6b中所示的细菌的生长或增殖的抗细菌剂,以便患者的消化道和粪便中的此类有害的细菌的水平被显著降低(例如,每种为不大于总细菌的0.01%、0.02%、0.03%、0.04%、0.05%、0.06%、0.07%、0.08%、0.09%或0.1%)。类似地,通常或具体而言,在开始旨在用于治疗agvhd的fmt程序之前,可以给予患者有效量的能够抑制表7b中所示的真菌的生长或增殖的抗真菌剂,以便患者的消化道和粪便中的此类有害的真菌的水平被显著降低(例如,每种为不大于总真菌的0.01%、0.02%、0.03%、0.04%、0.05%、0.06%、0.07%、0.08%、0.09%或0.1%)。
84.对于溃疡性结肠炎(uc)的治疗,通常或具体而言,在开始旨在用于治疗uc的fmt程序之前,可以给予患者有效量的能够抑制表8a中所示的病毒的生长或增殖的抗病毒剂,以便患者的消化道和粪便中的此类有害的细菌的水平被显著降低(例如,每种为不大于总病毒的0.01%、0.02%、0.05%或0.1%)。类似地,通常或具体而言,在开始旨在用于治疗uc的fmt程序之前,可以给予患者有效量的能够抑制表10a中所示的细菌的生长或增殖的抗细菌剂,以便患者的消化道和粪便中的此类有害的细菌的水平被显著降低(例如,每种为不大于总细菌的0.01%、0.02%、0.05%或0.1%)。
85.为此目的,在其fmt程序之前将至少两次测定患者的有害的细菌或真菌或病毒的水平:一次在初始筛选阶段,第二次在初始水平被认为对有益fmt结果而言太高之后以及在已给予患者抗细菌剂之后。一旦证实有害的细菌或真菌或病毒的水平降低至将允许令人满意的fmt结果的水平或百分比,即表示患者已准备好接受fmt治疗。
86.其次,对于由于在其粪便中低水平的诸表1a、2、3a、4、5、6a、7a、8b、10b、11、15或16中所示的那些的一种或多种有益细菌或真菌或病毒而已被认为不适合用作fmt供体的候选者,其可能作为供体是不合格的,而更偏向于粪便样品显示更有利的细菌、真菌或病毒特性的另一个体。在该替代选择中,其粪便物质可能仍被使用,且预期的不令人满意的fmt结果可以通过在供体粪便物质中补充有效量的有益细菌或真菌或病毒来进行补救。例如,可以
在其被处理以用于治疗肥胖症或代谢综合征或ii型糖尿病的fmt之前,从外部来源向供体粪便物质中引入表1a中所示的一种或多种细菌,以便增加粪便物质中的细菌水平(例如,达到粪便物质中的总细菌的至少0.1%、0.2%、0.3%、0.4%、0.5%、0.6%、0.7%、0.8%、0.9%、1%、1.2%、1.4%、1.5%、1.6%、1.7%、1.8%或2%)。类似地,可以在其被处理以用于治疗肥胖症或代谢综合征或ii型糖尿病的fmt之前,从外部来源向供体粪便物质中引入表2或3a中所示的一种或多种真菌,以便增加粪便物质中的真菌水平(例如,达到粪便物质中的总真菌的至少0.5%、0.6%、0.7%、0.8%、0.9%、1%、1.5%、2%、2.5%、3%、3.5%、4%、4.5%、5%、5.5%、6%、6.5%、7%、7.5%、8%、8.5%、9%、9.5%或10%)。
87.在根除耐多药细菌如cre或vre的情形下,可以在其被处理以用于fmt之前,从外部来源向供体粪便物质中引入表4或15中所示的一种或多种细菌,以便增加粪便物质中的细菌水平(例如,达到粪便物质中的总细菌的至少0.1%、0.2%、0.5%、0.8%、1%、1.5%、2%、2.5%或3%)。类似地,可以在其被处理以用于fmt之前,从外部来源向供体粪便物质中引入表5或16中所示的一种或多种真菌,以便增加粪便物质中的真菌水平(例如,达到粪便物质中的总真菌的至少0.01%、0.02%、0,05%或0.1%)。
88.在治疗agvhd的情形下,可以在其被处理以用于fmt之前,从外部来源向供体粪便物质中引入表6a中所示的一种或多种细菌,以便增加粪便物质中的细菌水平(例如,达到粪便物质中的总细菌的至少0.1%、0.2%、0.3%、0.4%、0.5%、0.6%、0.7%、0.8%、0.9%、1%、1.5%、2%、2.5%、3%、3.5%或4%)。类似地,可以在其被处理以用于fmt之前,从外部来源向供体粪便物质中引入表7a中所示的一种或多种真菌,以便增加粪便物质中的真菌的水平(例如,达到粪便物质中的总真菌的至少0.1%、0.2%、0.5%、0.8%、1%、1.5%、2%、2.5%、3%、3.5%、4%、4.5%、5%、5.5%、6%、6.5%、7%、7.5%、8%、8.5%、9%、9.5%、10%、11%、12%、13%、14%或15%)。
89.在治疗溃疡性结肠炎(uc)的情形下,可以在其被处理以用于fmt之前,从外部来源向供体粪便物质中引入表10b中所示的一种或多种细菌,以便增加粪便物质中的细菌水平(例如,达到粪便物质中的总细菌的至少0.1%、0.2%或0.5%)。类似地,可以在其被处理以用于fmt之前,从外部来源向供体粪便物质中引入表8b中所示的一种或多种病毒,以便增加粪便物质中的病毒水平(例如,达到粪便物质中的总病毒的至少0.1%、0.2%或0.5%)。
90.在治疗克罗恩病(cd)的情形下,可以在其被处理以用于fmt之前,从外部来源向供体粪便物质中引入表11中所示的一种或多种细菌,以便增加粪便物质中的细菌水平(例如,达到粪便物质中的总细菌的至少0.1%、0.2%或0.5%)。
91.相反,对于由于在其粪便中较高水平的诸表1b、3b、6b、7b、8a或10a中所示的那些的一种或多种有害细菌或真菌或病毒而已被认为不适合用作fmt供体的候选者,其作为供体可能是不合格的,而更偏向于粪便样品显示更有利的细菌特性的另一个体。在该替代选择中,其粪便物质仍可以被使用,且预期的不令人满意的fmt结果可通过用有效量的能够分别抑制此类有害的细菌或真菌或病毒的生长或增殖的抗细菌剂或抗真菌剂或抗病毒剂处理候选供体或其粪便物质来补救,可以以与上文和本文中所述的工作基本上相同的方式给予,以抑制或清除受体的gi道中的不需要的细菌、真菌或病毒。任选地,可以通过人为添加诸表1a、2、3a、4、5、6a、7a、8b、10b、11、15或16中所示的那些的一种或多种有益细菌/真菌/病毒至达到大量水平(例如,每种分别为大于总细菌、真菌或病毒的0.1%、0.2%、0.5%、
0.8%、1%、1.5%、2%、2.5%、3%、3.5%、4%、4.5%、5%、5.5%、6%、6.5%、7%、7.5%、8%、8.5%、9%、9.5%、10%、11%、12%、13%、14%或15%),来进一步改善在处理后采自供体的粪便样品。因为供体的身体,特别是胃肠道,含有大量的微生物集合,其中的许多对肠微生物群的健康和fmt的成功很重要,所以为此目的的有用的抗细菌剂/抗真菌剂/抗病毒剂优选不是分别杀死所有细菌、真菌或病毒的广谱性的试剂。而是,其可以是较窄地和精确地靶向不需要的细菌、真菌或病毒的试剂,而不显著地影响其他的细菌、真菌或病毒,包括密切相关的那些。尽管试剂可以具有任何化合物性质,但小多核苷酸(例如,sirna、mirna、minirna、lncrna或反义dna/rna)在实现破坏所靶向的细菌、真菌或病毒的生命周期中的一种或多种关键基因的表达,以便仅特异性抑制靶标物种的增殖而不显著影响其他密切相关的物种的特定任务方面可能是最有效的。
92.在完成fmt程序后不久,可以通过基于每天连续测试粪便样品中的有益和有害的细菌、真菌或病毒的水平(直至fmt之后5天)来进一步监测受体,同时也监测治疗的病况的临床症状以及预期的健康益处以评估fmt结果和受体中的相应的微生物水平:在治疗肥胖症/患者体重操纵的情形下,可以结合实现的诸如体重减轻、胰岛素敏感性提高和血液胆固醇降低的健康益处的观察来监测表1a和1b中所示的细菌的水平和表2、3a和3b中所示的真菌的水平;在治疗由耐多药细菌如cre或vre引起的病况和根除此类有害细菌的情形下,可以结合实现的诸如相关症状的减轻和cre或vre的抑制或清除的健康益处的观察来监测表4或15中所示的细菌的水平以及表5或16中所示的真菌的水平;在治疗agvhd的情形下,可以结合实现的诸如agvhd相关症状的减轻的健康益处的观察来监测表6a和6b中所示的细菌的水平以及表7a和7b中所示的真菌的水平;在治疗溃疡性结肠炎(uc)的情形下,可以结合实现的诸如uc相关症状的减轻的健康益处的观察来监测表10a和10b中所示的细菌的水平以及表8a和8b中所示的病毒的水平;并且在治疗克罗恩病(cd)的情形下,可以结合实现的诸如cd相关症状的减轻的健康益处的观察来监测表11中所示的细菌的水平。
93.iv.用于改善的fmt的试剂盒和组合物
94.本发明还提供了通过涉及fmt的各种治疗性和/或预防性治疗方案递送的可用于提高治疗效力和健康益处的新的试剂盒和组合物。例如,在用于治疗需要fmt的患者(例如,用于肥胖症/体重控制、抑制或根除耐多药细菌如cre或vre、减轻急性移植物抗宿主病,以及减轻ibd如uc或cd)的试剂盒中,第一组合物旨在用于移植到患者或fmt受体中,且第二组合物用于:(1)增加一种或多种有益的细菌(表1a、4、6a、10b、11或15中所示的那些)、真菌(表2、3a、5、7a或16中所示的那些)或表8b中所示的病毒的水平;或(2)降低一种或多种有害的细菌(表1b、6b或10a中所示的那些)、真菌(表3b或7b中所示的那些)或表8a中所示的病毒的水平—该组合物可能旨在添加至第一组合物中,或者其可能旨在给予至受体,例如,直接放置在gi道中。第一组合物包含来自供体的粪便物质,其已根据在fmt程序中的递送方式被处理、配制和包装为合适的形式,其可以为通过直接放置在受体的下胃肠道中(例如,湿的或半湿润的形式)或通过口服(例如,冷冻干燥封装的)。在一些情形下,第二组合物可以包含足够的或有效量的一种或多种有益的细菌(表1a、4、6a、10b、11或15中所示的那些)、真菌(表2、3a、5、7a或16中所示的那些),或表8b中所示的病毒,以便可以在fmt之前将其添加至第一组合物中,目的是为了将实现治疗效力和/或向受体赋予健康益处的前景优化。在其他情形下,第二组合物包含能够抑制一种或多种有害的细菌(表1b、6b或10a中所示的那些)、
真菌(表3b或7b中所示的那些),或表8a中所示的病毒的生长/增殖的抗细菌剂或抗真菌剂或抗病毒剂,所述试剂可以为杀死细菌、真菌或病毒的广谱试剂,或者有害的细菌或真菌或病毒的特异性抑制剂,以及一种或多种药学上可接受的赋形剂,以便可以在程序之前不久给予fmt受体组合物,在程序期间同时给予组合物,或者在程序后立即给予组合物。组合物经配制以用于预期的递送抗细菌剂、抗真菌剂或抗病毒剂的方法,例如,通过注射(静脉内、腹膜内、肌内或皮下注射)或通过口服或通过局部放置(例如,栓剂)。第一和第二组合物通常单独保存在试剂盒的两个不同的容器中。在一些情形下,存在用于增加有益的细菌/真菌/病毒和用于抑制有害的细菌/真菌/病毒的组合物,并且其在单独的容器中提供,作为试剂盒的第二和第三组分。通常,试剂盒将还包括印刷物质,其为试剂盒用户提供详细的说明,如提供给予受体第一和第二(以及任选地第三)组合物的时间表和剂量安排的信息。
95.在本发明的另一方面,可以设计用于fmt的具有增加的效力的替代组合物,其含有至少这两种组分:(1)含有活的粪便微生物的供体粪便物质,和(2)抗细菌剂,其特异性地抑制一种或多种有害的细菌(例如,表1b、6b或10a中所示的那些)的生长或增殖,但对其他细菌,特别是表1a、4、6a、10b、11或15中所示的那些不显示这样的压抑性或抑制性效应;或者抗真菌剂,其特异性地抑制一种或多种有害的真菌(例如,表3b或7b中所示的那些)的生长或增殖,但对其他真菌,特别是表2、3a、5、7a或16中所示的那些不显示这样的压抑性或抑制性效应;或者抗病毒剂,其特异性地抑制一种或多种有害的病毒(例如,表8a中所示的那些)的生长或增殖,但对其他细菌,特别是表8b中所示的那些不显示这样的压抑性或抑制性效应。
96.组分(2)优选不是广谱性的杀细菌/真菌/病毒剂;而是,其应为分别特异性靶向有害的细菌/真菌/病毒(例如,表1b、3b、6b、7b、8a或10a中所示的那些)的抗细菌剂/抗真菌剂/抗病毒剂。例如,其可以具有短多核苷酸性质,例如,小抑制性rna、微小rna、小rna、lncrna或反义寡核苷酸,其能够破坏靶向的有害的细菌/真菌/病毒的生命周期中的至少一个关键基因的表达,使得试剂能够仅特异性靶向所述细菌/真菌/病毒,而不显著影响其他密切相关的细菌/真菌/病毒。组分(2)在供体的粪便含有太高的一种或多种有害的细菌/真菌/病毒水平而不能允许令人满意的fmt结果的情形下特别有用,因为其能够局部地和特异性地抑制此类不需要的细菌/真菌/病毒的增殖,以便确保fmt成功,即使供体粪便物质的初始质量不太令人满意。
实施例
97.以下实施例仅通过说明的方式而非通过限制的方式提供。本领域技术人员将容易认识到,可以改变或修改各种非关键参数以产生基本相同或相似的结果。
98.引言
99.本发明的目的是确定供体和受体粪便细菌、病毒组和真菌组是否以及如何影响fmt在各种人类病况中的效力。这些病况包括但不限于:肥胖症或营养不良、代谢性疾病、2型糖尿病、炎性肠病、肠易激综合征、耐抗生素感染和移植物抗宿主病。本发明的实际用途包括优化的供体选择、fmt实施之前和fmt实施期间受体和供体中的供体/患者粪便细菌、病毒和真菌特性分析、实施fmt之前根据具体细菌、病毒组和真菌水平/丰度(包括且达到物种水平)对患者分级,以及随后的在fmt治疗之前对这些受体进行连续的抗真菌或抗细菌处
理。已提供了确定的“有利的”细菌、病毒组和真菌标准集合以用于确立供体粪便、供体粪便库及其衍生的产品,从而优化诊断和治疗。
100.实施例1肥胖症和体重操纵
101.a.肥胖症和体重操纵的实验模型
102.背景
103.全世界范围内,肥胖症的流行率正以惊人的速度增长。在中国,估计有超过1亿人患有糖尿病。类似地,在过去的二十年中,中国超重和肥胖个体的患病率从3.7%增加到了19.0%,增长了四倍。目前,基于饮食和体育锻炼的非药物干预措施在产生持续的体重减轻方面取得了有限的长期成功。诸如减肥药物或减肥手术之类的替代方法受到疾病、副作用、高昂的费用以及与手术相关的发病率的未完全解决的限制。现有的疗法不足以降低肥胖症的发病率和死亡率。
104.最近,越来越多的证据表明,肥胖症与肠微生物群组成的变化有关,且肥胖微生物组从饮食中获取能量的效率更高。另外,瘦型(lean)动物与肥胖动物之间的细菌组成也存在差异。因此,改变肠道微生物群的组成已成为一种减轻体重和提高胰岛素敏感性的新的治疗方法。在鼠类和人类研究中,拟杆菌门和厚壁菌门分类在微生物群中占优(92.6%),但与瘦型对比物相比,肥胖个体具有较低比例的拟杆菌门和较高水平的厚壁菌门。相比用“瘦型微生物群”进行的定殖,用“肥胖微生物群”对无菌小鼠进行定殖导致总体脂明显更大的增加,这表明肠微生物群可作为肥胖症病理生理的另一贡献因素。还可以通过从人类供体转移粪便微生物群,在无菌的小鼠中诱导肥胖和瘦型表型。最后,动物研究暗示了因果关系,因为不良表型可以经粪便移植物转移。这些数据已导致使用微生物群治疗作为代谢综合征和肥胖症的潜在治疗方法。
105.粪便微生物群移植(fmt)可以恢复肠内微生物生态,并已被证明是治疗复发性艰难梭菌感染的一个突破。此外,正在进行临床试验以评估其在其他病况中的用途,包括炎性肠病、肠易激综合征、糖尿病,非酒精性脂肪性肝炎和肝性脑病。人类中的早期结果表明,当将来自瘦型供体的fmt移植到患有代谢综合征的对象中时,引起胰岛素的敏感性的显著提高以及肠微生物多样性的增加,包括产丁酸盐细菌菌株的显著增加。该疗法通常具有良好的耐受性且看上去很安全。fmt是否可以有效治疗肥胖症还有待确定。另外,从供体到营养不良或体重过轻的个体的fmt可以操纵微生物群,导致预防或逆转体重减轻。fmt在肥胖症和/或营养不良中的功效根据基于其微生物群特性(包括但不限于细菌、病毒组或真菌)的最优的/有利的供体的选择而有所不同。供体和受体微生物株系之间的相容性也可能是成功的移植结果的原因。
106.方法
107.人类对象
108.粪便样品获自13名健康供体(3名女性、7名男性和3名未报告性别的参与者,年龄21-67岁,体质指数bmi 18.3-23.0)。13名健康供体包括健康的中国人个体。这些供体为d4、d8、d9,其为人类临床试验的fmt供体;以及供体1-9和供体19,其为随机选择的。
109.动物模型和人类至小鼠fmt
110.年龄和性别匹配的c57小鼠被喂食高脂饮食4周,以建立肥胖症模型。如果其体重超过对照的20%,则认为肥胖症模型建立成功。然后每周两次给肥胖小鼠灌服来自13名健
康人类供体的粪便或pbs(对照)。其饮食从高脂饮食变为正常饮食。每周两次测量体重。第2次fmt之后进行口服葡萄糖耐量试验(ogtt)和胰岛素耐量试验(itt)。在研究结束时测量血浆葡萄糖水平和脂质特性,包括总胆固醇(tc)、甘油三酯(tg)、低密度脂蛋白胆固醇(ldl-c),以及高密度脂蛋白胆固醇(hdl-c)。
111.粪便dna分离和宏基因组测序
112.使用dneasy血液和组织试剂盒(qiagen),根据厂商的方案提取采自13名供体的粪便样品dna,并进一步纯化。通过首先根据厂商说明书(illumina)构建具有350bp的插入大小的配对末端文库,并在novaseq illumina测序仪上测序来进行宏基因组测序。利用metaphlan2,使用默认设置计算群落组成。在r程序包vegan(r package vegan)中计算细菌分类学概要、微生物多样性的稀疏性分析、组成差异(通过未加权的unifrac距离表示的差异度值)。
113.发现当一起分析所有供体时,fmt组中的体重减轻百分比并不显著高于pbs对照中的那些
114.将第二次fmt/pbs灌服后3天小鼠的体重与第一次fmt/pbs灌服之前小鼠的体重进行了比较。小鼠被分到fmt组(n=39)和pbs对照组(n=6)中。与基线相比,fmt组中的中值百分比体重减轻为13.17%(iqr:6.08%-18.89%),而pbs对照组中为11.36%(iqr:8.43%-15.61%)。观察到相比对照,通过fmt的倾向更高百分比体重减轻的趋势,但不显著。
115.通过fmt的体重减轻效应根据供体而不同
116.为了分析供体的影响,根据供体对小鼠分组。13个组的小鼠接受来自不同供体的fmt(每组包含3只小鼠),且1个对照组接受pbs(6只小鼠)。11个组相比对照实现了更高百分比的体重减轻。接受来自供体m9的粪便的小鼠实现了最高量的体重减轻[平均百分比体重减轻19%;标准偏差(sd)4.9%]。尽管fmt总体诱导了体重减轻,但效果根据供体而不同。因此选择最佳供体是必需的。
[0117]
人类至小鼠fmt与肥胖小鼠中提高的胰岛素敏感性有关
[0118]
在胰岛素耐量试验(itt)中总共纳入了60只小鼠,54只接受fmt,且6只接受pbs。与pbs对照组相比,fmt组中的小鼠显示显著减小的itt曲线下面积(auc)(p《0.05),这表明提高的从血流清除葡萄糖的能力。这些数据表明fmt提高了肥胖小鼠中的胰岛素敏感性。
[0119]
相比接受pbs的那些,接受来自人类粪便的fmt的肥胖小鼠中的血液血清总胆固醇(tc)和低密度脂蛋白(ldl)水平显著的降低
[0120]
在第二次fmt/pbs灌服后测量了总共33只小鼠(10个每组3只小鼠的fmt组,每组接受来自10名不同的供体的fmt,以及1个3只小鼠的对照组,接受pbs)中的血液血清tc和ldl水平。相比pbs对照组,所有fmt组均显示显著降低的tc和ldl水平,而与供体无关(p《0.001)。
[0121]
人类供体粪便的细菌特性显示细菌组成和丰度的极大变化
[0122]
13名供体之间的比较发现,细菌α多样性(香农多样性指数和辛普森多样性指数)以及细菌在门水平上的相对丰度差异较大。
[0123]
对于体重减轻“有利的”和“不利的”细菌
[0124]
肥胖小鼠中的体重减轻比例显示与22种细菌的显著的相关性
[0125]
从宏基因组测序结果计算特定细菌的相对丰度。为了鉴定与fmt对体重减轻的供
体效应相关的特定细菌,将在接受来自13名不同的供体的第二次fmt的每组小鼠(n=3)中观察到的特定细菌的相对丰度与平均百分比体重减轻进行关联。发现5种细菌与平均百分比体重减轻具有显著的正相关性,且发现17种细菌与平均百分比体重减轻具有显著的负相关性。
[0126]
选择用于诱导体重减轻的“有利的”fmt供体的细菌标准
[0127]
在替代性的分析中,将13名供体分类为“有利的”供体和“不利的”供体。“有利的供体”定义为相比13个小鼠组间的均值(13.17%)或中值(13.67%)百分比体重减轻,能够诱导更多的体重减轻的供体,且余下的定义为“不利的供体”。使用线性判别分析(lda)效应量(lefse)分析来分析2个组之间的细菌相对丰度(线性判别分析效应量》2,调整的p值《0.05被认为显著)。
[0128]
本发明人鉴定了在“有利的”供体(对于体重减轻的有利的细菌)中过表达的13种细菌分类和在“不利的”供体(对于体重减轻不利的细菌)中过表达的7种细菌分类。
[0129]
集合了上述鉴定的对于体重减轻“有利的”和“不利的”细菌及其相对丰度的概要显示在表1a和表1b中。
[0130]
b.用于肥胖症和体重操纵的fmt的人类研究
[0131]
方法
[0132]
人类中的横断面研究
[0133]
采集了来自23名肥胖对象和15名对照的粪便样品,以比较其微生物特性。肥胖对象定义为具有的bmi≥28kg/m2,而对照对象定义为具有的bmi≥18.5kg/m2且《23kg/m2。
[0134]
粪便微生物群移植(fmt)的随机对照试验
[0135]
在横断面研究所招募的肥胖对象中,也招募了还患有2型糖尿病的12名对象,临床试验标题为“患有2型糖尿病的肥胖对象中的影响体重和血糖控制的粪便微生物群移植(fmt)的随机的安慰剂对照研究(arandomised placebo-controlled study of fecal microbiota transplant(fmt)to impact body weight and glycemic control in obese subjects with type 2diabetes mellitus)”(clinicaltrials.gov上的参考号为:nct03127696)。在该研究中,对象被随机分到3个臂中:1)fmt连同生活方式改造计划(lmp),2)仅fmt,和3)假试验连同lmp。主要结果定义为相比基线5%的体重减轻,其为在接受任何干预之前随机化的体重。粪便样品在基线处采集。在第0、4、8、12、16、20、24和52周测量体重。
[0136]
fmt程序
[0137]
来自一般人群、配偶或伴侣、一级亲属、其他亲属、朋友和对象了解或不了解的其他人的志愿者被招募为供体以提供用于fmt的粪便。为了确保供体是健康的且适合粪便捐赠,首先利用问卷调查对供体进行筛选,然后进行粪便和血液测试以排除任何感染。另外,仅纳入了bmi《23kg/m2的瘦型供体。在供体于威尔斯亲王医院(the prince of wales hospital)提供粪便后不久,用无菌盐水(0.9%)稀释粪便。将该溶液混合并用过滤器过滤。然后将所得的上清液保存为冷冻的fmt溶液,以用于将来的fmt。对于随机化的接受fmt的对象,使用来自单个供体的fmt溶液或来自多个供体的混合的粪便。对于随机化的接受假试验的对象,输注生理盐水。在程序过程中,经ogd在2-3分钟内将100-200ml fmt溶液或无菌盐水注入远端十二指肠或空肠。
[0138]
生活方式改造计划(lmp)
[0139]
由营养师在第0、1、2、4、6、8和12周诊断随机分配到lmp的对象。营养师在他们的饮食习惯、体育活动方式和其他生活方式习惯方面为对象给予指导和纠正。在每次咨询营养师之前,对象还记录了他们7天的饮食史。
[0140]
粪便dna提取和宏基因组测序
[0141]
使用rsc purefood gmo and authentication试剂盒,根据方案分离粪便dna。通过末端配对、纯化和pcr扩增的过程来构建dna文库。在dna文库构建之后,由中国北京的novogene通过illumina novaseq 6000,利用配对末端150bp测序策略对dna文库进行测序。
[0142]
读取质量控制和预处理
[0143]
通过fastp对原始序列读取进行质量筛选,并去除适配子。通过kneaddata,利用默认参数(参考数据库:grch38 p12)去除人宿主污染读取。对于宏基因组数据表,通过归入ncbi真菌refseq数据库(2018年9月20日下载)中,在kraken2中处理干净读取(clean reads)。使用bracken来估计物种相对丰度表以用于下游分析。
[0144]
统计分析
[0145]
使用线性判别分析效应量(lefse)模型来鉴定具有不同组间相对丰度的物种。仅满足》2的lda阈值的分类被认为是显著的。对于通过lefse模型鉴定的物种,进行了替代性分析以通过wilcoxon秩和检验验证其组间相对丰度的差异。p值《0.05被认为是统计上显著的。
[0146]
发现
[0147]
对照中的甜菜生尾孢和纳加哈萨克斯坦酵母的相对丰度明显高于肥胖对象中的那些
[0148]
在横断面研究中,比较了23名肥胖对象和15名对照[肥胖对象的中值年龄为52岁(iqr:47
–
60岁),且对照为57岁(iqr:54
–
60岁);60%的肥胖对象为男性,且69.6%的对照为女性]之间的粪便真菌群落。通过lefse分析,发现对照中的两种真菌甜菜生尾孢和纳加哈萨克斯坦酵母的相对丰度明显高于肥胖对象中的那些。肥胖对象中的中值丰度为0.045(iqr:0.038-0.050),且对照中的为0.056(iqr:0.045-0.063)(p=0.016)。肥胖对象中的中值丰度为0.004(iqr:0.003-0.006),且对照中的为0.006(iqr:0.004-0.007)(p=0.044)。这2种真菌是对体重减轻有利的真菌(表2)。接受fmt或lmp后实现体重减轻的对象和未实现体重减轻的对象之间的4种真菌的相对丰度存在显著差异
[0149]
来自随机对照试验,已达到16周随访的12名对象被纳入分析中。为了鉴定能够预测体重减轻的真菌,将对象分成“体重减轻”和“非体重减轻”组,且对其基线粪便真菌特性进行了比较。如果其在16周时的体重减轻相比基线为大于5%,则将对象分入“体重减轻”组;而如果其在16周时的体重减轻相比基线为小于5%,则将对象分入“非体重减轻”组。3例被分入“体重减轻”组(中值百分比体重减轻为5.3%),且9例被分入“非体重减轻”组(中值百分比体重减轻为0.2%)。
[0150]
通过lefse分析,发现“体重减轻”组中的1种真菌法夫驹形氏酵母(komagataella phaffii)明显高于“非体重减轻”组中的。该物种在基线粪便样品中的较高相对丰度能够预测成功的随后的通过fmt或lmp干预的体重减轻。补充该“有利的物种”可以促进体重减轻
(表3a)。
[0151]
另一方面,lefse分析还显示鉴定出了“非体重减轻”组中的3种真菌的相对丰度明显高于“体重减轻”组中的。这些真菌是戴尔凯式有孢圆酵母(torulaspora delbrueckii)、蚱蜢微孢子虫(encephalitozoon romaleae)和乳酸克鲁维酵母(kluyveromyces lactis)。基线粪便样品中这些“不利的”物种的较高的相对丰度能够预测对抗通过fmt或lmp的体重减轻(表3b)。
[0152]
实施例2耐多药生物体(耐碳青霉烯的肠杆菌科(cre)和耐万古霉素的肠球菌(vre))
[0153]
cre中的fmt:疾病和fmt结果的细菌和真菌决定因素
[0154]
背景
[0155]
耐多药生物体(mdro)对全球人群构成日益严重的公众健康威胁。在世界范围内,包括耐碳青霉烯的肠杆菌科(cre)和耐万古霉素的肠球菌(vre)在内的各种mdro的发病率已日益增多,并且在某些国家或地区已经流行。例如,在邻近中国香港的国家或地区中,产肺炎克雷伯氏菌(klebsiella pneumoniae)碳青霉烯酶(kpc)和产新德里金属-β-内酰胺酶(ndm)的肠杆菌科在中国流行且分布广泛,而产imp的肠杆菌科则在中国台湾省和日本广泛存在。来自医院管理局的数据显示,产碳青霉烯酶的肠杆菌科(cpe)病例数量从2012年的36例增加到2015年的134例。最近在中国香港一家三级医院报道了vre大爆发,涉及》200例患者。在一些国家或地区,mdro的传播不仅限于医院环境,而且在人群中也很普遍。
[0156]
大多数mdro定殖和持续的主要场所是在胃肠道中。携带可以持续数月,在出院后一年,有多达40%的个体仍具有定殖。在医院和长期护理机构中已经报告了mdro暴发。约有10%的mdro定殖的患者会发展出由相同生物体引起的临床感染。这些mdro引起的感染具有很高的发病率和高达50%的死亡率,部分是由于安全和有效的抗微生物疗法的选择有限。目前,mdro传播的控制主要是通过感染控制措施,并且尚无行之有效的mdro肠道定殖根除疗法。
[0157]
越来越多的证据表明,肠道微生物群在控制肠道病原菌定殖和感染中起着重要作用。mdro携带者中肠道微生物群的组成和多样性与非携带者不同。肠道共生细菌例如通过诱导上皮细胞产生抗菌蛋白来帮助调节粘膜的先天免疫力。鞭毛蛋白已被证明可在小鼠中诱导产生regiiiγ(一种抗微生物蛋白),并减少vre定殖。也已证明给予小鼠专性厌氧共生细菌可显著减少vre定殖。初步证据(主要来自轶事报告)表明,mdro人类携带者中的粪便微生物群移植(fmt)在清除包括cre和vre在内的各种mdro的肠道定殖方面是安全的和潜在有效的,即使在免疫力低下的患者中也是如此。
[0158]
利用宏基因组测序,对健康对照和fmt受体的微生物特性进行评估,以鉴定与cre定殖相关的微生物。还对fmt供体的微生物特性以及fmt之前和fmt之后受体的微生物特性进行了比较,以鉴定与cre清除相关的物种。这些物种在为提高fmt效力的供体或微生物产品选择以及用于fmt之后成功的cre清除的预测标记物方面起着重要作用。
[0159]
方法
[0160]
根除cre和vre的fmt的人类临床试验
[0161]
年龄≥18岁、具有相隔一周的两次或更多次粪便或直肠拭子cre或vre阳性,并且在输注fmt之前至少48小时未接受抗微生物治疗的患者被招募至临床试验中。患有需要进
行抗微生物治疗的cre或vre活动性感染、怀孕、活动性胃肠道感染或炎症性病症、近期进行过腹部内手术、患有短肠综合征,或使用改变胃肠运动的药物的患者被排除在外。cre定义为存在对任何碳青霉烯类具有耐受性的任何肠杆菌科。vre定义为存在对万古霉素具有耐受性的肠球菌。在该研究中,患者接受2次利用冷冻供体粪便样本的fmt。在2-3分钟内,经ogd将100-200ml fmt溶液或无菌盐水注入远端十二指肠或空肠。在fmt之前和之后预先从患者采集粪便样品。
[0162]
无cre或vre的人类对象
[0163]
2名无cre或vre的对象的粪便样品被纳入作为对照。
[0164]
粪便dna提取和宏基因组测序
[0165]
通过末端配对、纯化和pcr扩增的过程来构建dna文库。使用nexteraxt dna文库制备试剂盒(illumina,california,usa),根据厂商指导制备测序文库。在novoseq pe150(novogene,tianjin,china;标准的2
×
150bp运行)上进行测序,每个样品产生12g原始数据。
[0166]
读取质量控制和预处理
[0167]
通过fastp对原始序列读取进行质量筛选,并去除适配子。通过kneaddata,利用默认参数(参考数据库:grch38 p12)去除人宿主污染读取。对于宏基因组数据表,通过归入ncbi真菌refseq数据库(2018年9月20日下载),在kraken2中处理干净读取。使用bracken估计物种相对丰度表以用于下游分析。
[0168]
统计分析
[0169]
使用线性判别分析效应量(lefse)模型来鉴定具有不同组间相对丰度的物种。仅满足》2的线性判别分析(lda)阈值的分类被认为是显著的。
[0170]
发现
[0171]
用于根除耐碳青霉烯的肠杆菌科肠道定殖的粪便微生物群移植
[0172]
招募至临床试验中的两名患者在fmt之后成功清除了cre。受体1(女性,年龄90岁)间隔5天进行了2次fmt,即第0天和第5天。cre在第11天测试为阴性,并保持阴性直至第一次fmt之后第5周。然后她发展出脚部溃疡感染并在第一次fmt之后第6周至第19周接受了抗生素治疗。受体1的cre在第14周和第19周测试为阳性。在第22周,在完成4个疗程的奥格门丁(augmentin)后其再次测试为阴性。受体2(男性,年龄70岁)连续两天接受了两次fmt,并且在第1、3、6周cre随访测试的所有结果均为阴性。
[0173]
在fmt之前和fmt之后采集了来自受体1和受体2的粪便样品。两名受体接受了来自同一供体的fmt。
[0174]
在治疗cre中对选择fmt供体“有利的”和“不利的”细菌
[0175]
患有cre的患者的细菌特性与健康对照具有显著差异
[0176]
在横断面研究中,比较了cre组和健康对照组之间的粪便细菌特性。cre组由来自接受fmt之前的受体1(r1)和受体2(r2)的粪便样品组成,而健康对照组由来自fmt供体和招募至中国香港健康肠道微生物群调查(hong kong health gut microbiota survey)的2名其他的健康对照的粪便样品组成。
[0177]
在cre组和对照组之间,宏基因组测序确定的40种物种的相对丰度的lefse分析存在显著差异(lda》2)。这代表了对清除cre“有利的”和“不利的”细菌。
[0178]
fmt之前和fmt之后供体和cre受体中的细菌特性
[0179]
在前瞻性的先导试验中,相比供体,在对象中,在fmt之前和之后两名受体中的细菌α多样性均一致性地更低。然而,r1的细菌α多样性在fmt之后第18天显示增加,且r2中的结果显示在第3天和第8天的α多样性水平相比第14天更大。比较了fmt之前和之后单种细菌的相对丰度(在受体1中,为第7天vs第18天;在受体2中,为第3天vs第18天)。对于受体2,在fmt之前有2个粪便样品采集时间点。对于受体2,选择了第3天,因为其为更接近fmt的时间点。将第18天选作两名受体的fmt之后的时间点,因为到该时间细菌特性开始稳定。发明人鉴定了在受体1或受体2中具有增加的》1.0的倍数变化的细菌。这些物种以非常低的水平出现,或者在fmt之前的粪便样品中甚至检测不到。从供体移植这些物种可能与cre的清除有关。毛螺菌科细菌(lachnospiraceae_bacterium_5_1_63faa)在r1中于fmt之后显示最大的增加,且在r2中显示第二大的增加,倍数变化分别为1659.5和16.9。
[0180]
以上鉴定的对cre清除“有利的”细菌及其相对丰度的概要显示在表4中。
[0181]
fmt之前的和fmt之后的供体和cre受体中的粪便真菌特性
[0182]
在前瞻性的先导试验中,fmt之后在r1和r2中真菌α多样性的变化朝向相反的趋势,表明fmt对真菌多样性的影响在不同的患者中存在差异。分析了fmt之前和之后单种真菌的相对丰度。
[0183]
尽管利用真菌的fmt的短期供体移植并不像细菌那样明显,但一些真菌的相对丰度却显示出明显的变化。与fmt之前相比,fmt之后受体的真菌群落在结构上更类似于供体特性。下面列出了受体1或受体2中的倍数变化增加》1.0的真菌。特别地,海伦脑炎微孢子虫(encephalitozoon hellem)在两名受体中均显示出最高的倍数变化,分别为在r1中增加9.31倍和在r2中增加81倍。fmt之后移植和增加这些真菌可能是成功的cre去定殖(decolonization)的决定因素(表5)。
[0184]
实施例3急性移植物抗宿主病(agvhd)
[0185]
agvhd中的fmt:疾病和fmt结果的细菌和真菌决定因素
[0186]
背景
[0187]
同种异体造血干细胞移植(allo-hsct)是血液学病症的最有希望的肿瘤免疫疗法之一。急性移植物抗宿主病(agvhd)是allo-hsct的一种严重并发症,其发生在35%-45%的受体中,并与15%-25%的死亡率有关。特别地,下胃肠(gi)道受累会并发高死亡率。糖皮质激素被用作agvhd的一线疗法,但只有约一半的患者有反应,且二线治疗尚未建立。agvhd的一年生存率为小于30%。迄今为止,在患者生存方面,顽固性gvhd没有令人满意的改善。
[0188]
越来越多的证据表明,肠微生物群组成的变化与gvhd的发生密切相关。多种因素促成了患有allo-hsct的患者中的微生物群多样性的减少,包括反复使用抗生素、给予化疗和/或放疗,以及改变营养模式。同种异体骨髓移植(bmt)导致整体多样性的丢失和乳杆菌的扩增以及梭菌的丢失,这增加了随后发生gvhd的风险。此外,在allo-hsct后,在受体中观察到肠球菌,并且其与gi-agvhd的严重程度有关。也已报道改变的病毒与肠道gvhd有关联。例如,观察到了小双核糖核酸病毒(picobirnavirus)与早期移植后gvhd5的不可预期的关联。
[0189]
越来越多的证据表明,改变的肠微生物群与干细胞移植(sct)中的急性移植物抗宿主病(agvhd)有关。粪便微生物群移植(fmt)代表了agvhd的一种有前途的治疗方法。最
近,几个小案例系列已经指出了fmt可能作为难治性agvhd的治疗方法。在连续三名患有难治性gi-agvhd的患者中,fmt可以改善胃肠道症状,减少腹泻并重构肠微生物群。在allo-hsct后的患者中,给予fmt胶囊减少了agvhd的发生并提高了生存率。
[0190]
迄今为止,在hsct受体中使用fmt的经验有限。尽管必须进行更精心设计的临床研究以确认fmt对agvhd的安全性和有效性,但在一些患者中这种威胁生命的疾病需要立即注意。大多数研究集中在细菌多样性的恢复上,而噬菌体和真菌在fmt效力中的作用鲜为人知。在本研究中,提供了第一例成功的使用fmt治疗agvhd(iv级)的青少年案例,并使用宏基因组表征了fmt之后受体中的系列粪便细菌、病毒组和真菌特性,以研究改变的微生物组动力学与agvhd治疗之间的潜在关联。
[0191]
在一名患有对皮质类固醇和生物疗法难治的严重威胁生命的4级肠agvhd的小男孩中,重复的fmt(总共4次)恢复了微生物组的多样性并引起疾病改善。这是fmt用于小儿gi-gvhd的第一例,其强调了恢复细菌、病毒和真菌多样性及其稳定移植。鉴定了影响有利的fmt结果的潜在供体和受体细菌、真菌特性。
[0192]
病例展示
[0193]
一名患有具有单体型7的骨髓增生异常综合征的14岁男性,于2017年12月21日接受了hla同胞同种异体造血干细胞移植(allo-hsct)。他在allo-hsct后不久发展出了ii期皮肤gvhd(皮疹25%-50%)、肠agvhd(iv期,具有明显的功能受损),和总体iv级威胁生命的gvhd。他有腹泻、呕吐和腹痛。他在allo-hsct之后77天接受了第一次fmt,随后在第一次fmt之后的第5、13和25天再接受三次fmt。头3次fmt来自单个供体d8,且第四次fmt来自不同的单个供体d4。在四次fmt的过程中,患者还接受了甲基强的松龙、环孢霉素a、英夫利昔单抗、鲁索替尼、布地奈德(entocort)、奥曲肽、抗生素、抗病毒药和抗真菌药。
[0194]
在接受第一次fmt的前一天,患者具有的粪便量为465ml,且排便为5次。在第一次fmt的第二天,粪便量减少到0,而排便减少到1次。第一次fmt之后的第5天,粪便量增加到293ml,伴有血液和水样稠度,而排便增加到两次。患者在第7天接受来自相同供体的第二次fmt。在第11天,粪便量减少到100ml,且排便减少到1次。粪便形态良好,且患者仅有轻微的腹部绞痛。此后直到第35天,粪便量维持在每天约100ml,且每天排便一次或零次。免疫抑制剂被慢慢停掉。直到第一次fmt之后第117天的最后一次随访,患者仍保持稳定。
[0195]
fmt程序
[0196]
供体粪便获自香港中文大学肠微生物群研究中心(the center for gut microbiota research)的粪便库。
[0197]
方法
[0198]
来自供体和受体的粪便
[0199]
在第0天、第5天、第13天和第25天给予患者fmt。从第0天至第25天(患者进行4次fmt时)每天采集受体中的临床数据,然后每月采集直至第117天。对于该分析,通过宏基因组测序对1份fmt之前粪便样品以及第1次、第2次、第3次和第4次fmt之后的分别3、4、6和8份粪便样品进行细菌、病毒和真菌特性分析。
[0200]
采集了来自用于fmt的2名fmt供体d4和d8的粪便样品进行宏基因组测序。来自供体d8的粪便样品采自2周内的5个不同的时间点。这些样品标记为d8-26、d8-27、d8-28和d8-29。来自供体d4的粪便采自单个时间点并标记为d4。对所有这些样品单独进行细菌、病毒和
真菌特性分析。在第1次和第2次fmt中,使用了在不同的日期采集的来自供体d8的粪便。用于4次fmt的粪便样品的分配列出如下:
[0201]
第1次fmt:d8-26和d8-27
[0202]
第2次fmt:d8-28和d8-29
[0203]
第3次fmt:d8-34
[0204]
第4次fmt:d4
[0205]
粪便dna提取和宏基因组测序
[0206]
使用rsc purefood gmo and authentication试剂盒,根据方案分离粪便dna。通过末端配对、纯化和pcr扩增的过程来构建dna文库。在dna文库构建之后,由中国北京的novogene通过illumina novaseq 6000,利用配对末端150bp测序策略对文库进行测序。细菌和真菌宏基因组测序产生10-12g原始数据。
[0207]
读取质量控制和预处理
[0208]
通过fastp对原始序列读取进行质量筛选并去除适配子。通过kneaddata,利用默认参数(参考数据库:grch38 p12)去除人宿主污染物读取。对于宏基因组数据表,在humann2中处理干净读取以用于细菌分析,并在kraken2中处理以用于真菌和病毒分析。在r程序包vegan中计算细菌分类概要、微生物多样性的稀疏性分析、组成差异(通过未加权的unifrac距离表示的差异度值)。
[0209]
用于检测人粪便总dna中的总真菌载荷的定量pcr
[0210]
使用引物36:真菌-定量-f 5
’‑
ggraaactcaccaggtccag-3’;真菌-定量-r 5
’‑
gswctatccccakcacga-3’,以及探针:5
’‑
tggtgcatggccgtt-3’,通过taqman qpcr分析(premix ex taqtm,takara)提取的人粪便dna,对人粪便中的总真菌载荷进行定量。
[0211]
统计分析
[0212]
使用线性判别分析效应量(lefse)模型来鉴定具有不同组间相对丰度的物种。仅满足》2的lda阈值的分类被认为显著。对于通过lefse模型鉴定的物种,进行了替代性的分析以通过wilcoxon秩和检验验证其组间相对丰度的差异。p值《0.05被认为是统计上显著的。
[0213]
发现
[0214]
fmt之后的细菌变化
[0215]
fmt之后的患agvhd的患者中的粪便细菌群落的α多样性增加
[0216]
使用香农和辛普森指数来预估fmt之后(在第1次、第2次、第3次和第4次fmt之后)的患agvhd的受体和fmt供体(d4和d8)中的细菌群落的α多样性。在接受第一次fmt之后,受体粪便中的α多样性相比fmt之前显著增加,并且在第2次、第3次和第4次fmt之后,α多样性达到与供体d4和d8相似的水平。
[0217]
fmt之后agvhd患者中细菌群落结构的恢复
[0218]
使用主成分分析(pca)来研究fmt之前和fmt之后受体以及供体的粪便样品之间的群落结构差异。在重复的fmt之后,粪便细菌群落逐渐接近供体的那些,这表明患者的细菌群落结构得到恢复且变得与供体的那些相似。
[0219]
从供体转移的7种细菌在fmt受体中成为优势细菌
[0220]
通过条形图评估了fmt之后的患agvhd的患者中的来自供体的细菌移植。杰氏棒杆
菌(71.2%)在患者的肠细菌群落中占优,且在第一次fmt之后下降至小于0.1%。在接受重复的fmt之后在患者中观察到7种细菌的移植,且这些物种占据患者细菌群落的较大比例。这些物种是:alistipes onderdonkii、alistipes putredinis、鲍氏梭菌、系结梭菌、共生梭菌、未分类埃格特菌(eggerthella unclassified)、ruminococcus gnavu。
[0221]
当患者患有腹泻或无腹泻时4种细菌的相对丰度存在显著差异
[0222]
在fmt之前和fmt之后从患有agvhd的患者采集了总共22份粪便样品。为了鉴定在患者患有腹泻或无腹泻时具有不同的相对丰度的粪便细菌,根据患者在粪便采集当天是否患有或未患有腹泻对这22份粪便样品进行分类。腹泻定义为每天有2次或更多次排便,而非腹泻定义为每天有0或1次排便。使用lefse分析来鉴定相对丰度在来自“腹泻”或“非腹泻”组的粪便样品之间存在显著差异的细菌。腹泻组中直肠真杆菌的相对丰度明显更高,而非腹泻组中alistipes putredinis、alistipes onderdonkii和哈撒韦梭菌的相对丰度明显更高。“有利的”供体应当含有较高相对丰度的alistipes putredinis、alistipes onderdonkii和哈撒韦梭菌,以及较低相对丰度的直肠真杆菌。
[0223]
agvhd症状与5种细菌显著相关
[0224]
为了鉴定与治疗结果相关的特定细菌,通过线性回归将特定细菌的相对丰度与包括排便次数、粪便量和呕吐量在内的gvhd症状进行关联分析。发现一种细菌与排便次数和粪便量呈显著正相关。“有利的”供体应含有较低的杰氏棒杆菌相对丰度或没有该细菌。另一方面,4种细菌显示与呕吐症状的显著负相关性。“有利的”供体应含有较高的这些细菌的相对丰度(列出如下):alistipes putredinis;鲍氏梭菌;哈撒韦梭菌;系结梭菌。
[0225]
集合上述鉴定的对治疗agvhd“有利的”和“不利的”细菌及其相对丰度的概要显示在表6a和表6b中。
[0226]
fmt之后的真菌变化
[0227]
fmt之后agvhd中的粪便真菌多样性增加
[0228]
使用香农和辛普森指数来预估fmt之后的患agvhd的受体和fmt供体(供体4和供体8)中真菌群落的α多样性。在接受第一次fmt之后,α多样性相比fmt之前的那些显著增加。在随后的3次fmt之后,真菌的α多样性继续稳定增加,并达到与供体d4和d8相似的水平。
[0229]
fmt之后agvhd患者中的总真菌载荷增加
[0230]
通过qpcr测量总真菌载荷。患者中的总真菌载荷在接受来自供体d8的fmt之后增加至与供体相似的水平,然后在几天后再次下降并在接受第二次fmt之后保持低水平。在接受第三次fmt之后患者中的水平再次增加。在利用来自供体d4(其相比供体d8具有略低的总真菌载荷)的粪便的第四次fmt之后总真菌载荷略微减少。
[0231]
fmt之后2种真菌的相对丰度显著降低,而12种从供体转移的真菌在fmt受体中成为优势真菌
[0232]
通过条形图评估了fmt之后的患gvhd的患者中来自供体的真菌移植。尖孢镰刀菌(fusarium oxysporum)(61.44%)和灰葡萄孢(botrytis cinereal)(29.13%)在患者的肠真菌群落中占优,且在第一次fmt之后显著下降。这些被认为是“不利的”真菌。在接受重复的fmt之后12种物种移植到患者中,并占据患者真菌群落的较大比例。这些物种是:粟酒裂殖酵母(schizosaccharomyces pombe)、eremothecium sinecaudum、甜菜生尾孢、毒性镰孢菌(fusarium venenatum)、嗜热毁丝霉菌(thermothelomyces thermophile)、希金斯刺盘
孢(colletotrichum higginsianu)、拟轮生镰刀菌(fusarium verticillioides)、斯梭孢壳霉(thielavia terrestris)、杜氏假丝酵母(candida dubliniensis)、棉假囊酵母(eremothecium gossypii)、假禾谷镰刀菌(fusarium pseudograminearum)和粗糙脉孢霉(neurospora crassa)。这些被认为是“有利的”真菌。
[0233]
agvhd症状与21种真菌显著相关
[0234]
为了鉴定与治疗结果相关的特定真菌,通过线性回归将特定真菌的相对丰度与包括排便次数、粪便量和呕吐量在内的gvhd症状进行关联分析。发现两种真菌显示与排便次数和粪便量的显著的正相关性。基于这些发现,“有利的”供体应含有较低的这两种真菌即尖孢镰刀菌和灰葡萄孢(botrytis cinerea)的相对丰度。另一方面,19种真菌显示与至少一种症状的显著的负相关性。“有利的”供体应含有较高的这些真菌的相对丰度。
[0235]
集合上述鉴定的对治疗agvhd“有利的”和“不利的”真菌及其相对丰度的概要显示在表7a和表7b中。
[0236]
实施例4炎性肠病病毒组
[0237]
健康人群和溃疡性结肠炎中的粘膜病毒组
[0238]
背景
[0239]
溃疡性结肠炎(uc)——炎性肠病(ibd)的一种亚型,是一种影响到整个大肠的缓解后复发的炎症性疾病,其通常始于直肠并向上扩散。uc的发病率持续增加,尤其是在发展中国家以及新兴工业化国家。尽管ibd的病因学尚不明确,但ibd被认为是由于遗传易感个体中对肠微生物群的免疫反应加剧所致。已在人和小鼠中研究了ibd中的粪便病毒组改变,其特征是来自有尾噬菌体目的噬菌体的大量繁殖。然而,尚不清楚健康或ibd中的粘膜病毒组组成及功能,同时,关于uc中的粘膜细菌改变的了解也很有限。为了开始解决这些难题,本发明人从健康个体和患有uc的患者的直肠富集了病毒样颗粒(vlp),进行超深度病毒组宏基因组测序和16s rdna测序,以确定患有uc的对象相比健康对照中的粘膜病毒组、细菌组和病毒-细菌相互作用。本研究是迄今为止表征健康和uc中的粘膜病毒组的第一项和最大的研究。
[0240]
方法
[0241]
研究对象
[0242]
本研究在获取知情同意书的情况下招募了来自中国香港的48名健康对象相对于63名患有uc的患者、来自北京的20名健康对象相对于20名患有uc的患者,以及来自浙江省象山县的8名健康对象相对于8名患有uc的患者(均是中国人)。患者纳入标准包括这样的对象:≥18岁,经内窥镜检查、放射学和组织学确诊患有uc。对照由接受息肉结肠镜检查或结直肠癌筛查或胃肠道症状调查的个体,以及患者在当地医院的朋友和配偶或伴侣,或有兴趣参加本研究的任何个体组成。经内窥镜采集来自研究对象的直肠活检样品,然后在-80℃下保存,以用于下游的粘膜病毒组和细菌分析。
[0243]
病毒样颗粒(vlp)富集和测序
[0244]
使用根据先前描述的方法修改的方案从患有uc的患者和健康对象的直肠活检富集病毒样颗粒(vlp)。在cbot上扩增合格的文库,以在流动池(truseq pe cluster kit v3
–
cbot
–
hs,illumina)上产生簇。在hiseq xten system(truseq sbs kit-hs v3,illumina)(bgi,shenzhen,china;标准的2x 150bp运行)上对扩增的流动池进行配对末端测序,每个
13.8)进行比对。
[0262]
16s rrna测序数据分析
[0263]
将所得序列针对greengenes数据库进行分类,并以最深度水平分类进行注释,这通过朴素贝叶斯分类器的平均超过1,000次迭代的至少80%的伪自举置信度得分来表示。
[0264]
发现
[0265]
uc中粘膜病毒组多样性的改变
[0266]
在中国香港,将63名患有uc的患者的直肠病毒组与48名健康对象的那些进行了比较。平均从富集的直肠vlp制备物获得了56,632,558
±
14,330,713条干净配对末端读取。在目、属和种水平上研究了健康和uc中的粘膜病毒组组成。
[0267]
与健康个体相比,uc对象在粘膜中具有明显更高的病毒丰度(曼-惠特尼检验,p=0.017)和降低的病毒多样性、均匀度和丰富度(t检验,分别为p=0.013、0.020和0.029)。接下来研究了有尾噬菌体目噬菌体(caudovirales bacteriophages)——占优势的粘膜病毒的改变,且发现在uc中的有尾噬菌体丰度也得到扩增(曼-惠特尼检验,p=0.003),而有尾噬菌体目中的物种多样性、均匀度和丰富度均下降(t检验,分别为p=0.009、0.017和0.018)。总之,这些发现表明患有uc的患者中的粘膜病毒组失调。
[0268]
在uc患者中,炎症性粘膜中的总病毒和有尾噬菌体目噬菌体相比非炎症性粘膜富集得更多(曼-惠特尼检验,p=0.015和0.017)。相对于健康对照的那些比较uc患者的非炎症性粘膜的粘膜病毒组的α多样性差异,发现炎症性粘膜中的总病毒和有尾噬菌体目噬菌体的多样性、均匀度和丰富度的降低相对于健康对照的那些在统计上更为显著。因此,其表明肠道炎症是uc中粘膜病毒组失调的重要贡献因素。
[0269]
健康群体和患有uc的患者之间不同的粘膜病毒组结构
[0270]
在科水平上,微小噬菌体科(microviridae)(单链dna噬菌体)、肌尾噬菌体科(mycoviridae)、短尾噬菌体科(podoviridae)(来自有尾噬菌体目的双链dna噬菌体)和penumoviridae(真核病毒)在uc中比在对照中更为丰富,而对照中的指环病毒科(anelloviridae)(真核病毒)高于uc中。在属水平上,phix174微小病毒(phix174microvirus)、p1病毒(p1virus)、λ病毒(lambdavirus)、t4病毒(t4virus)、p22病毒(p22virus)(均为有尾噬菌体目噬菌体)和正肺病毒(orthopneuovirus)在uc中富集,而巨大病毒海洋球石藻病毒(coccolithovirus)、微小病毒(minivirus)和脊椎动物感染病毒正痘病毒(orthopoxvirus)(均为真核病毒)在对照中富集。与这些观察结果相一致,相对于健康对象粘膜,uc粘膜中更多的有尾噬菌体目噬菌体的丰度得到扩增,包括埃希氏菌噬菌体(escherichia phage)和肠道菌噬菌体(enterobacteria phage)。总之,这些发现表明uc粘膜中的原核病毒,特别是有尾噬菌体目噬菌体的失调占优势,而健康对照中的一些真核病毒更为丰富,表明uc中细菌失调与噬菌体扩增之间存在关联性,并且健康个体中的真核病毒感染与宿主免疫力成熟之间存在关联性,这可以保护宿主免受自身免疫性疾病的侵害。
[0271]
利用随机森林,发明人对北京和象山人群中的粘膜病毒组进行了分类。所有对象均被分类为肠型1。对中国香港人群中的健康对照和uc之间的所有肠型1对象的差异分析鉴定了一组不同的病毒。然而,仅有两种物种在验证人群中可被重复,分别为:感染藻的费氏褐藻病毒(feldmannia species virus),相对于象山人群中的对照肠型1对象,其在uc肠型
1对象中的存在明显更高;以及假单胞菌病毒(pseudomonas virus),相对于北京人群中的uc肠型1对象,其在对照肠型1对象中的存在明显更高。总之,其表明存在对粘膜病毒组结构的显著的地理影响,这造成了不同人群之间的粘膜病毒组组成的较大变异。
[0272]
uc中的粘膜病毒组的功能改变
[0273]
接着比较了健康和uc之间的粘膜病毒组功能。尽管最丰富的功能的丰度在健康和uc之间无差异,但健康个体显示更丰富的病毒组功能(根据go和pfam蛋白质功能),而uc对象则显示大量的功能废止。尽管如此,仍确定了uc中的几种分子功能比健康粘膜病毒组更为丰富,包括:转录的dna模板负调控、β-内酰胺酶、谷氨酰胺酰胺转移酶、糖水解酶、ii/iv型分泌系统和多铜氧化酶,其均与细菌宿主的噬菌体裂解以及细菌功能有关。该结果表明,uc中富集的粘膜病毒功能与细菌适应性、致病性和抗生素抗性有关,并且uc粘膜中可能存在细菌与噬菌体之间的密集遗传交换。
[0274]
粘膜处的粘膜细菌组改变和病毒组与细菌组之间的跨界相互作用
[0275]
进一步相比健康对照粘膜评估了uc粘膜中的细菌微生物组改变。细菌多样性和丰富度显著增加(t检验,分别为p=0.024和0.007),表明uc患者粘膜中存在不同细菌的扩增。uc粘膜细菌组显示相比对照在门、科和属水平上的不同的结构。定量差异分析鉴定了许多在健康和uc粘膜之间不同的细菌分类。其中,相比对照,在uc中厚壁菌(门)、假单胞菌科、瘤胃球菌科、栖热菌科、未分类的梭菌目、韦荣球菌科(vellonellaceae)(科)和粪球菌(属)大量富集。
[0276]
为了表征粘膜中的细菌组和病毒组之间的关联,评估了细菌组和病毒组的α多样性(多样性、均匀度和丰富度)之间的相关性。在对照中,存在显著的界内α多样性相关性。然而,在对照中观察到的细菌界内α多样性相关性的显著性在uc中丢失,表明在uc中粘膜细菌微生物群的失衡状态多于粘膜病毒群的失衡。
[0277]
实施例5克罗恩病和粘附侵袭性大肠杆菌(aiec)
[0278]
克罗恩病中的fmt:aiec的存在与fmt结果
[0279]
背景
[0280]
克罗恩病(cd)是两种主要的炎性肠病(ibd)之一,是一种终生致残性肠病。在中国香港,克罗恩病的发病率在过去十年中增长了7倍。引起克罗恩病的原因未知。尽管遗传因素可能起作用,但有力的证据表明,肠内细菌可能是疾病发展的基础。fmt目前正被探索作为ibd的潜在疗法。然而,尚不清楚影响治疗结果的机制和因素。粘附侵袭性大肠杆菌(aiec)可以侵袭肠上皮并在ibd患者的粘膜上定殖。它们还可以在巨噬细胞内生存而不诱导细胞死亡,从而使它们潜伏在粘膜中并长期造成损害。由于fmt直接改变了肠腔的内容物,我们假设fmt可能无法根除上皮细胞内存在的aiec细菌,并且巨噬细胞可能继续引起炎症。因此,我们的研究的目的是确定aiec菌株的存在是否会使fmt无效并恶化疾病的结果。
[0281]
方法
[0282]
研究对象
[0283]
在中国香港招募了患有回肠克罗恩病(疾病位置为根据蒙特利尔分型的l1-回肠或l3-回肠结肠)的患者。患者年龄≥18岁,通过内窥镜检查、放射学和组织学(回肠或回肠结肠)确诊为回肠克罗恩病。没有ibd的对象被招募为对照。这些由≥18岁的个体(他们将接受息肉结肠镜检查或结肠直肠癌筛查,或者胃肠道症状的调查),以及患者在当地医院的朋
友和配偶或伴侣,或任何有兴趣参加此研究的个体组成。使用标准化数据采集表格采集临床数据,并在回肠结肠镜检查期间采集回肠活检样品。然后将活检样品保存在-80℃下以用于下游分析。如果对象在采集活检样品的3个月内服用了抗生素、益生菌或益生元,则将其排除在外。所有对象都同意参加。
[0284]
粘膜大肠杆菌水平的定量和回肠粘膜上定殖的大肠杆菌菌株的分离
[0285]
将活检样品解冻并称重,以计算分离出的细菌相对于组织的重量。通过在pbs中轻轻摇动5分钟来分离与粘膜表面肠粘膜粘附生物群相关的细菌。通过用triton 1x和ultra-turrax处理活检样品来释放内在的细菌。将分离出的细菌在37℃下培养过夜。第二天对菌落形成单位(cfu)计数,以定量与粘膜相关的大肠杆菌。通过将菌落形成单位的数量除以粘膜活检样品的重量来计算粘膜大肠杆菌水平。
[0286]
对于每名患者,将在drigalski培养基上分离的且对乳糖代谢呈阳性(大肠杆菌差异特征)的来自粘膜相关大肠杆菌的48个细菌集落,在补充有15%甘油的luria-bertani培养基的96孔微孔板中进行培养并储存在-80℃下。
[0287]
aiec阳性的确定
[0288]
通过首先分离粘膜活检样品中的大肠杆菌菌株(按上文所述),然后筛选分离菌株中的aiec菌株的主要特征,并基于aiec的这些特征进行分级,来确定代表aiec存在的aiec阳性。aiec的主要特征包括粘附、对肠上皮细胞的侵袭和巨噬细胞内的存活。将相对于初始接种物具有大于或等于0.1的侵袭指数,且具有于感染后24小时在巨噬细胞内生存和繁殖的能力(在巨噬细胞中的%生存大于100)的大肠杆菌菌株视为aiec。
[0289]
dss结肠炎小鼠模型中的细菌给予和粪便微生物群移植
[0290]
使用8-9周大的雄性c57b/l6野生型小鼠(n=50)构建急性dss结肠炎小鼠模型,以研究fmt对aiec感染的小鼠的影响。一组小鼠仅给予干净的饮用水,以作为对照(n=6)。44只小鼠给予补充有2%dss的饮用水。
[0291]
在分离自cd患者的21种aiec菌株中,选择了一种具有最强的侵袭能力的菌株aiec 62d用于动物实验。从dss处理的第一天开始,连续3天给小鼠灌服109cfu剂量的该aiec菌株(n=22),或非致病性大肠杆菌菌株k12(n=22)。
[0292]
从健康小鼠采集粪便并用无菌pbs以1:10稀释。沉降后,连续3天给每只小鼠灌服200μl的上清液,以作为fmt处理。在第7天处死来自aiec组和k12组(n=6,每组)的小鼠,以作为“fmt之前”组。然后从第7天开始连续3天给剩下的32只小鼠灌服来自健康小鼠的粪便物质或无菌pbs(n=8,每组)。
[0293]
小鼠中的粪便aiec的定量
[0294]
通过在含有氨苄青霉素(50μg/ml)和红霉素(25μg/ml)的lb琼脂板上接种pbs重悬的粪便来进行计数,因为aiec菌株耐受这些抗生素,并且在未感染的小鼠中未发现这样的耐受性细菌。在第二天,对集落形成单位(cfu)计数,并评估每mg粪便的cfu数量。
[0295]
小鼠中的结肠炎严重程度的评估
[0296]
每天测量小鼠的体重。两天采集粪便样品。在处死时测量结肠长度和组织学评分,以评估结肠炎的严重程度。测量从盲肠至直肠的结肠长度。按如下对h&e染色的结肠组织进行盲化的组织学评分。基于上皮损伤和侵润至粘膜、粘膜下层和肌层/浆膜内的炎症的程度,为每个部分分配4个评分,使得每只小鼠的总评分范围为0
–
12。然后将对照组和dss处理
组的平均分数制成表格。
[0297]
小鼠样本的dna提取和16s rrna测序
[0298]
提取近端结肠组织dna以评估与粘膜相关的微生物群。来自在第7天处死的小鼠的粪便和组织被表征为“fmt之前”,而在第14天收获的粪便和组织被表征为“fmt之后”。根据厂商说明书,使用16组织dna纯化试剂盒提取dna。将提取的dna送至novogene(hk)有限公司进行文库构建,并在illumina pe250平台上进行16s rrna的v3-v4区的测序。
[0299]
生物信息学分析
[0300]
使用mothur pipline进行原始数据至out表的转换。通过97%相似性进行序列分类。
[0301]
发现
[0302]
aiec阳性cd患者中存在的粘膜大肠杆菌水平比aiec阴性cd患者和健康对照中的更高
[0303]
已报导当相比健康对照时,cd患者粘膜中的大肠杆菌被过分代表(over-represented)。为了评估在合并aiec的cd患者粘膜中大肠杆菌是否被进一步过分代表,测量了取自56名具有回肠受累的cd对象和24名健康对照的回肠粘膜中的总大肠杆菌载荷。
[0304]
在我们检测的所有对象中,37.5%(n=21)的cd患者和8.3%(n=2)的健康对照为aiec阳性。aiec阳性患者的总大肠杆菌载荷明显高于aiec阴性患者和健康对照(对数转换后为p=0.0323和p《0.001,turkey’s多重比较检验)。
[0305]
在fmt之后小鼠中的粪便aiec水平仅瞬时降低
[0306]
研究了fmt对感染了aiec的dss结肠炎小鼠中的aiec水平的影响。在粪便样品中评估了fmt之前和fmt之后小鼠中的aiec载荷的变化。在fmt处理的aiec小鼠中,在用fmt将小鼠处理连续3天后粪便aiec载荷立即下降,但随后逐渐上升。比较进行和未进行fmt的aiec小鼠发现,aiec感染后第9天和第12天fmt组中的粪便aiec载荷显著低于无fmt组中的那些。然而,在aiec感染后第14天,fmt组和无fmt组之间的aiec载荷差异变得显著。这些数据表明仅fmt可能不足以根除小鼠中的aiec。应合并特异性靶向aiec的治疗以根除持续性的aiec感染。
[0307]
fmt治疗结肠炎的功效受到aiec感染的损害
[0308]
接着研究了aiec对fmt治疗结肠炎的功效的影响。比较了感染了aiec的小鼠和感染了k12(一种非致病性大肠杆菌菌株)的小鼠之间的fmt影响。通过体重、结肠长度和组织学评分评估结肠炎的严重程度。
[0309]
对于体重,评估了fmt之后相比基线(第0天)的体重恢复百分比,在k12感染的小鼠中,以fmt处理的小鼠在第12天的体重恢复百分比高于无fmt的小鼠(99%vs 95%,p=0.0243,双因素anova)。另一方面,对于aiec感染的小鼠,在第14天有或无fmt处理的小鼠的体重未显示显著的差异(p=0.98,双因素anova)。比较fmt之后第14天的体重恢复发现,k12感染的小鼠的体重恢复至初始体重的97%,而感染了aiec的小鼠的体重仅恢复至91%(p=0.048,双因素anova)。
[0310]
对于结肠长度,在感染了aiec的小鼠中,fmt之前和fmt之后组间的结肠长度无显著差异(p=0.88,kruska-wallis检验,利用多重比较)。相反,在fmt之后k12感染的小鼠的结肠长度显著增加(fmt之前平均结肠长度
±
sem 6.80
±
0.12mm vs fmt之后8.02
±
0.27mm,p=0.0042,非配对t检验)。
[0311]
对于组织学评分,在fmt之后,aiec感染的小鼠相比感染了k12的小鼠中的组织学评分的改善较少(2.0vs 3.0,p=0.086,曼-惠特尼检验),表明aiec感染的小鼠中的结肠炎恢复较少。这些结果表明fmt改善了aiec阴性(k12感染的)小鼠中的dss诱导的结肠炎,但其功效在aiec存在下受到损害。
[0312]
尽管以fmt治疗但aiec感染的小鼠中缺乏有利的细菌
[0313]
分析了fmt之前和fmt之后上述aiec感染的和k12感染的小鼠的粘膜和粪便微生物群。小鼠肠道中存在的aiec造成小鼠粪便微生物群的细菌多样性减小。fmt治疗增加了k12感染的小鼠但非aiec感染的小鼠的α多样性。lefse分析揭示了几种成功移植k12小鼠但未能在aiec感染的小鼠中定殖的分类。这些分类中的大多数属于厚壁菌科,这类似于ibd患者粘膜微生物群的特征,表明aiec是小鼠粘膜中失调的一个驱动因素。这些数据表明aiec在ibd发病机理中的偶然作用。这些分类在表11中列出。
[0314]
aiec的存在可能会阻碍fmt效力。阻止潜在有益的共生生物的定殖可能是aiec影响fmt功效的一种机制。
[0315]
实施例6肥胖症
[0316]
方法
[0317]
fmt用于肥胖症和体重操纵的开放标记人类研究
[0318]
在肥胖对象中进行了粪便微生物群移植的开放标记的临床试验(nct03789461)。招募了年龄为18-75岁、具有≥28kg/m2和《45kg/m2的体质指数(bmi),且获得了知情同意书的对象。在本研究期间,对象接受了密集的fmt,为期总共20天。在治疗期间,对象每周接受5天的fmt(进行5天,和休息2天)。在同一时期,对象还接受了饮食和生活方式建议。
[0319]
fmt:粪便获自来自包括配偶或伴侣、一级亲属、其他亲属、朋友和受体了解或不了解的其他人在内的一般人群的志愿者。在粪便捐赠之前,通过问卷调查和实验室测试筛选志愿者。进行了一系列针对传染病的实验室测试和访谈。在该研究中使用了来自合格供体的粪便。在接受fmt之前,对象接受了5天的抗生素,其由以下内容组成:每天3次的万古霉素500mg;每天3次的甲硝唑500mg;以及每天3次的阿莫西林500mg,以增强来自fmt的微生物群的移植。然后对象接受了20天的fmt。在住院或门诊中通过标准程序向患者输注100-200ml的fmt溶液,包括食管-胃-十二指肠镜(ogd)、乙状结肠镜或灌肠。
[0320]
1.经ogd:经ogd在2-3分钟内向远端十二指肠或空肠中输注100-200ml的fmt溶液。输注后,对象在离开前监测1小时。
[0321]
2.经乙状结肠镜:经乙状结肠镜在2-3分钟内向远端结肠输注100-200ml的fmt溶液。输注后,对象在离开前监测1小时。
[0322]
3.经灌肠:通过自我给药或在研究小组的帮助下经灌肠给予100-150ml的fmt溶液。对象被指示保留灌肠剂20-30分钟。在每次灌肠前给予4mg洛派丁胺,以增加fmt溶液的保留。
[0323]
粪便dna分离和宏基因组测序
[0324]
使用dneasy血液和组织试剂盒(qiagen),根据厂商的方案提取采自供体的粪便样品dna,并进一步纯化。通过首先根据厂商说明书(illumina)构建具有350bp的插入大小的配对末端文库,并在novaseq illumina测序仪上测序来进行宏基因组测序。利用
metaphlan2,使用默认参数计算群落组成。在r程序包vegan中计算细菌分类概要、微生物多样性的稀疏性分析、组成差异(通过未加权的unifrac距离所指示的差异度值)。
[0325]
发现
[0326]
分析了达到第8周时肥胖对象的体重变化。5名连续的对象接受了来自3名不同的供体的fmt。通过宏基因组测序对这些供体的粪便细菌组进行特性分析。供体15和供体16具有2种和3种》0.1的相对丰度的对体重减轻有利的物种(表12);以及2种相对丰度≤0.01%的对体重减轻不利的物种(表13)。相反,供体8不具有供体15和供体16所具有的这些有利的细菌,并且2种不利的物种的相对丰度为》0.01%(表12和表13)。基于这些特性,供体8被认为是对体重减轻不利的供体,而供体15和16被认为是对体重减轻有利的供体。在第8周,接受来自供体15和16的fmt的对象具有比供体8的受体更多的体重减轻(表14)。
[0327]
实施例7肥胖症和脂质代谢
[0328]
用于肥胖症和脂质代谢的实验模型
[0329]
细菌和培养基
[0330]
华德萨特菌(sutterella wadsworthensis)培养条件
[0331]
华德萨特菌(sw)获自dsmz,脂质培养基无葡萄糖,补充有不同组合的对应于2%蔗糖浓度的糖浆;乳酸钠(chempur poland)7.41g/l;乙酸钠(chempur poland)7g/l;和0.2%酵母提取物(bd bioscences usa)。所有培养基的起始ph都是7.0。于37℃下,在由5.9%氧、7.2%二氧化碳、3.6%氢气和83.3%氮气组成的微需氧气氛下孵育培养物。使用来自microbiology b.v.(9200jb drachten,netherlands)的气氛生成系统产生该气氛。碎肉碳水化合物培养基(cm)购自bd。在厌氧条件(coy laboratory products,75%n2,20%co2,5%h2)下,于37℃在非震荡下培养培养物。每周评估板两次,维持达1个月。通过16s rrna基因测序和ncbi blast上的序列搜索来鉴定被认为是革兰氏阴性的和氧气敏感的(借助于室内空气中失败的亚克隆)任何细菌分离物。
[0332]
肠道罗斯拜瑞氏菌(roseburia intestinalis)培养条件
[0333]
肠道罗斯拜瑞氏菌(ri)购自dsmz保藏中心,制备了dsm-13018培养基,并使用无氧装置进行厌氧维持。通过在37℃下,于7
±
5ml等分的m2gsc培养基中培养16
–
18h来定期维持分离物。底物利用和水解作用。培养基由(100ml中)1g酪胨、0
±
2.5g酵母提取物、0
±
4g nahco3、0
±
1g半胱氨酸、0
±
0.45g k2hpo4、0
±
0.45g kh2po4、0
±
09g nacl、0
±
009g mgso4、0
±
009g cacl2、0
±
1mg刃天青、1mg氯化血红素、1μg生物素、1μg钴胺素、3μg对氨基苯甲酸、5μg叶酸和15μg吡哆胺组成。多酸光岗菌(mitsuokella multacida)培养条件
[0334]
多酸光岗菌(mm)作为甘油储存物在-20℃下保持冷冻。将含有麦芽糖和葡萄糖(0.1%w/v)的l-10液体或固体(1%w/v琼脂)培养基,或含有10%(v/v)瘤胃液、0.2%(w/v)葡萄糖、0.2%(w/v)纤维二糖和0.3%(v/v)淀粉[1]的改良scott和dehority培养基用于培养。在厌氧和静止条件下,在由co2/h2(90:10)组成的气氛中,在37℃的温度下,或者在39℃下,于100%co2中,在含有5ml培养基的亨盖特管中培养培养物。
[0335]
小鼠模型
[0336]
从香港中文大学购买八周大的雄性c57bl/6小鼠(平均初始重量20g),并在实验前使其适应动物设施环境两周。在所有实验中,均使用雄性小鼠。所有小鼠都保持在严格的24小时光照-黑暗周期下,光照时间为上午6点至下午6点。每个实验组由每组两个笼子组成,
以控制笼效应(n=5只/笼)。
[0337]
小鼠分成5组,即sw组、mm组、ri组、培养基组和联合(sw、mm和ri的组合)组。每5天给予小鼠1*109剂量的3种单一的细菌或联合(3种细菌的组合,且每种占33.33%)。每5天测量体重。研究设计显示在图11中。
[0338]
抗生素
[0339]
对于抗生素处理,按先前所述,在其饮水中给予小鼠卡那霉素(0.4mg/ml)、庆大霉素(0.035mg/ml)、粘菌素(850u/ml)、甲硝唑(0.215mg/ml)和万古霉素(0.045mg/ml)的组合,为期两周。
[0340]
立即将样品转移到动物设施的亨盖特厌氧培养管中,并通过口服灌喂将上清液和细菌给予小鼠。在预定日期,于黑暗阶段开始时采集粪便,并立即将其快速冷冻并转移以在80℃下储存,直至进一步处理。
[0341]
脂质特性
[0342]
第6次给予后20天,通过颈脱位法处死小鼠以用于血液采集。在非肝素化的管中采集血液样品并于4℃在1,600
×
g下离心10min。使用购自南京建成生物工程研究所(nanjing jiancheng bioengineering institute)(nanjing,china)的试剂盒,通过fisher multiskan fc多功能检测微孔板读数仪测定血清tg(gpo-pap测定;目录号a110-1)、tc(gpo-pap测定;目录号a111-1)、ldl-c(目录号a113-1)和hdl-c(目录号a112-1)的水平。tg和tc的水平在510nm下测定,并表示为mmol/l。ldl-c和hdl-c的水平在546nm下测定并表示为mmol/l。
[0343]
发现
[0344]
给予华德萨特菌(sw)显著降低了体重增加(p《0.001;双因素重复测量anova),而给予肠道罗斯拜瑞氏菌(ri)显示体重增加减少的趋势。在第15天后(在3次口服灌喂后)效应特别明显(图12)。计算了每只小鼠在第20天和第45天相比第0天的体重增加百分比。相比给予培养基的那些,给予sw和ri的小鼠第20天和第45天的体重增加百分比明显更低(图13)。平均食物摄取计算为克食物摄取/小鼠
·
天。在给予联合(sw、mm和ri的组合)、多酸光岗菌(mm)、ri和sw后,平均食物摄取显示降低的趋势,这与仅给予培养基相反,其显示增加的趋势。减少食物摄取的效应在ri和sw中最明显(图14)。平均食物效率计算为每只小鼠的5天中的体重增加(克)/这5天中总的食物摄取(克)。相比给予培养基,给予联合、mm、ri和sw的小鼠第15天之后的平均食物效率降低(图15)。研究了对脂质代谢的影响。仅给予sw降低了ldl-c、总胆固醇(tc)和甘油三酯(tg)。仅给予ri降低了ldl-c和tc。给予联合降低了ldl-c和tc。所有结果均与第45天的给予培养基的对照进行比较(图16)。
[0345]
缩写sw:华德萨特菌;ri-肠道罗斯拜瑞氏菌;mm:多酸光岗菌;hdl-c:高密度脂蛋白胆固醇;ldl-c:低密度脂蛋白胆固醇;tg:甘油三酯;tc:总胆固醇;ogtt:口服葡萄糖耐量试验;itt:胰岛素耐量试验。
[0346]
实施例8耐碳青霉烯的肠杆菌科
[0347]
方法
[0348]
fmt用于根除人类中的cre的临床试验
[0349]
年龄≥18岁、具有至少间隔一周的两次或更多次粪便或直肠拭子cre阳性,且在fmt输注前至少48小时未接受抗微生物治疗的患者被招募至临床试验(nct03479710)中。患
有需要进行抗微生物治疗的cre或vre活动性感染、怀孕、活动性胃肠道感染或炎症性病症、近期接受过腹部内手术、患有短肠综合征或使用改变胃肠运动的药物的患者被排除在外。cre定义为存在对任何碳青霉烯类具有耐受性的任何肠杆菌科。总共招募了3名患有cre的对象、供体和4名健康家庭成员对象,并获得了基线的粪便样品以用于微生物组分析。供体和受体的样品采集时间线显示在图17中。
[0350]
在本研究中,患者接受了利用冷冻的供体粪便样品的2次fmt。在2-3分钟内,经食管-胃-十二指肠镜(ogd)向远端十二指肠或空肠中输注100ml的于0.9%无菌盐水中的fmt溶液(原始粪便50g)。在fmt之前和fmt之后预先从患者采集粪便样品。对于这2次fmt,受体接受来自相同单一供体的fmt。
[0351]
用于fmt输注的粪便获自招募至香港中文大学医学院粪便生物库(stool biobank for the faculty of medicine,the chinese university of hong kong)的供体。供体为来自包括配偶或伴侣、一级亲属、其他亲属、朋友和潜在患者了解或不了解的其他人在内的一般人群的志愿者。供体需要满足一系列资格标准,并且通过了筛查包括cre和耐万古霉素的肠球菌(vre)在内的传染病的实验室测试。
[0352]
粪便dna提取
[0353]
将约100mg粪便样品用1ml ddh2o预洗涤,并通过以13,000
×
g离心1分钟来沉淀。将粪便沉淀重悬于补充有1.6μl 2-巯基乙醇和500u溶细胞酶(sigma)的800μl te缓冲液(ph 7.5)中,并在37℃下孵育60min。然后将样品以13,000
×
g离心2min,并弃去上清液。预处理后,随后使用rsc purefood gmo and authentication试剂盒(promega),按照厂商说明书,从沉淀物中提取粪便dna。简言之,向粪便沉淀物中加入1ml ctab缓冲液并涡旋30秒,然后将样品在95℃下加热5分钟。之后,将样品与珠以最大速度彻底涡旋15min。然后将40μl蛋白酶k和20μlrna酶a加入样品中,并将混合物在70℃下孵育10分钟。然后通过以13,000
×
g离心5分钟来获得上清液,然后将其加入到rsc机器中用于dna提取。对提取的粪便dna进行16s rdna测序和宏基因组测序。
[0354]
宏基因组测序和分析
[0355]
将合格的粪便dna切成片段,通过末端修复、向尾部添加a、纯化和pcr扩增的过程来制备测序文库。由北京基因组研究所(the beijing genomics institute,bgi),在illumina hiseqxten pe150平台上对粪便dna文库进行深度测序,且产生了每个样品平均4800
±
530万的读取(12g数据)。
[0356]
按如下方式通过trimmomatic v0.36 18对原始序列进行筛选和质量修剪:1)利用4:8的质量滑动窗口进行修剪;2)修剪序列以从开始去除20个碱基并从末端去除超过220的碱基;3)去除小于150bp长度的序列。然后通过kneaddata(https://bitbucket.org/biobakery/kneaddata/wiki/home,参考数据库:grch38 p12),利用默认参数滤除人宿主污染读取,以产生干净读取。
[0357]
在humann2 v0.11.1 19中执行细菌分类和功能特性分析,其过程包括:通过metaphlan2,利用分枝特异性的标记物biomarker20进行分类鉴定;通过bowtie2 21,利用chocophlan数据库进行物种泛基因组(pangenomes)的注释;利用diamond 22,针对uniref90通用蛋白质参考数据库23进行未映射的读取的翻译搜索,通路采集(pathway collection)利用metacyc数据库24从产生的基因列表获得。合并所有样品的基因家族和通
路丰度文件,然后标准化为相对丰度。
[0358]
使用kraken2 v2.0.7-beta从粪便dna宏基因组数据集中确定了真菌的分类特性。利用jellyfish程序,通过利用映射至具有精确的k-mer匹配的所有参考基因组的最低共有祖先的读取中的每个k-mer对参考文库中的独特31-mer计数,从ncbi构建了完整的ncbi真菌和病毒refseq数据库25。其后,通过修剪映射的基因组所属的一般分类树,将每次查询分入具有匹配的k-mer的最高总匹配的分类中。
[0359]
统计分析
[0360]
将细菌、病毒、真菌的丰度数据输入r 3.3.5中。使用phyloseq程序包进行丰富度、多样性和稀疏性的计算。通过vegan r程序包计算基于微生物群落结构的bray-curtis相异性矩阵的主成分分析主坐标分析(pcoa)。使用ggplot r程序包执行热图。
[0361]
发现
[0362]
瘤胃球菌(ruminococcus sp_5_1_39bfaa)、collinsella tanakaei和eubacterium sicaeum的相对丰度在fmt之前检测不到,且在fmt之后增加至与供体相似的水平或甚至更高(图18)。lefse分析也表明相比fmt之前样品,fmt之后样品中的这些细菌显著增加,其lda得分》2.0(图20)。这些代表了对cre去定殖有利的细菌(表15)。
[0363]
为了解答fmt是否影响肠微生物组的问题,进行了真菌富集的深度宏基因组测序,然后使用kraken2将序列读取与参考数据库进行比对以鉴定真菌分类。在fmt之后患者肠道真菌群落的α多样性显示随时间广泛的波动(图20a),fmt之后样品中的真菌群落显示与来自其相应的供体的真菌群落的降低的差异性(图20b),表明受体中供体真菌的可能的移植或受体真菌群落向健康状态的恢复。经lefse对fmt之前和fmt之后的粪便微生物组的进一步的判别分析显示xylonales、节担菌(wallemiales)、ceraceosorales为fmt之后的粪便中差异富集的属(图20c,lda效应量》2,p《0.05)。更详细的物种水平特性分析揭示了fmt之后每名受体的分类差异,例如cre患者移植了22种真菌,包括栎迷孔菌(daedalea quercina)、彩色豆马勃(pisolithus tinctorius)和落花生曲霉(aspergillus arachidicola)(图20d,表16)。虽然fmt之后转移的微生物群主要由细菌组成,但也可能存在一些真菌移植,尽管是以较小的数量。
[0364]
本技术中引用的所有专利、专利申请和其他出版物,包括genbank登录号和其他序列识别号,均通过引用整体并入本文中,用于所有目的。
[0365]
表1a用于诱导体重减轻的fmt供体中存在的“有利的”细菌
[0366][0367]
*相对丰度计算为属于分类的所有序列的数量除以样品中检测的所有序列的数量
[0368]
表1b供体中的对使用fmt诱导体重减轻最大“不利的”细菌
[0369]
[0370][0371]
*相对丰度计算为属于分类的所有序列的数量除以样品中检测的所有序列的数量
[0372]
表2供体中的对使用fmt诱导体重减轻“有利的”真菌
[0373][0374]
*相对丰度计算为属于分类的所有序列的数量除以样品中检测的所有序列的数量
[0375]
表3a受体中与成功的体重减轻相关的真菌
[0376][0377]
*相对丰度计算为属于分类的所有序列的数量除以样品中检测的所有序列的数量
[0378]
表3b受体中与体重减轻失败相关的真菌
[0379][0380]
*相对丰度计算为属于分类的所有序列的数量除以样品中检测的所有序列的数量
[0381]
#为了提高体重减轻干预的效力,受体中的相对丰度应保持低于这些值
[0382]
表4供体中对使用fmt治疗cre“有利的”细菌
[0383]
[0384][0385]
*相对丰度计算为属于分类的所有序列的数量除以样品中检测的所有序列的数量
[0386]
表5供体中对使用fmt治疗cre“有利的”真菌
[0387]
[0388][0389]
*相对丰度计算为属于分类的所有序列的数量除以样品中检测到的所有序列的数量
[0390]
表6a供体中对使用fmt治疗急性移植物抗宿主病“有利的”细菌
[0391][0392]
表6b供体中对使用fmt治疗agvhd“不利的”细菌的最大丰度
[0393][0394]
表7a供体中对使用fmt治疗agvhd“有利的”真菌
[0395]
[0396][0397]
表7b供体中对使用fmt治疗agvhd“不利的”真菌
[0398][0399]
表8a溃疡性结肠炎中过分代表的病毒分类
[0400][0401]
表8b uc中未充分代表的病毒分类
[0402][0403][0404]
表9a肠型2相比肠型1中过分代表的病毒
[0405][0406]
表9b肠型2相比肠型1中未充分代表的病毒
[0407]
[0408][0409]
表10a uc中过分代表的细菌分类
[0410]
[0411]
表10b uc中未充分代表的细菌分类
[0412]
分类(科/属/种)lda效应量变形菌(门)5.8313放线菌(门)4.7581梭杆菌(门)4.5352草酸杆菌(科)5.6387梭杆菌(科)4.5406纤维素单胞菌(科)4.4426梭杆菌(属)4.5392马赛菌(属)5.6450埃希菌(属)4.7503纤维素单胞菌(属)4.4122
[0413]
表11能够提高具有aiec的克罗恩病患者中的fmt效力的细菌的补充
[0414]
[0415][0416]
*通过重要性顺序排序
[0417]
表12来自d8、d15和d16的有利粪便样品的相对丰度(%)。
[0418][0419]
表13来自d8、d15和d16的不利粪便样品的相对丰度(%)。
[0420][0421]
表14 fmt受体在接受来自d8、d15和d16的fmt之后的特征和体重减轻
[0422]
受体研究编号fb001fb002fb003fb004fb005性别mmfff粪便供体d8d8d8d16d15原始体重113.4127.195.5111.698.3第4周时的体重减轻-2.4%0.3%-0.5%-2.4%-1.8%第6周时的体重减轻-2.4%-1.3%-2.4%-3.3%na第8周时的体重减轻-2.8%1.0%-1.9%-3.8%-5.5%
[0423]
表15供体中对使用fmt治疗cre“有利的”细菌
[0424][0425]
表16供体中对使用fmt治疗cre“有利的”真菌
[0426]
[0427]
