1.本发明涉及液晶化合物技术领域,具体涉及一种新型的液晶化合物,同时还涉及其应用。
背景技术:
2.近年来液晶显示装置发展越来越迅速,也出现了不同类型的液晶显示装置,如车载小型液晶显示装置、便携式液晶显示装置、超薄型液晶显示装置等等。本领域开发正在取得进展,以液晶电视为例,其特点是重量轻、占据空间小、移动方便,同样还有笔记本型个人电脑、掌上电脑、手机等。
3.液晶材料在信息显示材料、有机光电子材料等领域中的应用具有极大的研究价值和美好的应用前景。目前,tft-lcd产品技术已经成熟,成功地解决了视角、分辨率、色饱和度和亮度等技术难题,大尺寸和中小尺寸tft-lcd显示器在各自的领域已逐渐占据平板显示器的主流地位。同时,现在对显示技术的要求也一直在不断提高,例如要求液晶显示器能实现更快速的响应,降低驱动电压以降低功耗等,也就要求液晶材料要具有低电压驱动、快速响应、宽的温度范围和良好的低温稳定性等性能。
4.液晶材料本身对改善液晶显示器的性能发挥着重要的作用,尤其是通过降低液晶材料旋转粘度、提高液晶材料的介电各向异性
△
ε,可以显著改善液晶显示器的性能。因此,为了改善液晶材料的性能使其适应新的要求,新型结构的液晶化合物的合成及结构-性能关系的研究已成为液晶领域的一项重要工作。
技术实现要素:
5.本发明的目的在于开发一种新的液晶化合物,特别是一种含氟苯并呋喃类液晶化合物,该类化合物具有较高的负介电各向异性、良好的液晶互溶性、相对低的旋转粘度等,可以改善液晶材料性能,具有重要的应用价值。
6.第一方面,本发明提供了一种液晶化合物,所述液晶化合物具有如通式(i)所示的结构:
[0007][0008]
其中,r1和r2彼此独立地表示具有1-12个碳原子的烷基、烷氧基或烯基;
[0009]
a1、a2和a3彼此独立地表示1,4-亚苯基、1,4-亚环己基、1,4-亚环己烯基或氟代1,
4-亚苯基;
[0010]
z1、z2和z3彼此独立地表示单键、双键、氧原子、-cf2o-、-ch2ch
2-、-ch2o-、-och
2-或-ch=ch-;
[0011]
x表示氧原子、硫原子、-ch
2-、-cf
2-或-chf-;
[0012]
m、n、p彼此独立地表示0,1或2。
[0013]
其中,所述氟代1,4-亚苯基为单氟代1,4-亚苯基、二氟代1,4-亚苯基、三氟代1,4-亚苯基或四氟代1,4-亚苯基;优选地,所述氟代1,4-亚苯基为单氟代1,4-亚苯基或二氟代1,4-亚苯基。
[0014]
作为本发明一种优选的实施方案,所述x表示氧原子。
[0015]
作为本发明一种优选的实施方案,所述m、n、p彼此独立地表示0或1。
[0016]
作为本发明一种优选的实施方案,所述r1和r2彼此独立地表示具有1-5个碳原子的烷基、烷氧基或烯基。
[0017]
进一步优选地,所述r1和r2彼此独立地表示具有2-5个碳原子的烷基、烷氧基或烯基。
[0018]
更优选地,所述r1和r2彼此独立地选自乙基、正丙基、正丁基、正戊基、乙氧基、丙氧基、丁氧基。
[0019]
作为本发明一种优选的实施方案,所述z1、z2和z3均表示单键。
[0020]
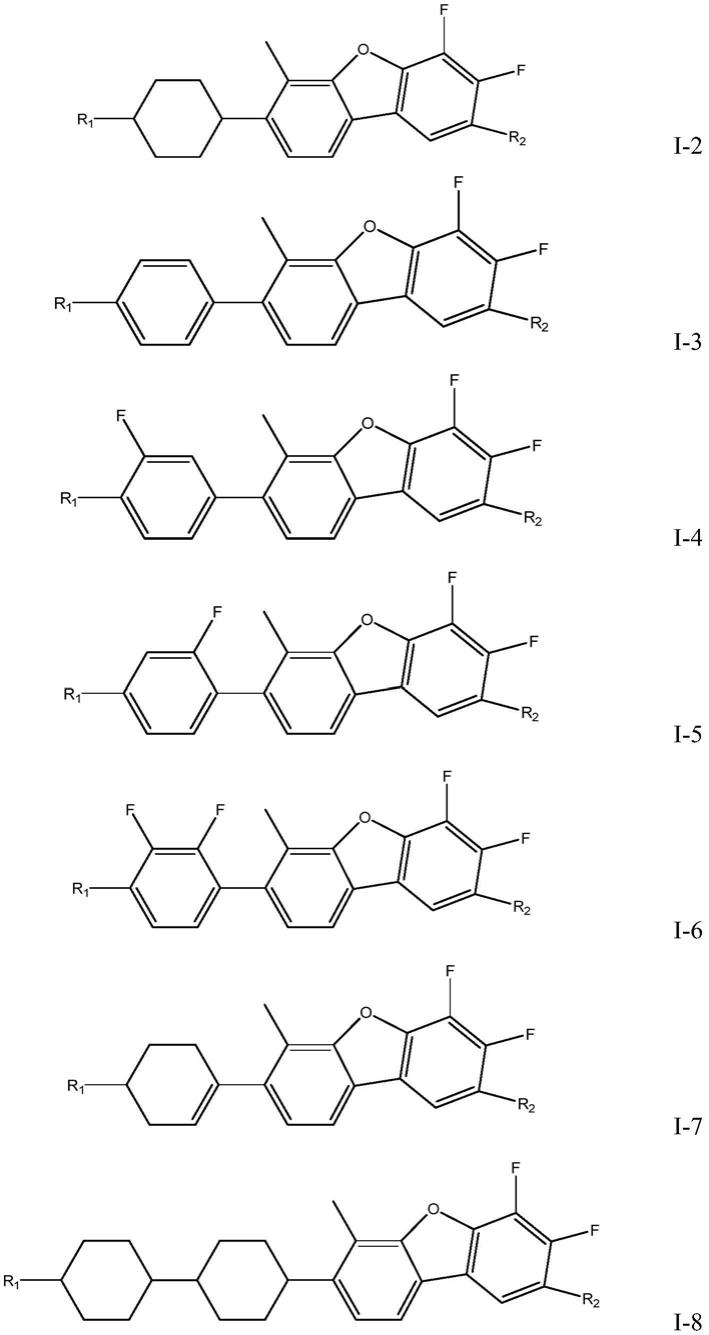
作为本发明一种优选的实施方案,所述液晶化合物选自如下通式i-1~i-17任一所示的结构:
[0021]
[0022]
[0023][0024]
其中,上述通式i-1~i-17中,所述r1和r2均彼此独立地表示具有1-5个碳原子的烷基、烷氧基或烯基。
[0025]
进一步优选地,上述通式i-1~i-17中,所述r1和r2均彼此独立地表示具有2-5个碳原子的烷基、烷氧基或烯基。
[0026]
更优选地,所述r1和r2彼此独立地选自乙基、正丙基、正丁基、正戊基、乙氧基、丙氧基、丁氧基。
[0027]
作为本发明一种优选的实施方案,所述液晶化合物任选自以下结构式所示化合物:
[0028]
[0029]
[0030][0031]
第二方面,本发明提供了一种所述的液晶化合物的制备方法,根据通式中取代基的不同,可以通过以下几种方法来合成。
[0032]
第一种方法,当通式(i)中m、n、p均为0时,即所述液晶化合物通式为:
[0033][0034]
合成路线为:
[0035][0036]
合成方法包括步骤:
[0037]
(1)以为起始原料,先与有机锂试剂反应,再与硼酸酯反应,得到
[0038]
(2)与通过suzuki反应,得到
[0039]
(3)所述在碱性条件下进行关环,得到
[0040]
(4)所述与有机锂试剂反应,再与硫酸二甲酯反应,得到
[0041]
其中,步骤(1)中,所述有机锂试剂、硼酸酯的投料摩尔比为1∶(1.0~4.0)∶(1.0~4.0),反应温度为-50~-100℃;
[0042]
所述有机锂试剂选自仲丁基锂、叔丁基锂、正丁基锂中的任一种或几种;
[0043]
所述硼酸酯选自硼酸三甲酯、硼酸三异丙酯、硼酸三丁酯、硼酸三异丁酯中的任一
种或几种;
[0044]
步骤(2)中,所述与的投料摩尔比为1∶(0.9~1.2),反应温度为60~120℃;
[0045]
步骤(3)中,所述关环时与碱的投料摩尔比为1∶(1.0~4.0),反应温度为70~150℃;
[0046]
所述碱为氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、叔丁醇钾中的任一种或几种,优选为叔丁醇钾和/或碳酸钾;
[0047]
步骤(4)中,所述有机锂试剂、硫酸二甲酯的投料摩尔比为1∶(1.0~4.0)∶(1.0~4.0),反应温度为-50~-100℃;
[0048]
其中,所述有机锂试剂选自仲丁基锂、叔丁基锂、正丁基锂中的任一种或几种。
[0049]
第二种方法,当通式(i)中n为0,m、p不同时为0时,即所述液晶化合物通式为:
[0050][0051]
合成路线为:
[0052][0053]
合成方法包括步骤:
[0054]
(1)以为起始原料,先与有机锂试剂反应,再与硼酸酯反应,得到
[0055]
(2)与所述通过suzuki反应,得到
[0056]
(3)所述在碱性条件下进行关环,得到
[0057]
(4)所述与有机锂试剂反应,再与硫酸二甲酯反应,得到
[0058]
其中,步骤(1)中,所述有机锂试剂、硼酸酯的投料摩尔比为1∶(1.0~4.0)∶(1.0~4.0),反应温度为-50~-100℃;
[0059]
所述有机锂试剂选自仲丁基锂、叔丁基锂、正丁基锂中的任一种或几种;
[0060]
所述硼酸酯选自硼酸三甲酯、硼酸三异丙酯、硼酸三丁酯、硼酸三异丁酯中的任一种或几种;
[0061]
步骤(2)中,所述与的投料摩尔比为1∶(0.9~1.2),反应温度60~120℃;
[0062]
步骤(3)中,所述关环时与碱的投料摩尔比为1∶(1.0~4.0),反应温度为70~150℃;
[0063]
所述碱为氢氧化钠、氢氧化钾、碳酸钠、碳酸钾、叔丁醇钾中的任一种或几种,优选为叔丁醇钾和/或碳酸钾;
[0064]
步骤(4)中,所述有机锂试剂、硫酸二甲酯的投料摩尔比为1∶(1.0~4.0)∶(1.0~4.0),反应温度为-50~-100℃;其中,所述有机锂试剂选自仲丁基锂、叔丁基锂、正丁基锂中的任一种或几种。
[0065]
以上制备方法中,所述r1和r2的定义同之前所述。
[0066]
采用上述制备方法能够稳定、高效地得到本发明所述的液晶化合物。
[0067]
第三方面,本发明提供了一种液晶材料组合物,所述液晶材料组合物中包含本发明所述的液晶化合物。
[0068]
所述液晶化合物在组合物中的质量百分比含量为0.1~60%,优选为1~40%,进一步优选为3~25%。
[0069]
第四方面,本发明提供了本发明所述的液晶化合物或者所述的液晶材料组合物在液相显示领域中的应用。
[0070]
作为一种优选的实施方案,本发明提供了本发明所述的液晶化合物或者所述的液晶材料组合物在液相显示装置中的应用。
[0071]
优选地,所述液晶显示装置包括但不限于tn、ads、va、psva、ffs、ips液晶显示器。
[0072]
本发明提供了一种新型的液晶化合物,特别是一种苯并呋喃类液晶化合物,该类化合物具有较高的负介电各向异性、良好的液晶互溶性、相对低的旋转粘度等,这些正是改善液晶材料所需要的,具有重要的应用价值。
[0073]
本发明所述液晶化合物或含有本发明所述液晶化合物的组合物具有极高的负介电各向异性,旋转粘度低,从而有效降低了驱动电压,提高了液晶显示装置的响应速度,同时具有光学各向异性数值适中、电荷保持率高等优点,是一种性能优良的液晶材料。
具体实施方式
[0074]
下面对本发明的技术方案进行详细说明。以下实施例用于说明本发明,但不用来限制本发明的范围。
[0075]
所述原材料如无特别说明,均能从公开商业途径获得。
[0076]
实施例1
[0077]
本实施例制备的液晶化合物的结构式为:
[0078][0079]
合成线路如下所示:
[0080][0081]
具体步骤如下:
[0082]
(1)化合物lc-01-1的合成:氮气保护下,向反应瓶中加入17.6g 3,4,5-三氟乙氧基苯(0.10mol)和160ml四氢呋喃,控温-75~-85℃滴加0.12mol正丁基锂的正己烷溶液,滴毕保温反应2小时,控温-75~-85℃滴加29.9g硼酸三丁酯(0.10mol),然后自然回温至-60℃保温2小时。加入200ml水淬灭反应,进行常规后处理,得到浅黄色固体(化合物lc-01-1)18.9g,hplc:98.8%,收率86.0%。
[0083]
(2)化合物lc-01-2的合成:氮气保护下,向反应瓶中加入18.9g化合物lc-01-1(0.086mol),30ml乙醇,甲苯60ml,水30ml,碳酸氢钠10g(0.12mol),2-羟基-4-丙基溴苯18.4g(0.086mol),升温至50℃,加入二氯二叔丁基-(4-二甲基氨基苯基)膦钯0.01g,继续升温至70℃-75℃回流2小时。反应后处理,得到白色固体24g,收率90%。采用gc-ms对所得白色固体lc-01-2进行分析,产物的m/z为310(m
+
)。
[0084]
(3)化合物lc-01-3的合成:氮气保护下,向反应瓶中加入24g化合物lc-01-2(0.077mol),n-n-二甲基甲酰胺200ml,碳酸钾15.9g(0.12mol),升温至110℃-120℃,反应4小时以上。反应后处理,得到白色固体21g,收率95%。采用gc-ms对所得白色固体lc-01-3进行分析,产物的m/z为290(m
+
)。
[0085]
(4)化合物lc-01的合成:氮气保护下,向反应瓶中加入21g化合物lc-01-3(0.072mol),四氢呋喃150ml,控温-75~-85℃滴加0.086mol正丁基锂的正己烷溶液,滴毕保温反应1小时,控温-70~-80℃滴加硫酸二甲酯18.9g(0.15mol)和四氢呋喃40ml,然后自然回温至室温保温反应10小时。加入100ml水淬灭反应,进行常规后处理,得到白色固体17.5g,收率80%,气相纯度99.9%。采用gc-ms对所得白色固体lc-01进行分析,产物的m/z为304(m
+
)。
[0086]
实施例2
[0087]
本实施例制备的液晶化合物的结构式为:
[0088][0089]
合成线路如下所示:
[0090][0091]
具体步骤如下:
[0092]
(1)化合物lc-02-2的合成:氮气保护下,向反应瓶中加入22g化合物lc-01-1(0.1mol),40ml乙醇,甲苯100ml,水40ml,碳酸钾22g(0.16mol),反式-4-丙基环己基-2-羟基-溴苯29.6g(0.1mol),升温至50℃,加入二氯二叔丁基-(4-二甲基氨基苯基)膦钯0.01g,继续升温至70℃-75℃回流2小时。反应后处理,得到白色固体35.3g,收率90%。采用gc-ms对所得白色固体lc-02-2进行分析,产物的m/z为392(m
+
)。
[0093]
(2)化合物lc-02-3的合成:氮气保护下,向反应瓶中加入35.3g化合物lc-02-2(0.09mol),n-n-二甲基甲酰胺260ml,叔丁醇钾12.3g(0.11mol),升温至110℃-120℃,反应4小时以上。反应后处理,得到白色固体31.8g,收率95%。采用gc-ms对所得白色固体lc-02-3进行分析,产物的m/z为372(m
+
)。
[0094]
(3)化合物lc-02的合成:氮气保护下,向反应瓶中加入31.8g化合物lc-02-3(0.085mol),四氢呋喃180ml,控温-75~-85℃滴加0.102mol正丁基锂的正己烷溶液,滴毕保温反应1小时,控温-70~-80℃滴加硫酸二甲酯22.4g(0.178mol)和四氢呋喃40ml,然后自然回温至室温保温反应10小时。加入100ml水淬灭反应,进行常规后处理,得到白色固26.2g,收率80%,气相纯度99.9%。采用gc-ms对所得白色固体lc-02进行分析,产物的m/z为386(m
+
)。
[0095]
实施例3
[0096]
本实施例制备的液晶化合物的结构式为:
[0097][0098]
合成线路如下所示:
[0099][0100]
具体步骤如下:
[0101]
(1)化合物lc-03-2的合成:氮气保护下,向反应瓶中加入22g化合物lc-01-1(0.1mol),40ml乙醇,甲苯100ml,水40ml,碳酸钾22g(0.16mol),4-丙基苯基-2-羟基-溴苯29g(0.1mol),升温至50℃,加入二氯二叔丁基-(4-二甲基氨基苯基)膦钯0.01g,继续升温至70℃-75℃回流2小时。反应后处理,得到白色固体34.7g,收率90%。采用gc-ms对所得白色固体lc-03-2进行分析,产物的m/z为386(m
+
)。
[0102]
(2)化合物lc-03-3的合成:氮气保护下,向反应瓶中加入34.7g化合物lc-03-2(0.09mol),n-n-二甲基甲酰胺260ml,叔丁醇钾12.3g(0.11mol),升温至110℃-120℃,反应4小时以上。反应后处理,得到白色固体31.2g,收率95%。采用gc-ms对所得白色固体lc-03-3进行分析,产物的m/z为366(m
+
)。
[0103]
(3)化合物lc-03的合成:氮气保护下,向反应瓶中加入31.2g化合物lc-03-3(0.085mol),四氢呋喃180ml,控温-75~-85℃滴加0.102mol正丁基锂的正己烷溶液,滴毕保温反应1小时,控温-70~-80℃滴加硫酸二甲酯22.4g(0.178mol)和四氢呋喃40ml,然后自然回温至室温保温反应10小时。加入100ml水淬灭反应,进行常规后处理,得到白色固25.9g,收率80%,气相纯度99.9%。采用gc-ms对所得白色固体lc-03进行分析,产物的m/z为380(m
+
)。
[0104]
以上在制备过程中,在必要时会涉及常规后处理,所述常规后处理具体如:用二氯甲烷、乙酸乙酯或甲苯萃取,分液,水洗,干燥,真空旋转蒸发仪蒸发,所得产物用减压蒸馏或重结晶和/或色谱分离法提纯等。
[0105]
按照本领域的常规检测方法,通过线性拟合得到了本发明实施例1-实施例3制备的液晶化合物的各项性能参数,其中,各性能参数的具体含义如下:
[0106]
△
n代表光学各向异性(25℃);
[0107]
△
ε代表介电各向异性(25℃,1000hz);
[0108]
γ1代表旋转粘度(mpa.s,25℃);
[0109]
cp代表液晶的清亮点。
[0110]
性能试验例1
[0111]
将实施例1所制得的化合物lc-01和对比例1的液晶化合物性能参数数据进行对比整理,检测结果如表1所示。
[0112]
表1
[0113][0114]
由表1的检测结果可以明显看出,本发明提供的液晶化合物与传统的相似化学结构的负介电各向异性化合物相比,具有较高的负介电各向异性、旋转粘度γ1适中,良好的低温互溶性和较高的清亮点性能,这些正是改善液晶材料所需要的,可以有效提高液晶组合物的介电各向异性
△
ε,降低驱动电压,得到响应速度更快的液晶组合物。
[0115]
性能试验例2
[0116]
同样,将实施例2所制得的化合物lc-02和对比例2的液晶化合物性能参数数据进行对比整理,检测结果如表2所示。
[0117]
表2
[0118][0119]
由表2的检测结果可以明显看出,本发明提供的液晶化合物与传统的相似化学结构的负介电各向异性化合物相比,具有较高的负介电各向异性、旋转粘度γ1适中,良好的低温互溶性和较高的清亮点性能,这些正是改善液晶材料所需要的,可以有效提高液晶组合物的介电各向异性
△
ε,降低驱动电压,得到响应速度更快的液晶组合物。
[0120]
性能试验例3
[0121]
将实施例3所制得的化合物lc-03和对比例3的液晶化合物性能参数数据进行对比整理,检测结果如表3所示。
[0122]
表3
[0123][0124]
由表3的检测结果可以明显看出,本发明提供的液晶化合物与传统的相似化学结构的负介电各向异性化合物相比,具有较高的负介电各向异性、旋转粘度γ1适中,良好的低温互溶性和较高的清亮点性能,这些正是改善液晶材料所需要的,可以有效提高液晶组合物的介电各向异性
△
ε,降低驱动电压,得到响应速度更快的液晶组合物。
[0125]
此外,将本方面的化合物具体应用在常规体系的液晶组合物中后发现,其可以提高液晶组合物的介电各向异性
△
ε,同时保持较低的旋转粘度γ1和适当的折射率各向异性
△
n,所得液晶组合物具有显著的快速响应特点和低电压驱动特点。
[0126]
虽然,上文中已经用一般性说明、具体实施方式及试验,对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
