1.本发明涉及了生物检测分析技术领域,特别是涉及了氟苯尼考半抗原、人工抗原、抗体及其合成方法和应用。
背景技术:
2.氟苯尼考(florfenicol,ff),又名氟甲砜霉素,是在八十年代后期人工合成的甲砜霉素单氟衍生物。作为一种新的兽医专用氯霉素类广谱抗菌药,我国于2000年批准其为国家二类新药。其药理作用机制主要是通过抑制肽酰基转移酶活性干扰细菌蛋白质的合成,从而产生广谱抑菌作用。由于氯霉素被禁用,氟苯尼考因其较强的抗菌效果和较低的毒副作用,已成为当前使用最广泛、用量最大的抗菌药物之一,广泛用于畜禽及水产养殖过程中疾病的预防和治疗。
3.然而,氟苯尼考消除半衰期长,临床上用药不合理易产生残留,通过食物链进入人体后,对消费者的健康安全造成威胁。为加强对动物性食品中氟苯尼考的残留监管,保证动物产品质量安全,欧盟委员会规定了动物组织中氟苯尼考的最大残留限量,其中在牛肌肉、肝脏和肾脏组织中的最大残留限量分别为200、3000和300μg/kg,泌乳期家畜禁用;我国农业部也规定了动物组织中氟苯尼考的最大残留限量,其中在家禽肌肉、脂肪、肝脏和肾脏组织中的最大残留限量分别为100、200、2500和750μg/kg,产蛋期家禽禁用。
4.目前,我国行业标准中对动物源性食品中氟苯尼考的残留检测主要采用液相色谱-串联质谱法。此方法虽然特异性强、灵敏度高,但是样品前处理复杂繁琐,检测时间长,成本也较高,难以实现快速、简便的现场检测要求,推广使用受到限制。
5.免疫分析方法是一种基于抗原与抗体特异性反应的定性定量分析方法,该方法特异性强、灵敏度高,反应快速,操作简单,适合现场大量样本的实时检测。抗原决定了抗体的特异性及灵敏度,因此制备高质量氟苯尼考人工抗原,开发灵敏度高的抗氟苯尼考抗体,对实现氟苯尼考药物残留的快速检测十分重要。
技术实现要素:
6.本发明提供氟苯尼考半抗原、人工抗原、抗体及其合成方法和应用。
7.本发明所要解决的技术问题通过以下技术方案予以实现:
8.第一方面,氟苯尼考半抗原,其特征在于,其结构式如式ⅰ所示:
[0009][0010]
作为本发明提供的所述的氟苯尼考半抗原的合成方法的一种优选实施方式,所述合成方法包括如下步骤:
[0011]
s1、以dmf为溶剂,加入氟苯尼考胺和4-(3-溴丙基)苯甲酸甲酯,向混合物中加入碘化钾和碳酸氢钠,搅拌;
[0012]
s2、将步骤s1的产物冷却至室温,加入水,并用乙酸乙酯萃取,用盐水洗涤合并有机层,用无水硫酸钠干燥,在真空下除去溶剂得到残留物;
[0013]
s3、以甲醇和thf作溶剂,加入步骤s2的产物、lioh水溶液,室温搅拌;
[0014]
s4、将s3得到的混合物浓缩,向残余物中加入水,然后用乙酸乙酯萃取混合物;向水层中添加h2so4将ph值调节至5左右;通过过滤收集混合物中的沉淀物,在真空下干燥,得到的白色固体为氟苯尼考半抗原。
[0015]
作为本发明提供的所述的氟苯尼考半抗原的合成方法的一种优选实施方式,所述合成方法包括如下步骤:
[0016]
s1、以dmf为溶剂,加入4.95g氟苯尼考胺和5.14g4-(3-溴丙基)苯甲酸甲酯,向混合物中加入3.60g碘化钾和3.36g碳酸氢钠,搅拌;
[0017]
s2、将步骤s1的产物冷却至室温,加入水,并用乙酸乙酯萃取,用盐水洗涤合并有机层,用无水硫酸钠干燥。在真空下除去溶剂得到残留物;
[0018]
s3、以甲醇和thf作溶剂,加入2.54g步骤s2的产物、20mllioh水溶液,室温搅拌;
[0019]
s4、将s3得到的混合物浓缩,向残余物中加入水,然后用乙酸乙酯萃取混合物;向水层中添加0.5mh2so4将ph值调节至5左右;通过过滤收集混合物中的沉淀物,在真空下干燥,得到的白色固体为氟苯尼考半抗原。
[0020]
第二方面,氟苯尼考人工抗原,所述氟苯尼考人工抗原由上述的氟苯尼考半抗原与载体蛋白偶联得到的;其中,所述载体蛋白为牛血清白蛋白、人血清白蛋白、甲状腺蛋白、卵清白蛋白或钥孔血蓝蛋白。
[0021]
第三方面,上述的氟苯尼考人工抗原的合成方法,其是采用活泼酯法将载体蛋白偶联于上述氟苯尼考半抗原的羧基端。
[0022]
第四方面,氟苯尼考抗体,其是由上述的氟苯尼考人工抗原经动物免疫得到。
[0023]
作为本发明提供的所述氟苯尼考抗体的一种优选实施方式,所述氟苯尼考抗体包括多克隆抗体、单克隆抗体或重组抗体。
[0024]
第五方面,上述氟苯尼考人工抗原的以下任一应用:
[0025]
(1)在检测氟苯尼考中的应用;
[0026]
(2)在制备氟苯尼考检测试剂盒中的应用;
[0027]
(3)在制备氟苯尼考免疫层析试纸条中的应用。
[0028]
第六方面,上述抗体的以下任一应用:
[0029]
(1)在检测氟苯尼考中的应用;
[0030]
(2)在制备氟苯尼考检测试剂盒中的应用;
[0031]
(3)在制备氟苯尼考免疫层析试纸条中的应用。
[0032]
本发明具有如下有益效果:
[0033]
(1)本发明首次公开了一种新的氟苯尼考半抗原、人工抗原及其制备方法,用所述氟苯尼考人工抗原免疫动物,可得到效价高,灵敏度高的抗体,制备过程简单、经济,制备的多克隆抗体对氟苯尼考的检测灵敏度可达2.08ng/ml。本发明所提供的氟苯尼考半抗原及其制备的抗体,为建立快速、简便、价廉、灵敏、特异的氟苯尼考检测方法提供了新手段;
[0034]
(2)利用本发明提供的半抗原与载体蛋白的偶联物制备氟苯尼考抗体,制备过程简单、经济,抗体的检测灵敏度高、实用价值高,在兽药残留检测中具有重大价值。
附图说明
[0035]
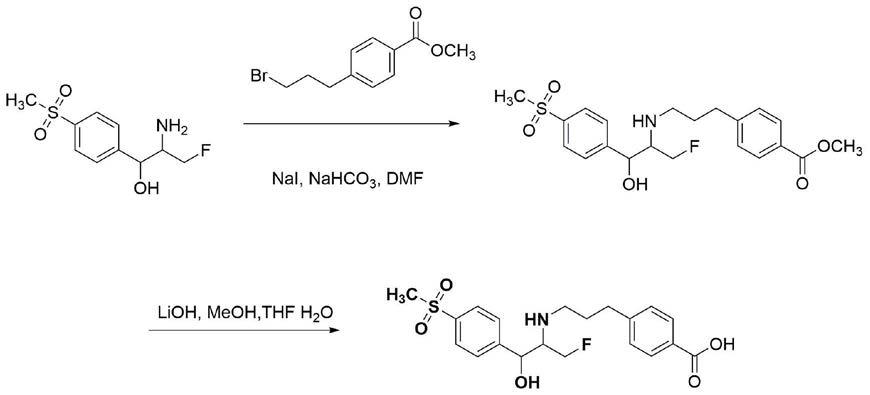
图1为本发明实施例1中式i所示氟苯尼考半抗原制备的流程图;
[0036]
图2为本发明实施例1中式i所示氟苯尼考半抗原的质谱图;
[0037]
图3为本发明实施例1中式i所示氟苯尼考半抗原的1h nmr核磁谱图;
[0038]
图4为本发明实施例2中ffa-e-klh的uv-vis光谱图;
[0039]
图5为本发明实施例2中ffa-e-bsa的uv-vis光谱图;
[0040]
图6为本发明实施例4中利用多克隆抗体检测氟苯尼考的标准曲线图。
[0041]
图7为加强免疫后,兔子的抗血清鉴定结果。
具体实施方式
[0042]
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为本领域技术人员所熟知的常规方法。下述实施例中所用的试验材料,如无特殊说明,均为从常规生化试剂厂商购买得到。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。以下实施例中所用的磷酸盐缓冲液(简称 pbs)均为ph 7.4、0.01m的磷酸盐缓冲液,所用碳酸盐缓冲液(简称cb)均为ph 9.6、0.05m的碳酸钠缓冲液。牛血清白蛋白简称bsa,钥孔血蓝蛋白简称klh。
[0043]
实施例1氟苯尼考半抗原的制备和表征
[0044]
一、氟苯尼考半抗原的制备
[0045]
式i所示氟苯尼考半抗原的制备如图1所示,具体包括以下步骤:
[0046]
s1、以dmf(n,n-二甲基甲酰胺)为溶剂,加入4.95g氟苯尼考胺和5.14g 4-(3-溴丙基)苯甲酸甲酯,向混合物中加入3.60g碘化钾和3.36g碳酸氢钠,40℃搅拌30h;
[0047]
s2、将步骤s1的产物冷却至室温,加入水,并用乙酸乙酯萃取,用盐水洗涤合并的有机层,用无水硫酸钠干燥;在真空下除去溶剂得到残留物;
[0048]
s3、以甲醇和thf(四氢呋喃)作溶剂,加入2.54g步骤s2的产物、20ml lioh(756mg)水溶液(是指756mglioh加水定容至 20ml),室温搅拌16h;
[0049]
s4、将s3得到的混合物浓缩,向残余物中加入水(30ml),然后用乙酸乙酯(30ml)萃取混合物;向水层中添加0.5m h2so4将 ph值调节至4.5~5.5;通过过滤收集混合物中的沉淀物,在真空下干燥,得到白色固体为式ⅰ中氟苯尼考半抗原,命名为ffa-e。
[0050]
式ⅰ结构如下所示:
[0051][0052]
二、氟苯尼考半抗原的表征
[0053]
1、质谱鉴定
[0054]
上述式i所示氟苯尼考半抗原的质谱检测结果如图2所示,结果分析如下,ms m/z[m+h]
+
理论值为410.47,实测值为410.3,与目标产物的分子量相吻合。
[0055]
2、核磁共振鉴定
[0056]
上述式i所示氟苯尼考半抗原的核磁氢谱鉴定结果如图3所示,结果分析如下,1h nmr(400mhz,dmso-d6)δ1.77-1.87(m,2h), 2.63(t,j=7.2hz,2h),2.75-5.85(m,2h),3.20(s,3h),3.31-3.38(m, 1h),4.18-4.33(m,1h),4.51-4.66(m,1h),4.88(d,j=7.2hz,1h),7.28 (d,j=8.4hz,2h),7.69(d,j=8.0hz,2h),7.87(d,j=8.0hz,2h),7.94 (d,j=8.4hz,2h),8.21(s,br,1h).分析上述数据结果表明,所合成的产物即为目标产物。
[0057]
上述式i所示氟苯尼考半抗原的核磁碳谱鉴定结果如图4所示,结果分析如下,
13
c nmr(100mhz,dmso-d6)δ28.69,32.11,43.50, 45.76,61.79,61.96,69.56,69.61,80.24,81.93,126.89,127.79,128.43, 128.67,129.41,140.02,146.61,147.70,167.39.lr-ms found 410 (m+h).分析上述数据结果表明,所合成的产物即为目标产物。
[0058]
实施例2氟苯尼考人工抗原的制备和表征
[0059]
一、氟苯尼考包被原的制备和鉴定
[0060]
1、氟苯尼考包被原的制备
[0061]
(1)将15mg实施案例1制备的式i氟苯尼考半抗原溶于0.5mldmf中,加入15mg edc和8mg nhs,室温条件下磁力搅拌反应 10小时,得到溶液a。
[0062]
(2)将10mg klh溶于10ml pbs缓冲液中,得到溶液b。
[0063]
(3)将a液逐滴加到b液中,室温搅拌,过夜反应,得到反应产物即为氟苯尼考免疫原ffa-e-bsa。将反应产物在pbs中透析72 小时,中间换6次水。透析后将反应产物分装于2ml离心管中,-20℃保存备用。
[0064]
二、氟苯尼考包被原鉴定
[0065]
将上述合成的产物采用uv-vis鉴定免疫原是否偶联成功。如图5 所示,λ
max
(ffa-e-bsa)与λ
max
(bsa)相比发生了蓝移,与λ
max
(ffa-e) 相比发生了蓝移。
[0066]
三、氟苯尼考免疫原的制备
[0067]
制备方法与上述氟苯尼考包被原的制备方法类似,区别在于,用 klh代替bsa。式i所示化合物合成氟苯尼考免疫原简称ffa-e-klh。
[0068]
四、氟苯尼考免疫原的鉴定
[0069]
将上述合成的产物采用uv-vis鉴定免疫原是否偶联成功。如图6 所示,λ
max
(ffa-e-klh)与λ
max
(klh)相比发生了红移,与λ
max
(ffa-e) 相比发生了红移。
[0070]
实施例3氟苯尼考抗血清的制备
[0071]
将实施例2制备的ffa-e-klh免疫2组3-4月龄,体重1.5-2.0kg 的雌性新西兰大白兔,每组2只。
[0072]
将免疫原用生理盐水稀释至1mg/ml,与等量弗氏佐剂乳化。
[0073]
首次免疫采用弗氏完全佐剂,颈背部皮内多点注射,免疫剂量为 1mg/只;4周后进行加强免疫,每隔3周加强免疫1次,共加免5 次,佐剂改为弗氏不完全佐剂,免疫剂量不变,改为颈背部皮下多点注射;第4次免疫1周后,用心脏采血的方法大量采血。
[0074]
取血后,将血液37℃静置2h,然后4℃静置过夜,然后3000rpm 离心20min,收集上
清液,即为抗血清,-20℃分装保存。
[0075]
实施例4氟苯尼考抗血清的鉴定
[0076]
采用间接竞争elisa方法,对实施例3得到的抗血清进行鉴定。具体操作步骤如下:
[0077]
(1)包被:用cb液将氟苯尼考包被原稀释到1μg/ml,每孔 100μl加至酶标板,37℃孵育2小时;
[0078]
(2)洗涤:倾去孔内液体,用洗涤液洗3遍,每次1min,在吸水纸上拍干;
[0079]
(3)封闭:每孔加入150μl封闭液,37℃孵育1小时,洗涤;
[0080]
(4)加样:每孔加入50μl pbs稀释的系列浓度的氟苯尼考或氟苯尼考胺标准品和50μl工作浓度的抗血清,37℃孵育30min,洗涤;
[0081]
(5)加二抗:每孔加入100μl hrp-羊抗兔igg,37℃孵育30min,洗涤;
[0082]
(6)显色:每孔加入100μl新鲜配制的tmb溶液,37℃避光显色15min;
[0083]
(7)终止:每孔加入50μl浓度为2mol/l的h2so4溶液终止反应;
[0084]
(8)读数:用酶标仪读取各孔的od
450nm
值;
[0085]
(9)建立标准曲线:以氟苯尼考或氟苯尼考胺标准品浓度的对数值为横坐标,以各个浓度对应的od值为纵坐标,绘制标准抑制曲线,并计算ic
50
值。
[0086]
加强免疫后,兔子的抗血清鉴定结果如图7所示,由标准曲线计算得到该抗血清对氟苯尼考的ic
50
分别为2.08ng/ml。
[0087]
以上所述实施例仅表达了本发明的实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制,但凡采用等同替换或等效变换的形式所获得的技术方案,均应落在本发明的保护范围之内。
