使用蛋白酶控制限制酶活性
背景技术:
1.限制酶、也称为限制性核酸内切酶是水解酯键的水解酶的一个子类,作为 dna或rna核酸酶并切割特定的dna或rna序列。当进行酶消化反应时,应优化所有涉及酶的活性,以精确获得预期的产品或结果。大多数限制酶随着时间连续催化底物(dna或rna),从而连续积累所需的dna或rna片段,偶尔也会积累不需要的副产物。
2.虽然通常通过特定的缓冲液和反应时间条件来尝试优化限制性核酸内切酶的酶反应,但有时也会存在不期望的反应和相关问题,特别是当酶在其主要活性之外还表现出非靶向活性时。优化的限制性核酸内切酶活性通常在设定时间内消化指定量的底物。然而,一些限制性核酸内切酶产生副反应和不需要的dna 或rna切割,具有累积的活性,尤其是在反应中酶过量时,其中反应在特定缓冲条件下持续很长时间,或者存在高甘油。在同源限制性位点以外的位点处的这种切割被称为星号活性。
3.控制酶的浓度或总反应时间、例如反应完成后通过热失活或其他纯化方法终止反应是限制酶总活性从而降低星号活性的常用方法。其他控制反应的方法可能更可取,特别是在需要精细控制以达到更高的分析可靠性时。
技术实现要素:
4.蛋白酶是水解蛋白质酶、消除其活性的酶。本发明利用蛋白酶的水解活性来控制限制酶的活性并消除或减少不需要的dna或rna片段的产生。
5.在本发明中,蛋白酶最初包含在限制性核酸内切酶反应混合物中或在某些点添加到其中,使得限制酶在它们的dna/rna消化反应过程中被蛋白酶灭活。以这种方式,总酶活性不仅受缓冲液和反应时间的控制,还受底物、限制性核酸内切酶和蛋白酶的相对量(有时包括蛋白酶添加时间)的控制,以便进一步限制过度消化和星号活性。蛋白酶抑制剂可任选地用于在反应的所需点停止或抑制蛋白酶活性。
6.本发明在以下附图和描述中、包括在实施例中进一步描述,
附图说明
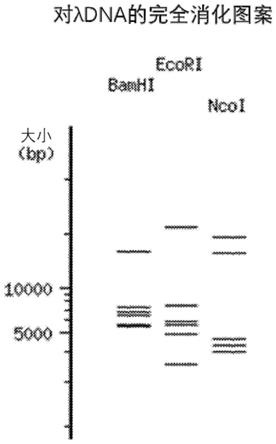
7.图1:根据dna序列及酶识别和切割特异性,bamhi、ecori和ncoi对λdna 的理论完整图案。该图案可以与图3-8中所示的任何条带对齐,以表示切割和星号活性的完成。
8.图2:模块a:预测的内在限制性核酸内切酶活性。实线:不含蛋白酶的限制性核酸内切酶活性;虚线,具有蛋白酶的限制性核酸内切酶。模块b:总限制性核酸内切酶活性。实线:不含蛋白酶的总限制酶活性;虚线,具有蛋白酶的总限制酶活性。
9.图3:在缓冲液a1和a1s2中ecori对λdna的酶活性。模块a:在缓冲液a1中1小时,模块b:在缓冲液a1s2中1小时,模块c:在缓冲液a1中 20小时,模块d:在缓冲液a1s2中20小时。下降三角形(顶部)代表限制性核酸内切酶的2倍连续稀释。
10.图4:在缓冲液a2和a2s2中ecori对λdna的酶活性。模块a:在缓冲液a2中1小时,模块b:在缓冲液a2s2中1小时,模块c:在缓冲液a2中 20小时,模块d:在缓冲液a2s2中20小时。
下降三角形(顶部)代表限制性核酸内切酶的2倍连续稀释。
11.图5:在缓冲液a3和a3s2中ecori对λdna的酶活性。模块a:在缓冲液a3中1小时,模块b:在缓冲液a3s2中1小时,模块c:在缓冲液a3中 20小时,模块d:在缓冲液a3s2中20小时。下降三角形(顶部)代表限制性核酸内切酶的2倍连续稀释。
12.图6:在缓冲液a3和a3s2中bamhi对λdna的酶活性。模块a:在缓冲液a3中1小时,模块b:在缓冲液a3s2中1小时,模块c:在缓冲液a3中 20小时,模块d:在缓冲液a3s2中20小时。下降三角形(顶部)代表限制性核酸内切酶的2倍连续稀释。
13.图7:在缓冲液a3和a3s2中ncoi对λdna的酶活性。模块a:在缓冲液a3中1小时,模块b:在缓冲液a3s2中1小时,模块c:在缓冲液a3中20 小时,模块d:在缓冲液a3s2中20小时。下降三角形(顶部)代表限制性核酸内切酶的2倍连续稀释。
14.图8:ecori对λdna的酶活性结果。模块a:在缓冲液a2lysc中1小时,模块b:在缓冲液a2trypsin中1小时,模块c:在缓冲液a2lysc中22小时,模块d:在缓冲液a3trpsin中22小时。下降三角形(顶部)代表限制性核酸内切酶的2倍连续稀释。
15.图9:显示使用本发明的试剂和技术进行自动基因分型/测序/等位基因分型/ 基因表达分析的流程图。
16.图10:显示优化其中使用蛋白酶来控制它的限制酶反应的流程图。
具体实施方式
17.可用于本发明的限制酶包括核酸内切酶和催化性rna(核酶)、dna酶和 rna酶。dna酶包括大量的酶,根据它们的切割靶点,进一步分为i型、ii型 (以下实施例中的bamhi、ecori和nco1是iip型;回文)、iii型、iv型和v 型(例如来自crispr的cas9-grna复合物)以及人工限制酶,它们可以靶向大的dna位点(高达36bp),并且可以设计为与所需的dna序列结合。锌指核酸酶是最常用的人工限制酶。
18.蛋白酶可分为在内部切割目标蛋白质内肽酶;和外肽酶,其中羧肽酶从蛋白质的羧基末端消化氨基酸,氨肽酶从氨基末端消化蛋白质。
19.根据用于促进蛋白水解的催化残基,蛋白酶可以进一步分为七大类:丝氨酸蛋白酶(使用丝氨酸醇作为催化残基);半胱氨酸蛋白酶(使用半胱氨酸硫醇作为催化残基);苏氨酸蛋白酶(使用苏氨酸仲醇作为催化残基);天冬氨酸蛋白酶(使用天冬氨酸羧酸作为催化残基);谷氨酸蛋白酶(使用谷氨酸羧酸作为催化残基);金属蛋白酶(使用金属、通常是锌用于催化);以及天冬酰胺肽裂解酶—使用天冬酰胺进行消除反应(不需要水)。
20.证明适用于控制限制酶反应、包括为了降低星号活性的任何前述蛋白酶(除了以下实施例中的那些)可用于本发明。蛋白酶的具体示例包括:tev蛋白酶,其特异于序列enlyfqs;胰蛋白酶原;羧肽酶b;肠激酶;lys-c和凝血酶。
21.除了在反应混合物中加入蛋白酶与限制性核酸内切酶和底物外,还可以在反应过程的稍后时间加入蛋白酶以抑制或阻止核酸酶活性。添加组分的时间也可以通过常规实验进行优化。
22.蛋白酶抑制剂包括α1-抗胰蛋白酶、α1-抗胰凝乳蛋白酶、c1-抑制剂、抗凝血酶、纤溶酶原激活剂抑制剂-1和神经丝氨酸蛋白酶抑制剂。为了控制与抑制剂反应的蛋白酶部分,需要选择抑制剂以抑制反应中使用的蛋白酶消化反应中使用的限制酶。蛋白酶抑制剂
38.缓冲液a2:20mm tris-hcl,ph 7.5,40mm nacl,10mm mgcl2,0.1mm cacl239.缓冲液a3:20mm tris-hcl,ph 8.0,10mm mgcl2,0.1mm cacl240.缓冲液a1s2:缓冲液1加0.05单位/ml蛋白酶k
41.缓冲液a2s2:缓冲液2加0.05单位/ml蛋白酶k
42.缓冲液a3s2:缓冲液3加0.05单位/ml蛋白酶k。
43.ecori使用稀释剂c以2倍稀释连续稀释(图中每个连续泳道代表相对于前一个泳道的连续2倍稀释)。λdna的消化在缓冲液a1、缓冲液a2、缓冲液 a3以及缓冲液a1s2、缓冲液a2s2和缓冲液a3s2中进行。通过在1小时或20 小时添加6x终止溶液来停止反应。
44.在图3中,使用缓冲液a1:ecori可以在1小时在第8泳道完全消化λdna,但在第1至第3泳道之间显示出星号活性。ecori可以在20小时通过第11泳道完全消化λdna,但在第1至第6泳道之间具有星号活性。
45.在图3中,使用缓冲液a1s2:ecori可以在1小时通过第3泳道完全消化λdna,并在任何泳道中都没有星号活性。ecori可以在20小时通过第4泳道完全消化λdna,并在任何泳道中都没有星号活性。
46.在图4中,使用缓冲液a2:ecori可以在1小时通过第9泳道完全消化λdna,但在第1泳道中具有星号活性。ecori可以在20小时通过第12泳道完全消化λdna,但在第1至第5泳道之间显示出星号活性。
47.在图4中,使用缓冲液a2s2,ecori可以在1小时通过第5泳道完全消化λdna,但在任何泳道中都没有星号活性。ecori可以在20小时通过第6泳道完全消化λdna,但在任何泳道中都不显示星号活性。
48.在图5中,使用缓冲液a3,ecori可以在1小时通过第7泳道完全消化λdna,但没有显示星号活性。ecori可以在20小时通过第9泳道完全消化λdna,但在第1至第4泳道之间具有星号活性。
49.在图5中,使用缓冲液a3s2,ecori可以在1小时通过第6泳道完全消化λdna,但在任何泳道中都没有星号活性。ecori可以在20小时通过第6泳道完全消化λdna,但在任何泳道中都没有星号活性。
50.图3-5中所示的结果显示蛋白酶k的加入改变了所有缓冲液a1、a2和a3 中ecori的性能,当包括蛋白酶k时,它们分别被重新命名为缓冲液a1s2、 a2s2、a3s2。
51.实施例3:内部蛋白酶控制适用于任何限制性核酸内切酶
52.所有限制性核酸内切酶都是蛋白质,并且所有蛋白质都可以被蛋白酶k消化,因此该方法预计对其他限制性核酸内切酶与ecori一样有效。
53.在缓冲液a3和a3s2中除了ecori(参见实施例2),还测试了另外两种限制性核酸内切酶:bamhi和ncoi(来自new england biolabs,inc.)
54.bamhi和ncoi分别用稀释剂a(new england biolabs,inc.)以2倍稀释进行连续稀释,其中底物是λdna,缓冲液是缓冲液a3或a3s2。通过分别在1 小时和20小时加入6x终止溶液来终止反应。
55.在图6中,使用缓冲a3:bamhi可以在1小时通过第7泳道完全消化λdna,并没有星号活性。bamhi可以在20小时通过第9泳道完全消化λdna,但在第 1至第4泳道之间显示出星号活性。
56.在图6中,使用缓冲液a3s2:bamhi可以在1小时通过第6泳道完全消化λdna,并没有星号活性。bamhi可以在20小时通过第6泳道完全消化λdna,并在任何泳道中都没有星号活性。
57.在图7中,使用缓冲液a3:ncoi可以在1小时通过第8泳道完全消化λdna,并没有星号活性。ncoi在20小时在第14泳道完全消化λdna,并在第1至第5 泳道之间具有星号活性。
58.在图7中,使用缓冲液a3s2,ncoi可以在1小时通过第8泳道完全消化λdna,并在任何泳道中都没有星号活性。ncoi可以在20小时通过第13泳道完全消化λdna,但在任何泳道中都没有星号活性。
59.本实施例表明,除了实施例2中的ecori外,bamhi和ncoi的所需酶活性可以通过添加蛋白酶k来改变。
60.实施例4:使用蛋白酶k以外的蛋白酶进行内部蛋白酶控制
61.蛋白酶k对蛋白质消化具有广泛的特异性,并且在大多数缓冲液中都具有活性。如果在初级反应酶的特定反应缓冲液中具有活性,其他蛋白酶可以替代蛋白酶k作为内部蛋白酶控制。
62.内切蛋白酶lysc是在赖氨酸的羧基侧切割肽键的丝氨酸内切蛋白酶,而胰蛋白酶是在赖氨酸或精氨酸的羧基侧切割肽键的丝氨酸内切蛋白酶。两种酶均购自new england biolabs。
63.缓冲液a2lysc:缓冲液a2加400ng/ml内切蛋白酶lysc。
64.缓冲液a2胰蛋白酶:缓冲液a2加25ng/ml胰蛋白酶。
65.ecori用稀释剂c以连续2倍稀释进行稀释,底物是λdna,消化在缓冲液 a2lysc或缓冲a2trpsin中进行。分别在1小时和22小时加入6x终止溶液终止反应。
66.在图8中,使用缓冲液a2lysc:ecori可以在1小时通过第5泳道完全消化λdna,其中没有星号活性,可以在22小时通过第4泳道完全消化λdna,其中没有星号活性。使用缓冲液a2trpsin:ecori可以在1小时通过第6泳道完全消化λdna,其中没有星号活性,可以在22小时通过第6泳道完全消化λdna,其中没有星号活性。
67.该实施例表明,能够消化限制性核酸内切酶的其他蛋白酶可用作限制性核酸内切酶活性的内部蛋白酶控制。
68.本发明方法的应用
69.本发明方法的用途包括其中通过使用凝胶电泳捕获的核酸的片段化图案来鉴定核酸的任何应用,并且包括使用此类鉴定手段的dna或rna测序或基因分型,或等位基因分型。具体应用包括组织、血液或体液(活的或非活的)的生物特征识别,或其他样本供体识别,例如法医学或治疗;确定血统信息,以及在鉴定核酸来源或其序列时需要高度可靠性的其他研究应用。本发明的方法也可用于基因表达分析,其中增加的基因表达会出现在凝胶结果中,作为某些较粗和/或较暗的条带。
70.使用本发明的试剂和方法对样品进行自动测序、基因分型、等位基因分型或基因表达分析的一种方法在图9中以流程图形式阐述。图9中的步骤可以自动执行(使用例如机器人,其以特定的时间间隔从特定的容器中添加试剂)。在最后一步中,凝胶结果由中央处理器自动读取和处理,该中央处理器能够将它们与已知结果相关联,以识别样品来源或指示样品供体的可能血统(基于切割后的某些片段的存在)。
71.反应优化
72.除了下面举例说明的那些之外,确定与特定限制性核酸内切酶一起使用的蛋白酶的一般方法是使蛋白酶和限制性核酸内切酶的其他组合以及适当的缓冲液进行以下实施例中列出的实验,并进行在本文中描述和举例说明的活性测定,其中如本文以适当水平连续稀释限制性核酸内切酶,以找到最适合特定功能的组分的组合,包括找到具有诸如每单位限制性核酸内切酶和蛋白酶最活跃、并且可以最有效地减少星号活性的属性的那些组分。
73.某些功能需要或优选某些限制性核酸内切酶或其某些类型,并且它们可以与相容的蛋白酶以相容的比例和在适当的缓冲液中组合,所有这些都可以通过常规实验按照相同方法用于寻找以下实施例中列出的组合。
74.可用于本发明的其他类型的限制酶包括蛋白质核酸内切酶和催化性rna (核酶),以及dna酶和rna酶。可以进行与本文所述实验类似的实验以找到合适的rna酶/蛋白酶组合,用于控制rna酶反应和/或降低此类rna消化反应中的星号活性。当使用未知的限制性内切酶re,并且希望使用蛋白酶来控制反应或抑制或消除星号活性时,可以按照图10的流程图中的步骤来优化反应条件。图10中的步骤跟随图3至8中阐述的步骤,用于确定列出的限制酶的最佳反应条件。一个重要的步骤是进行连续稀释以确定反应混合物中的最佳浓度。图10中的步骤可以用每种限制性内切酶re进行,希望确定最佳使用条件。
75.在此描述的具体过程、方法和组合物代表优选实施方式并且是示例性的并且不旨在限制本发明的范围。考虑到本说明书,本领域技术人员将想到其他目的、方面和实施方式,并且包括在由权利要求的范围限定的本发明的精神内。对本领域技术人员来说显而易见的是,在不脱离本发明的范围和精神的情况下,可以对本文公开的发明进行各种替换和修改。在此说明性地描述的本发明可以在没有作为必要而具体公开的任何一个或多个要素、或一个或多个限制的情况下适当地实践。因此,例如,在本文的每个实例中,在本发明的实施方式或实例中,任何术语“包括”、“包含”、“含有”等应被广泛地而非限制性地解读。本文中说明性描述的方法和过程可以以不同的步骤顺序适当地实践,并且它们不一定限于本文或权利要求中指出的步骤顺序。
76.本发明已经在本文中广泛地和一般性地进行了描述。落入一般公开的每个较窄的物种和亚属组也构成本发明的一部分。已使用的术语和表达被用作描述而非限制,并且使用此类术语和表达无意排除所示和描述的特征或其部分的任何等同物,但应认识到在所要求保护的本发明的范围内可以进行各种修改。因此,应当理解,虽然本发明已经通过优选实施方式和可选特征具体公开,但是本领域技术人员可以对这里公开的概念进行修改和变化,并且这种修改和变化被认为是属于所附权利要求书所限定的本发明范围。
